高血壓腦出血合并頸動脈瘤感染新型冠狀病毒1例
欒濤 廉坤 王振 王帥穎 高永軍 徐蔚 葉寶琴 張曙
新型冠狀病毒肺炎(coronavirus disease 2019,COVID-19)疫情可能將在世界范圍內長時間流行[1]。因此,總結早期救治經驗對今后疫情防控有一定的參考價值。筆者報道2019年12月26日武漢市新洲區人民醫院收治的1例高血壓腦出血合并頸動脈瘤感染新型冠狀病毒(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)患者的診治經過,以期為臨床診治提供參考。
患者 女,69歲。2019年12月26日“因突發頭昏頭痛伴神志不清近2 h”入院。體格檢查:體溫36.8℃,脈搏77次/min,呼吸22次/min,血壓191/107 mmHg;雙側瞳孔等大,直徑約3 mm,光反射靈敏;格拉斯哥昏迷指數(Glasgow coma scale,GCS)9分(E2V3M4),口角左歪,吐字不清;左側肢體偏癱,肌力約0~1級,左側病理征陽性;右側肢體肌力、肌張力正常,右側病理征未引出。急診顱腦CT檢查示:小腦出血破入腦室、腦室積血,見圖1a;后急診行“雙側腦室穿刺引流術”。術后第2天CT血管造影(CT angiography,CTA)檢查示小腦積血,右側頸內動脈海綿竇段動脈瘤;胸部CT檢查示雙肺正常,見圖1b-c。與家屬溝通后,動脈瘤暫不作處理,行左側小腦開顱血腫清除術,術后患者病情平穩。當時預計患者需要較長時間(可能>2周)的人工氣道和呼吸支持,12月30日行氣管切開術。2020年1月6日拔除雙側引流管;1月9日患者意識逐漸清醒,GCS 15分,予以吡拉西坦注射液(4 g/次、1次/d)、銀杏莫達注射液(20ml/次、1 次 /d)靜脈滴注。在院康復治療期間動態檢查顱腦及胸部CT,見圖2。
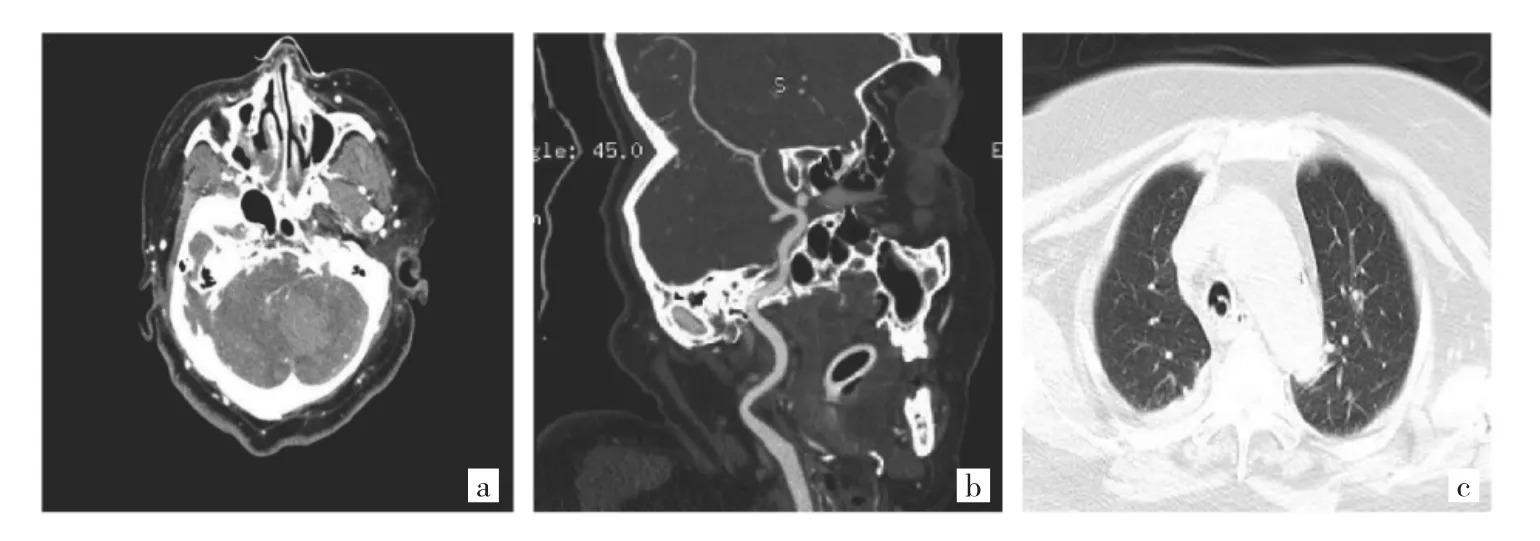
圖1 2019年12月26日急診顱腦CT檢查及雙側腦室穿刺引流術后影像學檢查所見(a:左側小腦片狀出血;b:右側頸內動脈海綿竇段動脈瘤;c:雙肺正常)
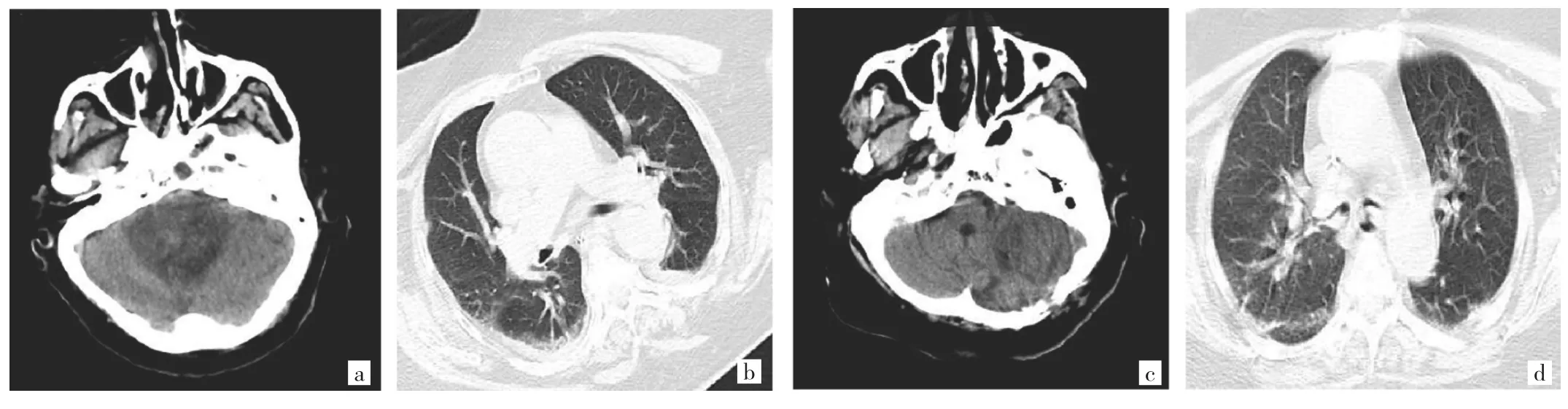
圖2 患者院內康復期顱腦及胸部CT檢查所見(a、b:1月6日小腦片狀低密度軟化灶,雙肺正常;c、d:1月31日左側小腦內血腫吸收良好,雙肺紋理增多增粗,雙下肺墜積性肺炎)
2月6日患者體溫升高至38.4℃,嗜睡,GCS 14分(E3V5M6),復查 CT見四腦室擴大,右肺大面積感染,見圖3a-b;根據痰培養予以左氧氟沙星(0.4 g/次、1次/d)靜脈滴注;病毒核酸檢測陰性。2月9日患者神志恍惚、躁動不安,GCS 12分(E3V4M5),心率較快、呼吸急促、全身紫紺,血氧飽和度60%,并發急性呼吸窘迫綜合征(acute respiratory distress syndrome,ARDS),予以床邊氣管造瘺口插管,呼吸機正壓給氧,血氧飽和度回升92%,復查CT見小腦軟化灶吸收良好,雙肺高密度影,重度感染,見圖3c-d;病毒核酸檢測陽性,確診為COVID-19,加用洛匹那韋(400 mg/次,2 次 /d)、利巴韋林(0.4 g/次、4次 /d)、干擾素(600 U/次、2 次/d)、甲潑尼龍(40 mg/次、2次 /d)。2月10日轉入ICU,患者淺昏迷,呼之不應,氣管切開狀態,雙肺呼吸音粗,查血氣分析:pH 7.45,PaCO231.8mmHg,PaO270mmHg。2 月11日患者淺昏迷,呼吸機輔助呼吸,呼吸模式間歇正壓通氣+呼氣末正壓通氣5 cmH2O,氧濃度40%,支持壓力16cmH2O,潮氣量440 ml,復查CT見四腦室擴大,雙肺感染面積較前擴大,見圖3e-f;加用免疫球蛋白20 g抗感染。
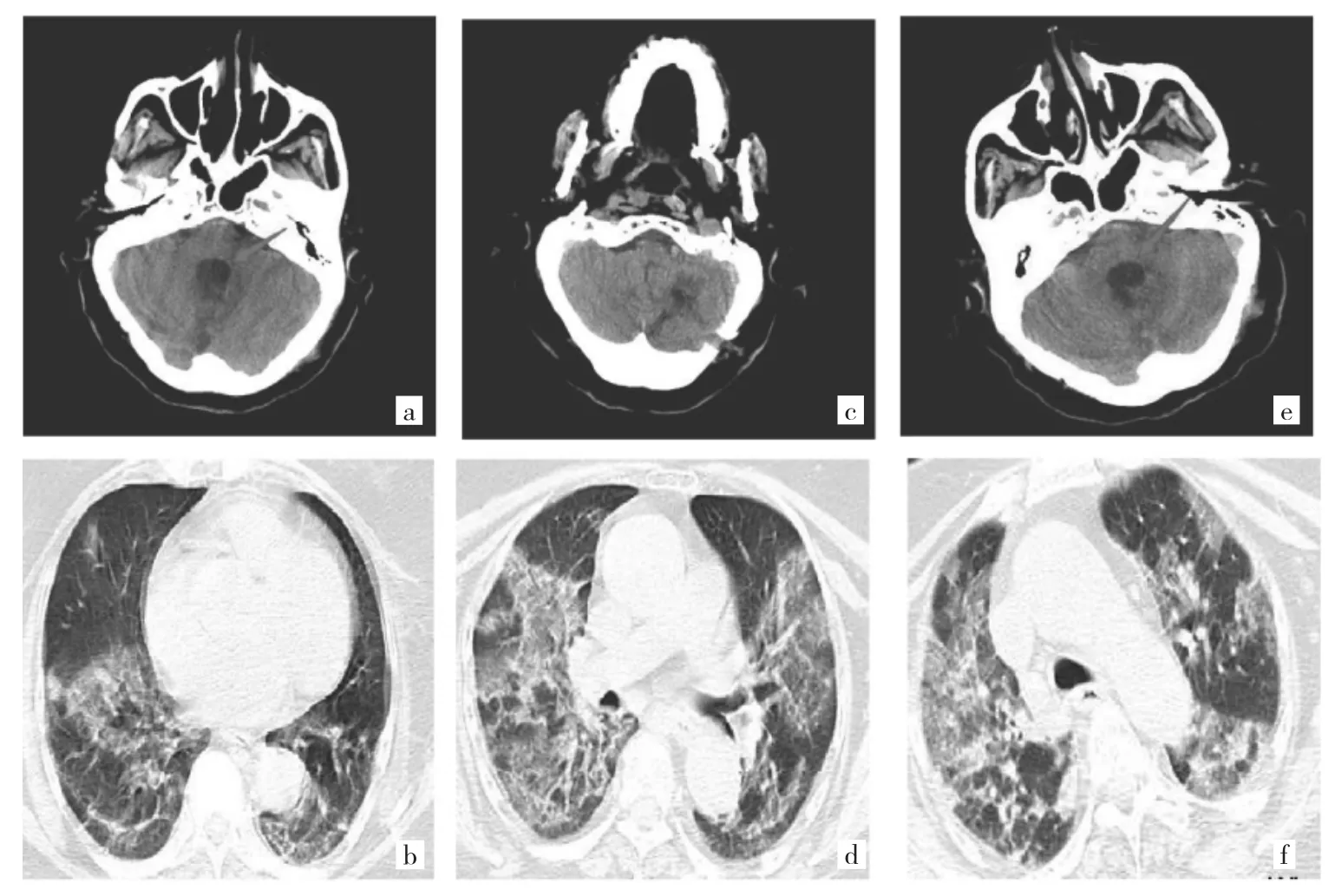
圖3 患者感染新型冠狀病毒(SARS-CoV-2)前后顱腦及胸部CT檢查所見[a、b:2月6日四腦室擴大,雙肺肺紋理增多增粗、紊亂,散在斑片狀模糊影,感染性病變,懷疑病毒性肺炎;c、d:2月9日小腦軟化灶吸收良好,雙肺大片磨玻璃樣改變,結合病毒核酸檢測結果確診為新型冠狀病毒肺炎(COVID-19);e、f:2月11日四腦室擴大,雙肺彌漫性磨玻璃密度影,氣管插管術后,上腔靜脈見條形高密度影]
2月12至14日維持前期治療方案。2月15日患者持續發熱,加用抗生素頭孢哌酮鈉舒巴坦鈉3 g,每6 h靜脈滴注1次。2月16日腦鈉肽(brain natriuretic peptide,BNP)8 552 ng/L,靜脈推注呋塞米20 mg,減少液體攝入量。2月17日血氧飽和度95%,給予多巴胺8 mg/min靜脈泵入,血壓在102/65 mmHg左右。復查血氣分析:pH 7.35,PaCO238.7 mmHg,PaO2112 mmHg,乳酸0.5 mmol/L;復查BNP 948 ng/L。2月18日給予多巴胺8 mg/min靜脈泵入,血壓在107/63mmHg左右,血氧飽和度95%,PO2152 mmHg,下調呼吸機氧濃度,為行快速容量復蘇,行股靜脈穿刺置管術。2月19日突發血壓下降至70/43 mmHg,血氧飽和度下降至66%,搶救未成功死亡。
討論 患者自2019年12月26日入院,急診行雙側腦室穿刺引流術,術后第2天CTA檢查見小腦積血,并查出有頸內動脈瘤,考慮患者年齡較大,其動脈瘤暫不作處理,行小腦血腫清除術,術后體征平穩,預計患者需要長時間(可能>2周)的人工氣道與呼吸支持,遂行氣管切開術[2],后在院康復治療。2020年2月6日,患者出現呼吸困難,血氧飽和度不斷下降,根據影像學表現,懷疑感染SARS-CoV-2,但病毒核酸檢測陰性,暫不能確診。2月9日,患者出現ARDS,且雙肺大面積感染,病毒核酸檢測陽性,確診為COVID-19。根據《COVID-19診療方案(試行第六版)》:呼吸道飛沫和密切接觸傳播是SARSCoV-2的傳播途徑。在相對封閉的環境中,長時間暴露于高濃度氣溶膠情況下存在經氣溶膠傳播的可能。考慮患者切開的氣道暴露于空氣中,可能是感染SARS-CoV-2的具體原因[3]。
病毒核酸檢測是目前確診COVID-19的“金標準”。但根據報道,一些臨床高度疑似感染SARS-CoV-2的患者,核酸檢測陽性率并不高,為30%~50%[4]。本例患者5次病毒核酸檢測中有2次陰性,可能原因如下:(1)第1次陰性的檢測時間為2月6日,而COVID-19患者IgM抗體一般在1周時出現峰值[5],故可能出現假陰性;(2)第2次陰性的檢測時間為2月15日,自2月9日確診COVID-19后,開始使用利巴韋林、洛匹那韋等抗病毒藥物,可能使患者體內病毒量低于檢測下限,從而造成假陰性[6]。
細胞因子風暴(cytokine storm,CSS)是決定肺外多器官功能衰竭的關鍵因素[7],血管緊張素轉化酶2是介導SARS-CoV-2激活人體免疫系統產生CSS的關鍵環節。發生CSS后,患者淋巴細胞計數、氧合指數下降,乳酸脫氫酶、D-二聚體水平升高[8]。患者在2019年12月27日至2020年2月6日期間實驗室檢查結果趨于穩定,2月17至19日(死亡前3 d)多項實驗室指標異常,肺部CT檢查可見大片白色實變影,這些是CSS的具體表現[9]。糖皮質激素應用于病毒性肺炎的作用機制是通過降低炎癥細胞因子來減輕對組織的損傷作用,即減輕肺的滲出、損傷和后期的肺纖維化[10]。本例患者在2月9至15日使用甲潑尼龍40 mg/次、2次/d;2月16日停用后,多項實驗室指標出現大范圍波動,病情繼續惡化。目前尚無任何可靠證據證實某種藥物對COVID-19有效[11],當前治療核心仍是對癥支持治療,同時謹慎使用糖皮質激素。有研究報道冠狀病毒累及神經系統[12-13]。患者自2月6日意識逐漸減弱、體溫升高、腦室擴張,表現為中樞神經系統感染,給予左氧氟沙星治療7 d未見療效,后加用頭孢哌酮鈉舒巴坦鈉也無明顯好轉。相關共識指出,對于中樞神經系統感染,治療藥物應選擇易透過血腦屏障的抗生素,以靜脈給藥途徑為主,治療原則以最大藥物劑量與長療程治療為主;對于靜脈給藥48~72 h效果不明顯、病情嚴重者,可行腦室注射或腰椎穿刺鞘內注射給藥[14-15]。本例患者若行腰椎穿刺,對腦脊液進行培養,再加用抗生素鞘內注射治療中樞神經系統感染,可能會有積極效果。
綜上所述,本例患者住院康復期間感染COVID-19,可能與院內流動人群傳播有關。該患者感染SARS-CoV-2后病情迅速加重,呼吸功能逐漸減弱,實驗室指標出現異常,但無頸動脈瘤破裂癥狀,死亡原因可能是CCS。筆者認為,若患者實驗室指標出現紊亂,應注意CCS的發生,合理給予糖皮質激素;若COVID-19患者出現昏迷與神經反應性降低,應考慮中樞神經系統感染,積極給予相應治療。

