同期推量放射治療食管癌的療效分析
韓 翔,畢曉蕾,竇超超,邢曉波,張 真
(青島大學附屬青島市中心醫院 a.放一科;b.關節與運動醫學科,山東 青島 266042)
食管癌是我國常見的惡性腫瘤之一,發病時常為中晚期,僅有15%~25%患者可行手術治療,放療為治療食管癌的主要手段之一[1]。食管癌的局部控制率直接影響生存率,而局控率的提高則依賴于放療劑量[2]。調強放療技術(intensity-modulated radiation therapy,IMRT)擁有較好的靶區適形度,與三維適形放療相比不良反應輕[3],是目前常用的放療手段之一。同期推量放射治療(simultaneous integrated boost radiotherapy,SIB)可給予局部腫瘤及轉移灶較高劑量,該技術在頭頸部腫瘤中得到廣泛應用,但在食管癌腫瘤及轉移淋巴結中使用同期推量的報道較少。本文旨在研究應用同期推量調強放療(SIB-IMRT)技術治療食管癌的近期療效及放療副反應,為臨床提高一種有效的治療手段。
1 資料與方法
1.1 一般資料選取2016年1月至2018年6月于我院治療的食管癌患者69例,納入標準:①所有患者均經病理學證實;②KPS≥70分;③均經外科醫師證實無手術指征或不愿行外科手術治療;可耐受放療。排除標準:①影像學證實遠處轉移;②有穿孔、瘺道形成或深達縱膈的深潰瘍;③既往未行胸部腫瘤放療;④嚴重器官臟器損傷。其中男49例,女20例,年齡55~85歲[(64.51±8.88)歲],上段食管癌18例,中段食管癌32例,下段食管癌19例。分期為Ⅰ~Ⅲ期。64例患者證實有區域淋巴結轉移,45例患者行替吉奧或順鉑方案同步化療。根據放療計劃不同將其分為同期推量組及序貫組,其中同期推量組38例,序貫組31例,兩組一般資料比較,差異無統計學意義(P>0.05),具有可比性,見表1。所有患者均知情同意,且經過我院倫理委員會批準。
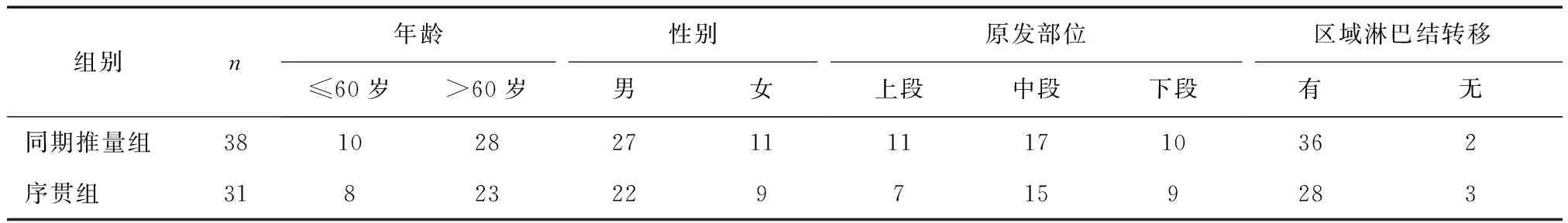
表1 兩組患者臨床資料比較 (n)
1.2 方法病灶位于中上段者采用頭頸肩熱塑面罩及頭枕固定,下段者采用真空體墊固定,采用螺旋CT強化掃描,5 mm每層,上界至顱底,下界至顱底下L2下緣。同步推量組設定腫瘤靶區(gross tumor volume,GTV)為CT圖像可見腫瘤,其中GTVnx為原發腫瘤,GTVnd為轉移淋巴結,計劃腫瘤靶區(plan gross tumor volume,PGTV)為GTV外放5 mm,臨床靶區(clinical tumor volume,CTV)為區域淋巴結引流區及轉移淋巴結所在引流區,計劃靶區(planning tumor volume,PTV)為CTV外放5 mm。序貫組無PGTVnd、PGTVnx,其余同同步推量組。劑量設定為:同期推量組PGTVnx、PGTVnd 2.14 Gy/f,PTV 1.8 Gy/f,共28 f,5次/周,95%PGTVnx 59.92 Gy,95% PGTVnd 59.92 Gy,95%PTV 50.4 Gy;序貫組PTV 2 Gy/f,共25 f,5次/周,結束后給予局部腫瘤及轉移淋巴結加量,2 Gy/f,共5 f,95%PTV 60 Gy。其中危及器官(肺、脊髓、心臟、大血管等)劑量均在允許范圍內。
1.3 觀察指標比較兩組放療計劃重要危及器官受量,并在放療后1年內對患者進行隨訪,觀察患者放療后主觀癥狀改善情況、CT結果,近期療效為放療后1月復查患者影像學檢查,按照RECIST1.1標準[4]區分,規定完全緩解(CR)、部分緩解(PR)、穩定(SD),其中CR+PR為有效,有效率=有效例數/該組總例數。不良反應多為放射性食管炎、放射性肺炎及食欲減退等。按照射腫瘤治療協作組(RTOG)標準進行分級[5]。同時觀察近期不良反應及6個月、1年生存率。
1.4 統計學方法采用SPSS 19.0統計學軟件進行處理。計量資料以均數±標準差表示,組間采用t檢驗進行比較;計數資料以例數或率表示,組間比較采用卡方檢驗;生存分析采用Kaplan-Meier生存分析。P<0.05為差異有統計學意義。
2 結果
2.1 兩組計劃危及器官受量比較兩組重要危及器官如脊髓最大量Dmax、雙肺平均劑量MLD、雙肺V5、V20比較,差異均無統計學意義(P>0.05),見表2。
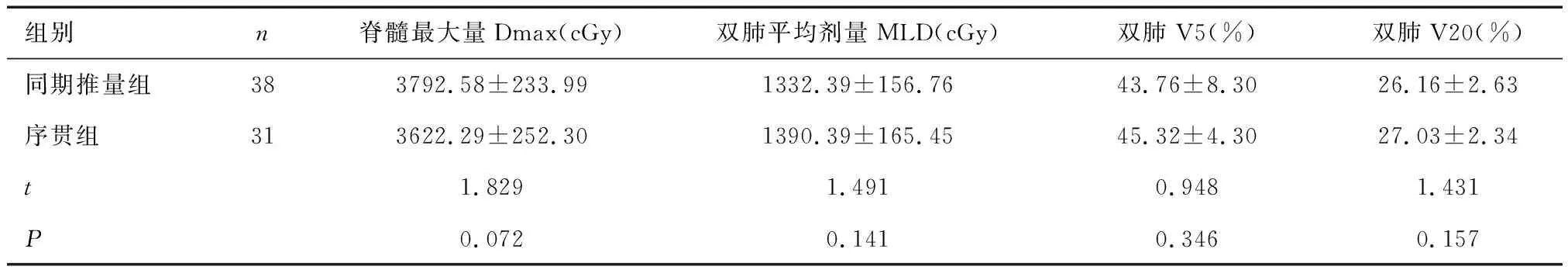
表2 同期推量組與序貫組腫瘤控制率的比較
2.2 兩組近期療效比較兩組患者均完成放療,兩組近期療效比較,差異無統計學意義(P>0.05),見表3。
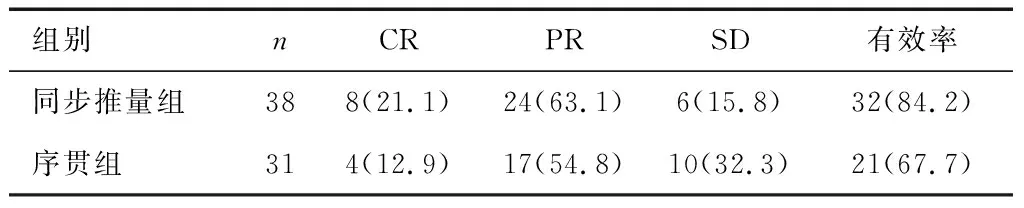
表3 同期推量組與序貫組腫瘤控制率的比較 [n(%)]
2.3 兩組中位生存時間及生存率比較所有患者均完成隨訪,隨訪率100%。同期推量組與序貫組的中位生存期分別為21.8月和19.8月,兩組比較,差異均無統計學意義(χ2=1.233,P=0.267)。其中同步推量組6個月及1年生存率分別為100%、84.21%;序貫組為90.32%、77.41%,兩組間6個月及1年生存率比較,差異無統計學意義(P>0.05)。生存曲線見圖1。
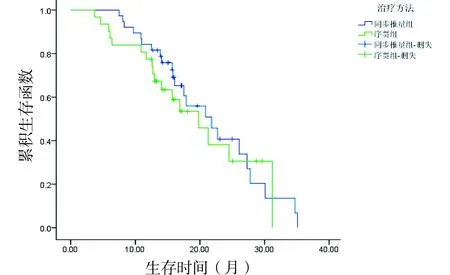
圖1 同步推量組與序貫組生存曲線
2.4 兩組近期不良反應比較兩組放射性肺炎及放射性食管炎多為Ⅱ級及以下,其中兩組放射性肺炎發生率比較,序貫組高于同步推量組,且差異有統計學意義(χ2=6.043,P<0.05),放射性食管炎的發生例數比較,差異無統計意義(P>0.05)。見表4。
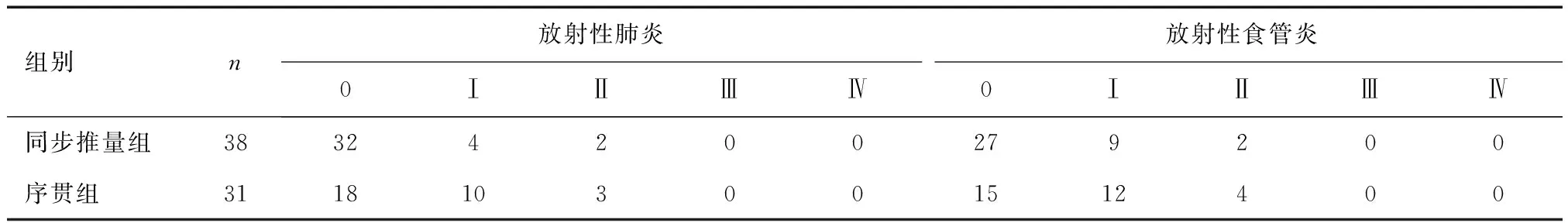
表4 同步推量組與序貫組相關不良反應的比較 (n)
3 討論
約80%的食管癌患者就診時即為中晚期,無手術指征,放療即成為其治療的主要手段之一。食管解剖位置特殊,周圍有心臟、雙肺、脊髓、大血管等重要臟器,大劑量的放療照射能明顯增加這些組織的毒性反應,從而限制劑量的進一步提升,且降低患者生活質量。根據RTOG研究顯示[6,7],食管癌同步放化療中,放療劑量由50.4 Gy提高到64.8 Gy,并未帶來生存獲益,這可能是由于當時放療技術多為二維技術,提高局部劑量的同時,周圍重要危及器官受量相應增高,放療的不良反應也明顯增加。
IMRT相比二維放療技術、三維適形放療擁有較高的適形度,聯合同步推量技術,能夠在保證腫瘤適形度的同時,對周圍危及器官受量進行限制,且縮短治療時間,減少反復制定放療計劃。研究顯示[8~10],SIB-IMRT在提高靶區劑量分布的同時降低周圍危及器官如脊髓、心臟的平均劑量,雙肺V30、V20、V5明顯偏低,且脊髓最大量及放療靶區中最小劑量均與普通調強放療計劃差異有統計學意義[11]。本研究中,SIB-IMRT組脊髓最大量Dmax、雙肺MLD、V5、V20與序貫組比較,差異無統計學意義,可能與物理師制定計劃習慣和樣本量偏少有關。SIB-IMRT在一次計劃中即可實現,縮短治療時間,減少因再次加量所造成的再次定位及計劃設計,減少醫保費用支出,避免過程中出錯的可能。研究證明,在頸部及胸上段食管癌中,7野調強計劃與3、5野計劃相比,靶區適形性指數和不均勻指數較好,適形度高,而雙肺V5明顯低于9野計劃,可作為SIB-IMRT計劃首選[12]。
有研究報道,SIB-IMRT在近期有效率上有明顯優勢,治療頸段及胸上段食管癌,SIB-IMRT組的1年、2年局部控制率提高,具有統計學差異,但生存率未達到統計學意義,且放射性肺炎、放射性食管炎的發生率降低[13],與本研究結果相似。但也有報道局部晚期食管癌同步加量照射與選擇淋巴引流照射療效及毒副反應相近[14]。本研究中顯示SIB-IMRT組雖緩解率高于序貫組,但無統計學差異,兩組患者6個月及1年生存率、中位生存期無明顯差別,可能與研究中樣本數目較少且含有胸下段食管癌患者有關,應在已證實SIB-IMRT在食管癌治療方面的安全性及有效性后,加大樣本數量進一步證實。
雖然同期推量放射治療治療食管癌在近期有效率及中位生存期方面無明顯差異,但其放射性肺炎發生率明顯降低,安全可靠,有效改善患者生活質量,且治療時間縮短,可作為今后食管癌放射治療的首選方案。

