慢加急性乙型肝炎肝衰竭患者發生感染和急性腎損傷危險因素分析*
陳丹丹,龍志達,黃順東,王文虎,尹明紅,李忠斌
肝功能衰竭是多種因素引起的嚴重肝臟損害導致其合成、解毒、排泄和生物轉化等功能嚴重障礙或失代償,出現以凝血機制障礙、黃疸、腹水和肝性腦病等為主要表現的一組臨床癥候群。根據組織病理學特征和病情發展速度,肝衰竭被分為急性肝衰竭、亞急性肝衰竭、慢加急性肝衰竭(acute-on-chronic liver failure,ACLF)和慢性肝衰竭。在我國,以ACLF最為常見,它是指在慢性肝病的基礎上,在急性損傷因素作用下短期內肝臟功能急劇惡化并出現肝衰竭。由于ACLF的發病機制尚未十分明確,無特異有效的治療藥物,使其治療成為世界性的難題,病死率很高。對ACLF患者的預后判斷一直是臨床研究的熱點問題,準確的預后判斷對于指導治療至關重要。慢加急性乙型肝炎肝衰竭(acute-on-chronic hepatitis B liver failure,HBV-ACLF)患者以出現極度乏力、高膽紅素血癥、凝血功能障礙和腹水為特征,可出現各組織器官嚴重感染或出血,致死率極高,嚴重威脅患者的生命健康[1]。研究表明,并發各組織器官感染和急性腎損傷(acute kidney injury,AKI)是導致ACLF患者預后不良和病死率居高不下的主要原因[2]。本研究探討了HBV-ACLF 患者發生感染和AKI的危險因素,現報道如下。
1 資料與方法
1.1 臨床資料 2017年9月~2019年9月我院診治的HBV-ACLF患者102例,男67例,女35例,年齡為35~61歲,平均年齡為(49.0±5.5)歲。符合中華醫學會發布的《慢性乙型肝炎防治指南》[3]和《肝衰竭診治指南(2012年版)》[4]的診斷標準,在慢性肝病的基礎上,短期內發生急性或亞急性肝功能失代償的臨床癥候群,患者表現為①極度乏力,存在嚴重的消化道癥狀;②血清總膽紅素(total bilirubin,TBIL)明顯升高,每日上升≥17.1 μmol/L;③存在明顯的出血傾向;④伴有失代償性腹水;⑤伴有或不伴有肝性腦病。參照文獻報道的標準診斷AKI[5]:①48 h內血清肌酐上升26.5 μmol/L;②已知或假定腎功能損害發生在7 d之內,血清肌酐上升至基礎值的1.5倍以上;③尿量<0.5 ml/kg/h,且持續6 h。排除標準:合并其他嗜肝病毒感染、其他肝病、惡性腫瘤和嚴重腹部外傷史。
1.2 檢測 采用PCR法檢測HBV DNA(深圳凱杰生物工程有限公司試劑和美國ABI公司生產的ABI7500全自動實時熒光定量PCR儀);使用美國貝克曼庫爾特有限公司生產的AU5800全自動生化分析儀檢測血生化指標;使用德國BE公司生產的血凝分析儀檢測凝血酶原時間(prothrombin time,PT),自動計算國際標準化比值(international normalized ratio,INR)ISI。
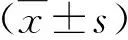
2 結果
2.1 兩組一般資料的比較 在治療觀察的90 d內,本組病例發生感染48例(47.1%);感染組在住院日≥15 d、存在侵入性操作、合并上消化出血、腹水、肝性腦病和糖尿病的比率顯著高于未感染組,感染組血清膽紅素水平和MELD評分顯著高于,而血清白蛋白水平顯著低于未感染組(P<0.05,表1)。

表1 兩組一般資料比較
2.2 HBV-ACLF患者合并感染的Logistic多因素回歸分析 分析發現,住院日長、侵入性操作、上消化道出血和肝性腦病是HBV-ACLF患者發生感染的獨立影響因素(P<0.05,表2)。

表2 HBV- ACLF患者合并感染的Logistic多因素回歸分析
2.3 HBV-ACLF患者發生AKI的危險因素分析 本組32例發生AKI。腎損傷組合并糖尿病和上消化道出血的比率顯著高于非腎損傷組,血清膽紅素、INR和MELD評分顯著高于非腎損傷組(資料未列出,P<0.05)。多因素分析顯示合并糖尿病和上消化道出血是影響HBV-ACLF患者并發AKI的危險因素(P<0.05,表3)。

表3 HBV-ACLF患者并發AKI的Logistic多因素回歸分析
3 討論
由乙型肝炎導致的ACLF是指慢性乙型肝炎患者在急性誘因的作用下突發急性肝衰竭,其主要發病基礎是急性因子作用于慢性肝病誘發肝衰竭。急性誘因包括感染性因素和非感染性因素。肝衰竭患者并發感染易出現感染性休克、彌散性血管內凝血、多器官功能衰竭等,往往病情嚴重,多預后不良[6,7]。此外,研究表明,AKI是HBV-ACLF患者合并器官損傷的主要類型之一,且與其存在感染密切相關[8,9]。為探討HBV-ACLF患者感染和AKI發生的原因及其相互影響,我們開展了本研究。
本研究結果顯示,住院天數≥15 d、進行了侵入性操作、并發上消化道出血和肝性腦病是HBV-ACLF患者發生感染的獨立影響因素,說明住院時間過長、侵入性操作等會增加患者感染的危險性。究其原因,我們認為可能是醫院存在各種致病菌,患者長期處于醫院的環境下,暴露于致病菌的時間過長,會增加其感染發生的風險[10];其次,肝性腦病患者多存在機體全身性炎癥反應,其肝細胞大量壞死、消化系統如腸道黏膜屏障功能受損,機體防御能力下降,且受患者吞咽和咳嗽等的影響,使口腔及其他部位的致病菌大量繁殖,繼而引發感染[11]。上消化道出血患者內環境紊亂,身體狀況較差,且出血會導致患者血液免疫物質減少、丟失,使其免疫功能下降[12]。此外,侵入性操作已是較多報道明確證實的引發感染的危險因素[13,14],侵入性操作會破壞機體與外界的屏障,有利于病菌入侵。故而可通過減少或縮短侵入性操作時間、預防上消化道出血和肝性腦病等降低患者出現感染的危險性。相關研究指出,MELD評分也與HBV-ACLF患者并發感染有關[15]。感染與未感染患者MELD評分差異顯著,MELD評分太高的患者顯然病情更重,更容易存在感染。
研究表明,AKI是一種涉及多學科的臨床常見危重癥,由多種病因造成腎功能在短期內急性減退[16]。AKI患者腎小管上皮細胞發生損傷、壞死,釋放大量促炎癥因子,破壞機體內環境穩態,使機體免疫功能降低,而影響患者預后[17]。故而分析導致AKI發生的危險因素,并給予合理的干預,或可起到改善預后的作用。本研究結果顯示,合并糖尿病和上消化道出血是HBV-ACLF患者并發AKI的獨立影響因素,提示可通過合理干預和預防上消化道出血,控制血糖水平等降低患者出現AKI的危險性。在糖尿病患者,由于血糖水平高,其體內糖基化蛋白會對腎臟造成損傷,降低腎小球濾過率,損傷腎小球基底膜,進而可導致AKI的發生,嚴重時可并發糖尿病腎病[18]。并發上消化道出血的患者肝功能損傷,肝臟解毒能力降低,導致內毒素和炎癥因子進入體循環,可使腎小管周圍毛細血管壁纖維蛋白沉著,且出血致機體有效循環血量降低,腎血流量灌注不足,導致腎灌注損傷[19]。相關研究指出,HBV-ACLF患者并發AKI的發病機制可能與消化道出血有關,患者血流動力學變化會激活腎素血管緊張素醛固醇系統和交感神經系統,分泌各種血管活性因子,進而可引起腎血管廣泛收縮和鈉水潴留,從而導致AKI的發生[20]。
綜上所述,住院天數≥15 d、進行了侵入性操作或多次操作、并發上消化道出血和肝性腦病是HBV-ACLF患者發生感染的獨立危險因素,合并存在糖尿病或并發上消化道出血是影響HBV-ACLF患者并發AKI的危險因素。了解這些特征,及時進行有效的干預,對改善預后非常重要。本研究不足之處在于對感染未分層,感染的部位和程度不同,可能影響臨床結局。嚴重的感染,如腹腔和肺部感染,可能造成內毒素血癥和后續的連鎖反應,從而導致腎損傷或多器官功能衰竭。一些未感染患者的判斷也比較主觀,臨床也缺乏準確判斷感染與非感染的界限。血清降鈣素原(PCT)、C-反應蛋白(CRP)和外周血白細胞等可以幫助判斷感染征象,血培養或其他標本培養,可以幫助了解致病菌,指導臨床治療。

