HPLC法同時測定參蓮顆粒中三種姜黃素的含量
張小折 葉曉婭

【摘 要】 目的:建立參蓮顆粒中姜黃素、去甲氧基姜黃素、雙去甲氧基姜黃素的含量測定方法。方法:色譜柱,Agilent SB-C18色譜柱(4.6 mm×250 mm,5 μm),流動相甲醇-3%冰醋酸(35∶65,v/v);流速1.0 mL·min-1;柱溫30℃,檢測波長418 nm,進樣量:10 μL。結果:參蓮顆粒中姜黃素、去甲氧基姜黃素、雙去甲氧基姜黃素的進樣質量分別在39.17 ~1530.0 ng(r=0.999 9)、48.90~1910.0 ng(r=1.000 0)、44.65~1744.0 ng(r=1.000 0)范圍內線性良好,平均回收率分別為97.86%(RSD=1.01%)、95.46%(RSD=1.07%)和99.69%(RSD=0.46%)。結論:該方法經方法學驗證具有操作簡單、分析速度快,準確度高的優點,可以用于參蓮顆粒中三種姜黃素類成分的含量測定。
【關鍵詞】 參蓮顆粒;姜黃素;高效液相色譜;含量測定;質量控制
【中圖分類號】R284.1 【文獻標志碼】 A 【文章編號】1007-8517(2021)15-0023-04
Abstract:Objective To propose as method for determination of curcumin, demethoxycurcumin and bisdemethoxycurcumin in Shenlian granules by HPLC method. Methods The Agilent-C18 (4.6 mm×250 mm, 5 μm) chromatography column was performed for separation with methanol(A)–3% HAc(B) as the mobile phase (35∶65, V/V). The flow rate was 1.0 mL·min-1, detection wavelength was set at 412 nm, column temperature was maintained at 30℃ and the injection volume was 10 μL. Results The curcumin, demethoxycurcumin, and bisdemethoxycurcumin had good linearity with the range of 39.17 ~1530.0 ng(r=0.999 9), 48.90~1910.0 ng(r=1.000 0) and 44.65~1744.0 ng(r=1.000 0), respectively. The average recoveries were 97.86%(RSD=1.01%), 95.46%(RSD=1.07%) and 99.69%(RSD=0.46%), respectively. Conclusion The established method was verified by methodology which has a good advantage of simple operation, analysis rapidly and high accuracy which can be used for the determination of curcumin, demethoxycurcumin, and bisdemethoxycurcumin in Shenlian granules by HPLC.
Keywords:Shenlian Granules; Curcumin; HPLC; Content Determination; Quality Control
參蓮顆粒是由苦參、山豆根、防己、三棱、莪術、丹參、補骨脂、苦杏仁、烏梅和白扁豆等七位藥組成,具有活血化瘀、清熱解毒和軟堅散結的作用,臨床主要用于氣血瘀滯、熱毒內阻而導致的中晚期肺癌和胃癌病患者[1]。方中三棱具有消積止痛、破血行氣的作用[2],莪術具有行氣破血、消積止痛的功效[3],二者合用共同為方中君藥,有報道[4-5]稱莪術的主要成分為姜黃素類和揮發油,姜黃素類是其主要活性成分,主要有姜黃素、去甲氧基姜黃素、雙去甲氧基姜黃素[6-7],這三種化合物結構相似,均具有抗動脈粥樣硬化、抗癌、抗氧化、抗誘變和清除自由基的作用[8-10],且有報道稱去甲氧基姜黃素可以抑制TPA (12—O—tetradecanoyl phorbol—13-acetate)引起的癌細胞增生以及多種癌細胞[11],作用大于其它兩種姜黃素類,由于參蓮顆粒主要是治療癌癥等癥狀,根據劉昌孝院士提出的中藥質量標志物(Q-Marker)[12]的概念,把能夠作為與中藥功能主治和反映藥品安全性和有效性的活性成分作為中藥質量標志物從而對其進行質量控制。因此姜黃素類成分是其抗癌作用的有效活性成分,目前標準中未有對其進行控制,鑒于此本實驗參考莪術以及含有姜黃類成分的中成藥[13-15]建立參蓮顆粒中姜黃素、去甲氧基姜黃素、雙去甲氧基姜黃素三種成分的含量測定,從而為改進和提高參蓮顆粒的質量標準提供實驗參考。
1 儀器與試藥
1.1 儀器 高效液相色譜儀Waters e2695(美國Waters儀器公司);Empower 3 工作站;XPE204型十萬分之一電子天平(瑞士Mettler ToleDo儀器公司);KQ-500DE型雙頻數控超聲波清洗器(江蘇昆山超聲儀器有限公司)。Mili-Q超純水機(美國密理博公司)。
1.2 試藥 參蓮顆粒是由市場所購,規格:4.5 g/袋);批號分別標記為1#、2#和3#,20180516,20190706,對照品:姜黃素(批號:110823-201706,含量98.9%),去甲氧基姜黃素(批號:112003-201501,含量98.5%、雙去甲氧基姜黃素(批號:112004-201501,含量95.0%),對照品購于中國食品藥品檢定研究院,甲醇為色譜純(美國Merck公司),冰醋酸為分析純(天津科密歐化學試劑公司),水為超純水。
2 方法與結果
2.1 色譜條件 色譜柱:Agilent SB-C18色譜柱(4.6 mm×250 mm,5 μm),流動相:(A)甲醇-3%冰醋酸(35∶65,v/v);流速1.0 mL·min-1;檢測波長418 nm,柱溫30 ℃,進樣量:10 μL。
2.2 對照品溶液的配制 精密稱取用五氧化二磷干燥12h后的姜黃素5.36 mg、去甲氧基姜黃素6.12 mg、雙去甲氧基姜黃素5.58 mg分別置3個25 mL容量瓶中,加甲醇定容稀釋至刻度,分別作為對照品儲備溶液,然后分別精密吸取上述姜黃素對照品儲備溶液2 mL,去甲氧基姜黃素和雙去甲氧基姜黃素各1 mL置同一20 mL容量瓶中,加甲醇溶解并稀釋至刻度,作為對照品混合溶液(每1 mL含姜黃素21.44 μg、去甲氧基姜黃素12.24 μg、雙去甲氧基姜黃素11.16 μg)。
2.3 供試品溶液的配制 取批號為1#的參蓮靈顆粉末約5.0 g,精密稱定,平行制備2份樣品,然后精密加入甲醇25 mL,稱定重量,然后超聲(頻率40 kHz,功率300 W)處理30 min,用甲醇補足減失的重量,搖勻,用¢0.45 μm的微孔濾膜濾過,取續濾液作為供試品溶液。
2.4 陰性樣品的制備 按照參蓮顆粒的質量標準處方量及制備工藝,分別制備缺莪術、三棱藥材的陰性樣品,作為缺莪術、三棱的參蓮陰性樣品溶液。
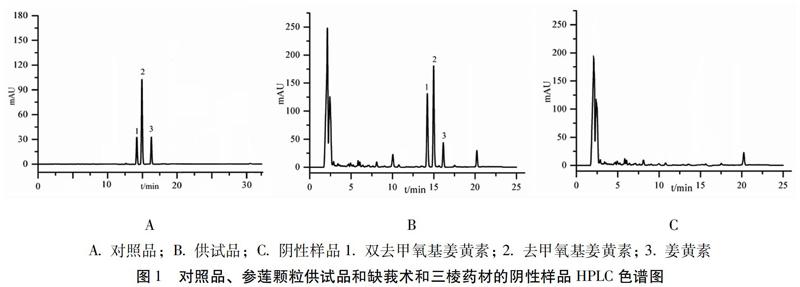
2.5 專屬性實驗 按照“2.1”項的色譜條件,分別取上述對照品和供試品溶液和陰性樣品溶液進行測定,記錄色譜圖,結果發現陰性樣品對姜黃素、去甲氧基姜黃素、雙去甲氧基姜黃素的測定無干擾。理論塔板數按姜黃素峰計算不低于5000,分離度均大于1.5,色譜圖如圖1所示。
2.6 線性關系的考察 精密稱取姜黃素7.65 mg、去甲氧基姜黃素9.55 mg、雙去甲氧基姜黃素8.72 mg分別置同一50 mL容量瓶中,加甲醇稀釋至刻度,作為V號對照品混合溶液,然后采用逐級稀釋法,精密吸取V號對照品溶液2 mL置5 mL量瓶中,加甲醇稀釋至刻度,作為IV號對照品溶液,精密吸取上述IV號對照品溶液2 mL置5 mL量瓶中,加甲醇稀釋至刻度,作為III號對照品溶液,精密吸取上述III號對照品溶液2 mL置5 mL量瓶中,加甲醇稀釋至刻度,作為II號對照品溶液,精密吸取II號對照品溶液2 mL置5 mL量瓶中,加甲醇稀釋至刻度,作為I號對照品溶液,分別吸取上述I~V號對照品溶液各10 μL,按照“2.1”項下的液相色譜條件進行測定,橫坐標(X)為進樣量的質量(ng),其相對應的峰面積(Y)為縱坐標,繪制標準工作曲線,進行線性回歸,結果三種成分的線性方程如下:姜黃素Y=0.901 1X–3.072 3,r=0.999 9,線性范圍為39.17~1530.0 ng;去甲氧基姜黃素Y=0.725 8X-1.108 2,r=1.000 0,線性范圍為48.90~1910.0 ng;雙去甲氧基姜黃素Y=0.561 9X+2.612 8,r=1.000 0,線性范圍為44.65~1744.0 ng。
2.7 精密度試驗 分別取“2.6”項下的I號、III號和V號三個不同濃度的對照品溶液,按照“2.1”項下的色譜條件各連續進樣6次,進樣量10 μL,結果I號對照品中姜黃素、去甲氧基姜黃素、雙去甲氧基姜黃素峰面積的RSD分別為1.98%、2.16%、和2.33%;III號對照品中各色譜峰面積的RSD為0.96%、1.12%、和1.07%;V號對照品中各色譜峰面積的RSD為0.35%、0.26%、和0.39%,結果說明該儀器的進樣精密度良好。
2.8 穩定性試驗 取“2.3”項下的供試品溶液,按照“2.1”項下的液相色譜條件,分別在0、1、2、4、8、12、24 h進行測定,連續考察24 h,記錄各個時間的色譜峰面積,結果姜黃素峰面積的RSD分別為2.39%、去甲氧基姜黃素峰面積的RSD為2.72%、雙去甲氧基姜黃素峰面積的RSD為2.96%,結果表明該參蓮顆粒供試品溶液在24 h內穩定性良好。
2.9 重復性試驗 取同一批號1#的參蓮顆粒,研細,按照“2.3”項下的制備方法平行制備6份供試品溶液,按照“2.1”項下的液相色譜條件進行測定,結果參蓮顆粒中姜黃素、去甲氧基姜黃素、雙去甲氧基姜黃素含量平均值為3.66 μg·g-1、12.45 μg·g-1和2.78 μg·g-1,RSD分別為0.86%、1.35%和0.79%,測定結果說明該方法的重復性良好。
2.10 中間精密度試驗 在相同實驗室,由不同操作者在不同時間、不同儀器,采用上述色譜條件和供試品溶液制備方法對同一批號的參蓮顆粒進行測定,結果與重復性項下對比,兩位操作者所測值得RSD均小于2.0%,因此表明該方法的中間精密度良好。
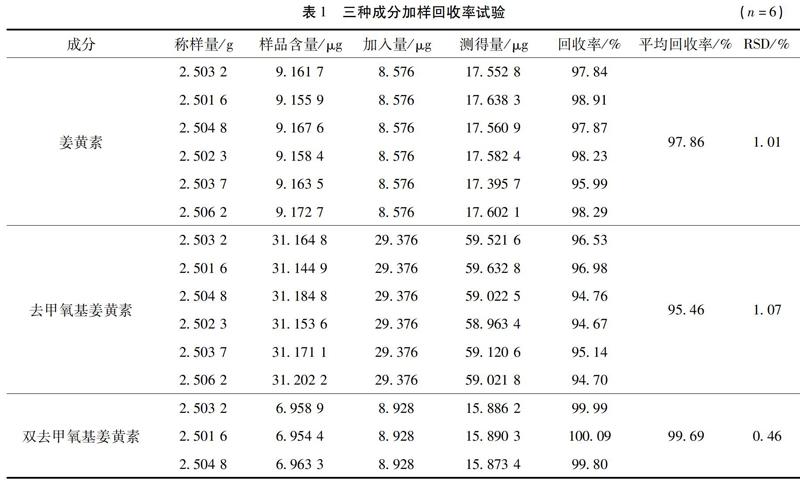
2.11 加樣回收率試驗 精密吸取“2.2”項下的1 mL、姜黃素對照品儲備溶液、去甲氧基姜黃素3 mL、雙去甲氧基姜黃素1 mL置同一25 mL量瓶中,作為待加混合對照品溶液,然后精密稱取已知含量的參蓮顆粒2.5 g置三角錐形瓶中,共6份,分別加入上述待加混合對照品溶液各1 mL,然后按照“2.3”項下的制備方法制備樣品溶液,“2.1”項下的液相色譜條件進行測定,分別計算姜黃素、去甲氧基姜黃素、雙去甲氧基姜黃素的回收率,測定結果見表1。
2.12 樣品的測定 取上述市場所購買的3批樣品,按照“2.3項”下方法制備供試品溶液,按“2.1”項下的液相色譜條件進行測定,采用外標法計算測定結果。見表2。
3 討論
3.1 供試品溶液的制備 供試品溶液的提取溶劑分別考察采用甲醇、50%甲醇和乙醇,結果發現甲醇作為提取溶劑時姜黃素、去甲氧基姜黃素、雙去甲氧基姜黃素三者含量最高,因此采用甲醇作為提取溶劑,接著考察回流、超聲、索氏提取三種方法,結果發現三種提取方法時含量基本一致,無明顯差異,由于超聲操作簡單,故選擇超聲作為提取方法。然后對時間(20 min、30 min、40 min)、超聲功率(200 W、350 W、500 W)進行考察,結果發現當超聲30 min,功率350 W為最佳提取工藝,因此選擇該方法為供試品溶液的制備方法。
3.2 測定條件的選擇 實驗首先采用文獻報道的270 nm作為檢測波長,結果發現三者色譜峰干擾較大,分不開且基線不平穩,然后采用DAD檢測器進行檢測,發現姜黃素的最大吸收波長為420 nm,去甲氧基姜黃素的最大吸收波長為418 nm、雙去甲氧基姜黃素的最大吸收波長為416 nm,由于三者中去甲氧基姜黃素的色譜峰較大,綜合考慮,選擇418 nm作為三者檢測波長,結果發現三者色譜峰形良好,沒有干擾,且可以很好的分離。流動相的選擇先后采用甲醇—3%醋酸、乙腈—0.1%磷酸緩沖溶液、乙腈—水三者作為流動相,結果發現當甲醇—3%醋酸時三者峰形較好,分離度較高,因此選擇甲醇—3%醋酸溶液作為流動相。
3.3 耐用性試驗 本實驗分別對不同柱溫(20 ℃、25 ℃、30 ℃、35 ℃、40 ℃);不同流速(0.8 mL/min、0.9 mL/min、1.0 mL/min、1.1 mL/min、1.2 mL/min);不同流動性比例:甲醇—3%冰醋酸(31∶69)、(33∶67)(35∶65)(37∶63)(39∶61);不同檢測波長(414 nm、416 nm、418 nm、420 nm和422 nm);不同色譜柱:Agilent SB-C18(250 mm×4.6 mm, 5 μm)、Waters Symmetry C18(250 mm×4.6 mm, 5 μm)和島津Shim-Pack VP-ODS液相色譜柱(250mm×4.6 mm, 5 μm),各種條件微小變動下,系統適用性均符合要求,同時分別采用Agilent1260.Waters2695和島津LC-2030液相色譜儀對同一批樣品測定,結果三者測定值RSD<1.5%,因此該方法的耐用性良好。
4 結論
本實驗對參蓮顆粒中具有藥理活性的指標性成分進行檢測,在實驗中發現姜黃和三棱均含有上述三種姜黃素成分,因此上述三個成分為兩種藥材的含量之和,且建立的同時測定參蓮顆粒中姜黃素、去甲氧基姜黃素、雙去甲氧基姜黃素的含量HPLC法,具有分析速度快、靈敏度高、專屬性強的優點,可以為該標準中三棱和莪術的質量控制提供一定的依據。
參考文獻
[1]陳桂紅,黃清松,曾繁濤.參蓮顆粒抗突變和抑瘤作用研究[J].中國藥房,2007,18(36):2809-2811.
[2]國家藥典委員會.中華人民共和國藥典(一部)[S].北京:中國醫藥科技出版社,2015:31.
[3]陳曉軍,韋潔,蘇華,等.莪術藥理作用的研究新進展[J].藥學研究,2018,37(11):49-53,67.
[4]賴艷妮,嚴一文,徐培平,等.基于系統藥理學探索莪術有效成分的藥理作用機制[J].中國實驗方劑學雜志,2017,23(14):185-190.
[5]馮婭茹,張文婷,李二文,等.三棱化學成分及藥理作用研究進展[J].中草藥,2017,48(22):4804-4818.
[6]崔語涵,安瀟,王海峰,等.姜黃化學成分研究[J].中草藥,2016,47(7):1074-1078.
[7]趙承光,梁廣,邵麗麗,等.姜黃素類化合物抗炎和細胞保護作用的構效關系研究進展[J].中草藥,2008,39(4):619-622.
[8]王玉玲,吳振,張喜軒.姜黃素類化合物的抗腫瘤活性[J].中國醫科大學學報,2006,35(4):380-381.
[9]吳杰,李丹,沈秉正,等.姜黃素類化合物的藥理活性研究進展[J].中國藥師,2013,16(12):1918-1920.
[10]姜黃素類化合物的提取分離鑒定及其與化療藥的協同抗腫瘤作用研究[D].煙臺:煙臺大學,2009.
[11]苗久旺,荊雪寧,高熒,等.自噬對雙去甲氧基姜黃素誘導肝癌HepG2細胞凋亡作用的影響[J].中國實驗方劑學雜志,2018,24(17):167-171.
[12]劉昌孝,陳士林,肖小河,等.中藥質量標志物(Q-Marker):中藥產品質量控制的新概念[J].中草藥,2016,47(9):1443-1457.
[13]史晶晶,馮素香,郝蕊,等.姜黃提取物中姜黃素、去甲氧基姜黃素、雙去甲氧基姜黃素的含量測定[J].中醫學報,2015,30(6):853-855.
[14]李文兵,盧君蓉,胡麟,等.一測多評法測定姜黃中姜黃素、去甲氧基姜黃素和雙去甲氧基姜黃素[J].中草藥,2017,48(3):573-577.
[15]孫靜,孫艷濤,張振秋.中藥莪術中姜黃素、去甲氧基姜黃素、雙去甲氧基姜黃素的含量測定[J].中國醫院藥學雜志,2010,30(8):714-716.
(收稿日期:2020-12-24 編輯:程鵬飛)

