司庫奇尤單抗治療紅皮病型銀屑病一例并文獻復習
朱慧英 施仲香 曹 楠 田洪青 杜東紅
1山東第一醫(yī)科大學(山東省醫(yī)學科學院),濟南,250002;2山東第一醫(yī)科大學附屬皮膚病醫(yī)院(山東省皮膚病醫(yī)院,山東省皮膚病性病防治研究所),濟南,250022
紅皮病型銀屑病(EP)是一種少見的炎癥型銀屑病,影響大部分體表面積(超過75%),可能會導致電解質異常、膜外液體及營養(yǎng)流失、體溫調節(jié)受損和潛在感染等并發(fā)癥,甚至會導致死亡。雖然生物制劑治療中重度斑塊型銀屑病的有效性和安全性已經得到了充分的證明,但關于其應用于紅皮病型銀屑病的報道較少。近年來,國外有超適應癥應用司庫奇尤單抗治療紅皮病型銀屑病的病例報道,且取得了較好的療效,而在國內報道較少。現(xiàn)報道1例司庫奇尤單抗治療紅皮病型銀屑病并對既往文獻進行復習。
1 臨床資料
患者,男,41歲。因“全身鱗屑性斑塊18年,加重半個月伴發(fā)熱”來我院就診,門診擬“紅皮病型銀屑病”第18次收入院。患者18年前無明顯誘因全身出現(xiàn)散在紅斑伴鱗屑,于當?shù)蒯t(yī)院診斷為“尋常型銀屑病”,給予口服及外用藥物(具體不詳)治療后緩解。此后病情逐漸加重,波及全身。于2007年以“紅皮病型銀屑病”第1次在我院住院治療,當時給予靜滴甲氨蝶呤(累積量70 mg)、UVB照射,輔以甘油浴、外用尿素乳膏治療,皮疹好轉出院。此后皮疹反復發(fā)作,先后16次以“紅皮病型銀屑病”在我院住院治療,系統(tǒng)給予甲氨蝶呤(累積量580 mg)、環(huán)孢素、白芍總苷等藥物,照射UVB,藥浴及外用藥物治療,治療有效,但病情反復。半個月前無明顯誘因皮疹加重,伴發(fā)熱,體溫最高至40.2℃。既往無其他病史,系統(tǒng)查體未見明顯異常。皮膚科情況:周身皮膚潮紅,呈彌漫性紅色斑片,表面覆以大量糠狀鱗屑,頭皮呈彌漫性暗紅色斑,見束狀發(fā),皮疹累及面積達100%(圖1)。無溝狀舌,雙手足指(趾)甲板增厚,可見點狀凹陷、縱嵴、橫溝,油滴狀改變。輔助檢查:血常規(guī)、血沉、肝腎脂糖肌酶、電解質、心電圖、胸部正側位片、腹部超聲未見明顯異常,乙肝五項(-),ANA+ds-DNA(-),T-SPOT(-),免疫球蛋白IgE:4240.9 KU/L。在排除肝炎、結核的基礎上,經知情同意后,患者接受司庫奇尤單抗標準治療方案:0~4周每周皮下注射300 mg,隨后每4周注射300 mg。共治療4個月(0~4周,第8周,第12周,第16周),共8次。在第4周達到PASI 75,全身彌漫性紅斑減退,顏色變暗,浸潤減輕,脫屑減少,第8周達到PASI 100,皮疹完全清除(圖2),隨訪32周,未見明顯復發(fā)和不良反應。
2 討論
紅皮病型銀屑病(EP)是一種少見、嚴重的銀屑病類型,約占銀屑病患者的1%~2.25%[1,2]。表現(xiàn)為全身皮膚(>75%[1,3,4])彌漫性潮紅、浸潤腫脹并伴有大量糠狀鱗屑,可伴有發(fā)熱、淺表淋巴結腫大等全身癥狀,是紅皮病最常見的原因(約占紅皮病的25%)[2,5]。治療中斷、感染、精神壓力是其常見的觸發(fā)因素[1-3,6]。由于發(fā)病率低,且急性發(fā)作性EP通常需要立即干預,缺少對照臨床研究,難以獲得基于高等級臨床證據支持的標準化治療方案,通常基于臨床經驗和坊間證據進行治療[1-3]。傳統(tǒng)治療包括系統(tǒng)應用阿維A、環(huán)孢素、甲氨蝶呤,外用糖皮質激素軟膏、維A酸制劑、維生素D3衍生物,以及紫外線光療、中醫(yī)治療等,多數(shù)患者能獲得緩解,但也有傳統(tǒng)治療效果不理想或患者不能耐受者。
銀屑病是一種慢性免疫性炎癥性系統(tǒng)性疾病,其病因和發(fā)病機制復雜,由多種免疫炎癥細胞及其產生的眾多細胞因子交互作用的網絡主導,其中IL-17系該網絡中的關鍵節(jié)點之一[7]。紅皮病型銀屑病(EP)作為銀屑病的類型之一,其確切發(fā)病機制尚不完全清楚,但它被認為涉及Th1、Th2和Th17炎癥通路的復雜相互作用[5]。近年來認為Th17細胞及IL-23/IL-17軸在銀屑病發(fā)病機制中可能處于處于關鍵地位,并成為新的治療靶標[8]。其中IL-17通過刺激角質形成細胞、樹突狀細胞(DCs)和其他免疫細胞產生幾種促炎細胞因子(如TNFα)和趨化因子,在T細胞激活部位招募中性粒細胞和單核細胞,在炎癥過程中發(fā)揮關鍵作用。Carrasquillo等[4]認為IL-17抑制劑似乎是一種很有前途的治療EP的生物制劑類別,根據其證據水平,也可以被認為是一線治療。IL-17家族現(xiàn)有6個成員:IL-17A、IL-17B、IL-17C、IL-17D、IL-17E(又稱IL-25)和IL-17F,其中IL-17A于1993年首次在人類外周血中被發(fā)現(xiàn),被認為是銀屑病發(fā)病過程中促炎細胞因子的關鍵“驅動因素”,因為它可以激活角質形成細胞并促進過度增殖,似乎是IL-17家族中最有效的細胞因子,也是研究最多的亞型[2]。
目前用于銀屑病的生物制劑主要有TNF-α、IL-12/23、IL-17抑制劑,生物制劑主要通過阻斷上述反應軸中某個途徑來發(fā)揮作用,主要應用于中至重度斑塊型銀屑病,在EP治療中應用較少[5]。最近發(fā)表的文獻顯示,不同臨床亞型銀屑病中幾種促炎細胞因子的表達存在差異,IL-17A可能是EP的主要炎癥通路[9]。與此一致,慢性斑塊狀銀屑病與EP活檢的微陣列分析表明IL-17A是斑塊狀銀屑病和EP的主要共享通路。近年來,IL-23/Th17軸在銀屑病發(fā)病機制中的重要性導致了新的生物藥物的開發(fā)。抗IL-17藥物正迅速成為重要的治療工具。目前有三種靶向IL-17信號的藥物正在測試用于治療銀屑病的藥物包括兩種抗IL-17A藥物司庫奇尤單抗(secukinumab)和依奇珠單抗(ixekizumab),以及一種IL-17R拮抗劑布洛魯單抗(brodalumab)。司庫奇尤單抗是一種針對IL-17A的全人類單克隆IgG抗體,經FAD和EMA在2015年批準用于治療斑塊狀銀屑病、銀屑病關節(jié)炎和強直性脊柱炎[2]。司庫奇尤單抗是中國首個獲批的全人源IL-17A抑制劑,臨床反應與表皮增生減少、IL17產生細胞減少以及各種細胞因子和趨化因子(如IL17A、IL21、IL22、CCL20、KRT16和DEFB4)的基因表達相關[10]。目前關于司庫奇尤單抗應用于中重度斑塊狀銀屑病的療效與安全性不斷被證實,國外多項研究顯示,司庫奇尤單抗治療中重度斑塊狀銀屑病療效顯著,不良反應少。何江曼等[7]報告6例中重度斑塊狀銀屑病患者,應用司庫奇尤單抗第4周全部達到PASI 75,治療8周,全部患者達到PASI 100。近年來有文獻證實了司庫奇尤單抗應用于EP的有效性和安全性,也提示了IL-17A可能是EP發(fā)生的主導細胞因子[2-4,6,11-15],見表1。且有文獻報道對于傳統(tǒng)治療療效不好或不能耐受或有其他嚴重合并癥如終末期腎功能衰竭、嚴重肝脂肪變性等EP患者,司庫奇尤單抗是最有利的藥物[13,14]。本文患者此前應用多種傳統(tǒng)治療方案,但皮疹反復發(fā)作,先后18次來我院住院治療,病情頑固,應用司庫奇尤單抗4周達到PASI 75,8周達到PASI 100,隨訪32周未見明顯復發(fā)及不良事件,較既往司庫奇尤單抗治療EP的病例報道,我們達到PASI 75和PASI 100的時間較短。我們的經驗進一步支持了司庫奇尤單抗對紅皮病型銀屑病患者的有效性和安全性。
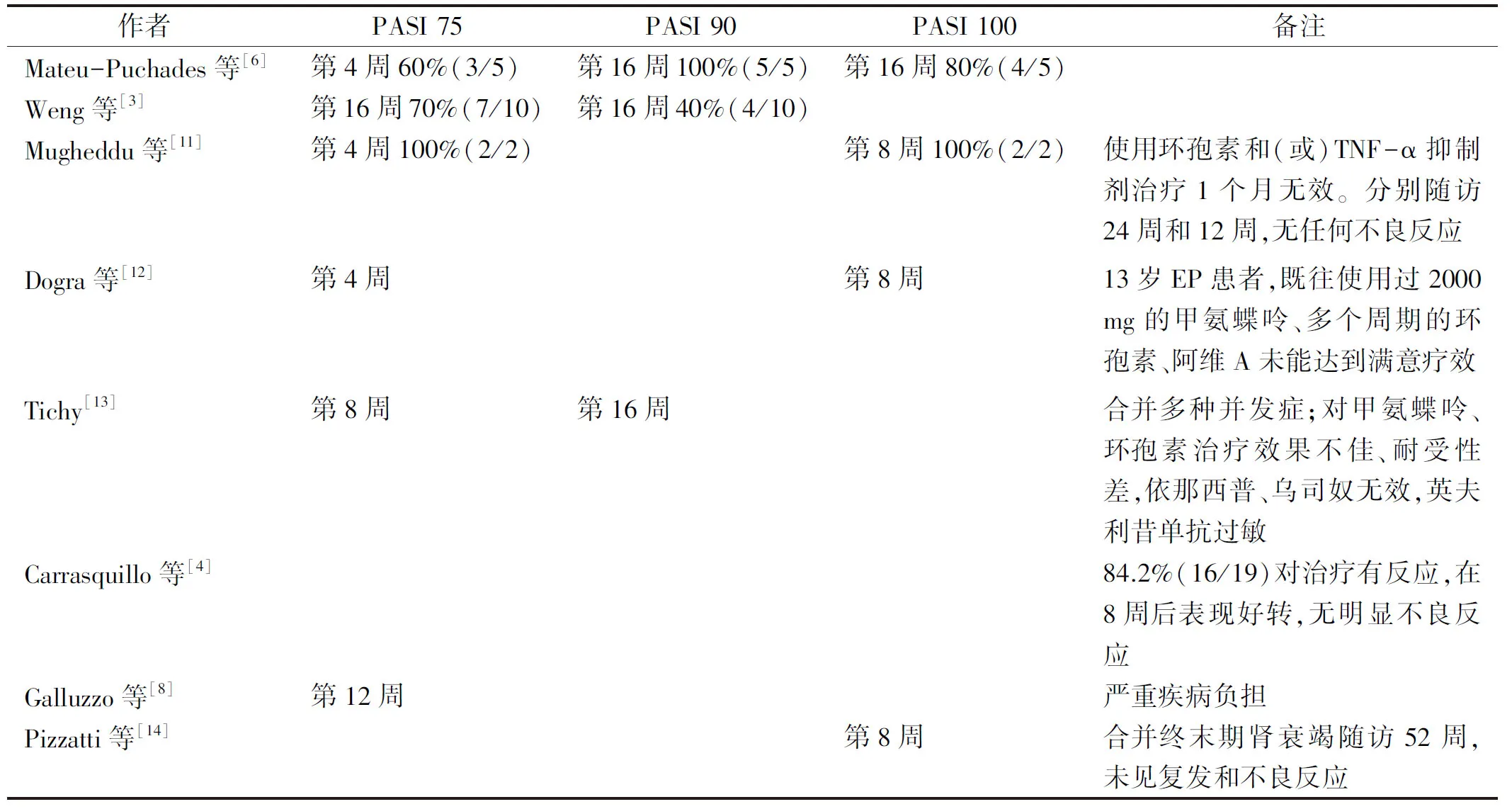
表1 司庫奇尤單抗治療紅皮病型銀屑病的相關文獻報道
綜上所述,盡管目前缺乏高質量的數(shù)據和研究,生物制劑治療紅皮病型銀屑病的長期療效還需要進一步的臨床研究,但越來越多的文獻證實了司庫奇尤單抗應用于EP的有效性和安全性,我們的經驗表明,司庫奇尤單抗對于紅皮病型銀屑病患者是一種有效的治療選擇。

