連續性腎臟替代治療急性腎功能衰竭療效及對T淋巴細胞炎癥因子和血清電解質水平的影響
韓瑞萍, 袁光新, 陳 慰, 蘇 清, 朱夢莉, 王智超
(1.湖北省武漢市第一醫院急診醫學科, 湖北 武漢 430000 2.泰康同濟(武漢)醫院重癥醫學科, 湖北 武漢 430033)
急性腎功能衰竭(Acute renal failure ARF)是臨床常見危重疾病之一,死亡率較高,可達10%~15%[1]。ARF患者多因嘔吐、呼吸急促等就診,可導致腎功能急速減弱,出現炎癥反應,降低免疫功能[2]。血液替代療法主要通過體外循環將各種代謝物質、異常血漿、藥物及毒素等進行有效清除,糾正內環境紊亂的技術,是臨床治療危重疾病常用方法,可有效改善患者臨床癥狀,但目前臨床對于治療過程中的用藥尚無統一規范,臨床用藥復雜,且治療周期長,因此采取科學有效的血液替代療法完成治療操作十分必要。間歇性血液透析(IHD)及連續性腎臟代替治療(CRRT)是臨床常用的兩種不同血液替代療法,其中IHD是治療ARF的主要手段,且在很長一段時間內取得了較好效果;而隨著科技的進步,CRRT因其安全性高,操作性強等特點逐步成為臨床首選方法。本次研究主要觀察兩種方式在ARF患者中的臨床療效,及其對T淋巴細胞、炎性因子及水電解質的影響,旨在為臨床提供更多的可行性方案,具體結果如下。
1 資料與方法
1.1一般資料
1.1.1研究對象:經醫學倫理委員會審批后,采用簡單隨機抽樣法將2019年6月至2020年6月在我院治療的161例ARF患者分為觀察組(n=81)與對照組(n=80)。兩組患者性別、年齡、原發病等一般臨床資料比較差異均無統計學意義(P>0.05),具有可比性,見表1。納入標準:①符合《腎臟病學》[3]中關于ARF的臨床診斷標準:腎小球濾率48h內突然下降,血肌酐絕對值增加≥0.3mg/dl(≥26.5μmoL/L),或在排出梗阻性腎病或脫水狀態下,超過6h以上時間尿量均<0.5mL·kg-1·h-1,B超可見腎體積增大、腎皮質增厚;②無凝血障礙,嚴重低血壓等,臨床治療依從性好;③知情且同意者。排除標準:①有嚴重低血壓,凝血功能障礙,惡性腫瘤者;②有腎移植手術史,或終末期腎病者;③參與其他研究或無法完成治療周期者;④嚴重過敏體質者。

表1 兩組患者一般資料臨床比較
1.2方 法
1.2.1治療方法:兩組患者均基于常規對癥治療,補充血容量,糾正水電解質紊亂,防感染,預防并發癥及營養支持等。觀察組患者在此基礎上給予IHD治療,具體如下:透析儀器為Prismaflex M100 set血液透析濾過器(法國 Gambro Industries 公司生產)和金寶透析機(Gambro Lundia AB 公司生產),超濾系數為40 mL /min,透過面積為1.3m2,4~5h/次,2~3次/周,每次透析液流量為500 mL /min,其中透析液為碳酸氫鹽溶液。觀察組患者采用CRRT治療,具體日下:選取患者頸內右側靜脈通過過 Seldinger技術進行雙腔導管留置(共72次)。其治療儀器設備為PRISMA機器、FH66D型血率器、FH55型濾器,置換液為Port配方,選取同步輸入模式,領單獨輸入碳酸氫鹽置換液。設定白天治療時間10~12h,輸入16~24L碳酸氫銨置換液,24h不間斷輸入Port配方液。注意檢查置管情況,透析過程中出現凝血則可根據重程度給予肝素或置換液沖洗濾器和管路,控制置管時間越長則效果越理想。
1.2.2指標檢測方法:于治療前、治療3個月后分別采集兩組患者空腹靜脈血樣,離心處理后置于-80℃冰箱,經流式細胞儀檢測兩組患者免疫功能指標(CD3+、CD4+、CD8+、CD4+/CD8+)水平。采用全自動生化儀測定兩組患者腎功能指標[血尿素氮(BUN)、血清肌酐(Scr)、內生肌酐清除率(Ccr)、β2微球蛋白(β2-MG)]及炎癥因子[白細胞介素-1(IL-1)、白細胞介素-6(IL-6)、白細胞介素-8(IL-8)及腫瘤壞死因子-α(TNF-α)]及血清電解質[鉀(K+)、鈉(Na+)、氯(Cl-)]水平。
1.3評定標準:顯效:各項指標恢復至正常標準;有效:治療后病情有所好轉,相關指標接近正常標準;無效:治療后病情無緩解或繼續惡化。臨床總有效=顯效+有效。
1.4觀察指標:比較兩組患者臨床療效,觀察治療前、治療3個月后兩組患者T淋巴細胞(CD3+、CD4+、CD8+、CD4+/CD8+)、炎癥因子(IL-1、IL-6、IL-8、TNF-α)、血清電解質(K+、Na+、Cl-)、腎功能指標(BUN、Scr、Ccr、β2-MG)變化情況。

2 結 果
2.1兩組患者臨床療效比較:治療3個月后,觀察組患者臨床總有效率為96.3%,明顯高于對照組的87.5%(P<0.05),見表2。

表2 兩組患者臨床療效比較n(%)
2.2兩組患者T淋巴細胞比較:治療3個月后,兩組患者CD3+、CD4+、CD4+/CD8+水平均高于治療前,CD8+水平均低于治療前,且兩組治療前后CD3+、CD4+、CD4+/CD8+、CD8+差值組間比較,差異具有統計學意義(P<0.05),見表3。
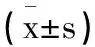
表3 兩組患者T淋巴細胞亞群比較
2.3兩組患者血清炎性因子水平比較:治療3個月后,兩組患者血清炎性因子IL-1、IL-6、IL-8、TNF-α水平均低于治療前,且兩組治療前后差值組間比較,差異具有統計學意義(P<0.05),見表4。

表4 兩組患者血清炎性因子比較
2.4兩組患者血清電解質水平比較:治療3個月后,兩組患者血清電解質K+、Na+、Cl-水平均低于治療前,且兩組治療前后差值組間比較,差異具有統計學意義(P<0.05),見表5。

表5 兩組患者血清電解質水平比較
2.5兩組患者腎功能指標比較:治療3個月后,兩組患者BUN、Scr、β2-MG水平均低于治療前,Ccr水平均高于治療前,且且兩組治療前后BUN、Scr、β2-MG、Ccr差值組間比較,差異具有統計學意義(P<0.05)見表6。
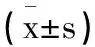
表6 兩組患者腎功能指標比較
3 討 論
ARF是腎內科常見危重疾病之一,其主要與患者機體腎小球濾過率急劇下降有關,發病后患者可出現突然嘔吐、呼吸急促、脫水、電解質紊亂等癥狀,造成腎功能衰竭,嚴重者還可危害患者生命安全,因此必須盡早治療。目前臨床多采用腎臟代替療法治療,IHD與CRRT均是臨床常用的腎臟代替療法,但有學者指出,IHD在治療過程中可導致ARF患者水、毒素處于高負荷狀態,加重血流動力學紊亂,引起低血壓等危害,損傷臟器功能,遠期治療效果并不十分理想[4]。
CRRT主要通過對流、彌散等方式對患者機體代謝物進行交換和清除,可持續代替已損傷的腎臟功能。本次研究結果顯示,觀察組患者臨床總有效率高于對照組,分析原因可能由于CRRT可持續、穩定代謝機體相關毒素,且不影響血流動力學及電解質水平有關。研究發現,CRRT可維持血流動力學、滲透壓穩定,具有減輕心血管不良事件的優勢[5]。嚴重感染是ARF發病的重要危險因素,可嚴重影響患者機體免疫力。有學者指出,外來抗原可降低機體T淋巴細胞等相關因子的分泌,導致免疫調節紊亂[6],本次研究結果顯示,治療3個月后,觀察組患者CD3+、CD4+、CD4+/CD8+水平均高于對照組;CD8+水平低于對照組。提示CRRT可較好改善患者免疫功能。分析原因可能是CRRT能連續、緩慢代謝患者體內毒素,降低炎性反應,重建免疫平衡有關。炎性因子的釋放是導致機體出現炎性聯級反應的主要原因之一,也是加重腎臟損傷的重要因素,對患者預后十分不利。研究報道,CRRT聯合血液灌流能有效改善ARF患者IL-1、IL-6、IL-8、TNF-α水平,減輕炎性反應,提高臨床療效[7]。另外,彭博[8]等研究認為,CRRT雖炎性介質的清除是沒有選擇性的部分清除。本次研究結果顯示,治療3個月后,兩組患者血清炎性因子IL-1、IL-6、IL-8、TNF-α水平均低于對照組,進一步證實CRRT在ARF中的抗炎效果。分析原因可能是CRRT能通過對流清除TNF-α,增加超濾速率,增加血清炎性因子清除效果。
急性ARF發病后可在短時間內出現腎功能急劇下降,導致電解質紊亂,大量代謝物質堆積,引起高血鉀癥等。CRRT治療疾病主要是代替腎臟將體內毒素等代謝物質進行有效代謝,維持機體內環境穩定[9]。本次研究結果顯示,觀察組患者血清電解質K+、Na+、Cl-水平均低于對照組。說明CRRT治療ARF可有效維持患者機體內環境穩定,分析原因推測一方面CRRT治療時,脫水速度慢,可維持血流動力學穩定,避免腎功能進一步損害;另一方面,CRRT幫助患者將體內多于水分緩慢排出,保證血管、細胞內外滲透壓處于平衡穩定狀態,維持酸堿平衡。
BUN、Scr是反應ARF患者腎臟損傷程度的重要指標。但腎臟代謝能力強,早期BUN、Scr水平變化并不十分明顯,且容易受到體重、尿量等多種因素的影響,導致其敏感性相對較低。β2-MG是近年來認為可有效反應早期腎損傷的敏感指標[10]。周爽[11]研究顯示,血液凈化可促進ARF患者腎功能恢復,提高臨床生存率。本次研究結果顯示,觀察組患者BUN、Scr、β2-MG水平均低于對照組,Ccr水平高于對照組。說明CRRT可有效改善ARF患者腎功能。分析原因為CRRT可長期平穩將體內毒素代謝出去,可維持血流動力學、電解質穩定,減少容量波動,加速BUN、Scr等清除速率,改善患者預后。
綜上所述,CRRT治療ARF患者效果顯著,可降低患者炎性水平,調節電解質平衡,提高機體免疫力,改善腎功能。

