Na離子修飾的Au/HZSM-5催化劑的制備、表征及催化合成氣羰基化反應性能
方亞平迪麗努爾艾力高希然畢坤豪馬鳳云艾沙努拉洪
(新疆大學 化工學院 煤炭潔凈轉化與化工過程新疆維吾爾自治區重點實驗室,新疆 烏魯木齊 830046)
目前,中國對傳統化石能源(煤炭、石油、天然氣等)特別是對石油資源的依賴性很強,而中國尤其是新疆的煤儲量非常豐富。隨著一碳化學的進一步發展,利用煤制氣,煤制天然氣、甲醇、二甲醚(DME)、乙二醇、甲酸甲酯、乙酸甲酯等技術受到人們的廣泛關注[1-5]。這一技術的發展不僅能利用豐富的煤炭資源來彌補石油資源的匱乏,對煤炭資源的清潔利用還能夠緩解能源和環境污染的矛盾。因此,開發和利用以煤為代表的一碳化學資源對新疆能源清潔利用發展有著深遠的意義。
合成氣作為碳氫化合物的載體,逐漸成為煤炭、天然氣及生物質等含碳資源潔凈化高效利用的橋梁和紐帶。因此,加快推進合成氣下游技術開發與產業化,通過高附加值下游產品來提升合成氣價值鏈,對合成氣行業發展已顯得至關重要[6-16]。在一定的溫度、壓力和催化劑存在的條件下,以合成氣為原料合成乙酸甲酯、高級醇等高附加值產品,是煤高值化利用需要開發的關鍵技術[17-21]。然而,這一過程非常復雜,需要研發高活性、長壽命、化學和熱穩定性好、可再生的催化劑。
目前以合成氣為原料合成乙酸甲酯需要多步反應和使用昂貴的催化劑[23-30],且存在目標產物收率低和分離困難等問題。研究發現[31-33],負載型納米Au催化劑對合成氣一步合成乙酸甲酯具有一定的催化活性,當Au粒子的尺寸比較小且具有一定酸中心時,其催化活性較高。因此如何制備出均勻尺寸較小和具有一定酸中心的納米Au催化劑是關鍵。HZSM-5沸石分子篩催化劑在石油化工領域應用較廣,主要用于脫氫、異構和重整、芳構化、烷基化等反應中,其具有納米級規則孔道結構和一定量的酸中心。以HZSM-5為載體制備高分散的Au催化劑[34],同時,調節HZSM-5沸石強酸中心,有利于其催化合成氣羰基化制備乙酸甲酯和甲酸甲酯等產品。
筆者以HZSM-5為載體,制備了具有金屬-酸雙功能催化作用的Au/HZSM-5沸石催化劑;引入助劑Na離子來調節其酸強度;對所制備催化劑進行物性表征,并考察了不同Na負載量、酸中心變化等因素對Au/HZSM-5催化劑催化合成氣羰基化制乙酸甲酯性能的影響。
1 實驗部分
1.1 試劑和原料
尿素,AR,天津市科密歐化學試劑廠產品;硝酸,質量分數為60%,天津市河東區紅巖試劑廠產品;氯金酸(HAuCI4·4 H2O),AR,國藥集團上海試劑公司產品;硝酸鈉,AR,河北旭興新能源科技有限公司產品;HZSM-5,實驗室自制,n(SiO2)/n(Al2O3)=25,粒徑20~50 nm;去離子水為自制。
1.2 催化劑的制備
1.2.1 Au/HZSM-5的制備
負壓沉積-沉淀法[35-36]:將HZSM-5與沉淀劑尿素以摩爾比0.5∶1混合后,在25℃、-0.06 MPa壓力下進行真空脫氣處理4 h,再加入41.86 m L的24.26 mmol/L的HAuCl4溶液,在80℃、-0.06~-0.04 MPa壓力下攪拌2 h、靜置2 h,過濾、洗滌、80℃干燥12 h,540℃焙燒4 h,制得Au負載質量分數為2%的2%Au/HZSM-5催化劑。
1.2.2 Na/HZSM-5的制備
向已配制好的Na NO3溶液(1 mol/L)中加入一定量的HZSM-5,在80℃下浸漬2 h,之后過濾、干燥、540℃焙燒6 h,得到產物wNa/HZSM-5,其中w為鈉的負載量(質量分數,以下同),w為0.2%、0.4%、0.8%、1.0%。
1.2.3wNa-2.0%Au/HZSM-5的制備
采用負壓浸漬法制備wNa-2.0%Au/HZSM-5系列催化劑。2.0%Au/HZSM-5催化劑在25℃、-0.06 MPa壓力下進行真空脫氣處理4 h,再分別加入不同濃度的NaNO3溶液,混合物在80℃、-0.06~-0.04 MPa壓力下攪拌2 h、靜置2 h,過濾、洗滌、80℃干燥12 h,540℃焙燒4 h,制備wNa-2.0%Au/HZSM-5系列催化劑,其中w為鈉的負載量,w為0.2%、0.4%、0.8%、1.0%。
1.3 催化劑的表征
催化劑的XRD表征在日本Rigaku-D/max-2004型X射線衍射儀上進行,掃描范圍2θ=5°~80°。催化劑NH3-TPD表征在美國Quantachrome公司生產的CHEMBET-3000型化學吸附分析儀上測定。脫附下來的NH3用GC-7890T型氣相色譜儀TCD來檢測。催化劑的酸類型及其羥基變化采用美國-Nicolet-IS10型吡啶吸附傅里葉變換紅外光譜儀(Py-FT-IR)進行表征。ICP在美國Leem Labs公司生產的Plasma-Spec-I型電感耦合等離子體原子發射光譜儀(ICP-AES)上進行。采用美國Quantachrome公司生產的AUTOSORB-1吸附儀進行物理吸附測定,并計算催化劑BET比表面積。
1.4 催化劑反應性能評價
催化劑的反應性能評價是在自建的可連續進樣的微型固定床反應裝置中進行,反應裝置如圖1所示。首先將制得的催化劑粉末壓片、粉碎、篩分,取粒度為40~60目的催化劑裝入20 cm×6 mm的U形反應管中。催化劑先在反應溫度下吹掃30 min,然后進行反應。反應條件:反應溫度為100~350℃,反應壓力為常壓、反應時間為4 h,進料為摩爾比為1∶1的純H2和純CO(體積分數均為99%)混合氣體。反應時,CO和H2分別通過質量流量計(5 m L/min)進入混合器進行混合、預熱后,再進入反應器進行反應。反應產物為甲酸甲酯、乙酸甲酯、二甲醚、甲醇等,采用GC-7890 T型氣相色譜儀(魯分分析儀器有限公司產品,2 HD2008型50 m×0.20 mm×0.5μm毛細管柱,FID檢測器)進行分析。

圖1 微型固定床實驗裝置示意圖Fig.1 Schematic of miniature fixed bed reactor
分別用CO轉化率、甲酸甲酯和乙酸甲酯選擇性來評價催化劑的活性,計算公式見式(1)~(4):

式中:X(CO)為CO轉化率,%;S(methyl acetate)為乙酸甲酯的選擇性,%;S(methyl formate)為甲酸甲酯的選擇性,%;S(by-products)為其他副產物的選擇性,%;m(methyl acetate)為產物中乙酸甲酯的質量,g;m(methyl formate)為產物中甲酸甲酯的質量,g;m(CO)為原料中CO的質量,g;m'(CO)為反應后CO的質量,g;m(by-products)為副產物的質量,g。
2 結果與討論
2.1 催化劑物性表征
2.1.1 元素組成分析
表1給出了制備的2.0%Au/HZSM-5、wNa/HZSM-5和wNa-2.0%Au/HZSM-5催化劑的元素組成理論值和實測值。
從表1可以看出:2.0%Au/HZSM-5催化劑中Au實際負載率為93%,單獨Na改性的Na/HZSM-5催化劑中Na實際負載率分別為90%、88%、88%、87%;雙金屬改性時,第一金屬Au的實際負載量與理論負載量相比,隨第二金屬Na負載量的增加而減少,說明負載第二金屬使得第一金屬有脫落現象,且隨Na負載量的增加,Au脫落得更多。

表1 2.0%Au/HZSM-5、w Na/HZSM-5和w Na-2.0%Au/HZSM-5沸石催化劑的ICP數據Table 1 ICP data of 2.0%Au/HZSM-5,w Na/HZSM-5 and w Na-2.0%Au/HZSM-5 zeolites
2.1.2 XRD表征
wNa/HZSM-5催化劑的XRD譜圖見圖2。由圖2可見,Na負載量分別為0.2%、0.4%、0.8%、1.0%時,Na/HZSM-5催化劑均在2θ為7.80°、8.70°、22.94°、23.60°、24.26°、29.12°、30.0°附近出現HZSM-5分子篩的特征衍射峰,但均未觀察到Na晶體的特征峰,這表明負載Na并沒有改變納米HZSM-5分子篩的晶體結構,Na能夠均勻地分散在HZSM-5分子篩的內外表面上。從特征衍射峰的強度來看,隨著Na負載量的增加,HZSM-5的特征衍射峰峰高沒有明顯變化,說明負載Na并沒有改變HZSM-5的結晶度。

圖2 w Na/HZSM-5催化劑的XRD譜圖Fig.2 XRD patterns of the w Na/HZSM-5catalysts
wNa-2.0%Au/HZSM-5催化劑的XRD譜圖見圖3。由圖3可見,單獨負載Au時,在2θ為38°、45°、65°、78°處有較明顯的Au的特征衍射峰。wNa-2.0%Au/HZSM-5催化劑在2θ為7.8°、8.7°、22.94°、23.6°和24.26°出現的HZSM-5的MFI結構特征衍射峰沒有明顯變化,說明負載的Au和Na基本沒有改變納米HZSM-5分子篩的晶體結構;在2θ為38°、45°、65°、78°處的Au的特征衍射峰有明顯的變化,且隨著Na負載量的增加,Au的特征衍射峰逐漸增加,峰面積變狹窄尖銳,說明負載Na后Au顆粒可能逐漸聚集、團聚長大。因此Na的負載量不能太高。
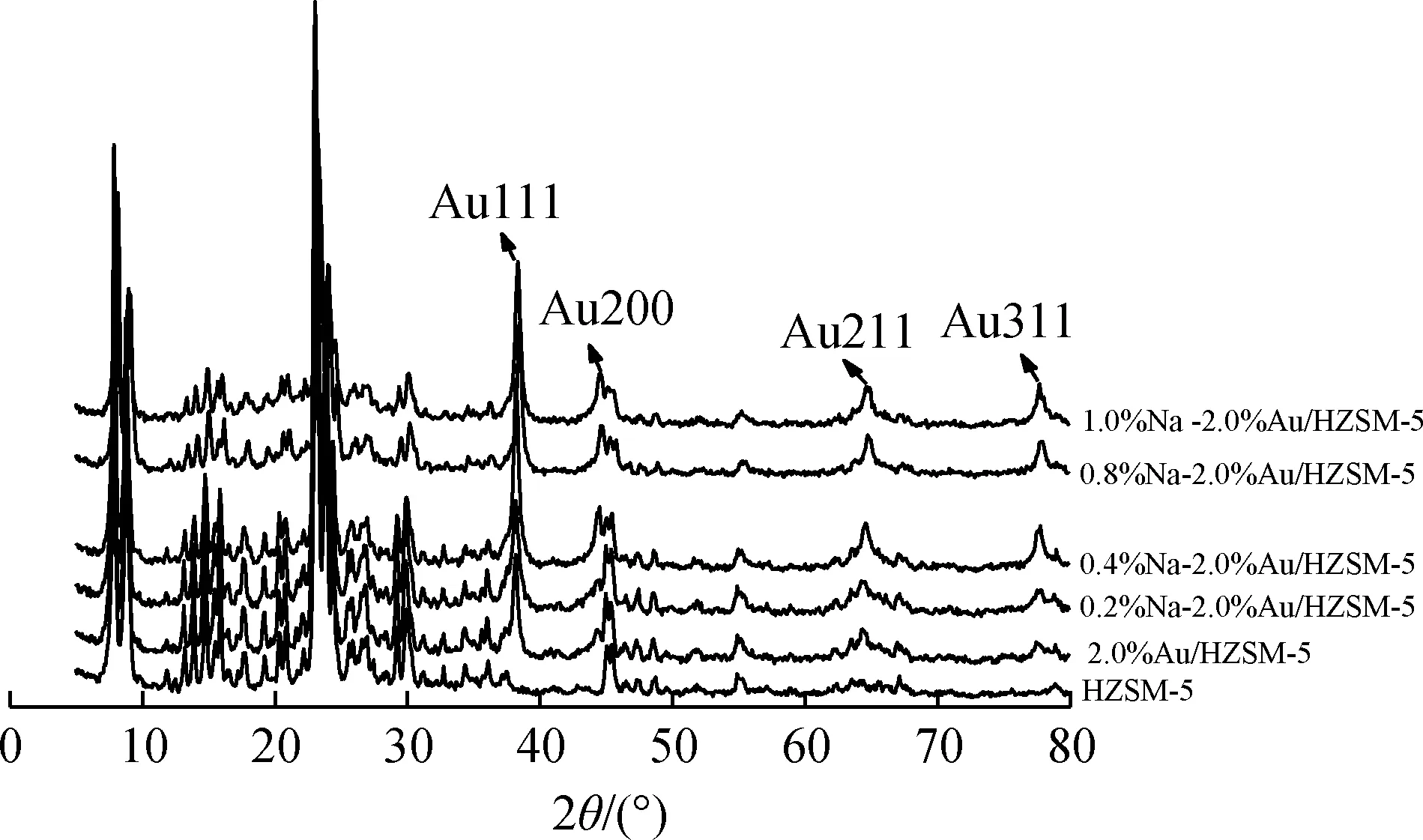
圖3 w Na-2.0%Au/HZSM-5催化劑的XRD譜圖Fig.3 XRD patterns of the w Na-2.0%Au/HZSM-5catalysts
2.1.3 比表面積和孔結構表征
HZSM-5、wNa/HZSM-5和wNa-2.0%Au/HZSM-5催化劑的比表面積和孔結構參數見表2。由表2可知:與HZSM-5相比,隨著Na負載量的增加,wNa/HZSM-5催化劑的比表面積先有所下降,而后增加,可能是因為Na負載量較大,堵塞了孔口,而隨著Na負載量增加,Na開始團聚,使得部分孔口重新暴露出來,因此使得催化劑的比表面積又有所增加;2.0%Au/HZSM-5催化劑的比表面積下降比較明顯,孔體積也有所下降,而平均孔徑有所增加,這可能是由于在制備過程中HZSM-5沸石分子篩的部分小孔被堵塞造成的;與HZSM-5相比,隨著Na負載量的增加,wNa-2.0%Au/HZSM-5催化劑的比表面積降低比較明顯,這進一步證明2.0%Au/HZSM-5催化劑上再負載Na時,可能因Na的加入使得Au顆粒聚集長大堵孔或堵塞孔口區,因而比表面積降低。說明堿性介質中Au顆粒大多數負載于催化劑外表面。這與圖3的XRD結果相符。

表2 2.0%Au/HZSM-5、w Na/HZSM-5和w Na-2.0%Au/HZSM-5催化劑的孔結構參數Table 2 Pore structural parameters of the 2.0%Au/HZSM-5,w Na/HZSM-5,w Na-2.0%Au/HZSM-5 prepared catalysts
HZSM-5、wNa/HZSM-5和wNa-2.0%Au/HZSM-5催化劑的氮氣物理吸附-脫附圖見圖4。由圖4可知,wNa/HZSM-5和wNa-2.0%Au/HZSM-5催化劑都出現了典型的Ⅳ型吸附等溫線,且有明顯的H3型回滯環。在相同的相對壓力時,脫附分支的吸附量大于吸附分支的吸附量。在高壓區出現的回滯環可能是由于晶體堆積產生的晶間介孔[14]。

圖4 w Na/HZSM-5和w Na-2.0%Au/HZSM-5催化劑的氮氣物理吸附-脫附等溫線Fig.4 N2 adsorption-desorption isotherms of the w Na-2.0%Au/HZSM-5 catalysts
2.1.4 表面酸性質
采用NH3-TPD對不同催化劑的表面酸性質進行了表征,結果見圖5。由圖5(a)可知,載體納米HZSM-5分子篩有2個明顯的NH3脫附峰:低溫脫附峰(240~300℃)為弱酸中心;高溫脫附峰(440~550℃)為強酸中心。當Na負載量較低,為0.2%和0.4%時,Na/HZSM-5催化劑位于450~550℃附近的高溫脫附峰強度明顯降低,說明wNa/HZSM-5催化劑上強酸中心減少。這是因為部分強酸中心被Na離子占據所致。當Na負載量增加到0.8%和1.0%時,Na/HZSM-5催化劑的高溫脫附峰基本消失,說明Na/HZSM-5催化劑的強酸中心基本被Na離子占據。特別值得注意的是,Na離子改性后,wNa/HZSM-5催化劑的低溫脫附峰強度沒有降低,Na負載量在0.4%~1.0%時峰面積反而有所增加,并向高溫脫附方向轉移。說明Na離子負載在強酸中心附近,使得強酸的酸中心減弱,并由強酸中心部分轉化為中強酸酸中心(300~400℃)。
由圖5(b)可知,2.0%Au/HZSM-5催化劑與載體HZSM-5沸石分子篩有相似的低溫脫附峰和高溫脫附峰,Au改性后高溫脫附峰有所增加。0.4%Na-2.0%Au/ZSM-5催化劑的低溫和高溫脫附峰峰高比0.4%Na/HZSM-5催化劑有明顯的增加,但比2.0%Au/ZSM-5催化劑的低了很多。這說明,2.0%Au/HZSM-5催化劑上負載Na離子可以降低原有的弱酸中心和強酸中心,產生中強酸中心。
采用Py-IR光譜對各催化劑的酸類型進行了表征,結果見圖6。由圖6(a)可知,HZSM-5沸石分子篩有明顯的L酸(1455 cm-1處吸收峰)和B酸(1548 cm-1處吸收峰)。Na離子改性后,wNa/HZSM-5催化劑的B酸中心隨著Na負載量的增加而逐漸減少,Na負載量達1.0%時基本消失;而L酸中心隨著Na的加入偏移到波數1442 cm-1處,且隨Na負載量的增加,峰面積增大,但峰強度有所下降,可能是由于Na離子優先負載在強B酸中心上,使得部分強B酸中心轉化為中強或弱的L酸中心,這與圖5(a)的NH3-TPD結果相符。
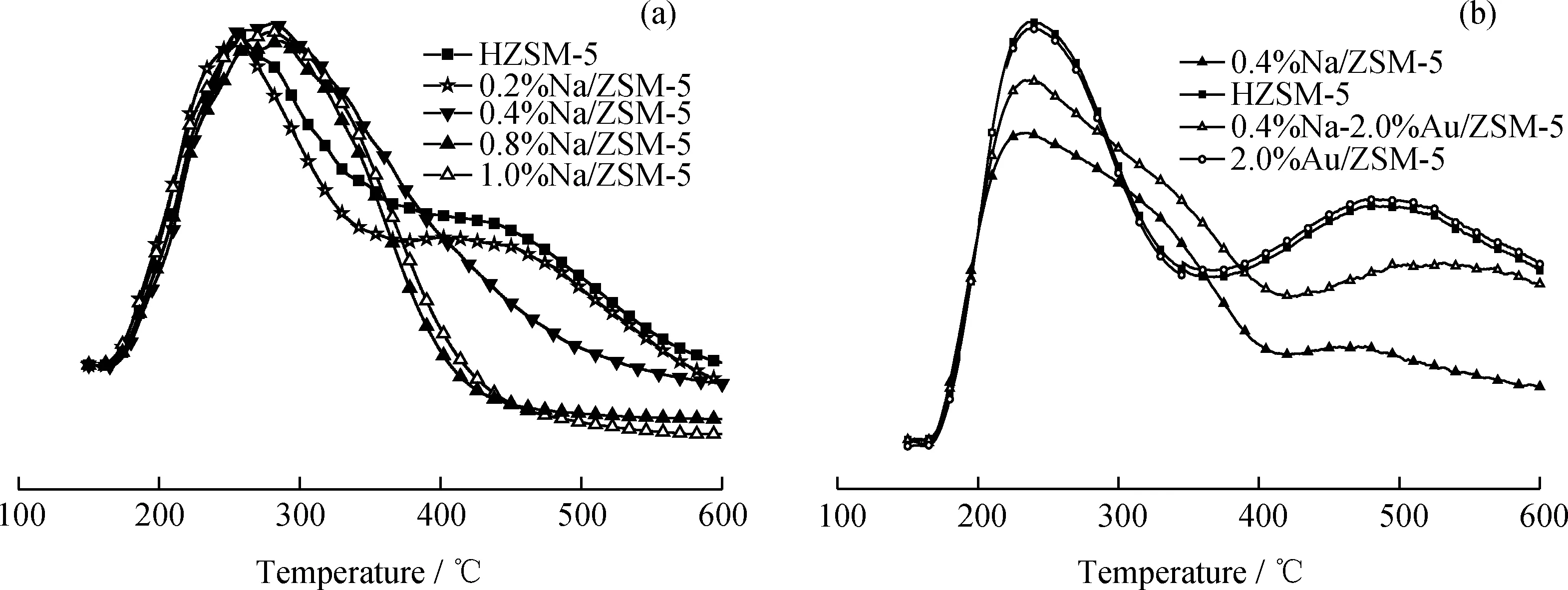
圖5 w Na/HZSM-5和0.4%Na-2.0%Au/HZSM-5催化劑的NH3-TPD譜圖Fig.5 NH3-TPD profiles of the prepared w Na/HZSM-5 and 0.4%Na-2.0%Au/HZSM-5 catalysts
由圖6(b)可知,2.0%Au/HZSM-5催化劑的B酸中心、L酸中心都比載體HZSM-5有所增加。文獻[33]曾指出波數1621 cm-1附近譜峰與L酸有關,而波數1636 cm-1處與B酸有關。Na改性后,wNa-2.0%Au/HZSM-5催化劑波數1549 cm-1處的B酸中心峰面積比載體HZSM-5沸石分子篩和2.0%Au/HZSM-5催化劑的小,而波數1442 cm-1處的L酸中心譜峰明顯增加;波數1622 cm-1和1636 cm-1的譜峰明顯降低;而波數1599 cm-1處出現了新的譜峰,可以理解為是Na和2.0%Au/HZSM-5催化劑相互作用而形成的新的譜峰。文獻[35]認為波數1599 cm-1處譜峰屬于中強B酸的可能性較大。這與NH3-TPD的結果較為一致。

圖6 w Na/HZSM-5和w Na-2.0%Au/HZSM-5催化劑300℃Py-FTIR譜圖Fig.6 Py-FTIR profiles of w Na/HZSM-5 and w Na-2.0%Au/HZSM-5 catalysts at 300℃
2.1.5 OH-IR光譜分析
采用OH-IR光譜對wNa-2.0%Au/HZSM-5催化劑的表面羥基進行了表征,結果如圖7所示。
圖7中位于波數3743 cm-1處的吸收峰歸屬于硅羥基,位于波數3612 cm-1處的吸收峰歸屬于硅鋁橋羥基,位于波數3662 cm-1處的吸收峰歸屬于鋁羥基[35]。由圖7看到,與HZSM-5沸石分子篩相比,負載Au后,2.0%Au/HZSM-5催化劑位于波數3724 cm-1處出現了新的吸收峰。根據文獻[14],波數3724 cm-1處的吸收峰歸屬于沸石分子篩中四元環的硅羥基的伸縮振動鋒,其與Au的負載有關,但是如何形成的等問題還尚未清楚。對于wNa-2.0%Au/HZSM-5催化劑,隨著Na負載量的增加,波數3612、3662和3743 cm-1處的吸收峰強度減弱,而波數3724 cm-1處的吸收峰變化不明顯。波數3612 cm-1處的硅鋁橋羥基屬于B酸中心,酸性較強[33],當把少量Na離子引入2.0%Au/HZSM-5催化劑時,強酸中心被Na離子中和,即硅鋁橋羥基,因此吸收峰強度減弱,強酸中心減弱。

圖7 w Na-2.0%Au/HZSM-5催化劑的OH-IR譜圖Fig.7 OH-IR spectra of w Na-2.0%Au/HZSM-5 catalysts
2.2 催化劑的羥基化反應性能
中心,從而使其具有酸催化反應的能力;Na負載量高達1.0%時,強酸中心完全消失,而且產生的中強酸中心比較少,因此催化反應性能下降。此結果說明酸性對催化劑活性有非常重要的影響。
從表3還看到,2.0%Au/HZSM-5催化劑的CO轉化率為81.01%,主產物甲酸甲酯和乙酸甲酯的選擇性之和為62.12%,高于HZSM-5沸石分子篩;而0.4%Na-2.0%Au/HZSM-5催化劑的CO轉化率與甲酸甲酯和乙酸甲酯的選擇性之和均為最高,分別為88.51%和68.56%,均高于0.4%Na/HZSM-5的,這說明Na負載量為0.2%、0.4%、0.8%的雙金屬負載的催化劑催化活性要高于單金屬負載的催化劑。1.0%Na-2.0%Au/HZSM-5的CO轉化率僅為11%,乙酸甲酯和甲酸甲酯選擇性之和降到15%,其他副產物的總選擇性最高達50%以上,這可能與該催化劑的中強酸中心和強酸中心少有關。
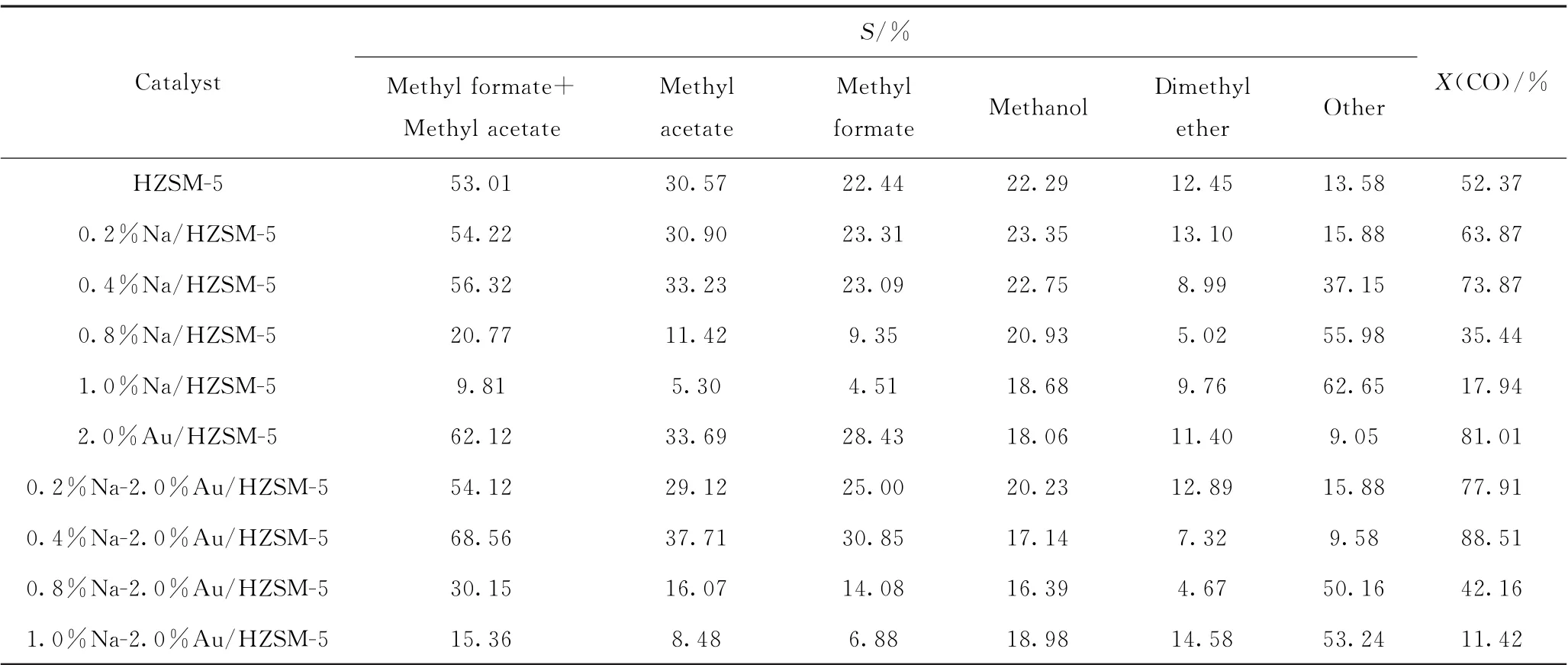
表3 合成氣在w Na/HZSM-5和w Na-2.0%Au/HZSM-5催化劑上CO轉化率和產物選擇性Table 3 CO conversion and product selectivity of syngas over w Na/HZSM-5 and w Na-2.0%Au/HZSM-5 catalysts
0.4%Na-2.0%Au/HZSM-5催化劑的酸性表征、羥基紅外表征結果均說明,該催化劑具有一定的強酸中心和中強酸中心。中強酸中心的量對催化劑性能的影響較大,中強酸中心的量較少時,催化性能較差;而中強酸中心的量達到一定程度時,催化劑的催化性能最好。此結果說明,合成氣羰基化反應活性與催化劑的酸性有密切的關系,即強酸中心要少,有一定量的中強酸中心和較多的弱酸中心對合成氣羰基化反應有利。
3 結 論
采用負壓沉積-沉淀法分別制備了wNa/HZSM-5、2.0%Au/HZSM-5和wNa-2.0%Au/HZSM-5(w=0、0.2%、0.4%、0.8%或1.0%)系列催化劑,進行了酸性表征、羥基紅外表征比表面積和孔結構表征等,并對催化劑催化羰基化反應性能進行考察。結果表明:
(1)對于wNa/HZSM-5催化劑,Na負載質量分數為0.4%時,其產生了一定量的中強酸中心,催化合成氣羰基化反應性能最好。
(2)0.4%Na-2.0%Au/HZSM-5催化劑的合成氣羰基化反應性能最好,CO轉化率最高達88.51%,目的產物甲酸甲酯和乙酸甲酯選擇性之和為68.56%,高于單獨Au改性和單獨Na改性的催化劑。
(3)對于合成氣羰基化反應,一定量的弱酸中心和中強酸中心,以及較少的強酸中心可提高催化劑的反應活性。

