基于量質傳遞及化學計量學的藥食同源名方青龍白虎湯質量控制研究
陳 姣,王繼森,鄧晶晶,朱宗萍,廖 婉*,陳 意,楊青松,王 琳,傅超美,朱雅寧, 3*
基于量質傳遞及化學計量學的藥食同源名方青龍白虎湯質量控制研究
陳 姣1,王繼森2#,鄧晶晶1,朱宗萍1,廖 婉1*,陳 意1,楊青松1,王 琳1,傅超美1,朱雅寧1, 3*
1. 成都中醫藥大學西南特色中藥資源國家重點實驗室,藥學院,四川 成都 611137 2. 成都市食品藥品檢驗研究院,四川 成都 610045 3. 雅安三九藥業有限公司,四川 雅安 625000
建立HPLC指紋圖譜檢測方法,探尋青龍白虎湯凍干粉制備過程工藝和量質傳遞規律,并結合化學計量學構建其質量控制體系。制備15批次青龍白虎湯凍干粉,采用HPLC法建立指紋圖譜,色譜結果導入《中藥色譜指紋圖譜相似度評價軟件》(2012版)并計算各部分相似度。測定15批樣品量質傳遞過程中沒食子酸、原兒茶酸、綠原酸、表兒茶素和鞣花酸的含量,計算轉移率和出膏率。結合化學計量學方法進行分析,以挖掘不同產地樣品間對質量控制具有顯著貢獻的主要成分。15批樣品指紋圖譜相似度均大于0.9,滿足規定要求,并標定凍干粉指紋圖譜24個共有峰,對其中6種成分進行了指認,分別為沒食子酸(1號峰)、原兒茶酸(4號峰)、綠原酸(8號峰)、表兒茶素(14號峰)、東莨菪內酯(19號峰)、鞣花酸(23號峰)。15批凍干粉表兒茶素、沒食子酸、鞣花酸、綠原酸、原兒茶酸的質量分數分別為0.724%~1.301%、2.184%~2.840%、0.607%~0.760%、0.061%~0.141%、0.017%~0.079%,轉移率分別為78.60%~89.38%、76.98%~89.88%、76.00%~89.78%、76.90%~90.49%、80.02%~90.25%,出膏率為12.87%~15.11%,均未出現離散數據,表明煎煮、濃縮和凍干過程有效成分轉移率較穩定。通過化學計量學分析,找到10個對模型貢獻較大的成分,其中包括指認的峰14 (VIP=2.812)、峰1(VIP=2.804)、峰23(VIP=2.715)、峰8(VIP=1.053)和峰4(VIP=0.887),可進一步深化青龍白虎湯質量控制研究。通過HPLC指紋圖譜結合多指標成分含量測定,首次建立了藥食同源名方青龍白虎湯的質量控制方法,此方法快速簡單可行,重復性、穩定性良好,能同時適用于飲片、煎煮液、濃縮液和凍干粉量質傳遞規律的相關性考察;進一步通過化學計量學為青龍白虎湯的質量控制研究提供了重要參考。
青龍白虎湯;量質傳遞;指紋圖譜;化學計量學;沒食子酸;原兒茶酸;綠原酸;表兒茶素;鞣花酸;質量控制
青龍白虎湯(Qinglong Baihu Decoction,QBD)出自清代著名醫家王孟英《王氏醫案》卷二,全方兩味。方中青果為主藥,具清熱解毒、利咽生津之效[1-3];萊菔又名白蘿卜,被譽為“蔬中圣品”,具有豐富的營養元素和藥用價值,能消食下氣、利尿化痰[4-6]、健脾寬中、清熱解毒,對于肺熱痰火、咳喘痰多、食停不化、脘腹脹滿等有很好的療效。此方為藥食兩用方,高度契合中醫藥學自古就有的“藥食同源”理論精髓,集預防、保健與治療等多種應用價值于一身,充分體現了中醫藥的傳統特色,其以“藥極簡易,性最平和,味不惡劣,易粉易服”等諸多優勢而備受青睞。青果色青,萊菔色白,合而為劑,可消經絡留滯之痰,解膏粱魚面之毒,喉病之可免[7]。本方最大特點為善于清熱利咽,主治熱毒內盛、上灼咽喉、津液損傷所致咽喉腫痛,是預防及治療呼吸道疾病的藥食同源上佳良方。
中藥質量評價標準欠完善、質量追溯性和均一性較差等問題一直是亟待解決的技術瓶頸,已成為行業發展的重中之重[8]。中藥復方質量易受其組成藥味多基原、多品種、多產地、藥材來源不穩定、多成分及相互作用復雜等因素影響,影響其質量一致性,不利于有效控制療效的穩定[9-12]。課題組前期圍繞QBD,已完成青龍白虎飲及利咽含片的研究,并初步建立相關質量標準體系[13-14]。但QBD中的化學成分群在煎煮、濃縮、干燥過程中的動態變化亟待進一步研究,以綜合、全面的對QBD進行質量控制。因此,本實驗采用15批青果飲片和市售新鮮萊菔,首次以古籍記載的煎煮方法為參考依據進行QBD的煎煮-濃縮-干燥工藝研究,以有效成分轉移率、出膏率等為質控指標,運用化學指紋圖譜分析技術和多指標成分含量測定方法,初步構建QBD全過程質量標準評價體系,再結合化學計量學手段分析QBD內在影響因素,探尋QBD質控影響關鍵成分,系統的、全方位的對工藝全過程進行質量評價分析,探尋其量質傳遞規律,以期為后續相關制劑的研究研發提供可靠的技術保障。
1 儀器與材料
1.1 儀器
UltiMate 3000型高效液相色譜儀,美國Thermo Fisher公司;色譜柱Thermo Hypersil GOLD C18(250 mm×4.6 mm,5 μm)和色譜柱AcclaimTM120 C18(250 mm×4.6 mm,5 μm),賽默飛世而科技(中國)有限公司;UPK-I-10T型純水機,四川優普超純科技有限公司;AR224CN電子天平,萬分之一,奧豪斯儀器(常州)有限公司;CPA225D型十萬分之一電子分析天平,賽多利斯科學儀器(北京)有限公司;FTS-10A全自動煎藥壺,潮州市一壺百飲電器實業有限公司;SCIENTZ-10N冷凍干燥機,寧波新芝生物科技股份有限公司;DL-720D數控超聲波清洗器,上海之信儀器有限公司。
1.2 試藥
甲醇、乙腈為色譜純,美國Sigma-Aldrich公司;色譜純磷酸,成都市科隆化學品有限公司;水為超純水,自制,其它試劑均為分析純;對照品沒食子酸(CAS號149-91-7,批號wkq20010905)、原兒茶酸(CAS號99-50-3,批號wkq20020706)、綠原酸(CAS號327-97-9,批號wkq20042702)、表兒茶素(CAS號490-46-0,批號wkq20012203)、東莨菪內酯(CAS號92-61-5,批號wkq20011001)、鞣花酸(CAS號476-66-4,批號wkq20011002),質量分數均≥98%,均購自成都省維克奇生物科技有限公司。15批青果藥材分別購于四川省合江縣、四川省廣安市、廣東省廣州市和福建省閩侯縣,包含道地藥材產地及主產區,均于秋季采收,保證了樣品的均一性和代表性,并根據《中國藥典》2020年版相關規定儲存于干燥處,防蛀,飲片具體信息見表1。經成都中醫藥大學藥學院標本中心蔣桂華教授鑒定為橄欖科橄欖屬植物橄欖Raeusch.的干燥成熟果實,藥材經炮制得到15批青果飲片,經檢驗藥材和飲片均符合《中國藥典》2020年版一部項下的相關規定[1];萊菔市售,產于溫江無公害蔬菜基地農場,經標本中心蔣桂華教授定其基原為十字花科植物萊菔L.的新鮮根莖。
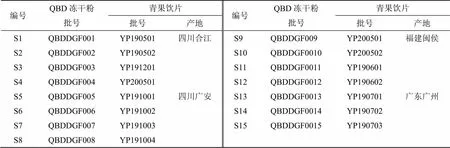
表1 15批青果飲片產地信息
2 方法與結果
2.1 QBD凍干粉的制備
結合QBD相關文獻報道[13-14]參考其制備工藝參數,并通過單因素考察確定QBD最佳工藝為青果與萊菔比例為1∶1,6倍量水提取2次,每次60 min。稱取青果飲片60 g加水浸泡30 min,然后加入切制小塊的新鮮萊菔60 g,6倍量水(720 mL)煎煮2次,每次1 h,合并2次QBD煎煮液得1200 mL。取煎煮液1200 mL減壓濃縮至約150 mL,得濃縮液;對濃縮液進行冷凍干燥,即得QBD凍干粉。
2.2 溶液的配制
2.2.1 對照品溶液的制備 稱取沒食子酸、原兒茶酸、綠原酸、表兒茶素、東莨菪內酯、鞣花酸對照品適量,精密稱定,加甲醇制成分別含沒食子酸、原兒茶酸、綠原酸、表兒茶素、東莨菪內酯、鞣花酸0.943、0.757、1.025、1.160、1.080、1.032 mg/mL的對照品儲備液I,再各量取0.5 mL到5 mL量瓶中混勻,用甲醇稀釋定容,得到混合對照品儲備液II。
2.2.2 供試品溶液的制備
(1)單味飲片樣品供試品溶液:按照“2.1”項下煎煮液制備方法,分別制備青果、萊菔的單煎樣品溶液,過0.22 μm微孔濾膜,取續濾液,即得。
(2)QBD煎煮液供試品溶液:取“2.1”項下所制備的QBD煎煮液,過0.22 μm微孔濾膜,取續濾液,即得。
(3)QBD濃縮液供試品溶液:精密量取“2.1”項下所制備的QBD濃縮液2 mL置10 mL量瓶中,加水至刻度,搖勻,濾過,取續濾液,即得。
(4)QBD凍干粉供試品溶液:取“2.1”項下所制備的QBD凍干粉約0.2 g,精密稱定,置10 mL量瓶中,加水超聲處理(功率500 W、頻率40 kHz)10 min使溶解,取出,放冷,定容至刻度,搖勻,濾過,過0.22 μm微孔濾膜,取續濾液,即得。
2.3 HPLC指紋圖譜分析
2.3.1 色譜條件 AcclaimTM120 C18色譜柱(250 mm×4.6 mm,5 μm);以乙腈-0.1%磷酸水溶液為流動相(流動相每天新鮮制備,通過0.45 μm濾膜,注射到色譜柱之前進行超聲脫氣),梯度洗脫:0~25 min,5%~12%乙腈;25~50 min,12%~15.4%乙腈;50~75 min,15.4%~22.5%乙腈;體積流量1.0 mL/min;檢測波長237 nm;柱溫30 ℃;進樣量10 μL。理論板數按沒食子酸峰計算不低于5000。
2.3.2 方法學考察
(1)精密度試驗:取QBD凍干粉供試品溶液(S1),按“2.3.1”項下色譜條件連續進樣6次,記錄色譜圖。以表兒茶素為參照峰,計算各共有峰相對保留時間和相對峰面積RSD,結果各共有峰相對保留時間RSD<1%,相對峰面積RSD<3%,以《中藥色譜指紋圖譜相似度評價系統軟件》(2012. 130723版)評價,6次進樣的相似度均為1.00,表明儀器精密度良好,符合指紋圖譜要求。
(2)重復性試驗:按“2.1”及“2.2.2”項下方法平行制備6份QBD凍干粉供試品溶液(S1),按“2.3.1”項下色譜條件進行測定,記錄色譜圖。以表兒茶素為參照峰,計算各共有峰相對保留時間和相對峰面積RSD,結果各峰相對保留時間RSD<1%,相對峰面積RSD<2.5%,以《中藥色譜指紋圖譜相似度評價系統軟件》(2012.130723版)評價,6次進樣的相似度均為1.00,結果表明該方法重復性良好,符合指紋圖譜要求。
(3)穩定性試驗:取QBD凍干粉供試品溶液(S1),分別于0、2、4、8、12、24、48 h按“2.3.1”項下色譜條件進行測定,記錄色譜圖。以表兒茶素為參照峰,計算各共有峰相對保留時間和相對峰面積RSD,結果各共有峰相對保留時間RSD<1.5%,相對峰面積RSD<3%,以《中藥色譜指紋圖譜相似度評價系統軟件》(2012.130723版)評價,7次進樣的相似度均為1.00,表明青果供試品溶液在48 h內穩定性良好,符合指紋圖譜要求。
2.3.3 化學指紋圖譜建立及相似度評價與分析 根據“2.3.1”項下色譜條件對15批青果飲片及QBD煎煮液、濃縮液和凍干粉的供試品溶液進行檢測,記錄各樣品色譜圖。采用國家藥典委員會《中藥色譜指紋圖譜相似度評價系統軟件》(2012.130723版)對記錄的色譜圖進行分析。以S1號樣品的特征圖譜作為參照譜進行指紋匹配(中位數法,時間窗為0.1 min),確定了24個共有峰。15批青果飲片及QBD煎煮液、濃縮液和凍干粉指紋圖譜見圖1;進行相似度計算,15批供試品的相似度均≥0.9,表明各批樣品的相似度較好,化學成分穩定,結果見表2;選取分離度較好的表兒茶素色譜峰(14號峰)作為參照峰,各峰的相對保留時間和相對峰面積見表3。
2.3.4 色譜峰的化學成分指認及歸屬 通過與對照品位置比較,指認了其中6個共有峰,分別為沒食子酸(1號峰)、原兒茶酸(4號峰)、綠原酸(8號峰)、表兒茶素(14號峰)、東莨菪內酯(19號峰)、鞣花酸(23號峰)。24個共有峰中,其中6號峰歸屬于萊菔,其余23個峰歸屬于青果飲片,占青果飲片總峰面積83.69%,占凍干粉總峰面積73.07%。結果表明,QBD凍干粉的主要物質群均可清晰地追溯到飲片,歸屬明確。
2.4 QBD凍干粉制備過程中有效成分的含量及出膏率的測定
2.4.1 色譜條件 同“2.3.1”項下的色譜條件。
2.4.2 方法學考察[12]
(1)專屬性試驗:分別精密吸取以上制備的混合對照品儲備液II、凍干粉供試品溶液(S1)、萊菔單煎樣品溶液、青果單煎樣品溶液(S1)、甲醇空白溶劑各10 μL,注入液相色譜儀,按照“2.4.1”項下色譜條件測定,結果供試品色譜中,在與沒食子酸、原兒茶酸、綠原酸、表兒茶素、東莨菪內酯、鞣花酸混合對照品色譜相應位置上有色譜峰,甲醇空白樣品色譜上沒有相應峰,結果表明樣品溶液中各成分分離度(>1.5)和理論板數(>5000)均較好,且陰性無干擾,見圖2。
(2)線性關系考察:取以上原兒茶酸、綠原酸儲備液I各0.2 mL,表兒茶素儲備液I 2 mL,鞣花酸儲備液I 1 mL定容到5 mL,四者配成混合對照品溶液III進行線性考察;取以上沒食子酸儲備液I 3 mL定容到5 mL配成沒食子酸對照品溶液IV進行線性考察。混合對照品溶液III和沒食子酸對照品溶液IV分別稀釋0、2、4、8、16、32、64倍后,注入液相色譜儀,按照“2.3.1”項下色譜條件測定,以各成分對照品質量濃度為橫坐標(),峰面積為縱坐標(),繪制標準曲線,進行線性回歸,得回歸方程:沒食子酸=0.162 2+1.667 1,2=0.999 1,線性范圍8.841~565.8 μg/mL;原兒茶酸=0.237 8+0.029 2,2=1.000 0,線性范圍 0.473 1~30.28 μg/mL;綠原酸=0.298 6+ 0.001 8,2=1.000 0,線性范圍0.640 6~41.00 μg/mL;表兒茶素=0.291 7+0.989 1,2= 0.999 9,線性范圍7.250~464.0 μg/mL;鞣花酸=0.978 4-2.100 3,2=0.999 4,線性范圍3.225~206.4 μg/mL;結果表明各成分在相應的質量濃度范圍內線性關系良好。
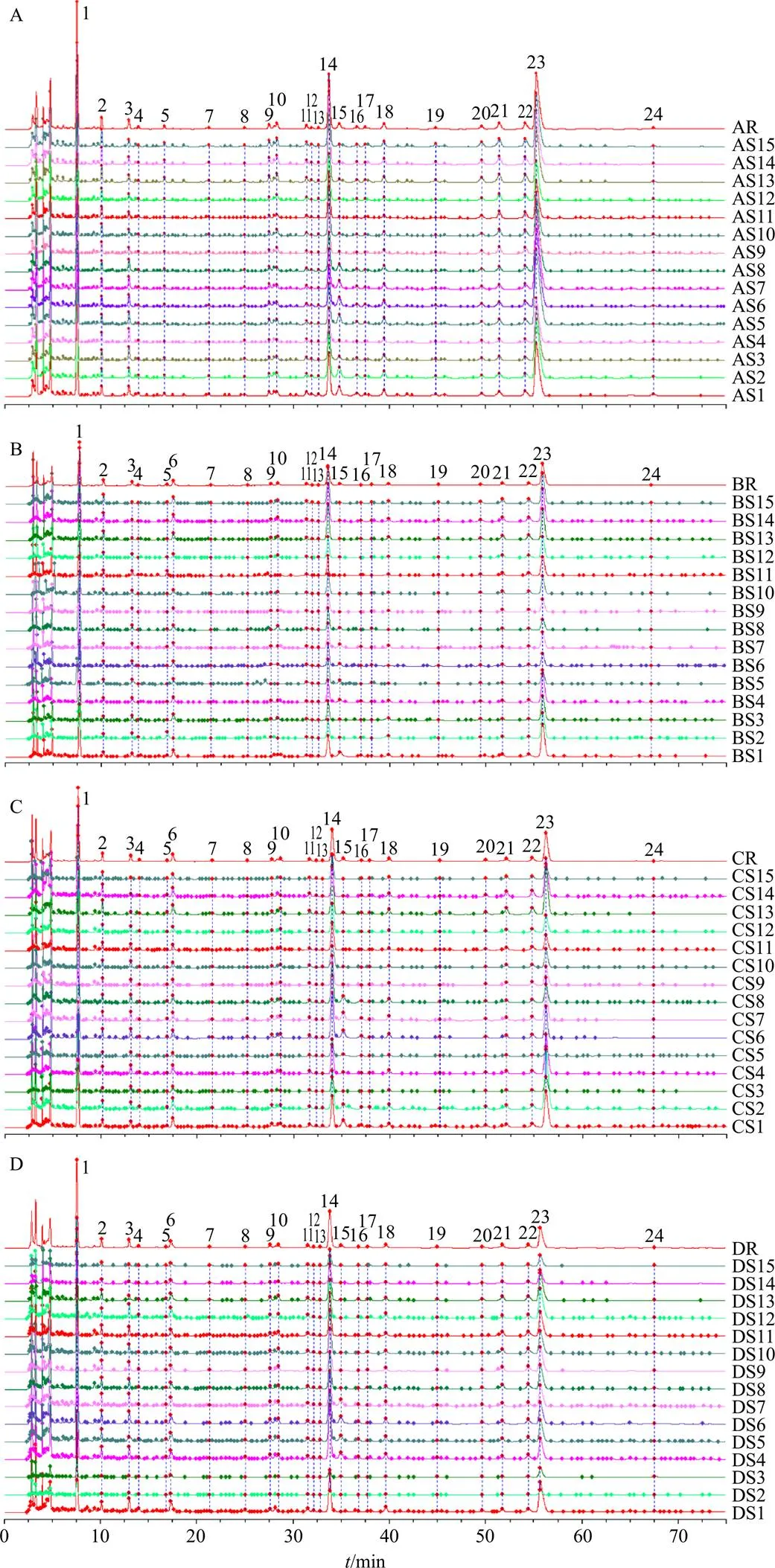
圖1 15批(S1~S15)青果飲片 (A)、QBD煎煮液 (B)、QBD濃縮液 (C) 和QBD凍干粉 (D) 的HPLC指紋圖譜及其對照指紋圖譜(AR、BR、CR、DR)

表2 15批青果飲片、QBD煎煮液、QBD濃縮液和QBD凍干粉與各自對照指紋圖譜的相似度
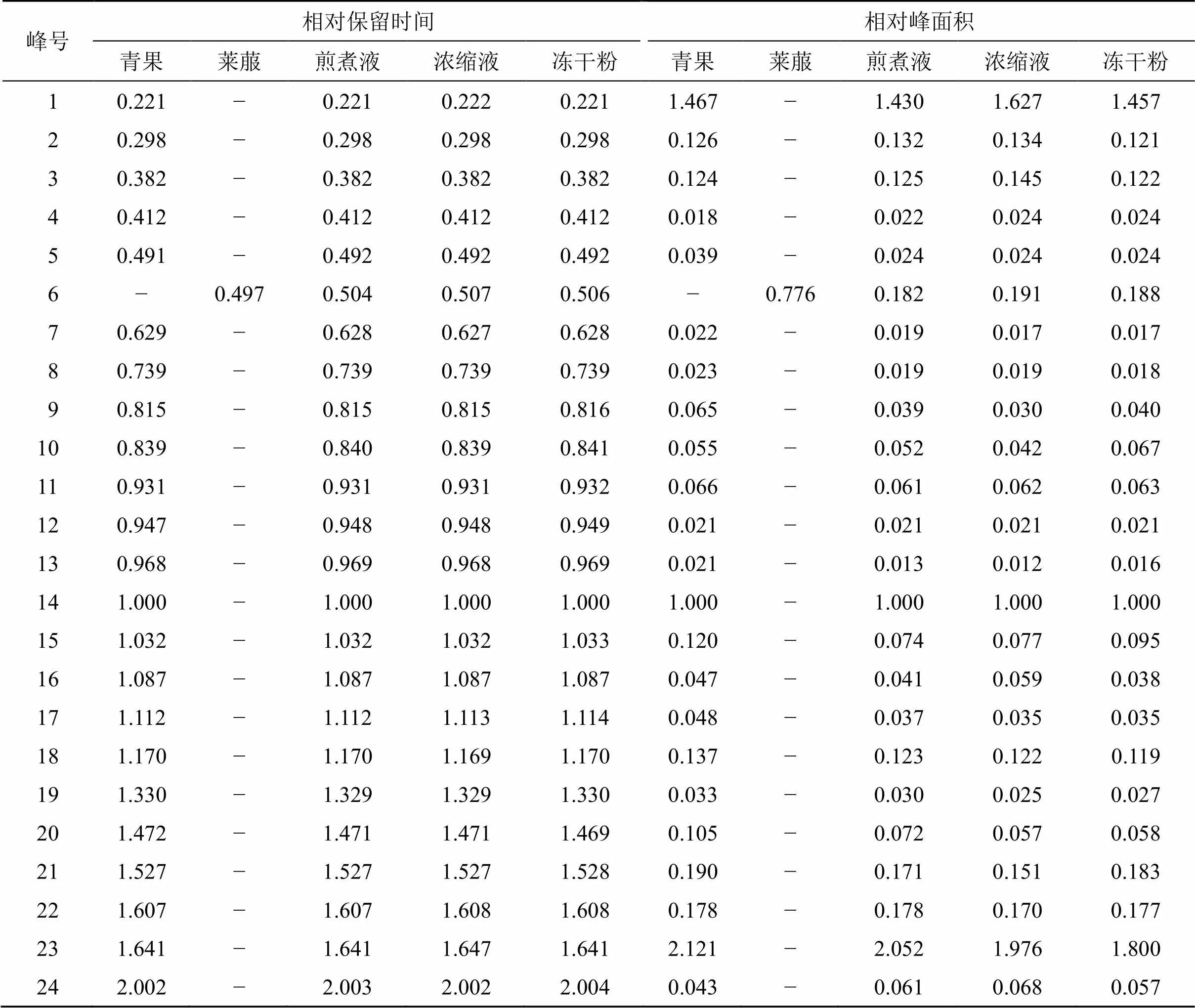
表3 QBD各單味藥、煎煮液、濃縮液和凍干粉特征峰相對保留時間與相對峰面積
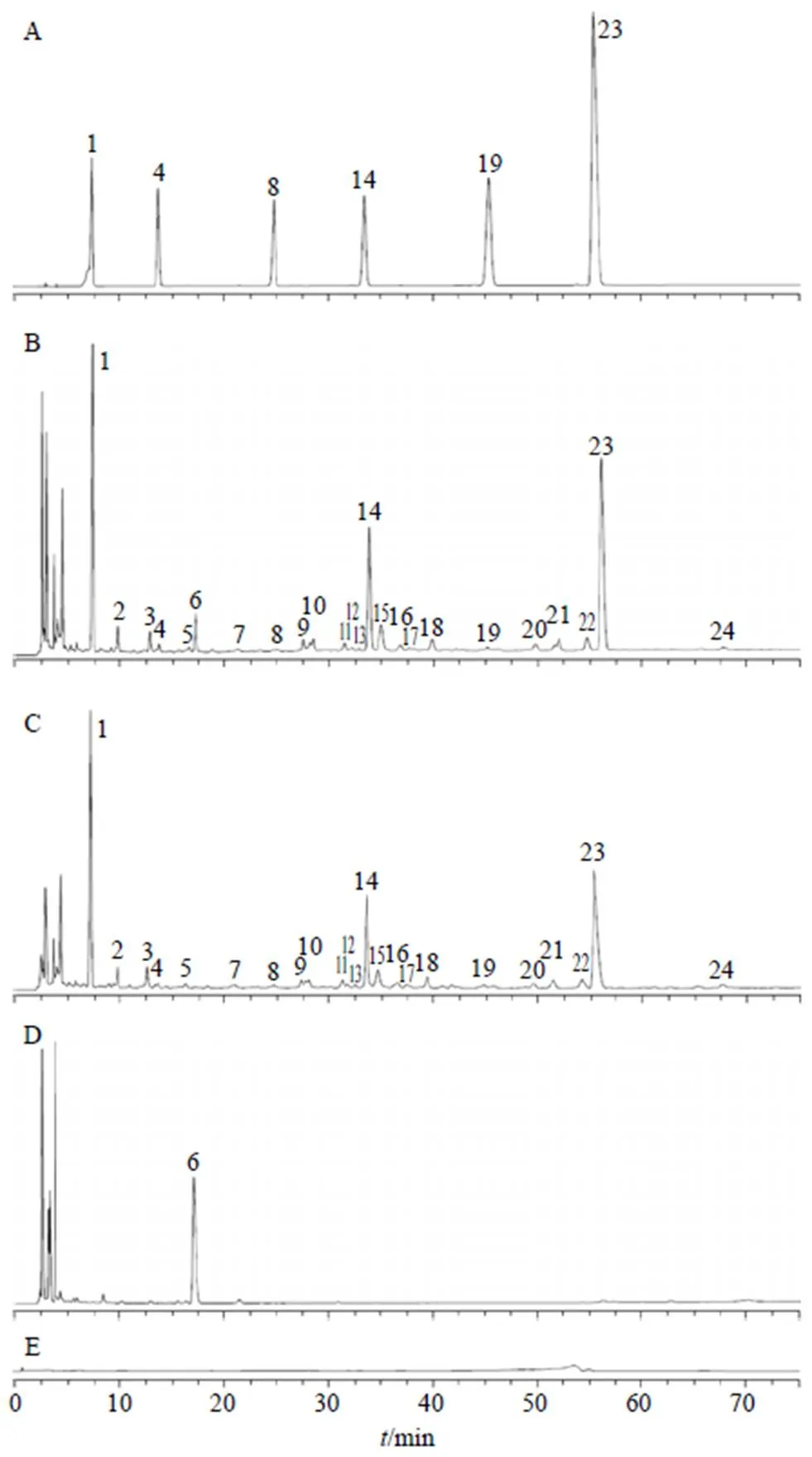
1-沒食子酸 4-原兒茶酸 8-綠原酸 14-表兒茶素 19-東莨菪內酯 23-鞣花酸
(3)精密度試驗:取同一QBD凍干粉供試品溶液(S1),按照“2.3.1”項下色譜條件測定,連續進樣6次,記錄峰面積,計算各成分色譜峰面積的RSD。計算沒食子酸、原兒茶酸、綠原酸、表兒茶素、鞣花酸峰面積的RSD分別為0.1%、1.37%、0.98%、0.31%、0.38%,表明儀器精密度良好。
(4)重復性試驗:按“2.3.2”項下方法平行制備6份QBD凍干粉供試品溶液(S1),按照“2.3.1”項下色譜條件測定,依次進樣分析,記錄峰面積,計算各成分質量分數的RSD。結果沒食子酸、原兒茶酸、綠原酸、表兒茶素、鞣花酸質量分數的RSD分別為0.78%、0.89%、1.32%、0.74%、1.13%,表明該方法重復性良好。
(5)穩定性試驗:取同一QBD凍干粉供試品溶液(S1),分別于制備后0、2、4、8、12、24、48 h按照“2.3.1”項下色譜條件測定,記錄峰面積,計算各成分色譜峰面積的RSD。沒食子酸、原兒茶酸、綠原酸、表兒茶素、鞣花酸峰面積的RSD分別為0.73%、0.85%、1.02%、1.12%、0.40%,表明供試品溶液在48 h內穩定。
(6)加樣回收率試驗:精密量取已知含量的QBD凍干粉0.2 g,平行6份,每份都分別加入對照品沒食子酸2.828 mg、原兒茶酸0.046 mg、綠原酸0.017 3 mg、表兒茶素1.080 mg、鞣花酸0.801 mg,按“2.2.2”項下方法平行制備各供試品溶液(S1),進樣量10 μL注入液相色譜儀,按照“2.3.1”項下色譜條件測定,記錄峰面積,分別計算各指標成分的實際測得量和回收率,再計算各指標成分的平均加樣回收率。結果沒食子酸、原兒茶酸、綠原酸、表兒茶素、鞣花酸峰面積的平均加樣回收率分別為99.5%、96.1%、97.0%、97.7%、99.4%,RSD分別為0.25%、0.49%、0.62%、0.62%、0.71%,結果表明該方法準確可靠。
2.4.3 含量測定[16-18]取15批QBD樣品,按“2.2.2”項下方法制備供試品溶液,按“2.3.1”項下色譜條件對供試品溶液進行指標成分含量測定。以QBD凍干粉制備過程穩定性成分為評價指標,分別計算沒食子酸、原兒茶酸、綠原酸、表兒茶素、鞣花酸的得率及轉移率,得率=總體樣品(指煎煮液、濃縮液和凍干粉)中指標成分質量/飲片投料量,轉移率=總體樣品(指煎煮液、濃縮液和凍干粉)中指標成分質量/總體飲片中指標成分質量,結果見表4~6。結果顯示,15批青果飲片沒食子酸、原兒茶酸、綠原酸、表兒茶素、鞣花酸平均質量分數分別為3.78、0.033、0.039 1、1.23、0.949 mg/g,RSD分別為18.18%、21.71%、14.81%、12.11%、25.83%。15批凍干粉中沒食子酸、原兒茶酸、綠原酸、表兒茶素、鞣花酸質量分數分別為2.184%~2.84%、0.017%~0.079%、0.061%~0.141%、0.724%~1.301%、0.607%~0.760%,以沒食子酸、表兒茶素、鞣花酸等成分含量較高。
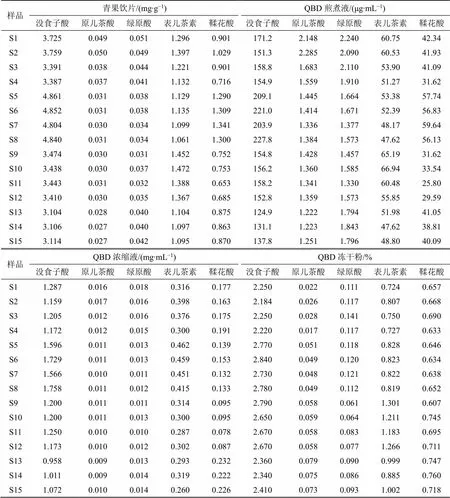
表4 15批青果飲片、QBD煎煮液、QBD濃縮液和QBD凍干粉中有效成分含量
煎煮液、濃縮液和凍干粉中,沒食子酸平均得率分別為0.327%、0.322%、0.320%;原兒茶酸平均得率分別為0.002 93%、0.002 86%、0.002 84%,綠原酸平均得率分別為0.003 38%、0.003 35%、0.003 31%,表兒茶素平均得率分別為0.107%、0.105%、0.104%,鞣花酸平均得率分別為0.081 6%、0.076 2%、0.079 9%。沒食子酸平均轉移率分別為86.35%、85.15%、84.60%,RSD分別為4.94%、5.14%、4.95%;原兒茶酸平均轉移率分別為87.81%、86.24%、85.63%,RSD分別為3.09%、3.97%、3.87%;綠原酸平均轉移率分別為86.45%、85.52%、84.47%,RSD分別為4.64%、4.45%、4.19%;表兒茶素平均轉移率分別為86.55%、85.63%、84.10%,RSD分別為3.99%、3.69%、4.54%;鞣花酸平均轉移率分別為85.89%、85.10%、84.10%,RSD分別為4.80%、4.51%、4.54%。

表5 15批QBD煎煮液、濃縮液和凍干粉中有效成分得率
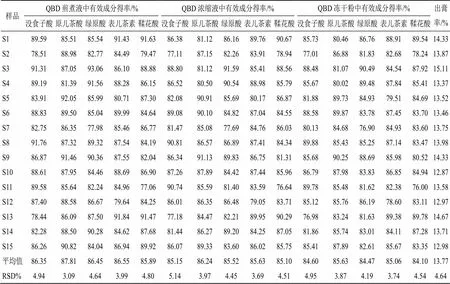
表6 QBD凍干粉制備過程中有效成分轉移率及出膏率
2.4.4 出膏率的測定[10]測定15批凍干粉的出膏率(出膏率=凍干粉干膏質量/飲片投料量),結果見表6。15批凍干粉平均出膏率為13.77%,RSD為4.64%,未出現離散數據,說明該制備工藝較合理,未造成明顯的批間差異。
2.5 基于化學計量學的QBD質量分析
2.5.1 主成分分析(principal component analysis,PCA)[19-22]將15批樣品峰面積信息經Z-Score標準化后獲得的數據矩陣導入SIMCA 14.1軟件中,進行PCA。15個樣品的二維PCA得分圖見圖3,從PCA得分圖可以清楚地看出,15批樣品被分成了3類,S1~S8屬于四川產地,S9~S12屬于福建產地,S13~S15屬于廣東產地。PCA結果駁斥了指紋圖譜的高相似性,縱然指紋圖譜顯示15批次樣品的相似度很高,但是它們仍舊被分成了3類。此外,分成的3類正好和樣品的產地有著密不可分的關系,而同一產地幾個批次的樣品都很好的聚集在一起,說明產地影響著這些樣品的質量。
2.5.2 聚類分析[19,23-24]從PCA評分圖來看,不同產地樣品是有差異的。聚類分析被用來再次驗證這一結果,因為聚類分析提供了不同產地樣品之間的相似性和變化的明確度量,顯示了復雜的數據相互關系。將不同產地的15批凍干粉指紋圖譜數據中的24個共有峰的峰面積導入SIMCA 14.1軟件中,進行聚類分析。聚類結果見圖4,以縱軸為參考依據,左邊3批樣品在數值小于1的時候已經聚攏,中間幾批樣品在數值約等于1的時候聚攏,右邊幾批樣品在數值明顯大于1的時候才聚攏,表明不同產地樣品屬不同類別,飲片的產地歸屬和內在質量差異有待進一步考察分析。
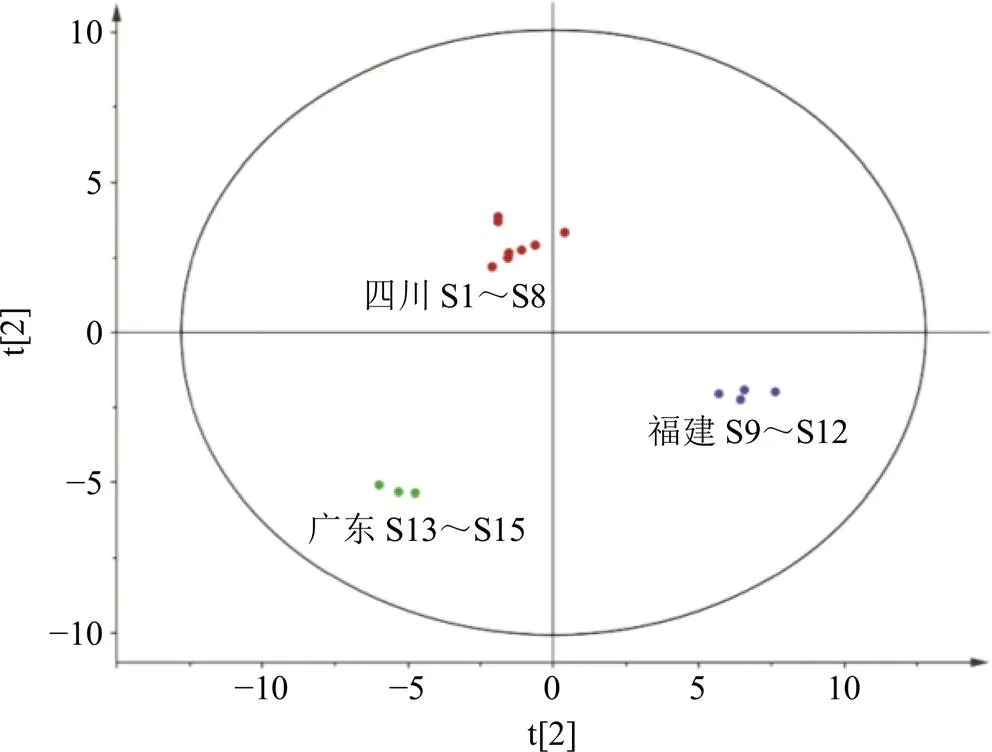
圖3 15批QBD凍干粉PCA評分圖
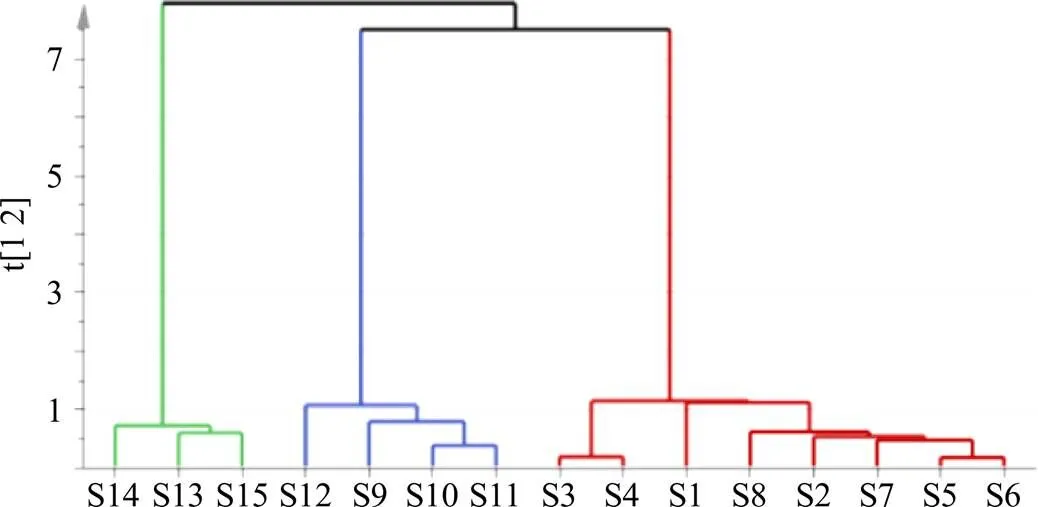
圖4 15批QBD凍干粉聚類分析
2.5.3 正交偏最小二乘-判別分析(orthogonal partial least squares-discriminant analysis,OPLS-DA)[25-27]采用有監督的OPLS-DA模型進行建模分析,篩選出對上述樣本分類貢獻較大的成分,為了確定每個變量對于辨別和獲得化學標記的重要性,以變量重要性投影值(variable importance in project,VIP,即該變量對整體模型的貢獻度高于平均水平)為有意義變量進行搜尋。VIP>1.0通常被用作衡量某個成分對差異的貢獻的共同閾值[28]。本實驗中,發現VIP>1的有9個峰,按照VIP值大小依次為峰14(表兒茶素)、1(沒食子酸)、23(鞣花酸)、9、16、24、22、8(綠原酸)、21,見圖5。同時峰4(原兒茶酸)的VIP值接近1(VIP=0.887),說明表兒茶素、沒食子酸、鞣花酸、綠原酸和原兒茶酸是影響樣品的主要成分,將這5種成分作為指導QBD湯劑凍干粉的定量質控指標。

圖5 24個共有峰的VIP值
3 討論
3.1 色譜條件的選擇
本實驗綜合考察了甲醇-0.1%磷酸水溶液、乙腈-0.1%磷酸水溶液、乙腈-0.5%磷酸水溶液、乙腈-水4種流動相、波長(214、237、254、273、280、306 nm)、柱溫(25、30、35 ℃)、體積流量(0.8、1.0 mL/min)以及色譜柱(Thermo Hypersil Gold C18(250 mm×4.6 mm,5 μm)、AcclaimTM120 C18(250 mm×4.6 mm,5 μm)等因素,結果表明在流動相為乙腈-0.1%磷酸水溶液、波長237 nm、柱溫30 ℃、體積流量為1.0 mL/min、色譜柱為AcclaimTM120 C18(250 mm×4.6 mm,5 μm)等條件下色譜峰峰形、分離度及出峰數量等較優,同時色譜圖基線更平穩,各峰之間的比例比較協調,直觀效果較好。在綜合考察峰形、基線等多項干擾因素下,確定此色譜條件進行指紋圖譜及含測相關研究。
3.2 指標成分的確定
QBD組方精簡,方中以青果中的酚類成分含量最高,為其主要藥效成分,天然硫苷是萊菔中的主要特征性化學成分[29]。結合相關文獻查閱[30-33],參照《中國藥典》2020年版[1]中對青果飲片明確規定的沒食子酸指標成分,并采用化學指紋圖譜與多成分含量測定相結合進一步確定該方與藥效相關聯的關鍵成分。因方中青果為歷版藥典收載中藥,萊菔為人們經常食用的蔬菜,因此本實驗對全方的質量控制研究側重在青果。青果中的多酚類成分如沒食子酸、綠原酸、原兒茶酸、表兒茶素和鞣花酸是發揮清熱解毒、利咽、抗氧化的主要成分[34-36],沒食子酸還為主要抗菌活性成分[34]。
本實驗通過建立HPLC指紋圖譜,從定性和定量2個層面對QBD進行質量控制,在定量指標成分選擇方面,由于后期發現東莨菪內酯峰型不太好且在標準湯劑中含量極微不好進行定量研究。綜合分析,選擇含量相對較高的主要藥效成分沒食子酸、綠原酸、原兒茶酸、表兒茶素和鞣花酸作為QBD凍干粉的含測指標,評價凍干粉批次間的一致性,有利于控制其質量穩定性。
此外,研究發現即使經過初步篩選并優化QBD梯度洗脫條件,色譜圖中也只顯示出萊菔中的唯一特征峰。課題組接下來將通過解吸電噴霧電離-離子化質譜成像技術(desorption electrospray ionization- mass spectrometry imaging,DESI-MSI)[37]、紫外-可見分光光度法等對HPLC未能檢測的未知成分如青果萊菔合煎后產生的新物質及萊菔中的天然硫苷類成分等進行分析鑒定,以更全面控制QBD凍干粉的質量。
3.3 檢測結果分析
指紋圖譜結果表明,飲片、煎煮液、濃縮液和凍干粉的相似度均大于0.9,一致性良好。QBD凍干粉指標成分質量分數為沒食子酸0.239%~0.435%、原兒茶酸0.002 31%~0.004 35%、綠原酸0.002 57%~0.004 43%、表兒茶素0.090 0%~0.128%、鞣花酸0.049 6%~0.112%。含量測定結果表明,15批QBD凍干粉樣品含量較高的3種成分中,沒食子酸含量的平均值為S5~S8>S9~S12>S1~S4>S13~S15,表兒茶素含量的平均值為S9~S12>S13~S15>S5~S8>S1~S4,鞣花酸含量的平均值為S5~S8>S13~S15>S1~S4>S9~S12。分析造成此含量差異的原因可能是產地不同所導致,化學計量學結果驗證了分析的合理性。PCA及HCA結果都表明了產地的不同導致15批樣品聚集成不同類別,也為后續實驗開展選擇青果產地來源明確了方向。
此外,通過OPLS-DA找到的VIP值大于1的已知成分表兒茶素、沒食子酸、鞣花酸和綠原酸是對區分不同批次樣品質量具有較大貢獻的幾個主要成分,此外其他VIP值大于1的未知成分將會是課題組接下來需要重點關注的部分。通過化學計量學發現萊菔的特征峰(峰6)的VIP值遠小于1,認定此峰可能不是影響QBD質量的主要成分,因此可將其作為定量因素進行研究。QBD凍干粉指標成分的含量范圍與轉移率范圍的結果表明指標成分轉移穩定可控。
因提取溶媒為水,5種指標成分極性較強且轉移率較高,說明煎煮、濃縮和凍干工藝較穩定,未造成有效成分的明顯損失[38]。在量質傳遞過程中,凍干粉具備穩定、均一的優勢,能很好地表達原方信息,而且便于儲存,可為QBD凍干粉后續作為物質基準的深入研究提供依據。
本研究所建立的QBD的HPLC特征圖譜、有效成分的含量測定和量質傳遞方法等質控手段,共同作為QBD的質量控制方法。在藥食同源名方的研發中,控制原藥材質量的均一性尤為重要,為進一步縮小指標成分含量的范圍,除了對產地進行分析外,還應展開對采收季節和采收年份等外界因素的分析研究。此外,若藥材因產地或批次不同而質量差異較大時,可固定產地或控制藥材的含量限度范圍,并且在生產加工中可采取飲片均一化投料的方法,可有效實現質量控制,有利于確切反映QBD的質量變化屬性,從而確保其功效的穩健發揮,為QBD復方制劑及大健康產品的開發研究提供可靠的質量評價依據。
利益沖突 所有作者均聲明不存在利益沖突
[1] 中國藥典 [S]. 一部. 2020: 206.
[2] Chen F Z, Yang L P, Huang Y N,. Isocorilagin, isolated from(Lour.) Raeusch, as a potent neuraminidase inhibitor against influenza A virus [J]., 2020, 523(1):183-189.
[3] Duan W J, Tan S Y, Chen J,. Isolation of anti-HIV components fromfruits by high-speed counter-current chromatography [J]., 2013, 46(7): 1057-1068.
[4] 蔣全德, 王景杰, 劉琳娜, 等. 白蘿卜提取物對大鼠胃排空、腸推進及豚鼠離體回腸平滑肌的影響 [J]. 山西醫科大學學報, 2007, 38(3): 215-217,257.
[5] 張旭, 馬波, 杜鋼軍, 等. 白蘿卜提取物對小鼠胃排空、腸推進及家兔離體回腸平滑肌的影響 [J]. 河南大學學報: 醫學版, 2011, 30(1): 36-38.
[6] 任秦有, 王勝智, 張超, 等. 萊菔提取物對功能性消化不良患者胃運動功能的影響 [J]. 貴陽中醫學院學報, 2011, 33(2): 15-17.
[7] (清) 王士雄著. 陸士諤輯. 達美君等校注. 王孟英醫案卷二 [M]. 北京: 中國中醫藥出版社, 1997: 39.
[8] 江華娟, 李敏敏, 何瑤, 等. 基于HPLC指紋圖譜和化學模式識別的經典名方桃紅四物湯制備過程質量評價研究 [J]. 中草藥, 2021, 52(4): 1000-1010.
[9] 樊啟猛, 賀鵬, 李海英, 等. 經典名方物質基準研制的關鍵技術分析 [J]. 中國實驗方劑學雜志, 2019, 25(15): 202-209.
[10] 周菲, 林美斯, 王琳, 等. 經典名方百合地黃湯物質基準制備及過程質量控制研究 [J]. 中草藥, 2019, 50(16): 3824-3832.
[11] 國家藥品監督管理局. 關于發布古代經典名方中藥復方制劑簡化注冊審批管理規定的公告 (2018年第27號) [EB/OL]. [2018-06-01]. http://www.nmpa.gov.cn/ WS04/CL2138/228247. html.
[12] 陳蒙, 林龍飛, 劉宇靈, 等. 經典名方苓桂術甘湯HPLC指紋圖譜的建立及3種成分含量測定 [J]. 中草藥, 2019, 50(17): 4152-4157.
[13] 閆莉. 青龍白虎利咽含片的藥學研究 [D].成都: 成都中醫藥大學, 2013.
[14] 閆莉, 傅超美, 季寧平, 等. 青龍白虎利咽含片的提取工藝研究 [J]. 中藥與臨床, 2012, 3(5): 18-21.
[15] 游宇, 羅林, 傅超美, 等. 青龍白虎保健飲料的研制 [J]. 中藥與臨床, 2018, 9(2): 20-22.
[16] 田萍, 位恒超, 韓德恩, 等. 真武湯HPLC-ELSD指紋圖譜及13種成分含量測定研究 [J]. 中草藥, 2020, 51(23): 5980-5989.
[17] 孟哲, 王麗君, 黃洋, 等. 中藥三七不同藥用部位的指紋圖譜及模式識別研究 [J]. 中國藥學雜志, 2020, 55(7): 504-509.
[18] Cao X X, Sun L L, Li D,. Quality evaluation ofby fingerprint chemical pattern recognition [J]., 2018, 23(9): E2307.
[19] 李雙雙, 李雙, 楊建明, 等. RP-HPLC法測定桃紅四物湯提取物中9種水溶性活性成分的含量 [J]. 中藥新藥與臨床藥理, 2017, 28(3): 364-367.
[20] 李耀磊, 左甜甜, 徐健, 等. 基于ICP-MS法對4種動物源性藥材中16種無機元素的測定及量變規律研究 [J]. 藥物評價研究, 2020, 43(2): 248-254.
[21] 劉沖, 劉蔭貞, 樂智勇, 等. 桂枝飲片標準湯劑質量標準研究 [J]. 中草藥, 2017, 48(8): 1577-1583.
[22] Shen J, Li P, He C N,. Simultaneous determination of 15 flavonoids from different parts ofand its chemometrics analysis [J]., 2019, 11(1): 20-27.
[23] Chen Z, Li Q, Yu Z,. Analysis of the similarities and differences betweenandrhizomes by chemical profiling and chemometric analysis [J]., 2020, 255: 112719.
[24] Gu F, Hall P, Miles N J. Performance evaluation for composites based on recycled polypropylene using principal component analysis and cluster analysis [J]., 2016, 115: 343-353.
[25] 徐男, 孫蓉, 崔煥月, 等. 化學計量學結合信息熵賦權優選半夏白術天麻湯提取工藝 [J]. 中草藥, 2020, 51(4): 995-1002.
[26] 楊冰月, 彭亮, 顏永剛, 等. HPLC指紋圖譜結合化學模式識別分析不同產地款冬花生品與蜜炙品 [J]. 中草藥, 2018, 49(21): 4991-4997.
[27] 肖琳婧, 劉瑩瑩, 趙禹, 等. HPLC指紋圖譜結合化學計量學的不同產地燈盞花藥材和近緣種樣品的質量評價 [J]. 中草藥, 2019, 50(14): 3438-3443.
[28] 聶欣, 龐蘭, 江華娟, 等. 經典名方化肝煎物質基準特征圖譜及多指標成分含量測定研究 [J]. 中草藥, 2020, 51(20): 5177-5186.
[29] 余輝攀. 萊菔化學成分和牡丹花提取物制備工藝及質量控制方法研究 [D]. 北京: 北京中醫藥大學, 2014.
[30] He Z Y, Xia W S. Analysis of phenolic compounds in Chinese olive (L.) fruit by RPHPLC- DAD-ESI-MS [J]., 2007, 105(3): 1307-1311.
[31] 姚瑞祺. 青果多酚的提取、分離及體外抗氧化活性研究[D]. 西安: 陜西師范大學, 2009.
[32] Chang Q, Su M H, Chen Q X,. Physicochemical properties and antioxidant capacity of Chinese olive (L.) cultivars [J]., 2017, 82(6): 1369-1377.
[33] 王恒, 宋良科, 湯昊, 等. 不同種質青果清熱利咽化學組分的研究 [J]. 中國中藥雜志, 2010, 35(6): 669-672.
[34] 孔庚星, 張鑫, 陳楚城, 等. 青果抗乙肝病毒成分研究 [J]. 解放軍廣州醫高專學報, 1997(2): 84-86.
[35] 張亮亮, 楊志偉, 林益明. 橄欖多酚抗氧化活性研究 [J]. 食品工業科技, 2008, 29(4): 57-59.
[36] 袁劍剛, 劉昕, 湯展球. 橄欖的抑菌效應及其藥效成分的初步研究 [J]. 食品科學, 2001, 22(3): 82-84.
[37] 曲緣章, 孫博, 朱廣偉, 等. DESI-MSI技術在經典名方芍藥甘草湯質量控制中應用研究 [J]. 中草藥, 2020, 51(13): 3433-3443.
[38] 洪婷婷, 張鈺明, 楊琳潔, 等. 經典名方半夏瀉心湯水煎液的HPLC指紋圖譜及黃芩、黃連量值傳遞研究 [J]. 中草藥, 2020, 51(20): 5166-5176.
Research on quality control of famous prescription with medicine and food homology of Qinglong Baihu Decoction based on quantity-quality-correlation and chemometrics
CHEN Jiao1, WANG Ji-sen2, DENG Jing-jing1, ZHU Zong-ping1, LIAO Wan1, CHEN Yi1, YANG Qing-song1, WANG Lin1, FU Chao-mei1, ZHU Ya-ning1, 3
1. State Key Laboratory of Southwestern Chinese Medicine Resources, School of Pharmacy, Chengdu University of Traditional Chinese Medicine, Chengdu 611137, China 2. Chengdu Institute of Food and Drug Inspection, Chengdu 610045, China 3. Ya’an Sanjiu Pharmaceutical Co., Ltd., Ya’an 625000, China
To explore the preparation process of lyophilized powder of Qinglong Baihu Decoction (青龍白虎湯, QBD) and the law of quantity-quality-correlation by establishing an HPLC fingerprint detection method, and build its quality control system combined with chemometrics.Fifteen batches of QBD lyophilized powder were prepared, the fingerprints were established by HPLC method, then imported the chromatographic results into(2012) and calculated the similarity of each part. The content of gallic acid, protocatechuic acid, chlorogenic acid, epicatechin, and ellagic acid were detected during the quantity-quality-correlation of 15 batches of samples, and the transfer rate and extractum rate were calculated. Combined with the chemometrics methods, the main components of samples from different producing areas which had significant contribution to the quality control were analyzed.The similarity of the fingerprints of 15 batches of samples was > 0.9, which met the specified requirements, and the 24 common peaks of the fingerprints of the lyophilized powder were calibrated, and six of them were identified, they were gallic acid (peak 1), protocatechuic acid (peak 4), chlorogenic acid (peak 8), epicatechin (peak 14), scopoletin (peak 19), and ellagic acid (peak 23). The content range of these components in 15 batches of lyophilized powder were 0.724%—1.301% epicatechin, 2.184%—2.840% gallic acid, 0.607%—0.760% ellagic acid, 0.061%—0.141% chlorogenic acid, 0.017%—0.079% protocatechuic acid, the transfer rates of epicatechin, gallic acid, ellagic acid, chlorogenic acid and protocatechuic acid were 78.60%—89.38%, 76.98%—89.88%, 76.00%—89.78%, 76.90%—90.49%, 80.02%—90.25% respectively, the extractum rate was 12.87%—15.11%, and without discrete data. It showed that during the process of decoction, concentration and lyophilized powder, the transfer rates of effective components were stable. Through chemometrics analysis, it was found that 10 component scontributed significantly to the model, including the designated peak 14 (VIP = 2.812), peak 1 (VIP = 2.804), peak 23 (VIP = 2.715), peak 8 (VIP = 1.053) and peak 4 (VIP = 0.887), which can further deepen the quality control research of QBD.The quality control method of the famous prescription with medicine and food homology of QBD was established for the first time through the HPLC fingerprint combined with the content determination of multiple index components. This method is rapid, simple, feasible, reproducible, stable and it can be applied to the correlation investigation of the quantity-quality-correlation law of decoction pieces, decoction, concentrate and lyophilized powder at the same time; Further through the chemometrics, which provided an important reference for the quality control research of QBD.
Qinglong Baihu Decoction; quantity-quality-correlation; fingerprint; chemometrics; gallic acid; protocatechuic acid; chlorogenic acid; epicatechin; ellagic acid; quality control
R283.6
A
0253 - 2670(2021)13 - 3872 - 13
10.7501/j.issn.0253-2670.2021.13.011
2021-02-25
四川省中醫藥管理局中醫藥開發專項(2018KF001);四川省科技廳國際合作項目(2018HH0122);成都市科技局國際科技合作項目(2017-GH02-00054-HZ);成都中醫藥大學科技轉化項目(CGPY1605)
陳 姣,女,碩士研究生,研究方向為中藥新制劑和新劑型研究。Tel: 18428303508 E-mail: 1922702305@qq.com
廖 婉,女,博士,教授,碩士生導師,主要從事新制劑、新劑型及中藥炮制工藝與機制研究。E-mail: liaowan2011@126.com
朱雅寧,高級工程師,博士生導師,研究方向為中藥理論、制藥技術與應用研究。E-mail: 676640058@qq.com
#共同第一作者:王繼森,男,主管藥師,碩士,從事藥品檢驗研究工作。E-mail: 93230623@qq.com
[責任編輯 鄭禮勝]