毛細管電泳法結合化學計量學分析評價云芝胞內糖肽的質量
孫玉娣,張圓,王文濤,石蓓佳,,陸益紅,*,李志裕*(.中國藥科大學藥學院,南京 0000;.江蘇省食品藥品監督檢驗研究院生物技術藥品檢驗一室,南京 009;.SCIEX中國,上海 00000)
云芝胞內糖肽是運用現代生物工程技術,雜色云芝菌[Polystictus versicolor(L).Fr.,又名Trametes versicolor]經深層培養后,菌體提取獲得的糖肽類物質,其具有增強機體免疫的功效,在臨床可用于慢性乙型肝炎、肝癌及老年免疫功能低下者的輔助治療。由于云芝胞內糖肽為大分子混合物,組成復雜,含有蛋白質、脂肪、多糖、葡聚糖、糖肽、氨基酸和無機鹽等物質[1],因此對云芝胞內糖肽的分離分析具有一定難度。有文獻報道糖類結構中的鄰二羥基與硼酸根離子可結合形成帶負電荷的絡合物,根據絡合物淌度的不同可實現毛細管電泳(CE)的有效分離[2]。除此之外,CE不受色譜填料對分子量的制約,在不破壞糖肽結構的前提下,通過特征的糖肽指紋圖譜體現其組成,對確保云芝胞內糖肽制劑的工藝穩定性具有積極作用。本試驗采用CE法,分離檢測云芝胞內糖肽原料及制劑特征色譜峰,用ChemPattern軟件建立指紋圖譜,對結果進行主成分分析(PCA)和系統聚類分析(HCA),為云芝胞內糖肽膠囊(片)的質量評價提供參考。
1 材料
SCIEX PA 800 Plus 毛細管電泳分析儀,二極管陣列檢測器(DAD);ChemPattern 2020版(科邁恩科技)。云芝胞內糖肽膠囊(片)(共計18批,原料均來自于A廠家,具體見表1),菌絲體水提醇沉產物1,培養液濾液醇沉產物2(以下簡稱產物1、產物2,A廠家),云芝胞內糖肽原料(Q廠家,批號:S-30200601),云芝胞內糖肽對照品(批號:140692-200301,原料來自Q廠家)。由于生產工藝的差異,A廠家原料中含有產物1和產物2,Q廠家原料中僅含有產物1。

表1 云芝胞內糖肽來源Tab 1 Source of coriolus versicolor intracellular glycopeptide
2 方法與結果
2.1 供試品溶液的制備
取云芝胞內糖肽膠囊內容物、云芝胞內糖肽片樣品研細,精密稱取10 mg,對照品、原料藥、產物1與產物2直接精密稱取10 mg,置于1.5 mL離心管中,加入1 mL去離子水,渦旋混勻后,3000 r·min-1離心5 min,取上清液進行分析。
2.2 電泳條件
石英毛細管(60.2 cm×75 μm,有效長度 50 cm);運行電壓15 kV;紫外檢測波長200 nm;背景電解質溶液(BGE)為50 mmol·L-1四硼酸鈉,pH 9.18;樣品緩沖液H2O;毛細管溫度25℃;樣品室溫度25℃;進樣條件0.5 psi 5 s;熔融石英毛細管初次使用時,依次用0.1 mol·L-1氫氧化鈉溶液、0.1 mol·L-1鹽酸溶液和二次去離子水在20 psi下各沖洗5 min,最后用BGE在20 psi下沖洗5 min,并在15 kV電壓下平衡10 min。在每針運行之間依次用0.1 mol·L-1氫氧化鈉溶液、0.1 mol·L-1鹽酸溶液和水在20 psi條件下各沖洗3 min,最后用BGE在20 psi下沖洗5 min。數據處理采用32 Karat軟件[3-4]。
2.3 數據分析
采用ChemPattern軟件,以A廠家制劑樣品中6個特征峰(保留時間分別為8.9、12.8、14.4、17.2、17.8、24.9 min)的峰面積建立共有模式,對樣本進行PCA和HCA分析[5-6]。
2.4 方法學驗證
2.4.1 進樣精密度試驗 取A企業原料(批號:20200101),按“2.1”項下方法制備供試品溶液,按“2.2”項下條件連續進樣6次,計算各峰峰面積的RSD(n=6)。結果顯示,各峰峰面積的RSD均小于1.0%,各峰相對保留時間的RSD均小于1.5%,表明該儀器進樣精密度良好。
2.4.2 穩定性試驗 取A企業原料(批號:20200101),按“2.1”項下方法制備供試品溶液,分別在0、4、8、12、18、24 h按“2.2”項下條件進樣分析,計算各峰峰面積的RSD(n=6)。結果顯示,各峰峰面積的RSD均小于0.3%,各峰相對保留時間的RSD均小于1.7%,表明供試品溶液在24 h內穩定。
2.4.3 重復性試驗 取A企業原料(批號:20200101),按“2.1”項下方法平行制備6份供試品溶液,按“2.2”項下條件進行分析,計算各峰峰面積的RSD(n=6)。結果顯示,各峰峰面積的RSD均小于1.0%,各峰相對保留時間的RSD均小于1.8%,表明該方法重復性良好。
2.5 毛細管電泳指紋圖譜的建立
2.5.1 樣品疊加圖譜的生成 取5個廠家云芝胞內糖肽膠囊(片)各1批,A廠家提供的產物1、產物2,Q廠家原料和對照品分別按“2.1”項下方法制成供試品溶液,按“2.2”項下條件進樣分析,記錄CE色譜圖。采用ChemPattern軟件,對圖譜進行中值基線濾波去背景,使用保留時間校正進行全峰匹配建立指紋圖譜,共有6個特征峰,見圖1。
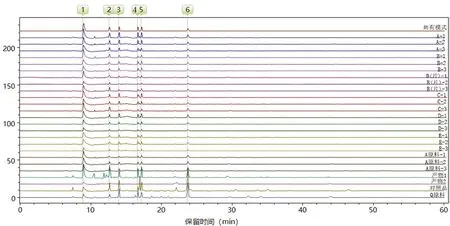
圖1 云芝胞內糖肽樣品的指紋圖譜疊加圖Fig 1 CE fingerprints of coriolus versicolor intracellular glycopeptide
2.5.2 共有模式圖譜的建立 各廠家云芝胞內糖肽制劑的原料均來自于A廠家,因此以A廠家3批樣品為代表性樣品,以A廠家圖譜的6個峰作為特征峰建立共有模式,見圖2。
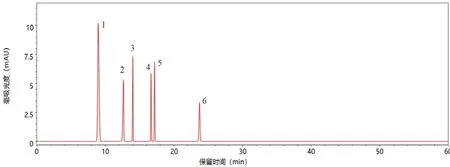
圖2 云芝胞內糖肽共有模式圖Fig 2 Common pattern of coriolus versicolor intracellular glycopeptide
2.6 毛細管電泳指紋圖譜的化學計量學分析
2.6.1 相似度分析[7-8]將18批云芝胞內糖肽膠囊(片)、A廠家原料、產物1、產物2、Q廠家原料和對照品的CE圖導入ChemPattern軟件,以共有模式圖譜為參照,計算夾角余弦相似度,結果見表2,相似度統計圖見圖3。表2結果顯示,A廠家及使用A廠家原料各廠家的制劑與共有模式相似度在0.96以上,圖3結果顯示產物2、A廠家原料及使用A廠家原料各廠家的制劑與產物1、Q廠家原料和對照品呈明顯區分。
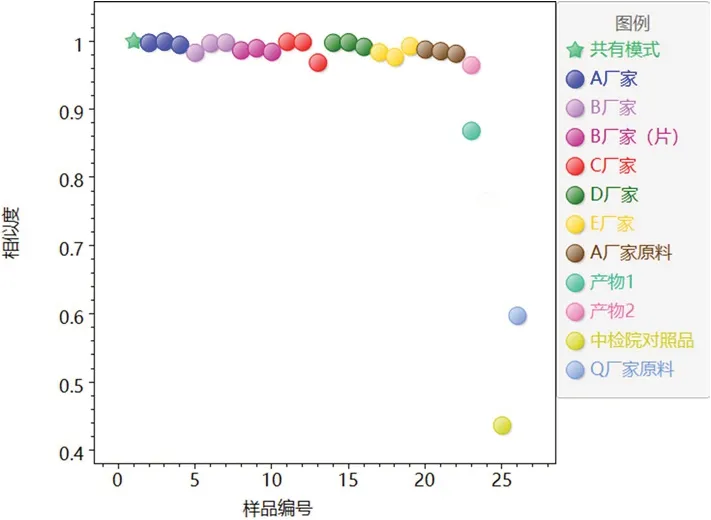
圖3 云芝胞內糖肽相似度結果統計圖Fig 3 Statistical chart of similarity of coriolus versicolor intracellular glycopeptide
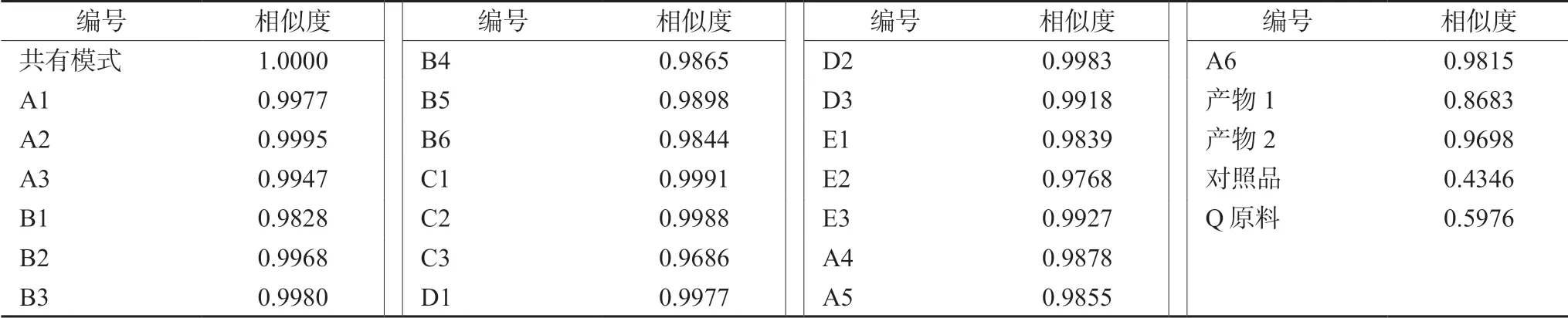
表2 相似度分析結果Tab 2 Similarity analysis
2.6.2 系統聚類分析[9-11]將所有CE圖導入Chem Pattern軟件,對圖譜進行UV標度化處理,以共有模式圖譜為參照,采用街區距離計算方法為測度,以最短距離法連接,進行HCA分析,結果見圖4。樣品間的分類距離值越大,差異性就越大。HCA樹狀圖結果表明,共有模式與A廠家原料、使用A廠家原料各廠家的制劑及產物2為一類,Q廠家原料和對照品為一類。
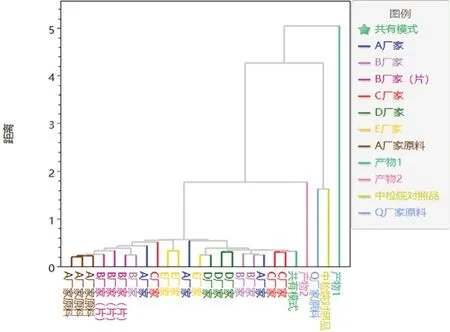
圖4 云芝胞內糖肽HCA結果圖Fig 4 HCA diagram of coriolus versicolor intracellular glycopeptide
2.6.3 主成分分析[12]使用ChemPattern軟件對圖譜進行UV標度化處理,用PCA程序分析樣品組間差異性。當提取 6個主成分時,檢驗因變量個數P=6,χ2=146.56,自由度df=15,顯著性P=0,按檢驗水平α=0.05,拒絕假設H0,差異有統計學意義。經PCA模型分析生成得分圖、載荷圖,分別見圖5~6。
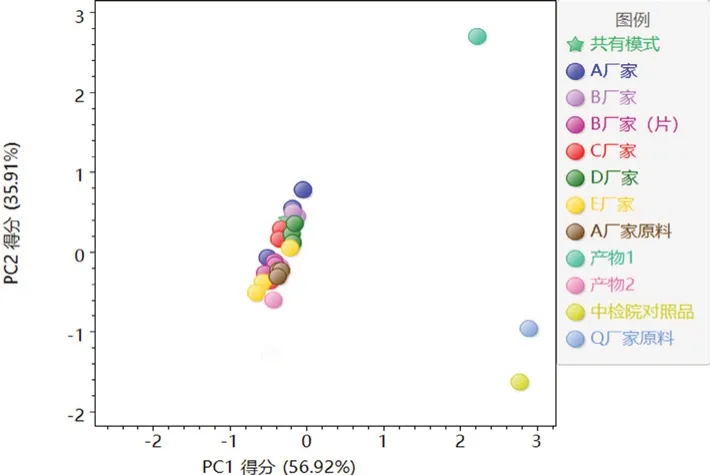
圖5 云芝胞內糖肽PCA得分圖Fig 5 PCA score diagram of coriolus versicolor intracellular glycopeptide
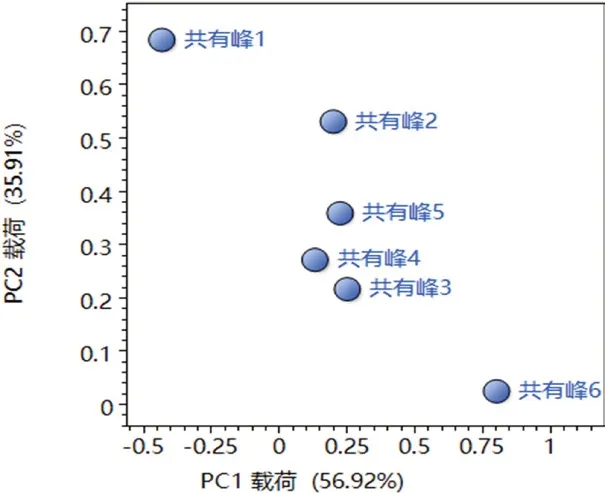
圖6 云芝胞內糖肽PCA 載荷圖Fig 6 PCA load diagram of coriolus versicolor intracellular glycopeptide
PCA得分圖中各點聚集狀態反映了樣品批之間內的異同,由圖5可知,產物2、A廠家原料及使用A廠家原料各廠家的制劑數據點與共有模式同群,說明同一原料廠家來源的制劑化學成分具有相似性。產物1、Q廠家原料和對照品與共有模式離群,說明不同生產廠家原料之間存在差異性,分類結果與HCA結果一致。結合PCA載荷圖和自變量主成分累計解釋方差表(見表3)可知,峰6為樣本識別的主要因素。
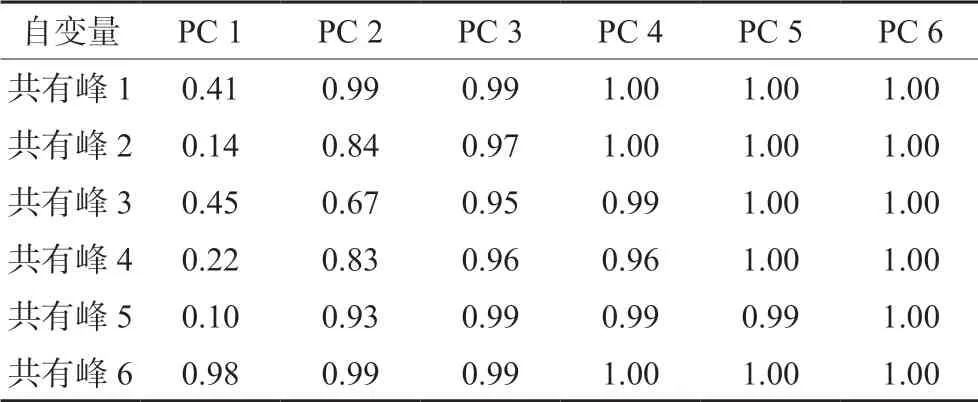
表3 自變量主成分累計解釋方差Tab 3 Principal component cumulative interpretation variance of independent variables
3 討論
本試驗采用CE法建立了5個生產廠家18批云芝胞內糖肽膠囊(片)、工藝中間產物1和產物2、對照品及兩個廠家(A、Q廠家)云芝胞內糖肽原料的指紋圖譜,采用ChemPattern軟件分析,確定6個共有峰。結果同一原料及其使用同一原料不同廠家的制劑的相似度均大于 0.96,說明云芝胞內糖肽膠囊(片)質量穩定。HCA和PCA可將樣品明顯聚類和區分,A廠家原料、使用A廠家原料各廠家的制劑和產物2間具有相似性,可聚為一類,而Q廠家原料、對照品和產物1有明顯差異,說明不同原料生產廠家之間共有峰存在差異。找到一個差異識別峰(峰6),可作為區分不同來源云芝胞內糖肽的手段。
A廠家原料生產工藝為:菌株Polystictus versicolor,28℃發酵培養40~50 h。發酵完成后,發酵液過濾分為菌絲與培養液兩部分。菌絲部分經水煮提取濾液,與培養液濾液合并。合并的濾液經濃縮、醇沉,75℃ 減壓干燥、粉碎過篩即得。制劑都是原料直接灌裝或者加乙醇濕法制粒的,無輔料干擾。將工藝中菌絲體水提醇沉即得產物1,培養液濾液醇沉即得產物2。Q廠家原料生產工藝與A廠家基本相似,但是在最后沒有與培養液濾液合并,因此沒有產物2。指紋圖譜顯示,產物1的1~6號CE特征峰均呈現較高峰,且出現多個額外的色譜峰;產物2幾乎沒有特征峰檢出。結合HCA和PCA可知,產物1因各峰面積顯著高于其他樣本而離群,對照品、Q廠家原料則因峰6峰面積高而離群。可以初步推測兩原料生產廠家的生產工藝不同是造成差異的主要原因。
CE無法對特征峰進行定性,無法確定各特征峰組成,后期可采用CE與質譜聯用技術對各未知峰進行定性分析[13-14],確定峰6的組成,針對峰6建立云芝胞內糖肽的質量控制體系,以提高產品的穩定性和一致性。
綜上所述,本研究建立的云芝胞內糖肽膠囊(片)CE指紋圖譜測定方法,經方法學驗證,準確、簡捷,具有較好的分析評價能力,可作為區分云芝胞內糖肽和質量評價的依據。

