嵌合抗原受體T細胞治療血液腫瘤所致凝血障礙及相關因素分析*
許倩文 薛磊 汪敏 強萍 王麗 徐慧 張旭晗 許漢英 劉欣 朱薇波 蔡曉燕 劉會蘭 孫自敏 楊林 王興兵
B細胞血液系統惡性腫瘤是常見的血液系統惡性腫瘤,盡管多數患者對目前的一線治療有反應,但復發率高、預后差,仍然是難治的惡性腫瘤之一[1,2]。CAR-T細胞治療,即嵌合抗原受體T細胞(chimeric antigen receptor T cells, CAR-T cells)治療技術是目前最具應用前景的治療腫瘤的新型靶向細胞治療技術之一[3],然而,作為一種免疫治療技術,免疫相關毒副反應是 CAR-T細胞治療腫瘤臨床試驗的難點,對其預防、控制及隨訪監測均存在較多問題有待解決。其中, 細胞因子釋放綜合征(cytokine release syndrome,CRS)是CAR-T細胞治療后最常見的并發癥,可表現為一般性全身反應如發熱、肌痛、關節痛、頭痛等,也可以影響到各個器官系統,嚴重者可危及生命[4]。其中,凝血功能異常是臨床上常見的表現之一。目前,針對CAR-T細胞治療后所致凝血功能異常的研究較少[5,6],本文旨在報道46例接受靶向CD19 CAR-T細胞治療的B細胞血液系統惡性腫瘤患者出現的凝血功能變化情況及其相關因素分析,以進一步提高對CAR-T細胞治療安全性的認識。
資料與方法
1 病例資料 收集2016年10月~2020年1月于中國科學技術大學附屬第一醫院(安徽醫科大學附屬省立醫院)血液內科接受靶向CD19 CAR-T細胞治療的患者臨床資料,排除標準:(1)輸注前即有凝血功能異常:包括PT(prothrombin time,PT)延長超過正常值3 s、APTT(activated partial thromboplastin time,APTT)延長超過正常值10 s或Fg(fibrinogen,Fg)<1.5 g/L);(2)治療前使用抗凝藥物;(3)有明確的感染征象或其他可引起凝血功能異常的合并癥。最終共46例患者納入本研究。本研究經本院醫學倫理委員會批準(ClinicalTrials.gov臨床試驗注冊號:NCT02851589;倫理批件號:2016倫審第101號)。所有患者或其法定監護人均已簽署臨床試驗知情同意書。
2 CAR-T細胞制備和輸注 本研究中CAR-T細胞由博生吉安科細胞技術有限公司制備,其結構包括抗CD19 scFv、CD28共刺激分子和CD3ζ信號域。通過Ficoll-PaqueTM(GE醫療集團)方法采集所納入患者的外周血單核細胞,使用CD4磁珠(Miltenyi Biotec GmbH)和CD8磁珠(Miltenyi Biotec GmbH)分選富集T細胞。接著通過慢病毒包被、T細胞轉染、CAR-T細胞培養等過程完成CAR-T細胞的制備。回輸前2周內所有患者均接受FC方案(氟達拉濱,30 mg/m2/天 ×3天;環磷酰胺,300 mg/m2/天×3天)預處理化療。29例患者為單次回輸,17例患者為逐步遞增分次回輸。4例患者接受人源化CAR-T細胞輸注,42例患者接受鼠源化CAR-T細胞輸注。
3 資料收集 通過本院電子病歷系統收集患者基線信息包括年齡、性別、疾病類型及基因突變、染色體異常、既往治療情況和輸注前腫瘤負荷等。將骨髓原始細胞比例≥5%或存在髓外浸潤定義為高腫瘤負荷,將骨髓原始細胞比例<5%但微小殘留病變(minimal residual disease, MRD)陽性定義為低腫瘤負荷。分別在預處理化療前、輸注前1天以及CAR-T細胞輸注后28天內收集患者外周血,分析全血細胞計數、D-二聚體(D-dimer,D-D)、PT、APTT、凝血酶時間(thrombin time,TT)、Fg和纖維蛋白原降解產物(fibrinogen degradation products,FDP)等水平。D-D、PT、APTT、TT、Fg、FDP的正常范圍分別為(0~0.5) mg/L、(10~14) s、(20~40)s、(1.7~4.0) g/L和(0.01~5.00) mg/L。
4 分級與分度 根據ASBMT分級標準[7]對CRS進行分級,根據常見不良反應事件評價標準CTCAE v4.0.3[8]、DIC診斷專家共識[9]及D-D相關研究[10]對凝血指標進行分級。本研究中將D-D>5 mg/L、PT延長>正常值3 s、APTT延長>正常值10 s、TT延長超過正常值、FDP>20 mg/L、Fg<1.5 g/L定義為凝血功能異常。
5 統計學處理 采用描述性統計方法描述患者特征,分類變量用計數(百分比)表示。在相關因素單因素分析中,二分類變量之間的比較采用Fisher精確概率法;兩組間服用正態分布的連續性資料采用正態分布的獨立樣本t檢驗,用均值±標準差表示;兩組間非正態分布的連續性資料采用非參數秩和檢驗,用中位數(上四分位數~下四分位數)表示。相關因素為連續型變量時采用皮爾遜相關分析;采用K-M曲線分析生存情況,采用Cox回歸分析凝血功能異常與長期生存之間的關系。雙側P值<0.05被認為有統計學意義。所有的統計分析均通過SPSS 26.0軟件進行。
結 果
1 患者臨床特征 共46例接受靶向CD19 CAR-T細胞治療的復發難治B細胞血液系統惡性腫瘤患者入組,其中男21例,女25例,中位年齡31(6~66)歲。疾病類型包括急性B淋巴細胞白血病40例、B細胞淋巴瘤5例和慢性淋巴細胞白血病1例。治療前有移植病史者10例。
2 CRS分級及凝血功能異常的發生與處理情況 所有患者均發生CRS反應,各級CRS發生率分別為1級12例(26.1%)、2級14例(30.4%)、3級15例(32.6%)、4級4例(8.7%)、5級1例(2.2%)。回輸后1月內出現凝血功能異常的患者為37例(80.4%),D-D、PT、APTT、TT、FDP最大值分別為8.66(0.31~80.00) mg/L、14.35(10.10~29.20) s、51.20(29.00~94.90) s、19.80(14.50~80.60) s、23.38(1.60~120.00) mg/L,Fg最小值為1.565(0.320~5.120) g/L。31例(67.4%)患者出現D-D升高(>5 mg/L),D-D升高的達峰時間為7(3~17)天;7例(15.2%)患者出現PT延長(>正常值3 s),達峰時間為7(6~9)天;25例(54.3%)患者出現APTT延長(>正常值10 s),達峰時間為7(1~14)天;19例(41.3%)患者出現TT延長,達峰時間為9(6~15)天;部分患者因本院DIC全套檢測項目更改,未監測FDP水平,18例監測FDP水平的患者中,12例患者(66.7%,n=18)出現FDP升高,達峰時間為6(3~13)天;22例(47.8%)患者出現Fg下降(<1.5 g/L),達谷底時間為9(9~20)天。根據2017年彌散性血管內凝血(disseminated intravascular coagulation, DIC)診斷與治療專家共識,納入的患者中有13例患者CDSS評分≥6分,診斷為DIC。4例出現DIC的患者同時出現腎功能損害,但因未進行外周異常紅細胞、Coombs試驗、血清補體、腎活檢等檢測,無法明確診斷為血栓性微血管病(thrombotic microangiopathy,TMA)。所有凝血異常均在輸注后1個月內恢復。無患者出現危及生命的出血。針對凝血異常的處理方法包括輸注血漿、冷沉淀或纖維蛋白原。其中,18例患者接受了纖維蛋白原替代治療,5例患者接受了冷沉淀輸注,28例患者接受了新鮮冰凍血漿的輸注。
3 凝血功能異常的相關因素分析 分類變量與凝血指標相關性分析結果見表1。患者性別、腫瘤類型、是否有移植病史、腫瘤負荷和回輸的CAR-T細胞種類與各項凝血指標的變化均無顯著相關性。單次回輸的患者較逐步遞增分次回輸的患者PT延長更明顯(P=0.040),見圖1。連續型變量與凝血指標相關性分析結果見表2,年齡以及輸注時血細胞水平與各項凝血指標的變化無顯著相關。輸注后的炎癥指標水平與凝血指標的變化有相關性。其中,輸注后CRP的水平與APTT、FDP相關;SF的升高水平與D-D、TT、Fg相關;白介素(interleukin, IL)-6升高與TT延長相關;IL-10升高與D-D升高、FDP升高密切相關;IL-2、干擾素(interferon, IFN)γ、腫瘤壞死因子(tumour necrosis factor,TNF)α及Granzyme B的水平與各項凝血指標均無明顯相關。進一步分析顯示,CRS等級與所有指標均有相關性,見圖2,CRS等級越高,D-D升高、PT、APTT、TT延長、FDP升高更明顯,Fg下降更明顯,其中相關性程度FDP>D-D>APTT>TT>Fg>PT。

圖1 CAR-T細胞輸注后PT最大值在單次回輸組和逐步遞增分次回輸組中具有統計學差異,逐步遞增多次回輸的患者PT延長較輕
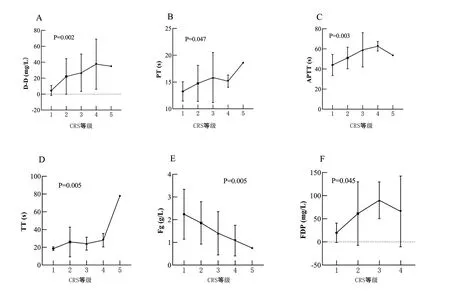
圖2 CAR-T細胞輸注后出現CRS等級與各凝血指標最大值之間均有顯著相關性,CRS等級越高,D-D升高、PT延長、APTT延長、TT延長、Fg下降、FDP升高越明顯
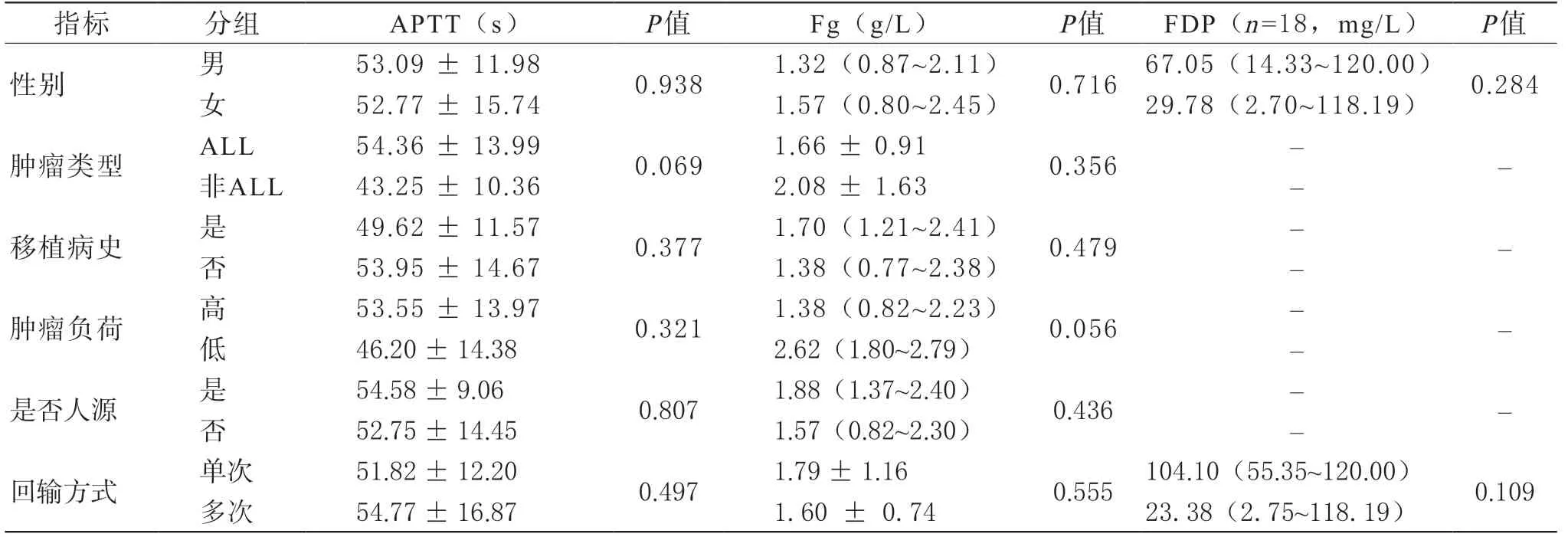
表1 (續) 分類變量與凝血指標的相關因素分析
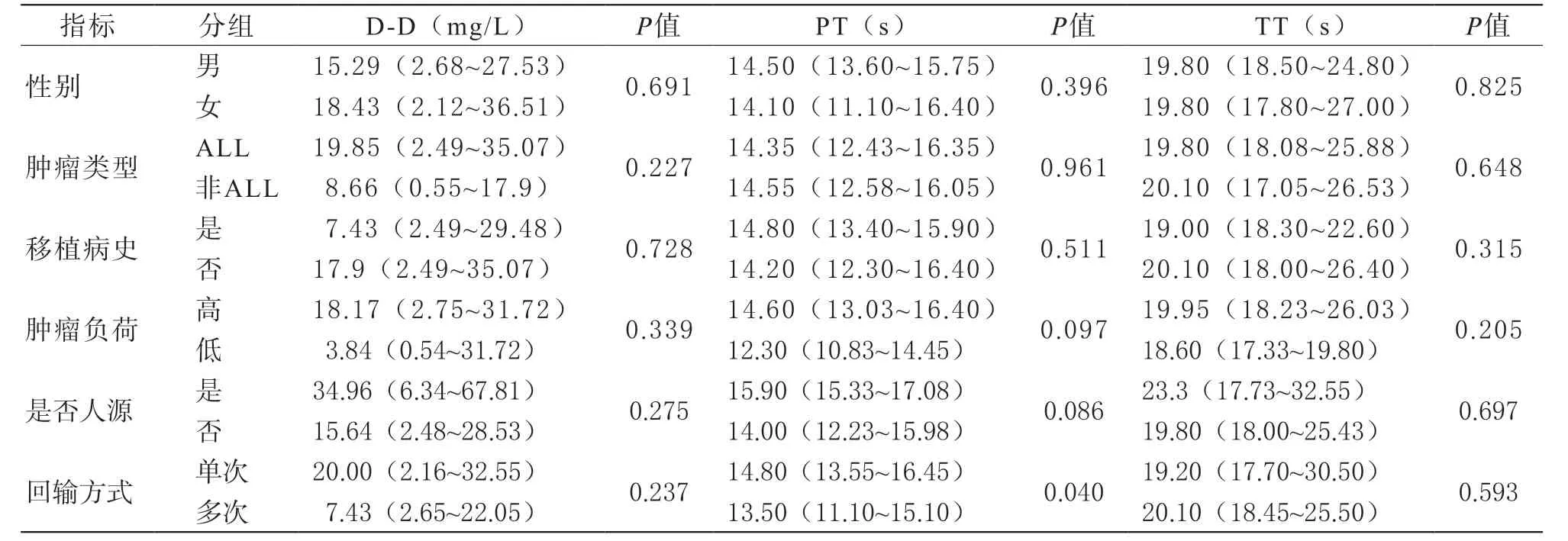
表1 分類變量與凝血指標的相關因素分析

表2 連續型變量與凝血指標的相關因素分析
我們進一步分析了DIC的發生與CRS嚴重程度的相關性。因ASBMT分級標準未將凝血功能異常納入,我們根據Penn分級系統對CRS進行分級,將≥3級CRS定義為重度,<3級CRS定義為輕度。結果顯示DIC的發生與嚴重CRS具有顯著相關性(表3,P<0.001)。

表3 DIC與CRS嚴重程度相關因素分析
4 凝血功能異常與長期生存的相關因素分析 納入的46名患者中,3例治療無效,1例因不良反應較重,治療后2周內去世,無法評估療效,總CR率為91.3%(42/46)。ALL患者CR率為92.5%(37/40),獲得CR的患者在11.4個月的中位隨訪時間內(范圍:1.2~41.1個月),中位EFS和OS分別為10和20.4個月,1年EFS率和OS率分別為40.6%和62.2%;對總患者進行長期生存的相關因素分析(表4),結果提示治療后D-D的峰值(P=0.014)、FDP峰值(P=0.022)、Fg谷值(P=0.024)與EFS有顯著相關性,各項凝血指標與OS均無顯著相關性。 進一步分析提示DIC的發生與否與EFS(P=0.872)和OS(P=0.263)均無顯著相關性。

表4 凝血指標與EFS及OS相關因素分析
討 論
在目前的臨床試驗中,CAR-T細胞治療血液系統惡性腫瘤后凝血功能異常的發生率較高[6,11-13],我們的研究中,37例(80.4%)患者出現凝血指標異常。誘發凝血功能異常的常見病因包括嚴重感染、外傷、惡性腫瘤等[9]。相關研究顯示,炎癥反應與凝血功能之間也存在密切聯系[14]。炎癥誘導凝血激活的主要介質是促炎細胞因子,例如,IL-6、TNF-α和IL-1在凝血機制中起了重要作用[15-17]。CAR-T細胞治療后會引起廣泛性免疫激活以及血清炎癥標志物如C反應蛋白(C-reactive protein,CRP)、血清鐵蛋白(serum ferritin,SF)及炎癥因子如IFN-γ、IL-6、IL-8、IL-10等水平顯著升高[18],從而影響各器官系統功能。血小板內皮細胞粘附分子(platelet endothelial cell adhesion molecule,PECAM-1)是一種在內皮細胞間連接處高度表達并維持血管內皮完整性的分子[19],大量釋放的炎性因子會破壞血管內皮細胞及內皮屏障的完整性,導致細胞表面PECAM-1減少,血漿可溶性PECAM-1升高[20]。并且內皮損傷會導致組織因子(tissue factor,TF)過度表達,激活外源性凝血途徑[21]。研究顯示發生嚴重凝血功能障礙患者血漿的TF和PECAM-1濃度同步升高[21],這證實大量細胞因子釋放可導致血管內皮細胞功能障礙,破壞內皮屏障的完整性,從而出現凝血功能障礙[22]。我們的研究發現,輸注后的炎癥標志物如CRP、SF及炎癥因子包括IL-6、IL-10水平與凝血指標的變化具有明顯相關性,其他類似的研究同樣提示CRP、SF、IL-6與凝血指標的變化有關[6,23]。進一步分析提示CRS的嚴重程度與凝血指標的變化有明顯相關性,CRS等級越高,D-D升高、PT延長、APTT延長、TT延長、Fg下降、FDP升高則越明顯,且嚴重CRS與DIC的發生有著明顯的相關性。在本研究中,我們觀察到細胞因子和炎癥標志物的升高與凝血功能紊亂的嚴重程度相關,另一方面,IL-6、CRP和SF在出現嚴重CRS的患者血清中明顯升高,尤其是IL-6似乎在CRS的病理生理過程中起著關鍵作用[24,25]。這些結果進一步證實了CAR-T細胞治療后的CRS、炎癥因子升高以及凝血功能異常之間的密切聯系。
值得一提的是,我們還發現劑量遞增分次回輸CAR-T細胞可以減輕細胞輸注后的PT延長。患者首先接受低劑量的CAR-T細胞,如果沒有觀察到明顯的不良反應,再予以更高的劑量輸注。這種回輸方式或許可以通過減輕腫瘤負荷來減輕輸注后的炎癥反應,從而減輕凝血功能異常。由于CAR-T細胞治療的藥代動力學和毒性反應有顯著的個體差異性,劑量遞增分次回輸也許是一種可以減輕不良反應的回輸方式[26],但仍需更多的樣本量來進一步證實。
本研究中,凝血功能異常主要發生在細胞輸注后1月以內,經對癥處理均可恢復正常。WANG等人報道凝血障礙主要發生在CAR-T細胞輸注后第6~20天[6],MEI等人報道D-D、FDP和APTT水平在輸注后第8天和第9天達到峰值[5],我們觀察到的凝血參數的變化與他們的相似。因此,臨床上應警惕接受CAR-T細胞后的患者出現凝血功能障礙,特別是在輸注后1~3周之間。
本研究納入的患者中,共18名患者接受了纖維蛋白原輸注,多為出現3級及以上CRS且Fg<1.5 g/L,或有明顯的出血癥狀的患者;部分患者同時接受了冷沉淀的輸注。對于PT、APTT明顯延長的患者予以輸注新鮮冰凍血漿。根據最新的文獻報道[27],低纖維蛋白原是CRS相關性凝血障礙的一個敏感的指標,建議在3級或4級CRS期間和之后加強監測,并且對纖維蛋白原<1.5 g/L的患者予以纖維蛋白原替代治療。對于出血風險高或者已出現較嚴重出血癥狀的患者接受纖維蛋白原輸注也是可以的,可以降低出血風險。根據治療CRS相關性凝血障礙和低纖維蛋白原血癥的臨床指南,也可以用冷沉淀或纖維蛋白原濃縮物替代纖維蛋白原[27]。本研究中,盡管未發現DIC的發生與長期生存之間的相關性,但D-D、Fg、FDP的異常水平能一定程度上影響EFS,所以對于CAR-T細胞治療的患者,尤其是術后出現較重CRS、明顯的凝血功能異常或DIC的患者,建議加強監測纖維蛋白原、PT、APTT、血小板水平和臨床出血情況,及時進行干預,以防止在嚴重血小板減少和凝血障礙的情況下增加出血風險,影響患者的長期預后情況。
總的來說,我們的研究表明CAR-T細胞輸注后的凝血功能障礙較常見,且與CRS嚴重程度及輸注后的細胞因子水平密切相關,選擇逐步遞增分次回輸的方式可以減輕輸注后的凝血功能異常。早期識別和有效及時的處理對于控制凝血功能障礙引起的更嚴重并發癥是至關重要的。
利益沖突所有作者均聲明不存在利益沖突

