一期斜外側腰椎椎間融合術聯合Wiltse入路椎弓根螺釘固定治療非特異性腰椎間隙感染
高放 熊偉 李鋒 方忠
非特異性腰椎間隙感染是指椎間盤及相鄰軟骨板的感染性病變,又稱為化膿性椎間盤炎。由于脊柱有創操作增加、人口老齡化、靜脈藥物濫用等原因,椎間隙感染的發病率呈上升趨勢[1]。非特異性腰椎間隙感染病人的臨床癥狀和體征多無特異性,也難以借助實驗室及影像學檢查結果與結核、布氏桿菌等脊柱特異性感染區別,早期診斷較為困難。
非特異性腰椎間隙感染在治療方式的選擇上也存在很多爭議,包括選擇保守治療還是手術治療,以及手術方式的選擇等[2]。一期后路病灶清除植骨融合內固定手術是治療非特異性腰椎間隙感染的一種可選方案[3],但后路手術難以徹底清除椎間隙和椎旁病灶,而病灶和內植物的直接接觸可能影響感染的控制。斜外側腰椎椎間融合術(oblique lumbar in_terdody fusion,OLIF)是近年來脊柱外科領域興起的一種新的手術方式,目前已經在包括腰椎滑脫癥、退變性脊柱側凸等多種脊柱疾病的治療中得到了廣泛應用,但對于OLIF治療腰椎間隙感染的研究報道較少[4_6]。本文回顧性分析21例在我院接受一期OLIF技術聯合Wiltse入路椎弓根螺釘固定治療非特異性腰椎間隙感染病人的臨床資料,探討該手術方案治療非特異性腰椎間隙感染的臨床療效。
資料與方法
一、納入標準與排除標準
納入標準:①年齡≥18歲;②臨床、實驗室檢查及影像學檢查符合非特異性腰椎間隙感染表現,并獲得細菌培養或病理證實;③L2~L5單節段病變;④經過2周以上保守治療效果不佳者,或伴節段不穩(即腰椎過伸過屈位X線片示矢狀面上下相鄰椎體的位移≥4 mm,或/和相鄰椎體上下終板間的角度變化≥10°)。
排除標準:①存在明顯椎管內硬膜外膿腫;②既往有惡性腫瘤或腦梗病人;③既往有腹部手術病史。
二、一般資料
納入2014年1月至2018年12月收治的21例非特異性腰椎間隙感染病人,其中男12例,女9例,年齡為(57.6±10.0)歲(38~78歲)。所有病人均為單節段病變,累及L2/3節段4例,L3/4節段5例,L4/5節段12例。21例均存在明顯腰痛癥狀,疼痛視覺模擬量表(visual analogue scale,VAS)評分為5~9分,7例病人伴有輕微根性疼痛,VAS評分為1~3分。12例病人白細胞升高(11.7~20.3×109/L),9例正常;21例病人C-反應蛋白(36~119 mg/L)及紅細胞沉降率(27~90 mm/L)均升高,提示急性炎癥。術前腰椎正側位X線片顯示椎間隙高度正常或降低,動力位片顯示5例病人存在節段不穩;CT顯示受累終板及鄰近骨質有不同程度破壞;MRI見病變椎間盤及鄰近椎體T1加權信號減低,T2加權及壓脂像高信號;MRI增強顯示椎間盤、相鄰椎體及椎旁軟組織異常強化。
三、手術方法
病人全身麻醉后取右側臥位,“C”型臂X線機透視定位手術節段。左前側腹部作4 cm左右切口,鈍性分離腹壁肌肉,經腹膜后間隙到達腰大肌前緣顯露椎間盤。安裝工作通道。切開纖維環,徹底清除病變椎間盤、軟骨終板及椎旁膿腫,病變組織送細菌培養、病理及結核基因檢查。使用雙氧水和活力碘反復沖洗椎間隙和椎旁膿腔。取適當大小髂骨塊植入椎間隙。透視確認位置良好,撤出通道,縫合切口。將病人調整為俯臥位,透視定位,常規消毒鋪巾,取目標節段正中縱向長約5 cm切口,切開皮膚、皮下組織、筋膜,經雙側最長肌和多裂肌間隙暴露目標節段上下椎弓根螺釘進釘點(人字嵴),在目標節段上下植入左右各2枚椎弓根螺釘,上鈦棒固定,適當加壓。沖洗放置引流管,縫合切口。
根據細菌培養及藥敏結果選擇合適抗生素抗感染治療。抗生素使用療程:靜脈應用6周,口服6周,必要時延長抗生素使用時間。
四、觀察指標
定期復查血常規、紅細胞沉降率、C-反應蛋白,評估感染情況。收集并比較術前和術后1、3、6、12個月及末次隨訪時的VAS評分、Oswestry功能障礙指數(Oswestry disability index,ODI),評估臨床療效。收集復查的腰椎正側位X線片、腰椎CT三維重建,評估是否存在內固定失敗及植骨融合情況。采用Siepe評價方法[7]評估植骨融合情況。
五、統計學方法
采用SPSS 21.0統計軟件包(SPSS公司,美國)進行統計分析,符合正態分布的計量資料采用均數±標準差(±s)表示,手術前后腰腿痛VAS評分、ODI、紅細胞沉降率、C-反應蛋白、白細胞計數等計量資料的比較采用配對t檢驗。檢驗水準α值取雙側0.05。
結 果
21例均順利完成手術,手術時間為(226.7±40.8)min(160~300 min),術中出血量為(232.4±58.0)mL(140~380 mL)。所有病人術中均未出現嚴重的神經、血管損傷等并發癥。2例病人術后出現大腿前內側麻木不適,2例病人術后即出現大腿前外側不適,未予以特殊處理,均在術后3個月隨訪時自行消失。切口愈合良好,均為一期甲級愈合。
病原學培養結果陽性者8例(47.6%),其中金黃色葡萄球菌4例(含多重耐藥金黃色葡萄球菌1例),大腸埃希菌3例,鏈球菌1例。提示急或慢性炎癥表現,無結核肉芽腫改變,結核基因x_pert檢測陰性。3例金黃色葡萄球菌感染者予以頭孢呋辛2.0 g q12,治療6周,然后改口服治療6周;1例鏈球菌感染者予以頭孢呋辛2.0 g q12,治療6周,而后改口服治療6周;3例大腸埃希菌感染者予以頭孢哌酮鈉他唑巴坦鈉2.25 g q12,治療6周,而后改口服治療6周;1例多重耐藥金黃色葡萄球菌感染者予以利奈唑胺0.6 g q12,治療6周,而后改口服治療6周。余13例病原學培養結果陰性病人,采用經驗性抗生素治療(三代頭孢+左氧氟沙星),其中11例效果良好,靜脈應用6周后改口服治療6周;余2例病人,三代頭孢和左氧氟沙星治療效果不佳,改為美羅培南和萬古霉素治療,效果良好,后降級抗生素至三代頭孢和左氧氟沙星,最后改為口服治療6周。
病人隨訪(15.3±6.9)個月(12~36個月)。所有病人在隨訪過程中,臨床癥狀逐漸減輕,無復發情況。術后病人的疼痛癥狀明顯緩解,VAS評分及ODI均持續下降,VAS評分由術前(7.0±1.2)分下降至末次隨訪(1.0±0.9)分,ODI由術前66.5%±10.0%下降至末次隨訪12.9%±3.1%,術后各觀察時間點的VAS評分及ODI與術前比較,差異均有統計學意義(P均<0.05,表1)。所有病人均未出現感染復發情況。隨訪過程中,所有病人的白細胞計數、紅細胞沉降率、C-反應蛋白均逐漸下降,術后6周內19例病人上述指標恢復至正常,術后3個月內所有病人上述指標均恢復正常(表2)。
隨訪期間復查腰椎X線片顯示無內固定松動、斷裂,術后1年CT顯示椎間融合率為100%。典型病例見圖1。
討 論
非特異性腰椎間隙感染大部分可以通過非手術治療治愈,但對于出現脊柱不穩、畸形、神經功能障礙或疼痛難以控制等情況時,仍然需要手術干預[2]。有研究表明早期手術治療相對保守治療可以獲得更好的臨床療效[8]。目前,對于非特異性腰椎間隙感染手術入路的選擇存在爭議,主要包括前路、后路和前后聯合入路[3,9_10]。后路手術可以直接清除椎管內病灶,但是對于椎間隙和椎旁病灶常常難以清除徹底,同時病灶和內植物直接接觸可能影響感染的控制;前路手術直達病灶,清除病灶更加徹底,同時植骨支撐好,利于恢復椎間隙高度及防止后凸畸形[11],但前路固定的生物力學強度較后路椎弓根螺釘固定差,同時也會造成病灶和內植物直接接觸而影響感染控制;前路病灶清除植骨融合輔以后路固定被眾多學者認為是椎間隙感染的標準手術方案[9_10],但傳統的前路開放手術治療非特異性腰椎間隙感染創傷大、出血多[9_10]。隨著脊柱微創化的發展,多種脊柱微創技術應運而生,如極外側腰椎間融合術(extreme lateral interbody fusion,XLIF)等,用于非特異性腰椎間隙感染的治療也獲得了良好的臨床療效[12]。
表1 21例病人手術前后的VAS評分及ODI(±s)

表1 21例病人手術前后的VAS評分及ODI(±s)
注:與術前比較,*P<0.05
VAS評分(分)ODI(%)術前7.0±1.2 66.5±10.0術后3 d 4.0±1.3-術后1個月2.9±0.8*30.7±7.0*術后3個月2.0±1.4*24.9±4.3*術后6個月1.6±0.9*16.4±4.3*術后1年1.3±0.7*14.9±5.1*末次隨訪1.0±0.9*12.9±3.1*
表2 21例病人手術前后的實驗室檢查結果(±s)
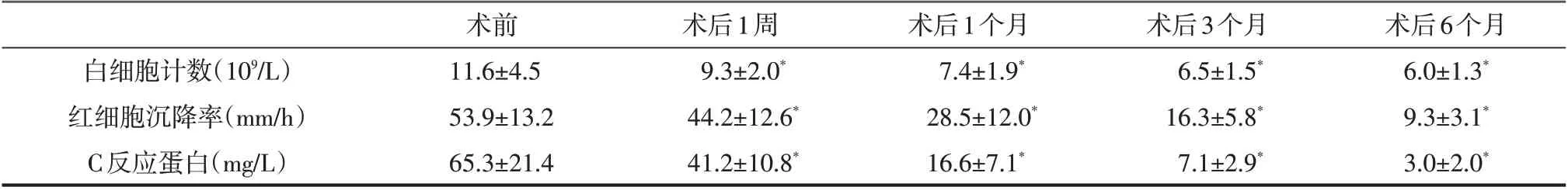
表2 21例病人手術前后的實驗室檢查結果(±s)
注:與術前比較,*P<0.05
白細胞計數(109/L)紅細胞沉降率(mm/h)C反應蛋白(mg/L)術前11.6±4.5 53.9±13.2 65.3±21.4術后1周9.3±2.0*44.2±12.6*41.2±10.8*術后1個月7.4±1.9*28.5±12.0*16.6±7.1*術后3個月6.5±1.5*16.3±5.8*7.1±2.9*術后6個月6.0±1.3*9.3±3.1*3.0±2.0*
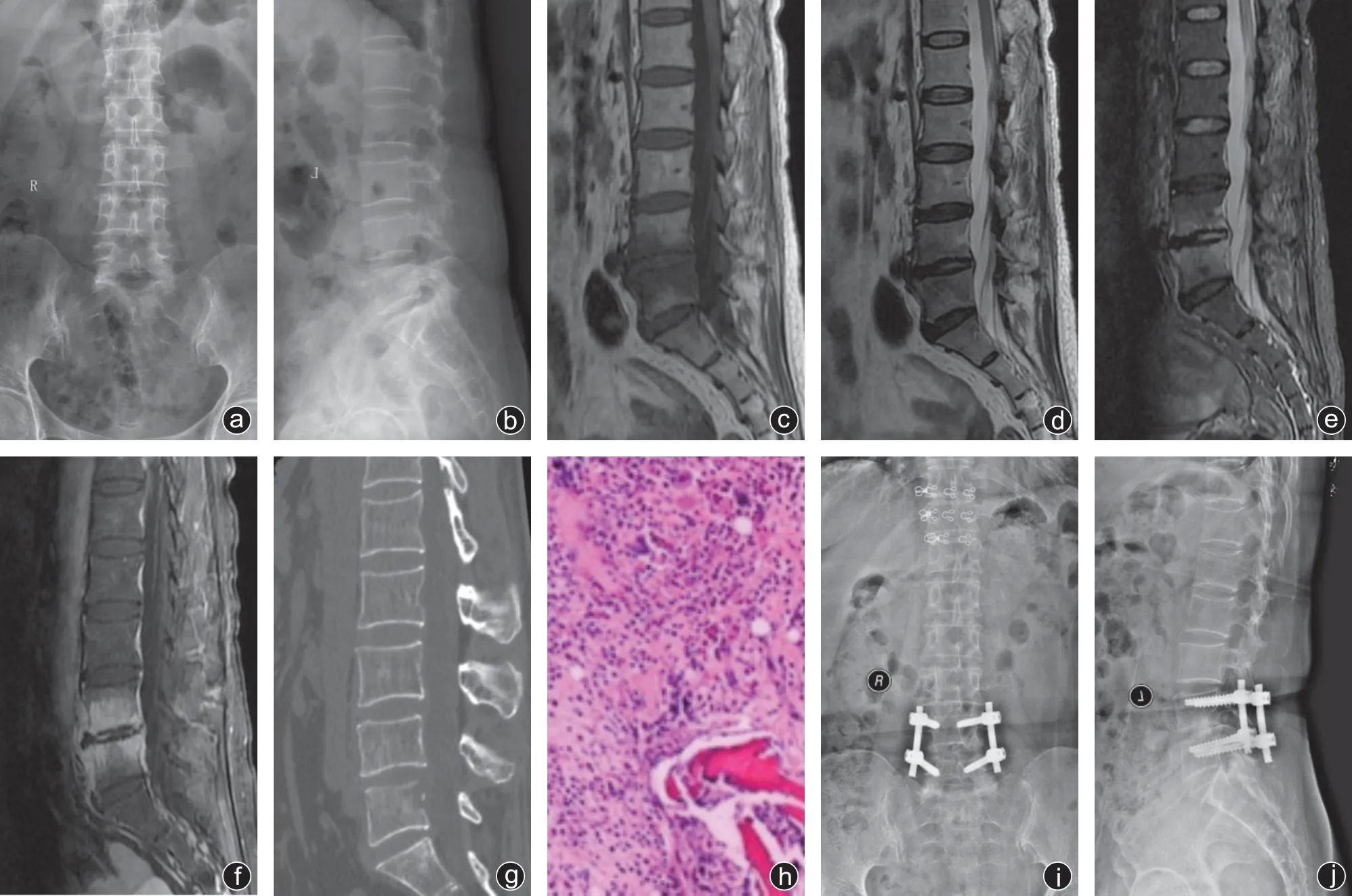
圖1 病人,女,55歲,L4/5腰椎間隙感染,保守治療效果不佳,采用一期斜外側入路病灶清除植骨融合聯合Wiltse入路椎弓根螺釘固定術治療,術中病變組織細菌培養為大腸埃希菌,術后采用頭孢哌酮鈉他唑巴坦鈉治療,效果良好 a、b:術前腰椎正側位X線片未見明顯異常;c~f:術前MRI顯示L4/5間隙及相鄰椎體T1加權像低信號,T2加權像和壓脂像高信號,增強呈高信號;g:術前CT三維重建顯示L5后上部骨質破壞;h:術后病理學檢查結果可見中性粒細胞、淋巴細胞浸潤,未見肉芽腫性病變,符合化膿性感染表現;i、j:術后18個月隨訪腰椎正側位X線片見內固定牢靠,無松動、斷裂,椎間已達到骨性融合
近些年來,OLIF技術在國內得到了大力推廣,該入路采用腰大肌和腹部大血管之間的間隙進行手術,手術微創。本研究采用OLIF通道下病灶清除、植骨融合并輔以Wiltse入路椎弓根螺釘固定治療21例非特異性腰椎間隙感染病人,均獲得了滿意的臨床療效。術后病人的VAS評分、ODI均較術前明顯改善,術后3個月內紅細胞沉降率及C-反應蛋白的水平均恢復至正常,術后1年時均達到了骨性融合。隨訪期間無感染復發、內固定松動等并發癥。
OLIF通道下病灶清除、植骨融合并輔以Wiltse入路椎弓根螺釘固定治療非特異性腰椎間隙感染的優勢總結如下。
1.手術微創 OLIF手術采用小切口通道下操作,術中鈍性分離,經腹膜后到達腰大肌和腹部大血管之間進行手術,手術更加微創,同時Wiltse入路椎弓根螺釘固定,避免廣泛剝離椎旁肌,也未進入椎管,創傷更小,出血也相對較少。楊小春等[13]采用后路病灶清除、植骨融合術治療單節段椎間隙感染,術中平均出血量為360 mL,而本研究的平均出血量僅232.4 mL。
2.清創徹底 較后路手術而言,該術式可以對病變的椎間盤、軟骨終板及椎旁病灶進行徹底清創,有利于徹底清除感染組織,便于感染控制。本研究中所有病人感染控制良好,無復發表現,也說明該手術方式清創徹底。
3.融合率高 該術式可以進行較大的椎間結構性植骨,有助于恢復椎間隙高度和防止后凸畸形發生,同時促進骨性融合。本研究術后1年椎間融合率達100%,術后無斷釘、斷棒及后凸畸形發生。
4.感染控制 輔助Wiltse入路椎弓根螺釘固定可以避免內固定和病灶直接接觸,有助于感染控制。同時后路固定有助于維持病變節段穩定性,減輕病人疼痛,也有助于感染的局限和控制。
5.血管損傷風險低 較傳統前路手術而言,OLIF技術可以減少血管損傷風險。前路手術對腹部大血管和骶前神經叢干擾大,有血管損傷的風險,研究報道血管損傷的發生率為2.3%~4.8%[14_15]。而OLIF術式采用腰大肌和腹部大血管之間的自然間隙手術,不牽拉及干擾腹部大血管,血管損傷風險較低。Silvestre等[4]報道OLIF手術血管損傷發生率為1.1%。本研究所有病人均未出現血管損傷相關并發癥。
6.降低肌肉神經損傷風險 較XLIF技術而言,OLIF技術可以減少對腰大肌以及腰叢神經損傷的風險。XLIF技術經腰大肌入路,必然會對腰大肌造成損傷,同時還有損傷腰叢神經的風險,文獻報道嚴重的永久性神經損傷發生率為2.46%~8.92%[16_17]。Silvestre等[4]報道179例OLIF手術病人永久性神經損傷發生率為0.6%。Fujibayashi等[18]報道28例OLIF手術病人無神經損傷并發癥。本研究中也未出現神經損傷的病例。
綜上所述,一期OLIF技術聯合Wiltse入路椎弓根螺釘固定治療非特異性腰椎間隙感染是一種安全有效的手術方案,具有微創、病灶清除徹底、植骨充分、固定可靠、安全性高、下床活動早、康復快的優點。但本研究為回顧性研究,納入病例較少,且未設立對照組,因而結果存在一定的局限性,需要更大樣本的對比性研究來進一步評價。

