miR-301a對(duì)三陰性乳腺癌細(xì)胞侵襲與增殖的調(diào)控作用*
劉恒 王鋼樂 李秀楠
(首都醫(yī)科大學(xué)附屬北京婦產(chǎn)醫(yī)院乳腺科,北京 100006)
三陰性乳腺癌(triple-negative breast cancer, TNBC)是乳腺癌的重要臨床亞型之一,是一類侵襲性、惡性程度高且復(fù)發(fā)轉(zhuǎn)移率較乳腺癌其他亞型更高的惡性腫瘤,其預(yù)后較非TNBC差[1]。目前TNBC首選的治療措施仍然是手術(shù)+化療,但患者的總體預(yù)后仍然不容樂觀,積極探索TNBC發(fā)生發(fā)展的分子機(jī)制,尋求有效的抗TNBC細(xì)胞增殖的治療措施對(duì)改善預(yù)后尤為重要。研究發(fā)現(xiàn),miR-301a可作為癌基因參與結(jié)直腸癌、肝癌、胃癌、胰腺癌等惡行生物學(xué)行為。FANG等[2]提出miR-301a通過靶向SOCS6促進(jìn)結(jié)直腸癌細(xì)胞的侵襲和增殖;He等[3]提出miR-301a對(duì)肝細(xì)胞癌具有潛在診斷價(jià)值。miR-301a表達(dá)上調(diào)可通過靶向RUNX3促進(jìn)胃癌細(xì)胞的遷徙和增殖[4],miR-301a過表達(dá)可增強(qiáng)胰腺導(dǎo)管癌的侵襲、遷移及成瘤能力[5]。本研究通過觀察miR-301a對(duì)TNBC細(xì)胞侵襲、增殖能力的影響,以探討miR-301a的作用機(jī)制,為TNBC的個(gè)體化治療提供實(shí)驗(yàn)依據(jù)。
1 材料與方法
1.1 主要材料與試劑 人正常乳腺上皮細(xì)胞MCF-10A與TNBC細(xì)胞系MDA-MB-231(中科院上海生命科學(xué)研究院細(xì)胞資源中心)。用100 U/mL青霉素、100 U/mL鏈霉素、10%胎牛血清(FBS)(美國GIBCO公司)的DMEM培養(yǎng)基(美國GIBCO公司)于5% CO2、37.5 ℃培養(yǎng)箱中培養(yǎng)。lipofectamine 3000購自美國Invitrogen公司, miRNA qPCR 試 劑 盒購自北京艾德萊生物科技有限公司,miR-301a模擬物、miRNA 逆轉(zhuǎn)錄試劑盒、miR-301a抑制物及其陰性對(duì)照均購自北京全式金生物技術(shù)有限公司,Transwell 小室試劑盒購自Corning公司;MTT試劑盒購自北京富龍康泰生物技術(shù)有限公司;RIPA 裂解液購自美國GIBCO公司。
1.2 實(shí)驗(yàn)方法
1.2.1 細(xì)胞轉(zhuǎn)染 首先將MDA-MB-231細(xì)胞均勻接種于6孔板中,密度1.2×105個(gè)/孔,培養(yǎng)至細(xì)胞融合度為 70%~80%。轉(zhuǎn)染時(shí),應(yīng)用 LipofectamineTM3000 分別將 miR-301a 模擬物(mimics)、Mimics NC、抑制劑(inhibitor)及Inhibitor NC轉(zhuǎn)染細(xì)胞,轉(zhuǎn)染終濃度為100 nmol/L,分為Mimics miR-301a組、Mimics NC組、 Inhibitor miR-301a組、Inhibitor NC組,空白組不予任何處理。用無雙抗100 mL/L 胎牛血清的DMEM 培養(yǎng)液培養(yǎng)8 h 后換成正常培養(yǎng)液進(jìn)行培養(yǎng),轉(zhuǎn)染48 h后收取細(xì)胞用于后續(xù)轉(zhuǎn)染效果檢測及相關(guān)功能實(shí)驗(yàn)。
1.2.2 real-time PCR檢測 應(yīng)用總RNA抽提(Trizol reagent)試劑分別提取MDA-MB-231細(xì)胞、MCF-10A細(xì)胞中的總RNA,用Nanodrop分光光度計(jì)測定所抽提RNA濃度和質(zhì)量。根據(jù)反轉(zhuǎn)錄試劑盒說明書將RNA反轉(zhuǎn)錄獲cDNA。使用real-time PCR試劑盒檢測miR-301a的表達(dá)。檢測 miR-301a 的相對(duì)表達(dá)量,每個(gè)樣品設(shè)置3個(gè)復(fù)孔。miR-301a 以U6 為內(nèi)參,相對(duì)表達(dá)量結(jié)果應(yīng)用 2-△△Ct法計(jì)算。其中,△Ct=(目的基因Ct-內(nèi)參Ct)的平均值±標(biāo)準(zhǔn)偏差; △△Ct=(待測樣品中目的基因△Ct-參照樣品中目的基因△Ct)的平均值±標(biāo)準(zhǔn)偏差;2-△△Ct反映各樣品相對(duì)NC組樣品目的基因的相對(duì)表達(dá)水平。
1.2.3 Transwell侵襲小室實(shí)驗(yàn) 采用Corning公司的transwell小室,上、下小室各加 500 μL 無血清培養(yǎng)基,37 ℃培養(yǎng)箱中放置 2 h使Matrigel 基質(zhì)層再水化,將小室轉(zhuǎn)移至新的孔板中,除去上室中培養(yǎng)基并加入500 μL細(xì)胞懸液,下室內(nèi)加入750 μL 30% FBS培養(yǎng)基。倒扣小室于吸水紙上以去除培養(yǎng)基,移去小室內(nèi)非侵襲細(xì)胞,0.5%結(jié)晶紫水溶液染色轉(zhuǎn)移細(xì)胞5 min,沖洗小室,室溫下晾干,侵襲細(xì)胞顯微鏡下拍照。
1.2.4 MTT實(shí)驗(yàn) 將轉(zhuǎn)染后的MDA-MB-231 細(xì)胞加入96孔板,培養(yǎng)細(xì)胞24、48 和72 h。72 h后每孔加入MTT液20 μL, 37 ℃下繼續(xù)孵育3 h,棄培養(yǎng)液,每孔加入150 μL二甲基亞砜(DMSO),震蕩10 min,選擇595 nm波長在酶標(biāo)儀測定各孔OD值并記錄。
1.2.5 熒光素酶報(bào)告實(shí)驗(yàn) 生物信息學(xué)軟件Targetscan(http://www.targetscan.org/vert_72/)預(yù)測miR-301a的靶基因,進(jìn)行熒光素酶報(bào)告實(shí)驗(yàn)驗(yàn)證,將細(xì)胞接種至12孔板中,等待細(xì)胞融合達(dá)70%~80%,分別向細(xì)胞中轉(zhuǎn)染野生型MEOX2基因熒光載體和miR-301a mimics或NC,48 h后收集細(xì)胞,參照雙熒光素酶報(bào)告實(shí)驗(yàn)試劑盒說明,檢測細(xì)胞的熒光素酶活性。
1.2.6 Western-blot實(shí)驗(yàn) 收集轉(zhuǎn)染慢病毒載體后的細(xì)胞,PMSF裂解液冰上裂解30 min,加入蛋白酶抑制劑;4 ℃離心5 min,收集上清液,加入5XSDS上樣緩沖液,煮沸10 min,放于-20 ℃保存;配膠,上樣,SDS-PAGE電泳,轉(zhuǎn)膜,室溫下封閉1 h,一抗4 ℃過夜孵育,TBST洗5次,每次5 min,室溫下二抗孵育1 h后,TBS-T洗5次,每次5 min,進(jìn)行化學(xué)發(fā)光反應(yīng)。
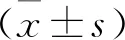
2 結(jié)果
2.1 miR-301a在TNBC細(xì)胞中呈高表達(dá) 應(yīng)用real-time PCR檢測TNBC細(xì)胞株MDA-MB-231與人正常乳腺上皮細(xì)胞株MCF-10A中miR-301a的表達(dá)水平,結(jié)果表明,miR-301a在MDA-MB-231細(xì)胞中的表達(dá)水平明顯高于MCF-10A細(xì)胞(P<0.05),見圖1。

圖1 miR-301a在MDA-MB-231和MCF-10A細(xì)胞株中的表達(dá)
2.2 miR-301a促進(jìn)MDA-MB-231細(xì)胞的侵襲 將miR-301a minics、miR-301a inhibitor分別轉(zhuǎn)染至MDA-MB-231細(xì)胞,real-time PCR檢測結(jié)果顯示,miR-301a mimics可明顯上調(diào)MDA-MB-231細(xì)胞中miR-301a的表達(dá)水平(P<0.05),miR-301a inhibitor能夠明顯下調(diào)MDA-MB-231細(xì)胞中miR-301a的表達(dá)水平(P<0.05)(圖2)。Transwell侵襲實(shí)驗(yàn)結(jié)果顯示,Minics miR-301a 組穿過小室膜的細(xì)胞數(shù)目(53±2.14)高于Minics NC組(41±3.96),差異有統(tǒng)計(jì)學(xué)意義(P<0.05),見圖3。

圖2 各組 MDA-MB-231細(xì)胞中miR-301a表達(dá)水平
2.3 miR-301a對(duì)TNBC細(xì)胞增殖的影響 MTT實(shí)驗(yàn)結(jié)果證明,將miR-301a minics轉(zhuǎn)染至MDA-MB-231細(xì)胞48、72 h后,細(xì)胞增殖能力明顯增強(qiáng)(P<0.05),而轉(zhuǎn)染miR-301a inhibitor 48、72h后,MDA-MB-231細(xì)胞增殖能力明顯被抑制(P<0.05)。結(jié)果提示過表達(dá)miR-301a能夠增強(qiáng)MDA-MB-231細(xì)胞的增殖能力,見圖4。

圖3 Transwell實(shí)驗(yàn)觀察過表達(dá)miR-301a對(duì)MDA-MB-231細(xì)胞侵襲的影響

圖4 MTT實(shí)驗(yàn)檢測miR-301a表達(dá)對(duì)MDA-MB-231細(xì)胞增殖能力的影響
2.4 miR-301a 的靶基因分析 應(yīng)用生物信息學(xué)軟件Targetscan預(yù)測發(fā)現(xiàn)MEOX2是miR-301a可能的靶基因,結(jié)合位點(diǎn)見圖5A。進(jìn)一步采用雙熒光素酶報(bào)告基因分析驗(yàn)證,MEOX2野生型質(zhì)粒(MEOX2-3′UTR-WT)和miR-301a mimics共轉(zhuǎn)染后,熒光素酶活性下降(P<0.05), MEOX2突變型(MEOX2-3′UTR-MUT)和miR-301a mimics共轉(zhuǎn)染后,熒光素酶活性無明顯變化(P>0.05),提示miR-301a可通過此結(jié)合位點(diǎn)被MEOX2靶向,見圖5B。

圖5 miR-301a的靶基因分析
2.5 Western-blot檢測過表達(dá)與下調(diào)miR-301a對(duì)MDA-MB-231細(xì)胞MEOX2蛋白的影響 MDA-MB-231細(xì)胞過表達(dá)miR-301a后,收集細(xì)胞總蛋白進(jìn)行Western-blot檢測。結(jié)果顯示: Mimics miR-301a組MEOX2蛋白表達(dá)量明顯低于Mimics NC組和空白組,差異有統(tǒng)計(jì)學(xué)意義(P<0.05),而Mimics NC組和空白組差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。結(jié)果提示過表達(dá)miR-301a可降低MEOX2蛋白的表達(dá)。
MDA-MB-231細(xì)胞轉(zhuǎn)染miR-301ainhibitor下調(diào)miR-301a后,收集細(xì)胞總蛋白進(jìn)行Western-blot檢測。結(jié)果顯示:Inhibitor miR-301a組MEOX2蛋白表達(dá)量明顯高于Inhibitor NC組和空白組,差異有統(tǒng)計(jì)學(xué)意義(P<0.05),而Inhibitor NC組和空白組差異無統(tǒng)計(jì)學(xué)意義(P>0.05)(圖6)。結(jié)果提示抑制miR-301a表達(dá)可提高M(jìn)EOX2蛋白的表達(dá)。

圖6 Western blot 驗(yàn)證各組細(xì)胞MEOX2蛋白表達(dá)
3 討論
乳腺癌是全球女性中發(fā)病率最高的惡性腫瘤,其中TNBC占乳腺癌的10%~17%,其特點(diǎn)是雌激素受體(ER)、孕激素受體(PR)和人表皮生長因子受體(HER-2)均為陰性,具有較高的侵襲性、復(fù)發(fā)轉(zhuǎn)移率高,缺乏有效的靶向治療方案,預(yù)后較差[6-9],因此針對(duì)TNBC的靶向治療是目前的研究熱點(diǎn)。
多種miRNAs已被證明是三陰性乳腺癌的潛在標(biāo)志物[10],miRNAs通過與靶mRNA 3′-UTR區(qū)完全或部分互補(bǔ)結(jié)合,導(dǎo)致靶mRNA降解或轉(zhuǎn)錄后翻譯抑制,從而調(diào)控靶基因的表達(dá)[11],最終可影響TNBC的高侵襲性生物學(xué)行為[12]。miR-301a是近年發(fā)現(xiàn)的一種促癌miRNA,其在多種惡性腫瘤,如前列腺癌、胃癌、肝癌、結(jié)直腸癌中高表達(dá),參與腫瘤的調(diào)控,研究發(fā)現(xiàn)miR-301a可提高前列腺癌細(xì)胞克隆形成能力及增殖能力[13],miR-301a可通過靶向SOCS6與TGFBR2增強(qiáng)結(jié)直腸癌侵襲性[2,14],文獻(xiàn)報(bào)道m(xù)iR-301a表達(dá)上調(diào)與三陰性乳腺癌的預(yù)后呈負(fù)相關(guān)[15],但其對(duì)于TNBC的發(fā)生、發(fā)展作用罕有報(bào)道,本研究證實(shí)miR-301a在MDA-MB-231細(xì)胞系中表達(dá)量顯著上調(diào),當(dāng)miR-301a水平上調(diào),MDA-MB-231細(xì)胞的侵襲、增殖能力隨之增強(qiáng);當(dāng)miR-301a水平抑制,MDA-MB-231細(xì)胞的侵襲、增殖能力隨之下降,表明miR-301a是TNBC的促癌基因,能夠促進(jìn)TNBC細(xì)胞的侵襲與增殖。
本研究中,來自生物信息學(xué)軟件Targetscan的結(jié)果顯示,miR-301a能夠與MEOX2基因的3′-UTR結(jié)合,認(rèn)為MEOX2為miR-301a的潛在靶基因。MEOX2也稱生長停滯特異性同源框蛋白(GAX)[16],有研究表明其參與調(diào)控多種細(xì)胞的增殖與分化,特別是對(duì)癌細(xì)胞增殖活力的調(diào)控也是最近的研究熱點(diǎn)[17-18]。國內(nèi)學(xué)者曾報(bào)道在乳腺癌中MEOX2可作為PI3K/AKT信號(hào)通路的上游因子,影響乳腺癌細(xì)胞的周期,減少細(xì)胞的有絲分裂,進(jìn)而抑制乳腺癌細(xì)胞的增殖[19]。因此,結(jié)合本研究結(jié)果推測,miR-301a可能通過靶向作用于MEOX2發(fā)揮其促TNBC的作用。為證實(shí)MEOX2為miR-301a的靶基因,本研究應(yīng)用熒光素酶報(bào)告實(shí)驗(yàn)和Western blot實(shí)驗(yàn)對(duì)二者進(jìn)行驗(yàn)證,結(jié)果提示,MEOX2 mRNA的3′-UTR是miR-301a的靶點(diǎn),miR-301a可與MEOX2靶向結(jié)合負(fù)向調(diào)控TNBC細(xì)胞中的MEOX2表達(dá)水平。故推測,TNBC細(xì)胞中miR-301a可通過下調(diào)MEOX2來影響PI3K/AKT信號(hào)通路的調(diào)節(jié),PI3K/AKT信號(hào)通路是促進(jìn)乳腺癌細(xì)胞增殖、轉(zhuǎn)移以及抑制細(xì)胞凋亡的關(guān)鍵通路,為治療TNBC提供重要靶點(diǎn)[20]。然而miR-301a/MEOX2軸是否通過PI3K/AKT信號(hào)通路進(jìn)行調(diào)控TNBC的侵襲與增殖仍需更深入的研究。
4 結(jié)論
miR-301a在TNBC中高表達(dá),并可通過靶向作用于MEOX2促進(jìn)TNBC細(xì)胞的侵襲、增殖,從而作為TNBC的促癌基因發(fā)揮作用。
- 西部醫(yī)學(xué)的其它文章
- 醫(yī)院-社區(qū)-家庭閉環(huán)式模式在老年糖尿病周圍神經(jīng)病變患者中的應(yīng)用價(jià)值*
- CT對(duì)肝細(xì)胞癌射頻消融術(shù)后療效的評(píng)價(jià)*
- 圍手術(shù)期免疫營養(yǎng)支持對(duì)口腔癌患者手術(shù)預(yù)后的影響*
- 肝癌組織miR-146b-5p和miR-134的表達(dá)下調(diào)及臨床意義*
- 局麻下牙髓失活術(shù)與直接拔髓治療磨牙急性牙髓炎的療效對(duì)比*
- MTHFR、MTRR基因多態(tài)性與不良妊娠結(jié)局的相關(guān)性

