CYP3A5*3基因多態性對他克莫司治療膜性腎病血藥濃度及臨床療效的影響
許宏磊,徐炳欣*,王申偉,沈志偉,趙 艷,王 瓊
(1 河南科技大學附屬許昌市中心醫院,許昌 461000;2 許昌市分子醫學重點實驗室,許昌 461000)
膜性腎病(membranous nephropathy,MN)是誘發成人腎病綜合征最常見的病理類型。近年來的發病率逐年上升,且發病年齡有年輕化的趨勢[1]。該病具體發病機制目前仍不明確,多數學者認為其與免疫性疾病有關[2-3]。目前,他克莫司作為強效免疫抑制劑,常用于MN的治療。然而,他克莫司治療指數較低,治療MN的臨床療效有較大個體差異,在同一治療方案下不同患者治療后的有效性和安全性均有所不同[4]。因此,探索影響他克莫司臨床療效的影響因素對于MN患者疾病的治療具有積極意義。既往研究表明[5-7],CYP3A5*3基因多態性對腎臟、心臟、肝臟移植術后患者應用他克莫司有相關影響,但CYP3A5*3基因多態性是否會影響MN患者應用他克莫司的血藥濃度及臨床療效,目前尚缺少臨床研究證據。基于此,本研究將探討CYP3A5*3基因多態性對MN患者應用他克莫司治療后血藥濃度及臨床療效的影響,以期為MN患者的個體化藥物治療提供臨床研究證據。
1 資料與方法
1.1 一般資料
將2016年8月~2019年7月許昌市中心醫院腎內科收治的105例MN患者為研究對象。其中,6例患者中途退出,1例患者轉院治療,4例患者出院后失訪,共計脫落11例,最終共納入患者94例。記錄患者年齡、性別等臨床資料,告知患者檢測CYP3A5*3基因多態性的臨床意義。本研究經本院倫理委員會批準,所有參試者均簽署知情同意書。
納入標準:① 患者年齡在18~70歲,性別不限。② 經病理檢查確診為MN患者。③ 初始治療時患者血清肌酐水平在正常范圍內。④ 自起病以來,未曾使用過糖皮質激素、環磷酰胺、他克莫司、五酯軟膠囊等藥物者。
排除標準:① 繼發性MN患者。② 不能耐受激素及免疫抑制劑治療者。③ 合并糖尿病者。④ 孕婦、哺乳期婦女。⑤ 對他克莫司藥物過敏者。⑥ 依從性差,不能按照要求服藥者。⑦ 合并惡性腫瘤、急性冠脈綜合征等嚴重疾病者。
1.2 研究方法
給藥方法:患者入組后藥物治療方案為他克莫司聯合激素常規治療。其中他克莫司膠囊(普樂可復,Astellas Pharma Co.Ltd.,注冊證號H20150197,規格1 mg)初始給藥方案為1粒/次,bid,早餐和晚餐前1 h內給藥后,根據血藥濃度監測結果調整給藥劑量;醋酸潑尼松片(上海上藥信誼藥廠有限公司,國藥準字H31020675,規格5 mg)起始劑量為口服給藥0.5 mg/(kg·d),2個月后根據患者復查結果減量,每1~2個月減量5 mg,減至10 mg/d維持給藥。患者均給予五酯膠囊、他汀類藥物及抗血小板藥物等治療。30天為一個療程,連續治療6個療程。
基因型檢測方法與分組:采用熒光染色原位雜交技術檢測入組患者CYP3A5*3基因多態性,并依據檢測結果將患者分為GG、GA和AA 3組。具體檢測過程為:用EDTAK2抗凝的采血管取患者空腹靜脈血2 ml,取全血100 μl置于900 μl預處理液中(10×NH4Cl稀釋10倍,北京華夏時代基因科技發展有限公司),渦旋震蕩10 s,靜置5 min后,3000 r/min離心5 min,去除上清液,留取下層白細胞備用。取耀金染試劑(北京華夏時代基因科技發展有限公司)30 μl加入白細胞中得到白細胞懸液。取白細胞懸液2 μl加入到CYP3A5*3基因(rs776746)耀金分試劑(北京華夏時代基因科技發展有限公司),置入TL998A熒光檢測儀(西安天隆科技有限公司),其結果由Microseq軟件分析和自動判讀,給出CYP3A5*3基因多態性檢測結果。
他克莫司血藥濃度檢測采用均相酶免疫分析法測定,于患者規律服藥至少7天后檢測他克莫司血藥濃度谷值(C0,在下一次給藥前0.5 h抽血)。他克莫司檢測試劑[西門子醫學診斷產品(上海)有限公司,國食藥監械(進)字2009第2400651號]。他克莫司劑量調整血藥濃度以MN患者體重校正他克莫司日劑量(D),并以C0計算劑量調整血藥濃度(C0/D)mg/(ml·d)。高密度脂蛋白、低密度脂蛋白、三酰甘油、血糖、總膽固醇、肌酐等生化指標應用,采用Cobas8000型全自動生化免疫分析儀(德國羅氏診斷有限公司)檢測,操作嚴格按照對應試劑盒的使用說明書進行。
1.3 評價標準
有效性評價指標包括:完全緩解、部分緩解和治療無效[8]。其中,完全緩解:① 患者尿蛋白檢測結果轉陰。② 患者24 h尿蛋白定量<0.3 g。③ 患者血清白蛋白≥35 g/L。④ 患者血清肌酐<140 μmol/L。部分緩解:① 患者24 h尿蛋白定量比入組時有所降低,降低幅度>50%。② 患者血清白蛋白≥30 g/L。③ 患者血清肌酐<140 μmol/L。治療無效:① 患者24 h尿蛋白降低幅度<50%或較治療前升高。② 患者血清白蛋白<30 g/L或較治療前更低。治療總有效率(%)=(完全緩解例數+部分緩解例數)/總例數。記錄患者在治療期間所發生的全部藥物不良反應,用于評價治療的安全性。其中藥物不良反應發生率的計算方式為:藥物不良反應發生率(%)=不良反應發生例數/總例數。
1.4 統計學方法
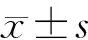
2 結果
2.1 CYP3A5*3基因類型的Hardy-Weinberg遺傳平衡
94例患者檢出CYP3A5*3基因:GG組45例、GA組32例、AA組17例。CYP3A5*3各基因型的實測值與理論值無統計學差異,符合Hardy-Weinberg遺傳平衡(χ2=2.904,P=0.234),說明本研究納入的樣本具有群體代表性。見表1。
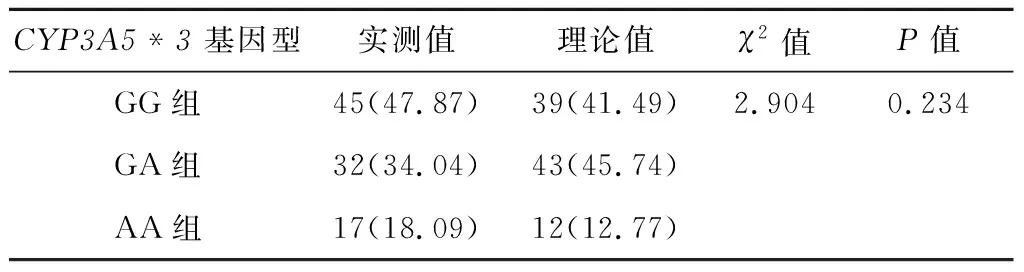
表1 CYP3A5*3基因類型的Hardy-Weinberg遺傳平衡 n(%)
2.2 3組一般資料比較
完成研究的94例患者,GG、GA和AA 3組患者例數及所占的比例分別為45例(47.87%)、32例(34.04%)和17例(18.09%)。GG組:男性30例,女性15例;年齡41~68歲,平均年齡(53.21±12.74)歲;GA組:男性23例,女性9例;年齡36~65歲,平均年齡(56.58±14.17)歲;AA組:男性9例,女性8例:年齡38~70歲,平均年齡(51.26±13.58)歲。3組基線資料相比較,無統計學差異(P>0.05)。見表2。
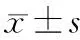
表2 3組一般資料比較
2.3 3組他克莫司C0及C0/D差異
治療1周后,GG組患者他克莫司C0為(6.42±3.31) ng/ml,高于GA組(5.22±2.76) ng/ml和AA組(4.14±2.57) ng/ml。單因素方差分析顯示,不同基因型患者間他克莫司C0比較,具有統計學差異(F=3.924,P=0.022);兩兩比較經Bonferroni校正,GG組患者他克莫司C0高于AA組,具有統計學差異(P=0.014)。以患者每天他克莫司給藥總劑量除以體重,得到D;3組他克莫司D和C0/D數據不符合正態分布,經kruskal-Wallis檢驗顯示,3組他克莫司D無統計學差異(χ2=2.524,P=0.081);3組他克莫司C0/D具有統計學差異(χ2=4.803,P=0.015),兩兩比較經Bonferroni校正,GG組與AA組C0/D具有統計學差異(P=0.009)。見表3。
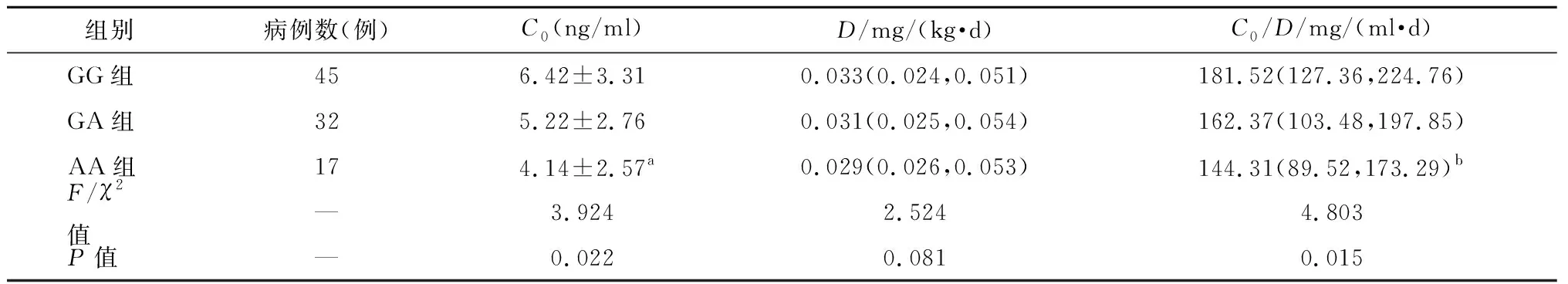
表3 3組他克莫司C0及C0/D的差異
2.4 3組治療有效率的差異
經過6個月的治療,GG組患者治療有效率為34例(75.56%)、GA組治療有效率為22例(68.75%)、AA組治療有效率為11例(64.71%)。GG組患者治療有效率高于GA和AA組,但無統計學差異(χ2=0.861,P=0.650)。見表4。
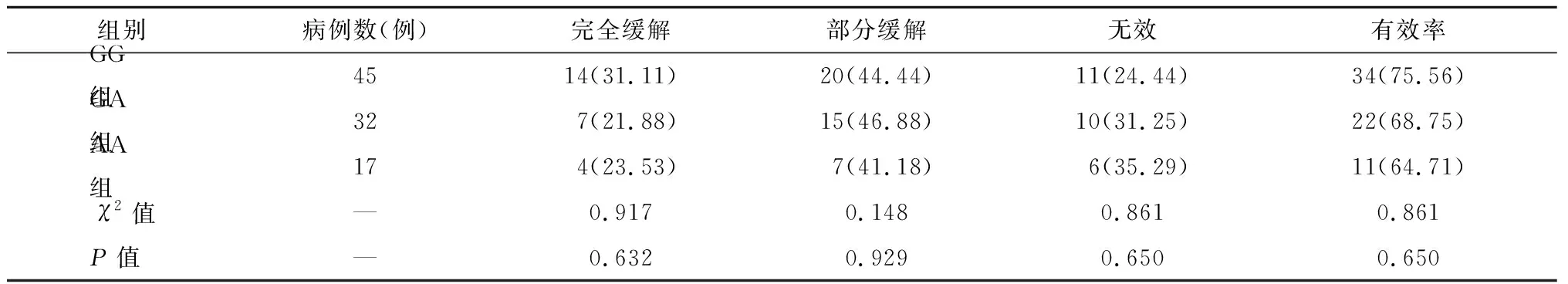
表4 3組治療有效率比較 n(%)
2.5 3組藥品不良反應發生情況
治療期間,3組患者所發生的藥物不良反應主要有胃腸道反應(惡心、腹瀉、消化不良等)、空腹血糖受損、血尿酸水平升高、肝酶異常和肌肉震顫。按照國家藥物不良反應分級,3組患者所發生的藥物不良反應均為一般藥物不良反應,經對癥處理后均得到緩解或者消失。A組患者肝酶異常發生率和空腹血糖受損發生率均大于B和C組,具有統計學差異(P<0.05);3組其他藥物不良反應發生率及藥物不良反應總發生率無統計學差異(P>0.05)。見表5。
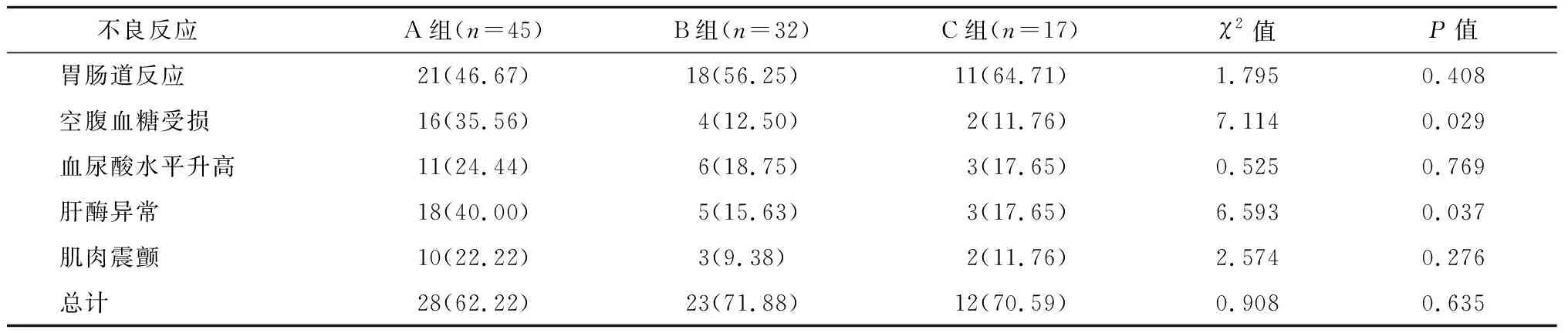
表5 3組藥物不良反應發生率比較 n(%)
3 討論
本研究中患者他克莫司起始給藥劑量為每天 2 mg,略低于改善全球腎臟病預后組織推薦的給藥劑量[9],主要原因在于所有患者均聯合給予五酯膠囊。研究顯示[10],五酯膠囊可通過抑制CYP3A5酶的活性提升他克莫司的血藥濃度,MN患者聯用五酯膠囊后可通過減少他克莫司用藥量降低經濟負擔[11]。
本研究中采用血藥濃度監測調整他克莫司的維持給藥劑量,主要因為他克莫司治療指數低且個體差異大[12]。研究考察了CYP3A5*3基因多態性對他克莫司血藥濃度的影響,結果顯示,在同一給藥劑量下不同基因型患者的血藥濃度存在差異,且GG組患者血藥濃度高于AA組。為排除患者體重、給藥劑量對血藥濃度的影響,進一步研究考察了3組患者他克莫司調整血藥濃度的差異。結果顯示,3組他克莫司調整血藥濃度也存在差異,且GG組患者高于AA組。這表明CYP3A5*3基因多態性影響他克莫司的血藥濃度。研究顯示[5,13],他克莫司血藥濃度影響因素較多,以遺傳因素、患者的疾病狀態、飲食結構以及藥物相互作用為主,其中以遺傳因素的影響更為重要,這與魏傳梅等[14]的研究結論相符。
MN的治療是一個較為長期的過程,在用藥前明確不同基因類型患者藥物不良反應的發生情況,對于保障患者用藥安全有重要的意義。腎毒性是他克莫司常見的藥物不良反應,血清肌酐和腎小球濾過率是監測患者腎功能常用的指標。本研究采用血清肌酐監測入組患者治療過程中腎功能的變化,治療過程中3組血清肌酐水平在正常范圍內。本研究考察了不同CYP3A5*3基因型患者應用他克莫司后藥物不良反應發生率的差異。結果顯示GG組患者空腹血糖受損和肝酶異常發生率高于GA和AA組患者,表明CYP3A5*3基因多態性對他克莫司不良反應的發生情況有影響。提示臨床為了保障治療安全,在患者應用他克莫司前應檢測CYP3A5*3基因型并依據檢測結果個體化監測藥物不良反應的發生情況。臨床應加強GG組患者用藥期間的患者教育,患者自身也應加強血糖和肝功能監測。有研究指出[15],他克莫司導致血糖異常的機制在于他克莫司可通過血藥濃度依賴的方式抑制胰島素分泌,進而影響患者血糖水平,且這種抑制程度與血藥濃度的高低有關系。GG組患者對他克莫司代謝減慢,可能是空腹血糖發生率高的原因所在。
本研究中3組患者經過6個月的治療,GG組患者治療有效率為75.56%,高于GA(68.75%)和AA組(64.71%),但無統計學差異。既往研究顯示[16],他克莫司血藥濃度是影響他克莫司療效的關鍵因素。但本研究中3組有效率無統計學差異,考慮其可能原因為患者在治療過程中均通過血藥濃度監測結果調整他克莫司的給藥劑量,同時研究時間相對較短。CYP3A5*3基因多態性對他克莫司治療MN有效性的影響有待進一步研究。
綜上所述,CYP3A5*3基因多態性對MN患者應用他克莫司治療后的血藥濃度和不良反應的發生情況有影響,檢測CYP3A5*3基因多態性對提升MN患者治療的安全性有一定價值。但本研究是單中心研究,納入樣本量較少,這可能會導致研究結論有所偏倚,因此本研究結論有待多中心更大樣本量的研究予以證實。

