低聚殼聚糖對小鼠的輻射損傷防護作用探討
郭劍平,張華屏,周朝東,楊仲田
(1.中國輻射防護研究院GLP中心,太原,030006;2.山西醫科大學,太原,030001;3.中國輻射防護研究院, 太原,030006)
殼聚糖是自然界廣泛存在的甲殼素經脫乙酰化得到的產物,是天然多糖中唯一的堿性多糖。小于20個單糖的殼聚糖稱為低聚殼聚糖。有研究表明低聚殼聚糖具有抗輻射損傷作用[1-2],并且毒性極低。本文從組織、細胞、蛋白和基因表達水平探討低聚殼聚糖的輻射損傷防護效果及機理,為篩選高效、低毒的輻射防護藥物提供參考依據。
1 實驗材料
1.1 低聚殼聚糖
以食品級大分子殼聚糖為原料,敏化劑協同作用,經輻照降解氧化后制備而成。分子量<2 kD,分散系數1.21。使用前用蒸餾水配制成溶液。
1.2 實驗動物
6周雄性清潔級SX1近交系小鼠,山西省腫瘤研究所動物實驗室提供,許可證號:SCXK(晉)2007-001。
1.3 輻照源
60Co γ源,活度1.2×1015Bq,中國輻射防護研究院鈷源房。
1.4 主要儀器和試劑
1.4.1儀器
BD FACSAria型流式細胞儀,貝克曼公司;轉印槽/伯樂轉膜儀,BIO-RAD,Trana-Blot;化學發光檢測系統試劑,BIO-RAD;化學發光熒光成像系統,Chemi Doc XRS。
1.4.2試劑
凋亡試劑盒(Annexin V-FITC),凱基公司,國產;beta-actin抗體,sc-47778,Santa Cruz Biotechnology;P53抗體:sc-73566,Santa Cruz Biotechnology。
2 實驗內容和方法
2.1 小鼠30天存活率
實驗小鼠按給藥濃度隨機分5組,每組10只,口服灌胃,給藥劑量為0(單純照射組)、200、300、400和500 mg/kg,每天給藥1次,連續14天,給藥第7天對小鼠進行全身照射,吸收劑量7 Gy,劑量率70 cGy/min。觀察不同處理組30天小鼠存活情況,統計30天存活率、平均存活天數,計算保護指數[3]。
保護指數≥1.2為有保護作用。
2.2 骨髓有核細胞數
實驗小鼠隨機分為正常對照組、單純照射組、低聚殼聚糖組(300 mg/kg),每組10只。連續灌服低聚殼聚糖21天,每天1次。正常對照組和單純照射組灌服蒸餾水。給藥第7天后兩組小鼠均接受3.5 Gy60Co γ射線全身照射,劑量率0.5 Gy/min。照射后第14天取小鼠股骨,用1 mL白細胞稀釋液沖出骨髓液,并調整細胞濃度,用細胞計數板在顯微鏡下計數骨髓有核細胞數。
2.3 骨髓細胞凋亡
實驗小鼠隨機分為正常對照組、單純照射組、低聚殼聚糖組(300 mg/kg),每組6只。給藥第14天后兩組小鼠接受5 Gy60Co γ射線全身照射,劑量率0.5 Gy/min。
照射后6、12、24和48 h取出兩大腿股骨,用PBS液沖出骨髓細胞,混勻。處理并調整細胞濃度為105/mL,按試劑盒說明方法染色,用流式細胞儀檢測凋亡細胞率[4]。
2.4 脾臟器系數
實驗小鼠隨機分為正常對照組、單純照射組、低聚殼聚糖組(300 mg/kg)3個實驗組,每組40只。連續灌服低聚殼聚糖14天,每天1次。正常對照組和單純照射組灌服蒸餾水。給藥第14天后兩組小鼠均接受7 Gy60Co γ射線全身照射,劑量率0.33 Gy/min。在照后第5、10、15、20、30天,各組分別取5只存活小鼠脾臟,稱取并記錄脾臟重量。
2.5 細胞凋亡相關基因表達變化
實驗小鼠隨機分為正常對照組、單純照射組、低聚殼聚糖組(300 mg/kg)3個實驗組,每組10只。給藥第14天后兩組小鼠接受5 Gy60Co γ射線全身照射,劑量率0.5 Gy/min。
照射后6 h,摘取動物脾臟,每個脾組織分別進行RT-PCR方法檢測Bax、Bcl-2、Caspase-3,以GAPDH為參照,Photoshop 7.0分析條帶。各基因RT-PCR試驗條件見表1。

表1 各基因RT-PCR試驗條件一覽表
2.6 細胞P53蛋白質、Gadd45蛋白質
實驗小鼠隨機分為正常對照組、單純照射組、低聚殼聚糖組(300 mg/kg),每組10只。給藥第14天后兩組小鼠接受5 Gy60Co γ射線全身照射,劑量率0.5 Gy/min。照射后6 h,摘取動物脾臟,用Western blot方法檢測P53蛋白質和Gadd45蛋白質。
2.7 統計分析
用卡方檢驗對30天存活率進行檢驗,用t檢驗對兩樣本均數差別的顯著性進行檢驗。
3 結果和討論
3.1 結果
3.1.130天存活率
不同濃度低聚殼聚糖對受照小鼠30天存活率、平均存活時間和保護指數的影響檢測結果列于表2。
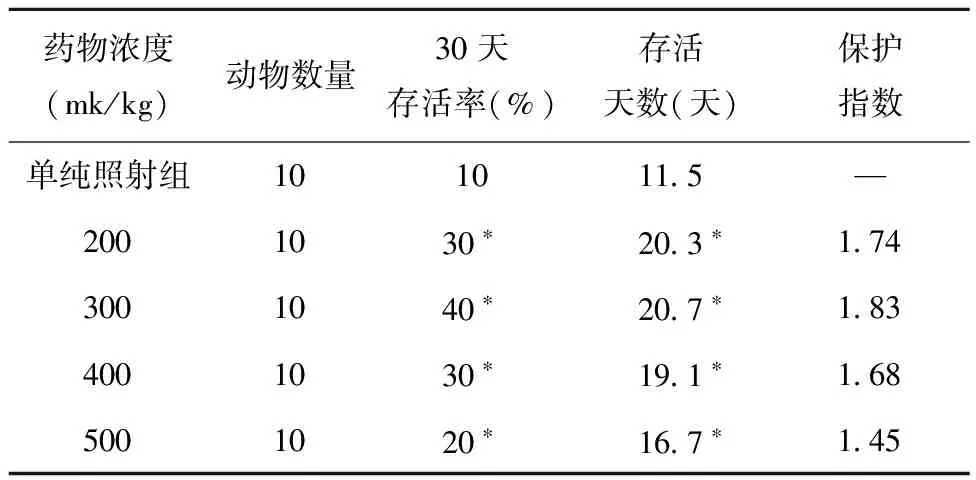
表2 不同濃度低聚殼聚糖對受照小鼠30天存活率、存活天數、保護指數的影響
由表2可見,與單純照射組相比,各低聚殼聚糖組(200~500 mg/kg)的小鼠30天存活率分別提高20%、30%、20%和10%,平均存活時間差異顯著,其中300 mg/kg組在各組中的30天存活率、平均存活天數和保護指數最高(保護指數≥1.2為有效)。故后期試驗采用的藥物濃度均為300 mg/kg(稱為“低聚殼聚糖組”)。
3.1.2有核細胞數和骨髓細胞凋亡
低聚殼聚糖對受照小鼠骨髓有核細胞數和骨髓細胞凋亡的影響結果列于表3和表4。由表3可見,低聚殼聚糖組骨髓有核細胞數顯著高于單純照射組。由表4可見,低聚殼聚糖組的凋亡細胞下降,6~12 h變化較大,與單純照射組相比差異顯著。

表3 低聚殼聚糖對受照小鼠骨髓有核細胞數的影響
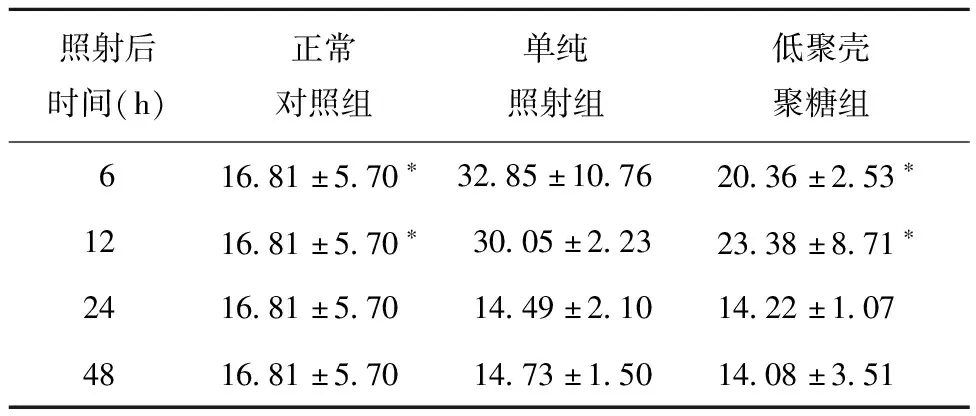
表4 低聚殼聚糖對受照小鼠骨髓細胞凋亡的影響
3.1.3脾臟器系數
低聚殼聚糖對受照小鼠不同時間脾臟臟器系數的影響結果列于表5。由表5可見,低聚殼聚糖組照射后第5~20天,脾臟器系數值有緩慢上升趨勢,與單純照射組相比差異顯著。
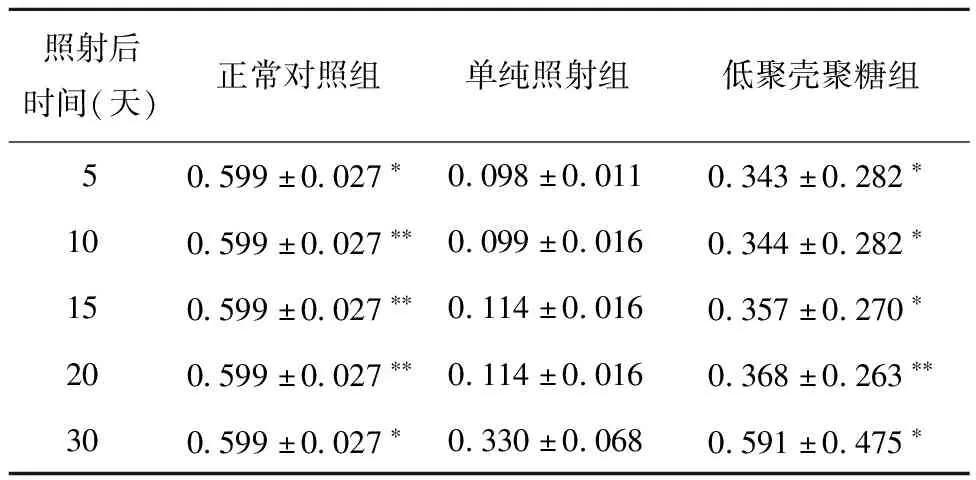
表5 低聚殼聚糖對受照小鼠不同時間脾臟臟器系數的影響
3.1.4脾臟凋亡基因
低聚殼聚糖對受照小鼠6 h脾臟凋亡基因的影響變化情況列于表6。由表6可見,與正常對照組相比,低聚殼聚糖組凋亡相關基因Caspas-3下調,Bax上調,Bcl-2上調,Bcl-2/Bax比值提高,比值高于1;與單純照射組相比差異顯著。
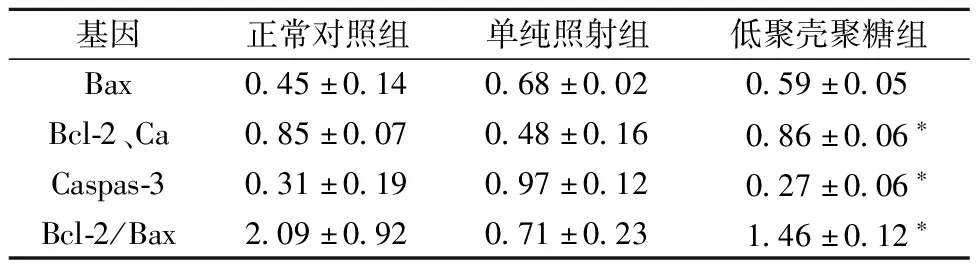
表6 低聚殼聚糖對受照小鼠6 h脾臟凋亡基因變化情況
3.1.5P53蛋白質、Gadd45蛋白質表達
圖1為 Western blot方法檢測P53、Gadd45蛋白結果。低聚殼聚糖對受照小鼠脾臟P53蛋白質表達水平的影響見圖2(a),對Gadd45蛋白質表達水平的影響見圖2(b)。由圖2可見,與單純照射組相比,低聚殼聚糖組的蛋白質表達水平降低。

圖1 Western blot方法檢測 P53、Gadd45蛋白結果
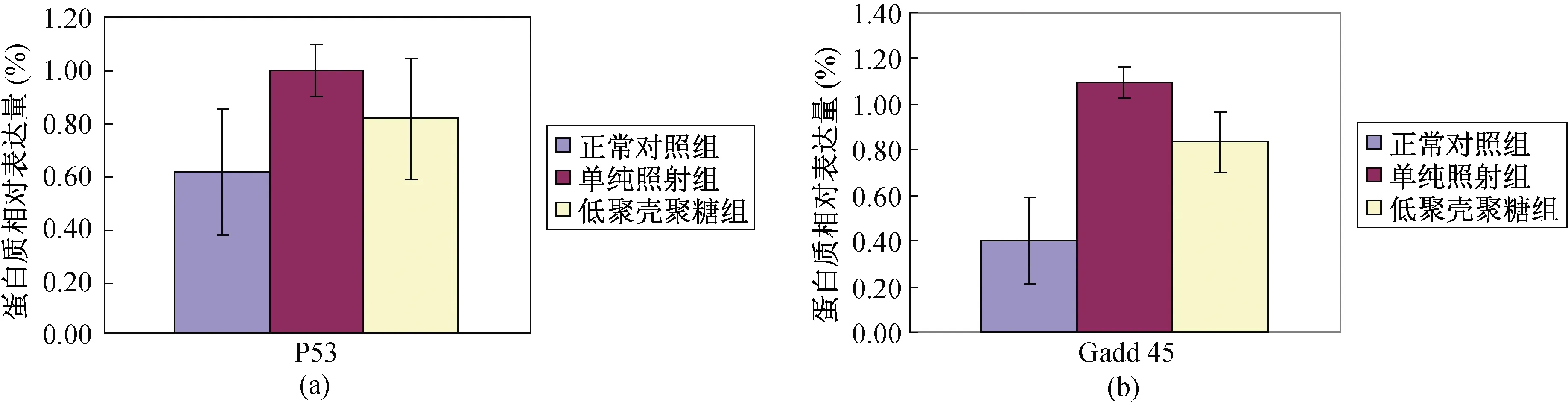
圖2 低聚殼聚糖對受照動物脾臟P53、Gadd45蛋白表達的影響
3.2 討論
電離輻射能夠引起機體組織器官的嚴重損傷,而機體的各個組織器官對輻射的敏感性是有差異性的,其中骨髓是機體重要的中樞免疫及造血器官,脾臟是機體重要免疫器官,含有大量的淋巴細胞和巨噬細胞,是機體細胞免疫和體液免疫的中心,同時脾臟也是機體血液儲存的重要器官。
小鼠受到照射后,骨髓有核細胞數降低,但低聚殼聚糖組有核細胞數顯著提高。5 Gy照射后骨髓細胞凋亡發生在6~12 h,24 h后下降,與文獻報道一致[5]。與單純照射組相比,低聚殼聚糖組6~12 h凋亡細胞發生數明顯下降,表明低聚殼聚糖能夠抑制輻射引起的細胞凋亡,減少由于照射造成的骨髓細胞損失,有效保護骨髓細胞的造血功能,具有一定的輻射防護作用。
低聚殼聚糖組小鼠脾臟器系數在照后20天內變化不大,到30天時,接近正常對照組。低聚殼聚糖在動物照射損傷后,調節脾臟相關凋亡基因表達,最后表現出降低脾臟臟器系數的減少,對受損動物免疫功能的恢復起到積極的作用。
細胞凋亡是影響細胞輻射敏感性的重要事件,減少細胞凋亡,保持細胞存活是輻射損傷防治的重要措施之一。P53在損傷細胞存活中起重要作用并因此被譽為“基因警察”。本實驗單純照射組P53蛋白質增加,而低聚殼聚糖組P53蛋白質表達水平降低,說明低聚殼聚糖對輻射所致的P53蛋白質表達水平有抑制作用。
P53誘導細胞凋亡的機制是通過Bax/Bcl-2這一比值的轉換而完成。Bcl-2和Bax是一對關系密切的凋亡基因,在細胞凋亡調控中起重要作用。Bcl-2抑制細胞的凋亡,Bax則促進細胞的凋亡。Bcl-2/Bax比例對決定細胞命運起著關鍵的作用。當Bcl-2/Bax比值>1時,細胞凋亡無明顯增加;而Bcl-2/Bax比值<1時,細胞凋亡增加明顯。本實驗中低聚殼聚糖組促凋亡基因Bax、Caspas-3表達均下調,抑制凋亡基因Bcl-2表達上調,Bcl-2/Bax比值>1,與單純照射組相比有差異顯著。表明低聚殼聚糖有抑制輻射損傷小鼠脾組織細胞凋亡的作用。研究表明,DNA損傷使P53蛋白活力上升,P53通過對Bcl-2和Bax表達的調節,降低細胞對凋亡刺激因素的耐力[6]。可見,P53能同時在mRNA水平激活Bax基因的表達和抑制bcl-2基因的表達。P53誘導凋亡可能部分通過改變細胞內Bax、Bcl-2的比例得以實現。本實驗中單純照射組結果與以上結論相同。低聚殼聚糖抑制P53蛋白表達,通過誘導凋亡,在mRNA水平激活Bcl-2基因的表達和抑制Bax基因的表達,改變細胞內Bcl-2、Bax的比例,提高細胞對凋亡刺激因素的耐力,導致凋亡細胞的減少,抑制了DNA損傷對細胞的凋亡作用。
Gadd45是一個生長阻滯和DNA損傷基因,是P53下游靶基因。Gadd45可以通過P53依賴及非依賴兩條途徑被誘導表達增高,參與細胞周期檢查點、細胞凋亡、DNA損傷修復以及信號傳導等重要細胞生命活動的調節[7-8]。在電離輻射的作用下,Gadd45可以通過P53依賴的方式表達上調。研究表明,高劑量X射線照射可引起P53蛋白增多誘導Gadd45增加[9],本實驗單純照射組Gadd45、P53蛋白質表達水平升高,與研究結果一致。但低聚殼聚糖組Gadd45、P53蛋白質表達水平均有降低趨勢。
低聚殼聚糖間接參與DNA損傷修復、細胞凋亡、細胞周期等重要細胞生命活動的積極調控,減少由于照射引起的造血細胞和免疫細胞數量損失,并維持其功能的實現,導致動物存活率的提高。低聚殼聚糖提高存活率的影響因素很多,其中抑制細胞凋亡是有效因素之一。
本研究結果證實低聚殼聚糖具有輻射損傷保護作用,它可能通過抑制P53蛋白、GADD45蛋白質水平表達,影響凋亡相關基因表達,從而抑制凋亡細胞的產生,促進骨髓和脾臟細胞數量的恢復,從而有效提高了受到致死劑量γ射線照射小鼠的30天存活率。
4 結語
核能屬于清潔能源,隨著人類對核能利用的日趨廣泛,對輻射損傷機制和防護藥物的研究逐漸成為人們關注的熱點,開發高效、低毒的理想抗輻射損傷藥物就變得尤為重要。氨磷汀(WR2721)作為唯一被美國食品藥品監督管理局(FDA)批準的輻射防護劑,可通過清除自由基、誘導細胞缺氧、保護DNA及促進DNA損傷修復等機制發揮輻射防護特性,但毒副作用較大,且臨床效果不盡人意。大多數傳統的輻射防護劑不良反應較大、防護時間窗較窄及給藥途徑受限等,臨床仍缺乏理想的抗輻射藥物。低聚殼聚糖來源廣泛,制備技術成熟,不僅具有良好的生物降解性,還有良好的生物相容性以及生物粘附性,其降解產物無毒性,無免疫原性,可以考慮作為輻射防護劑并進行更深入的開發研究。初步證明低聚殼聚糖具有一定的輻射損傷保護作用,藥物的防護作用機理研究將在今后的工作中進一步探討。

