葒草素通過激活PGC-1β 發揮抗糖尿病心肌病作用
王 倩,林文娟,王 娜,張 冰
糖尿病增加了患心臟病的風險,50%的糖尿病患者死于心血管疾病[1]。炎癥和氧化應激激活是糖尿病心肌損傷顯著的病理生理過程,也會導致心肌細胞內蛋白質量調控障礙,目前仍亟待探索有效的藥物和分子靶點來控制糖尿病心肌病的發展[1-2]。糖尿病患者的心力衰竭發病率非常高,而且糖尿病患者的預后比非糖尿病患者更差。實驗數據表明,多種機制導致糖尿病患者收縮期和舒張期功能受損,這些患者的心臟衰竭與冠狀動脈疾病或相關危險因素無關[3]。
葒草素(Orientin)是從天然植物中分離出來的黃酮類成分,在近幾年的研究中,葒草素已被探究證實具有豐富的細胞組織保護特性,如抗氧化應激、抗炎、抗癌和抗血栓活性[4-5]。葒草素能夠通過調節Toll 樣受體-4/核轉錄因子-κB/腫瘤壞死因子-α信號通路發揮抗炎作用,從而對大鼠腦缺血/再灌注損傷發揮保護作用[6]。近期研究證實,葒草素能夠通過調節內皮型一氧化氮合酶/一氧化氮(eNOS/NO)信號通路發揮抗氧化應激作用,從而能夠減輕小鼠心梗后心肌病理性重構[7]。迄今為止,葒草素是否能對糖尿病心肌病發揮保護作用尚無研究報道。本研究將探究葒草素在糖尿病心肌病中發揮的作用及潛在的分子機制。
1 材料與方法
1.1 實驗動物 雄性C57BL/6 小鼠(20~25 g,8~10 周齡)從實驗動物中心獲得,在22~24℃的12 h的光/暗周期下被籠養,吃定期的顆粒飼料。
1.2 實驗試劑 純度>98%的葒草素(融禾,上海),檢測超氧化物歧化酶(superoxide dismutase,SOD)活性和丙二醛(malonaldehyde,MDA)含量試劑盒(南京建城)。抗PGC-1β 的抗體(Abcam,美國),抗GAPDH 的抗體(cmcTAG 公司,美國),Trizol 試劑和RNA 提取試劑盒(天根,北京),引物合成(GenScript,南京),評價H9C2 細胞內活性氧(reac?tive oxygen,ROS)生成的熒光探針2′,7′-二氯熒光素二乙酸酯(DCFH-DA)(碧云天,上海)。
1.3 小鼠分組及處理方式 將雄性C57 小鼠隨機分為3 組:同籠陰性小鼠分為對照組(CON 組,n =12)、糖尿病組(DCM 組,n =12)和按常規腹腔注射鏈脲佐菌素(Streptozotocin,STZ)50 mg/kg)誘導小鼠糖尿病模型的外源補充葒草素小鼠糖尿病組(DCM+ORI 組,n =12)。DCM+ORI 組小鼠每天通過灌胃外源補充葒草素(溶于生理鹽水,劑量為40 mg/kg),DCM 組僅補充相同量的生理鹽水。喂養8周后進行后續實驗。
1.3.1 小鼠心臟超聲檢測 超聲工作者完全未知研究方案和動物組。使用VisualStulic 770 超聲儀器進行小鼠心臟超聲檢查,30 MHz 的傳感器記錄左胸骨旁胸腺的長軸和短軸。超聲心動圖檢測的指標包括左室射血分數(left ventricular ejection fraction,LVEF)和左室縮短分數(left ventricular fractional shortening,LVFS)、舒張末期室間隔(intraventricular septal thickness end diastasis,IVSd)和舒張末期左室后壁(left ventricular positerior wall end diastasis,LVPWd)厚度。以上參數由Vevo Lab 3.1.0 軟件計算得出。
1.3.2 小鼠心肌組織學染色 用蘇木精-伊紅(HE)或Masson 三色染色法分別對心肌組織的其他部分進行染色,以評估心肌細胞的橫截面積和膠原沉積。切片用數字掃描成像系統(Olympus FV1000,日本)進行可視化,心肌細胞橫截面積和纖維化程度用Image J 軟件(NIH,Bethesda,MD,USA)進行量化。
1.3.3 小鼠心肌組織MDA 和SOD 的測定 檢測心臟組織中氧化應激標記物MDA 含量和SOD 活性,步驟基于制造商的說明。通過SpectraMax M5 裝置使用分光光度法分析數據。
1.3.4 實時熒光定量聚合酶鏈反應(RT-qPCR)檢測mRNA 表達 采集左心室壁部分組織,按照RNA提取試劑盒的指示從標本(或處理后培養的H9C2細胞)中提取總RNA。然后利用上標第一鏈合成系統(Invitrogen,CA,USA)將RNA 反向轉化為互補DNA。用CFX96 實時聚合酶鏈反應系統C1000 熱循環儀(美國)進行RT-qPCR。磷酸甘油醛脫氫酶(GAPDH)是靶基因轉錄水平正常化的標準基因。本研究中使用的引物序列列于表1 中。
1.3.5 H9C2 心肌細胞的培養 將H9C2 細胞按(1~2)×105個/ml 均勻種于六孔板中,于含10%胎牛血清的低糖培養基中置于細胞培養箱(5% CO2、飽和濕度、37 ℃)無菌培養。細胞分為3:組對照組、高糖組和高糖+葒草素組。高糖+葒草素組同時加入葒草素生理鹽水溶液,使培養液中葒草素濃度為10 μmol,分別給予低糖和高糖培養基培養48 h,進行后續實驗。然后用DCFH-DA 進行共聚焦染色,DCFH-DA 在ROS 的作用下在細胞內脫酯化,轉化為高熒光分子2′,7′-二氯熒光素。通過激發波長488 nm 和發射波長525 nm 28 的熒光強度測定細胞ROS 的產生。
1.3.6 Western-blot 檢測PGC-1β 的表達 用RI?PA 裂解緩沖液提取左心室組織和H9C2 的總蛋白。測定蛋白濃度后用10%十二烷基硫酸鈉-聚丙烯酰胺凝膠電泳分離每個樣品的蛋白質,再轉移到聚偏二氟乙烯膜(Millipore,USA)。將5%脫脂奶粉溶解在洗膜緩沖液中(150 mmol NaCl、50 mmol Tris(pH 7.5)和0.1%吐溫-20℃封閉膜2~3 h(20~25℃)。根據分子量分離膜,在4℃下與相應的一級抗體孵育12 h,再用相應的辣根過氧化物酶結合的第二抗體在20~25℃孵育2 h,加入電化學發光試劑,并使用CeimDoc XR(Bio Rad,美國)掃描印跡。對蛋白質條帶的灰度值進行可視化分析,以GAPDH 為內參對照。
1.4 統計學分析 應用GraphPad Prism 7.0 進行處理和分析,所有數據均以均數±標準差(±s)表示,多組間差異的統計學意義用單向ANOV A 處理,P<0.05 有統計學意義。
2 結果
2.1 外源補充葒草素顯著改善糖尿病導致的心功能損傷 8 周后小鼠心臟超聲檢測發現,DCM 組小鼠心功能較CON 組顯著損傷,表現為LVEF 和LVFS 顯著降低,而DCM+ORI 組能夠顯著改善小鼠心功能(圖1 A~C)。又檢測了反映心臟重構的心肌肥厚指數之一心體比(heart weight/body weight,HW/BW),結果顯示,DCM 組小鼠心體比較CON 組顯著升高,而DCM+ORI 組小鼠心體比較DCM 組顯著下調(圖1 D)。
2.2 外源補充葒草素顯著減輕糖尿病導致的心肌肥厚和纖維化 HE 染色結果顯示,DCM 組小鼠心肌細胞較CON 組顯著肥大,而DCM+ORI 組能夠顯著減輕DCM 組小鼠心肌細胞病理性肥大(圖2 A 和B)。MASSON 染色結果顯示,糖尿病心肌病小鼠左室壁心肌組織纖維化較CON 組顯著加重,而DCM+ORI 組小鼠心肌纖維化顯著減輕(圖2 C 和D)。
2.3 外源補充葒草素顯著減輕糖尿病小鼠心肌組織氧化應激損傷 DCM 組小鼠心肌組織MDA 含量較CON 組顯著升高,SOD 含量顯著降低,而DCM+ORI 組可以顯著減弱這種效應(圖3 a 和b)。進一步通過RT-qPCR 檢測氧化應激標志物NOX2 和NOX4 的mRNA 表達,結果顯示DCM 組小鼠心肌組織NOX2 和NOX4 表達量較CON 組顯著升高,而DCM+ORI 組能夠顯著降低NOX2 和NOX4 的表達(圖3 C 和D)。
2.4 葒草素顯著減輕高糖培養的H9C2 細胞氧化應激損傷 高糖組H9C2 細胞ROS 生成量較對照組顯著升高,而DCM+ORI 組能夠顯著減少高糖誘導的心肌細胞內ROS 生成,從而減輕氧化應激損傷(圖4)。
2.5 葒草素顯著增強糖尿病小鼠心肌組織和高糖培養H9C2 細胞PGC-1β 的表達 糖尿病小鼠心肌組織PGC-1β 的表達量較CON 組顯著降低,而DCM+ORI 組顯著激活糖尿病小鼠心肌組織內PGC-1β 的表達(圖5 A)。高糖培養下H9C2 心肌細胞內PGC-1β 表達量較對照組顯著降低,而高糖+葒草素組心肌細胞內PGC-1β 表達量顯著升高(圖5 B)。結果提示葒草素能夠顯著增強糖尿病小鼠心肌組織和高糖培養H9C2 細胞PGC-1β 的表達。
3 討論
近年來,由于多種中草藥被證實具有抗炎、抗凋亡、抗氧化應激的保護作用,成為心血管疾病領域的研究熱點[8]。葒草素就是其中之一,本研究首次證實葒草素治療能有效地抑制高糖誘導的心肌細胞氧化應激,無論是在體內還是在體外,最終都能阻止糖尿病心肌病小鼠心肌纖維化和心肌肥厚,改善心肌功能。在機制上,葒草素能夠通過激活心肌組織中的PGC-1β 發揮抗氧化應激作用,從而保護糖尿病心肌病小鼠心肌組織。
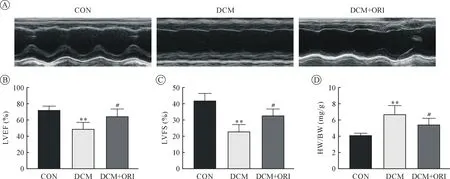
圖1 三組小鼠心臟超聲檢測LVEF、LVFS 和HW/BW 比較(n=6)
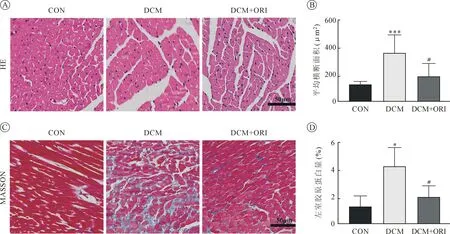
圖2 三組小鼠HE、MASSON 染色及橫截斷面積、左室膠原蛋白量比較(n=6)
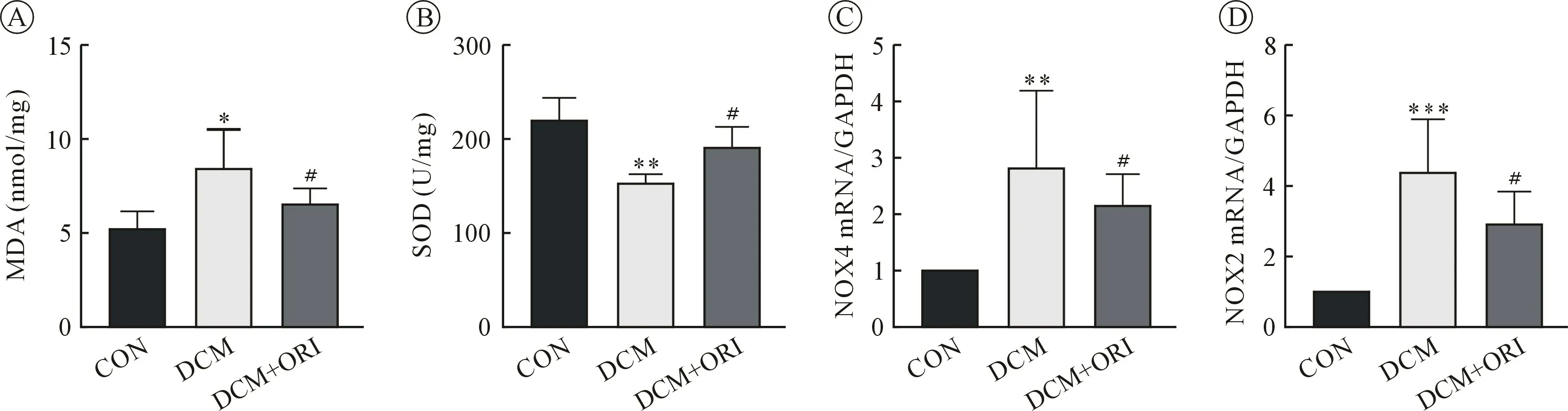
圖3 三組小鼠MDA、SOD、NOX4 和NOX2 表達的比較(n=6)
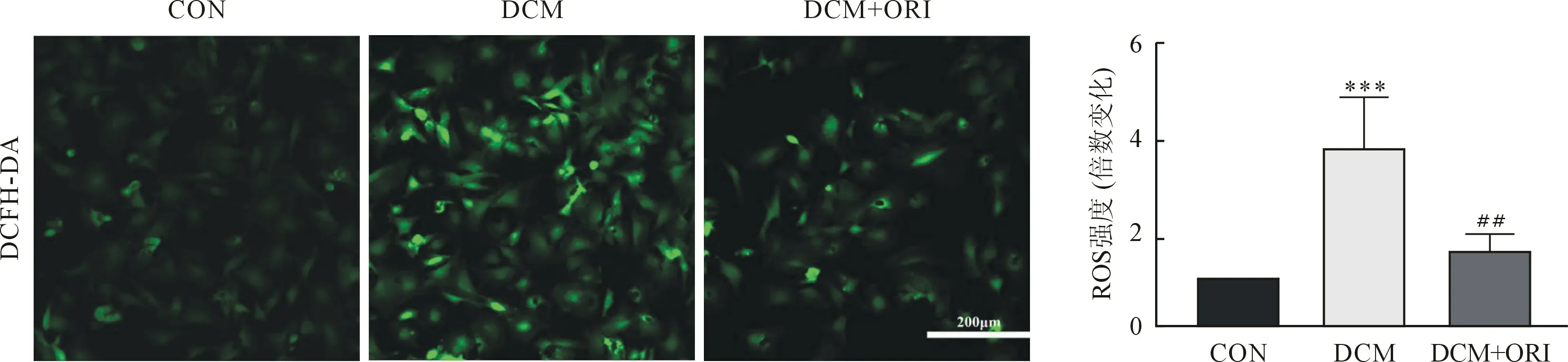
圖4 H9C2 細胞培養ROS 熒光強度比較(n=5)
糖尿病心肌病引起的心臟重塑的重要標志是心肌肥厚和心肌纖維化,心肌肥厚也通過增加的心臟質量反映。心肌纖維化和心肌細胞肥大是解釋糖尿病心肌病心臟改變的最常見機制。一些研究表明,糖尿病導致細胞鈣轉運缺陷、心肌收縮蛋白缺陷和膠原形成增加,導致心肌解剖和生理變化[9]。本研究結果顯示葒草素外源補充能夠顯著減輕糖尿病心肌病小鼠心肌組織肥厚和纖維化程度,提示葒草素能夠顯著改善糖尿病心肌損傷。在動物在體實驗中也有類似的發現,與對照動物相比,糖尿病動物的心率、收縮壓和收縮分數顯著降低[10]。臨床研究也提示,糖尿病與左室心肌收縮和舒張功能的附加損害獨立相關[11]。這些研究表明糖尿病是收縮功能障礙的原因之一,而本研究證實外源補充葒草素能夠顯著改善高糖導致的小鼠心功能障礙,也顯示了葒草素的心肌保護作用。
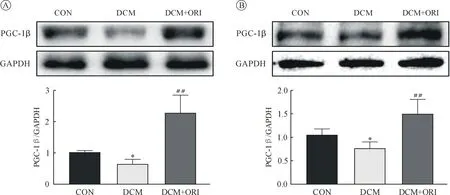
圖5 三組小鼠心肌組織和高糖培養H9C2 細胞PGC-1β 的表達
糖尿病心肌病的代謝異常刺激ROS 生成,如高血糖、高脂血癥和晚期糖基化終產物的積累,最終導致細胞內氧化應激[12]。持續升高的氧化應激狀態有過度消耗內源性抗氧化劑的趨勢,如SOD,并伴隨著氧化應激產物如MDA 在心臟中的積累[13-14]。檢測SOD、MDA 及ROS 的含量成為檢驗細胞或組織中氧化應激程度的重要檢測指標[15]。為了抵抗持續氧化應激的損害,已經形成了一系列內源性抗氧化機制,其中之一是過氧化體增殖活化受體γ 輔助活化受體因子(PGC-1β)[16]。PGC- 1β 主要在心臟等氧化組織中表達,并調節線粒體的生物合成和代謝以及包含電子傳遞鏈的蛋白質[17]。以往的研究表明,PGC-1β 在壓力超負荷誘導的心肌肥大過程中具有良好的保護作用,通過維持葡萄糖代謝和減輕氧化應激來抗心肌肥厚[18]。壓力超負荷下,心肌組織PGC-1β 的表達顯著降低,可導致心肌組織或心肌細胞ROS 生成、MDA 含量和NOX4 表達增加,SOD 活性降低,而通過激活PGC-1β 可以顯著逆轉這一效應[17]。本研究結果顯示,糖尿病心肌病小鼠心肌組織和高糖處理的H9C2 細胞PGC-1β 的表達較對照組顯著下調,而外源補充葒草素能夠顯著激活PGC-1β 的表達,提示葒草素能夠通過激活心肌細胞內PGC-1β 的表達發揮抗氧化應激作用,從而減輕高糖對心肌細胞的損傷。所有這些證據表明,靶向PGC-1β 可能是治療糖尿病心肌病的一種有前途的策略。葒草素前期被證實有多種藥理活性,如抗氧化應激、抗炎、抗癌和抗血栓活性[4-5]。葒草素能夠通過調節TLR4/NF-κB/TNF-α 信號通路發揮抗炎作用,從而對大鼠腦缺血/再灌注損傷發揮保護作用[6]。近期研究證實,葒草素能夠通過調節eNOS/NO 信號通路發揮抗氧化應激作用,從而能夠減輕小鼠心梗后心肌病理性重構[7]。
綜上所述,本研究從在體和離體兩方面展示了葒草素對糖尿病心肌損傷的保護作用,在機制上葒草素能夠通過激活PGC-1β 的表達,進一步減輕高糖誘導的心肌細胞氧化應激損傷,為糖尿病心肌病治療提供重要藥物治療靶點。后續實驗將進一步完善和深入,以增強論證強度,為葒草素進一步在臨床中糖尿病患者的應用提供理論依據。

