高效液相色譜-氫化物發生-原子熒光光譜法測定植物樣品中的4種砷形態
秦玉燕,藍 唯,蔣越華,王運儒,時鵬濤,呂麗蘭,呂玉蓮
(廣西壯族自治區亞熱帶作物研究所,農業部農產品質量安全風險評估實驗室(南寧),南寧 530001)
砷是一種毒性較強的重金屬污染物,是國際癌癥研究機構(IARC)最早確認的一類致癌物。攝入過量的砷可導致皮膚、消化、神經、生殖、造血以及免疫等系統不同程度的損傷。砷的毒性與其形態密切相關,無機砷包括砷酸[As(Ⅴ)]和亞砷酸[As(Ⅲ)],毒性均很強,且As(Ⅲ)毒性是As(Ⅴ)的60倍;有機砷如一甲基砷酸(MMA)、二甲基砷酸(DMA)毒性較弱;在海洋生物中分布較多的有機砷如砷膽堿(AsC)、砷甜菜堿(AsB)、砷糖、砷脂等基本無毒。因此,以總砷含量高低來評價食品的安全性并不科學,砷形態的分析對食品安全和環境健康風險評估具有重要意義。
目前,砷形態分析的前處理方式包括熱浸提[1]、振蕩提取[2]、超聲輔助提取[3]和微波輔助提取[4]等。文獻[5]在85 ℃下以0.15 mol·L-1硝酸溶液熱浸提菟絲子藥材1.5 h,得到其中6種砷形態的回收率為91.7%~105%。文獻[6]以體積比為1∶1的甲醇-水溶液超聲提取飼料樣品中的7種砷形態,得到的回收率為76.3%~108%。由于砷形態不穩定,樣品前處理過程的關鍵是在保證樣品中砷的原始形態不發生變化的同時獲得最大的提取效率。熱浸提和振蕩提取一般伴隨加熱,但溫度升高可能會引起砷形態的變化;超聲輔助提取可將樣品顆粒打碎,增加溶劑與顆粒的接觸面積,使包裹在顆粒內部的砷溶出;微波輔助提取操作較為復雜,實際應用較少[7]。另外,由于樣品中砷形態的差異和基質效應的影響,針對不同基質的樣品可能需要采用不同的前處理方法。
測定砷形態最常見的方法是高效液相色譜-電感耦合等離子體質譜法(HPLC-ICP-MS)[8-9]和高效液相色譜-氫化物發生-原子熒光光譜法(HPLCHG-AFS)[10-11]。HPLC-ICP-MS 具有靈敏度高的特點,近年來在元素形態分析方面發展迅速,但較高的儀器價格和運行費用使其無法在普通實驗室普及。HPLC-HG-AFS具有運行成本低、操作簡便和靈敏度高等特點,已廣泛應用于砷、汞、硒等元素的形態分析[12]。
蔬菜和谷類作物的砷攝入是人類攝取砷的主要途徑,其中,水稻、蔬菜(特別是水生蔬菜)等對砷的富集作用較強[13],且其中的砷主要以As(Ⅲ)、As(Ⅴ)、MMA、DMA 等4種砷形態存在[14-15]。因此,本工作以大米、蔬菜等植物性樣品為待測對象,通過優化樣品前處理方法和儀器工作條件,建立了As(Ⅲ)、As(Ⅴ)、MMA、DMA 等4 種砷形態的HPLC-HG-AFS分析方法。
1 試驗部分
1.1 儀器與試劑
SA-20型原子熒光形態分析儀,配有100μL進樣環的自動進樣器和933型原子熒光光度計;CNW IC-Guard RP凈化小柱(1 mL);ZHSY-50N 型振蕩培養箱;KQ-600型超聲波清洗器;Molcell 1810a細胞型超純水器;TGL-20M 型醫用離心機;AB204-S型電子天平。
4種砷形態混合標準儲備溶液:10 mg·L-1,介質為水。其他所需質量濃度均由此溶液用水稀釋制得。
砷酸根標準物質(GBW 08667,17.5μg·g-1,以硒計);亞砷酸根標準物質(GBW 08666,75.7μg·g-1);MMA 標準物 質(GBW 08668,25.1μg·g-1);DMA 標準物 質(GBW 08669,52.9μg·g-1)。大米粉 標準物 質 GBW (E)100356、GBW(E)100351、GBW(E)100348。
其他試劑均為分析純及以上;玻璃儀器均需在洗滌干凈后在25%(體積分數,下同)硝酸溶液中浸泡24 h,用水洗凈,晾干,備用。試驗用水為一級水(電阻率不小于18.25 MΩ·cm)。
1.2 儀器工作條件
1)HPLC 條件 Hamilton PRP-X100色譜柱(250 mm×4.1 mm,10μm);流動相為25 mmol·L-1磷酸氫二銨-甲酸溶液(pH 6.0),等度洗脫,流量1.0 mL·min-1;進樣體積100μL。
2)HG-AFS條件 還原劑為22.5 g·L-1硼氫化鉀和5 g·L-1氫氧化鈉混合溶液;載流為1.2 mol·L-1鹽酸溶 液;負高壓300 V;燈電流100 mA;輔助電流50 mA,載氣流量500 mL·min-1,屏蔽氣流量600 mL·min-1。
1.3 試驗方法
稱取1.000 g樣品于離心管中,加入0.15 mol·L-1硝酸溶液10 mL,超聲提取30 min,然后以8 000 r·min-1的轉速離心10 min,吸出上清液,重復提取1次,合并上清液,過0.45μm 水系濾膜后用CNW IC-Guard RP小柱凈化,按照儀器工作條件測定砷形態。
1.4 統計分析
試驗數據采用SPSS 22.0軟件進行統計分析,采用Duncan′s進行多重比較。
2 結果與討論
2.1 前處理方法的優化
砷形態的常用提取溶劑主要是水、酸溶液和甲醇溶液[16]。試驗對比了水、0.15 mol·L-1硝酸溶液和50%(體積分數,下同)甲醇溶液的提取效果。結果發現,水的提取效率最低;0.15 mol·L-1硝酸溶液的提取效率最高;50%甲醇溶液提取的樣品中As(Ⅲ)和As(Ⅴ)的峰形變寬,可能是由于樣品中殘留的少量甲醇引起的峰拖尾。因此試驗選擇0.15 mol·L-1硝酸溶液為提取溶劑。
基于文獻[17-18],以已知總砷含量為0.54 mg·kg-1的蓮藕為待測對象,試驗比較了70 ℃水浴振蕩提取2 h、90 ℃電熱板熱浸提2 h和超聲提取30 min等3種不同提取方式對砷形態的提取效果。計算3種方式下的4種砷形態提取率及含量總和,并對其進行顯著性差異分析,結果見表1。同時還進行了2個濃度水平的加標回收試驗,結果見表1。其中,測定值、砷形態總和和提取率為平均值±標準偏差(),a,b為差異顯著(P<0.05)標識;砷形態 總和為As(Ⅲ)、DMA、MMA 和As(Ⅴ)質量分數之和;提取率為砷形態總和占總砷含量的百分比。
由表1可知:蓮藕中主要的砷形態為As(Ⅲ)和As(Ⅴ);3種提取方式得到的砷提取率為87.7%~96.3%,其中,超聲提取的砷提取率最高。差異性分析結果表明,超聲提取得到的砷形態總和提取率的結果均顯著高于水浴振蕩提取和電熱板熱浸提(P<0.05);3種提取方式得到的回收率為75.6%~101%,其中,超聲提取對As(Ⅴ)、DMA 和MMA等3種砷形態的回收率均高于水浴振蕩提取和電熱板熱浸提的。綜合考慮,試驗選擇的提取方式為超聲提取。

表1 不同提取方式的影響Tab.1 Effect of the different extraction methods
試驗還發現,提取溶液經CNW IC-Guard RP小柱凈化后,可以有效去除樣品中的有機物雜質,改善色譜峰峰形和延長色譜柱的使用壽命。因此,試驗在對樣品進行提取后又增加了CNW IC-Guard RP小柱凈化這一步驟。
2.2 色譜分離條件的優化
2.2.1 流動相酸度
以40 mmol·L-1磷酸氫二銨溶液為流動相,用20%(體積分數,下同)甲酸溶液調節其酸度,考察了不同流動相酸度對砷形態分離效果的影響,結果見圖1。
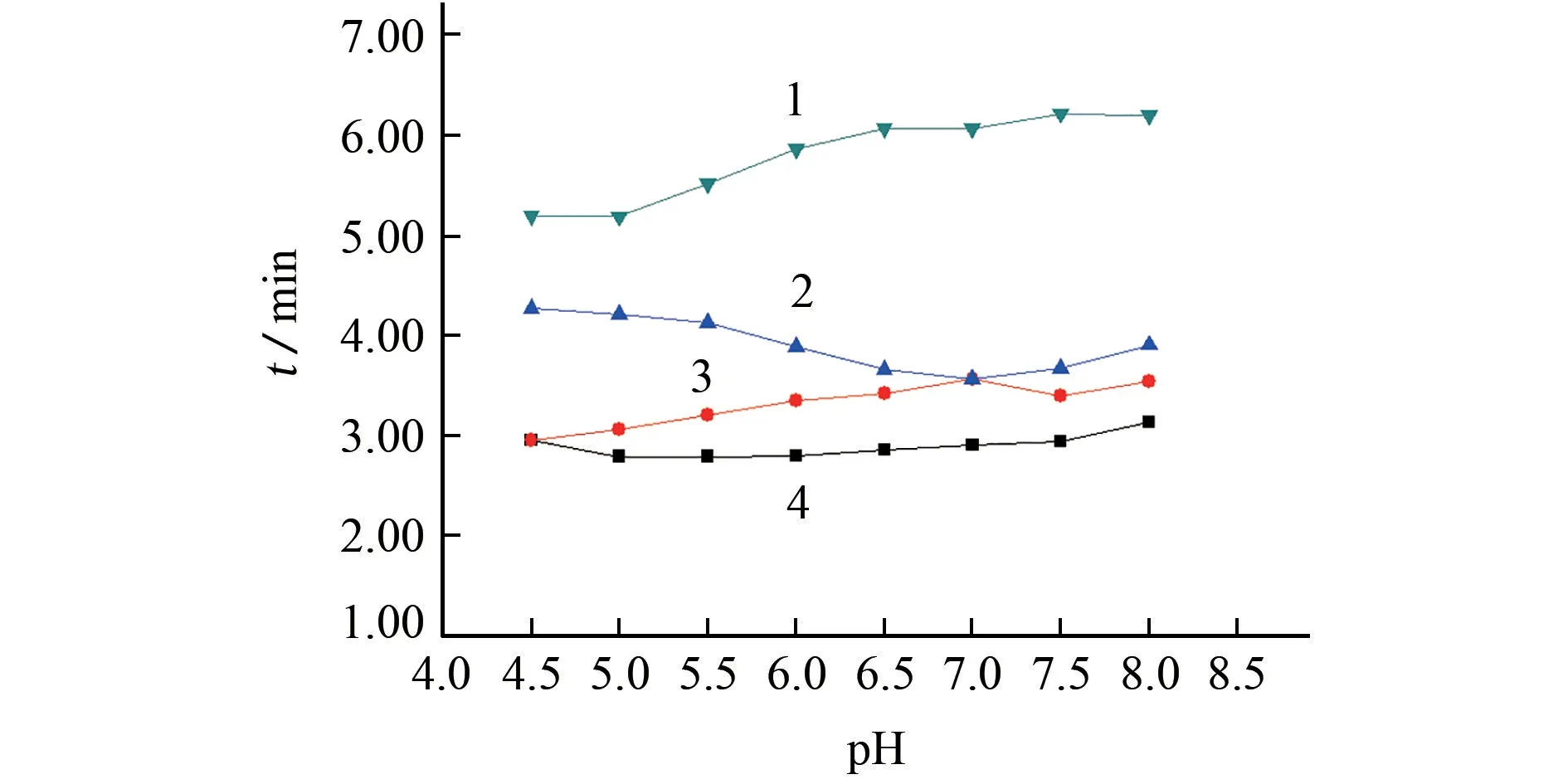
圖1 4種砷形態的保留時間隨流動相酸度變化的曲線Fig.1 Curves showing changes of retention time of 4 arsenic species with the acidity of mobile phase
由圖1可知:流動相pH 為4.5~8.0 時,隨著pH 增大,As(Ⅲ)的保留時間變化不明顯,DMA 和As(Ⅴ)的保留時間緩慢延長,MMA 的保留時間緩慢縮短。流動相pH 為4.5~5.0 時,As(Ⅲ)和DMA 部分重疊;pH 為6.5~8.0時,DMA 和MMA保留時間部分重疊;pH 為5.5~6.0時,4種砷形態可完全分離,其中,pH 6.0時分離效果最好,因此試驗選擇流動相的pH 為6.0。
2.2.2 流動相濃度
試驗考察了流動相濃度對4種砷形態分離效果的影響,結果見圖2。
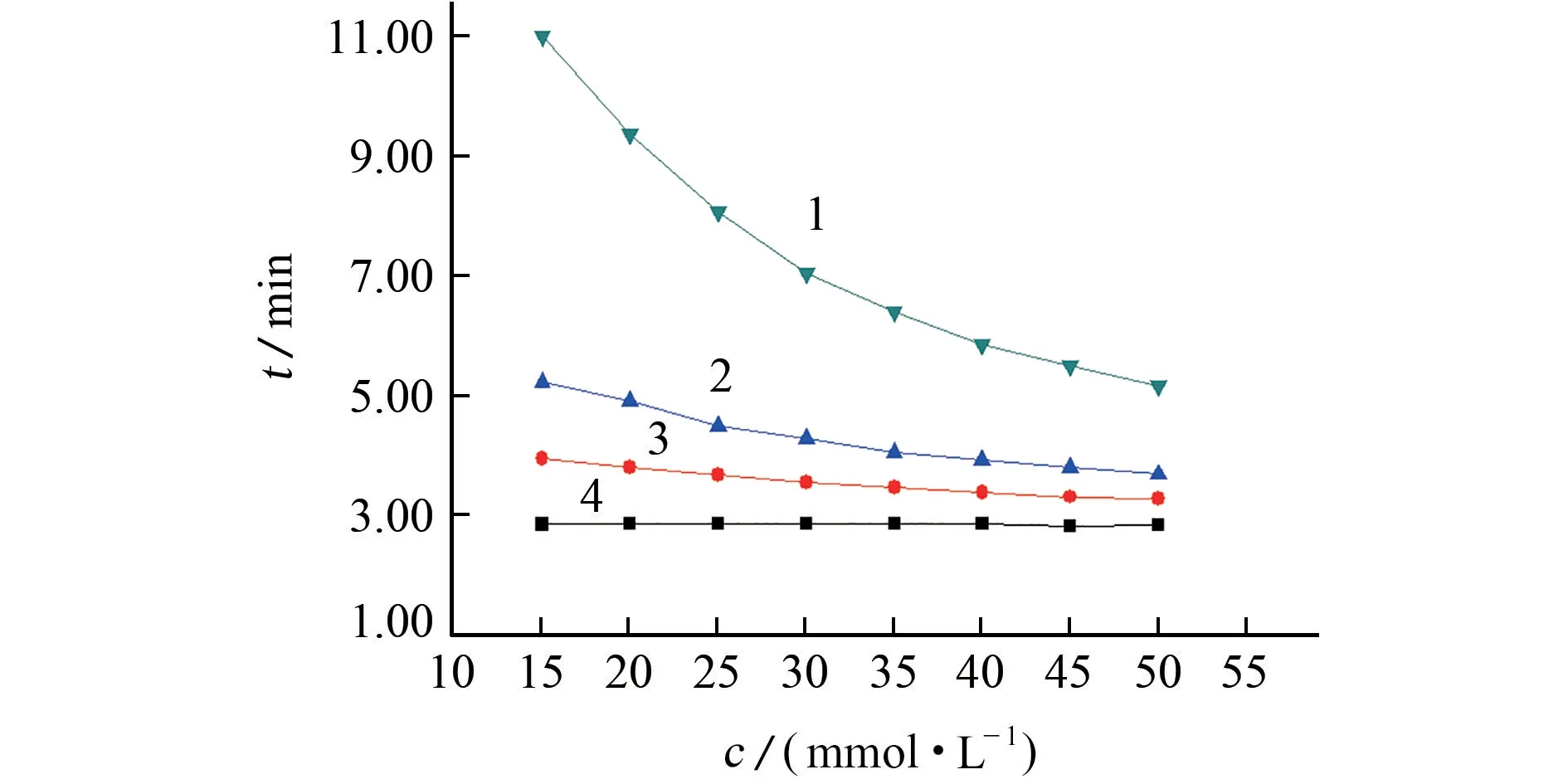
圖2 4種砷形態的保留時間隨磷酸氫二銨濃度變化的曲線Fig.2 Curves showing changes of retention time of 4 arsenic species with concentration of potassium hydrogen phosphate solution
由圖2可知:當磷酸氫二銨溶液的濃度為15~50 mmol·L-1時,隨著濃度的增大,As(Ⅲ)的保留時間變化不明顯,DMA 和MMA 的保留時間緩慢縮短,As(Ⅴ)的保留時間顯著縮短;當磷酸氫二銨溶液濃度為45~50 mmol·L-1時,As(Ⅲ)、DMA和MMA 會發生部分色譜峰重疊;當磷酸氫二銨溶液濃度為15~40 mmol·L-1時,4種砷形態可完全分離。綜合考慮分離度和工作效率,試驗選擇磷酸氫二銨的濃度為25 mmol·L-1,此時,4種砷形態在9 min內完全分離,色譜圖見圖3。
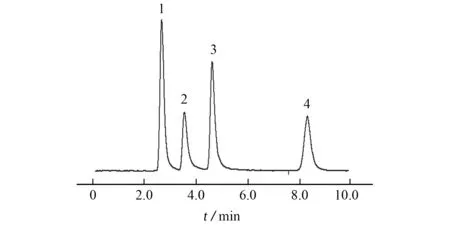
圖3 4種砷形態混合標準溶液的色譜圖Fig.3 Chromatogram of mixed standard solution of 4 arsenic species
2.3 氫化物發生條件的優化
2.3.1 硼氫化鉀質量濃度
試驗考察了硼氫化鉀的質量濃度對砷峰面積的影響,結果見圖4。
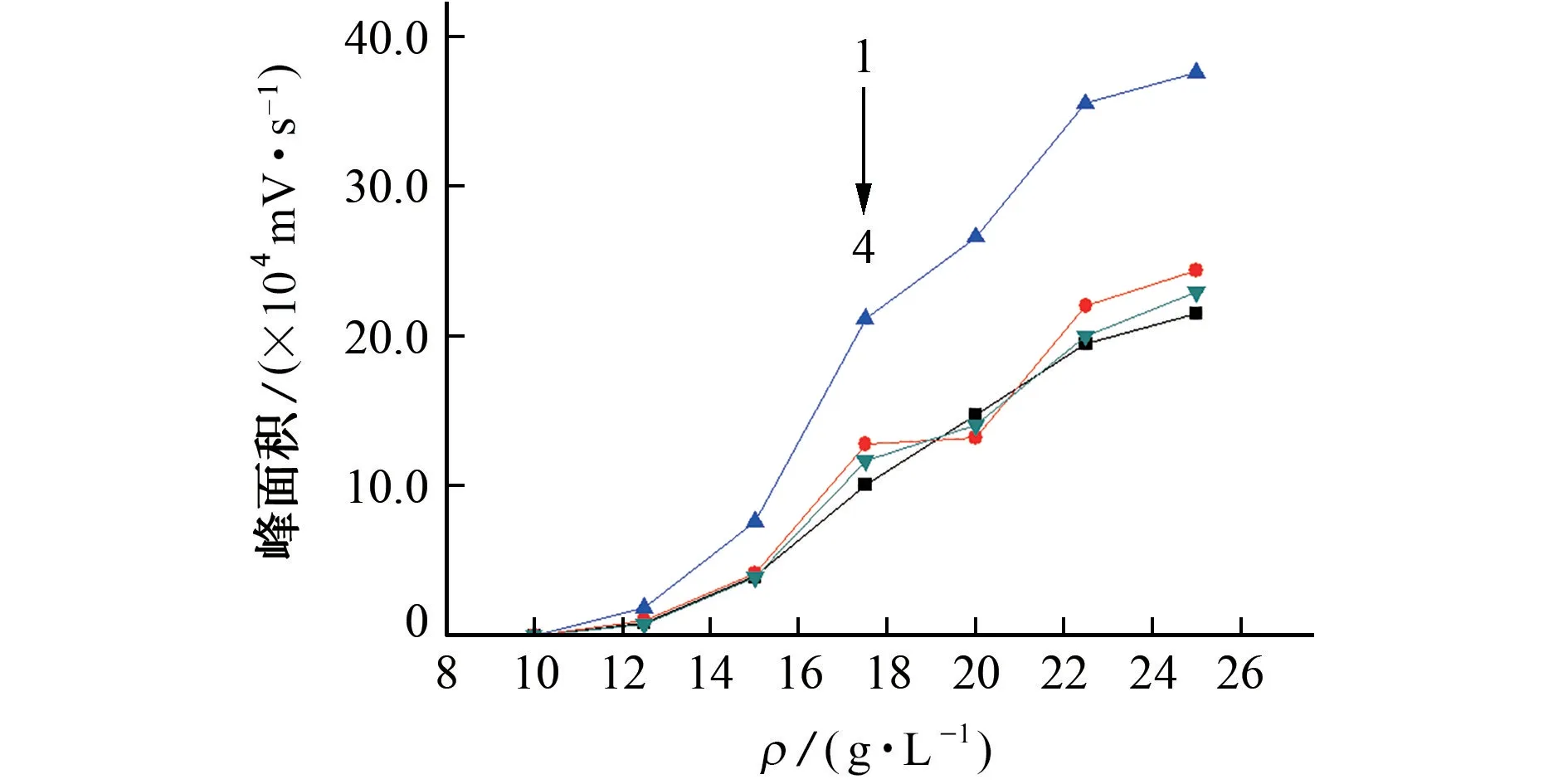
圖4 4種砷形態的峰面積隨硼氫化鉀溶液質量濃度變化的曲線Fig.4 Curves showing changes of peak area of 4 arsenic species with mass concentration of potassium borohydride solution
由圖4可知:當硼氫化鉀的質量濃度為10.0~22.5 g·L-1時,隨著質量濃度的增加,4種砷形態的峰面積均顯著增大;當質量濃度大于22.5 g·L-1時,峰面積增加幅度變緩,這是由于隨著硼氫化鉀質量濃度的增大,噪音逐漸增強所致。因此試驗選擇硼氫化鉀溶液質量濃度為22.5 g·L-1。
2.3.2 載流種類
當載流提供的氫離子濃度為1.2 mol·L-1時,其與硼氫化鉀反應產生的活性氫足夠將砷還原成氣態氫化物,故試驗考察了鹽酸溶液、硝酸溶液和硫酸溶液的濃度均為1.2 mol·L-1時對砷峰面積的影響,結果見圖5。
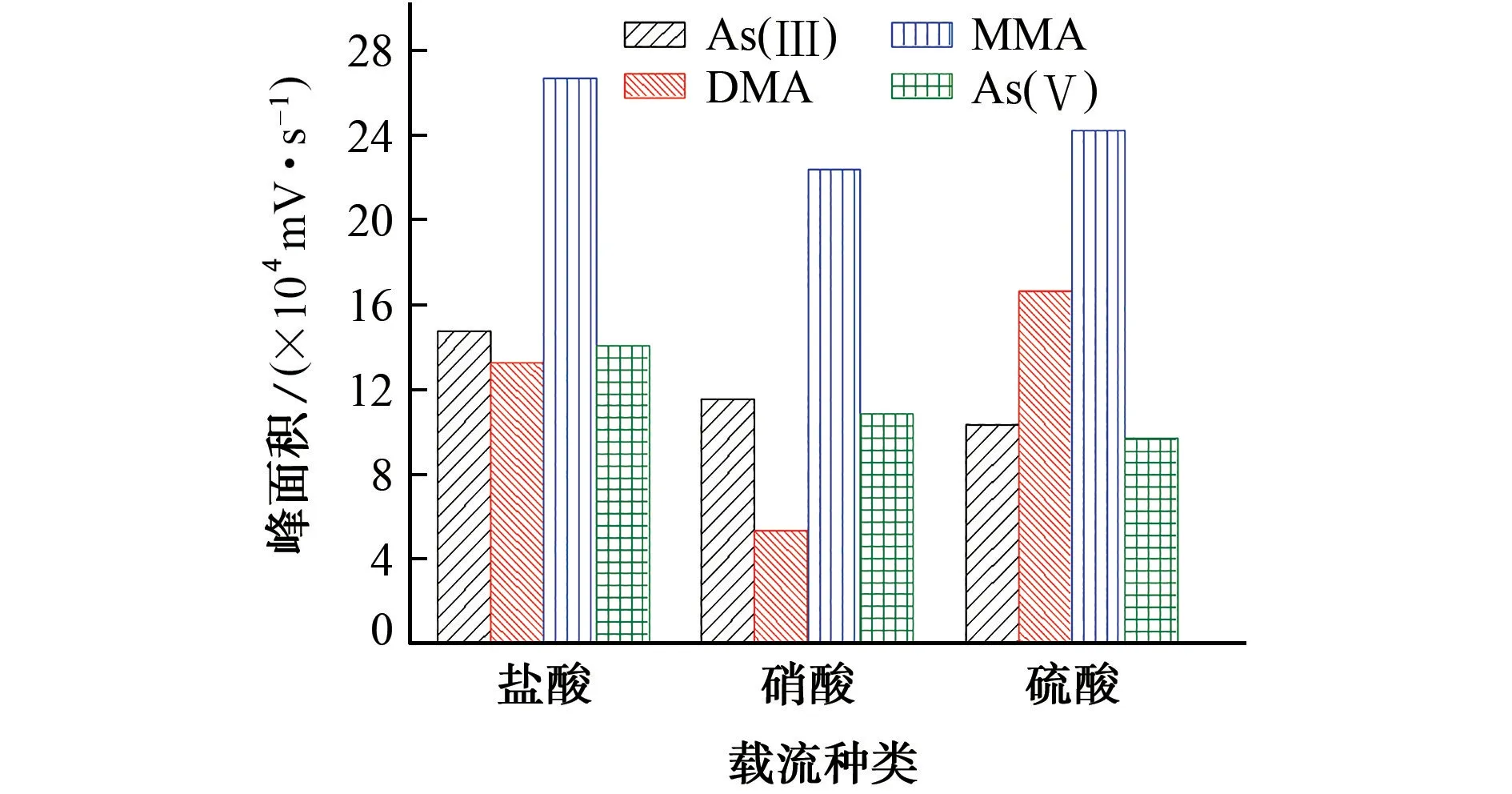
圖5 4種砷形態的峰面積隨酸種類變化的柱狀圖Fig.5 Histogram showing peak area of the 4 arsenic species with acid type
由圖5 可知:以鹽酸溶液為載流時,As(Ⅲ)、MMA 和As(Ⅴ)的峰面積均最高,DMA 的峰面積僅次于以硫酸溶液為載流時的,因此試驗選擇1.2 mol·L-1鹽酸溶液為載流。
2.4 標準曲線和檢出限
按照試驗方法測定5,10,20,50,100μg·L-1的混合標準溶液系列,以4種砷形態的質量濃度為橫坐標,其對應的色譜峰面積為縱坐標繪制標準曲線。結果表明:4 種砷形態的線性范圍均為5~100μg·L-1,線性回歸方程、相關系數見表2。
以3倍信噪比(S/N)計算4種砷形態的檢出限(3S/N),所得結果見表2。
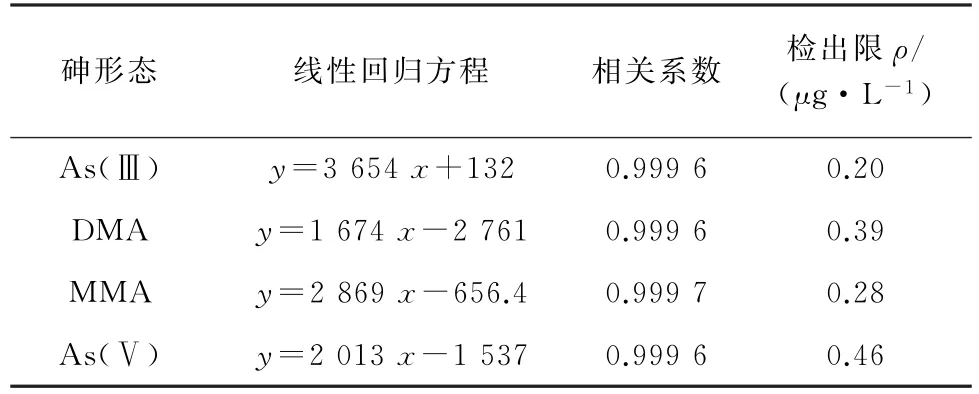
表2 4種砷形態的線性參數和檢出限Tab.2 Linearity parameters and detection limits of 4 arsenic species
2.5 精密度和回收試驗
按照試驗方法對空白樣品進行2 個濃度水平(0.25,0.50 mg·kg-1)的加標回收試驗,每個加標水平測定6次,計算回收率和測定值的相對標準偏差(RSD),4種砷形態的回收率為80.0%~101%,測定值的RSD 為2.1%~5.0%。
2.6 準確度試驗
按照試驗方法對3 種大米粉標準物質GBW(E)100356、GBW(E)100351和GBW(E)100348進行測定,結果見表3,其中無機砷值為As(Ⅲ)和As(Ⅴ)質量分數之和。
由表3可知:3種大米粉標準物質的無機砷值和砷形態總和都在推薦范圍之內,結果符合試驗準確度的要求。

表3 準確度試驗結果Tab.3 Results of test for accurary
2.7 樣品分析
按照試驗方法對大米、芥菜、空心菜、蓮藕、柑橘葉片等植物樣品中的砷形態進行測定,結果見表4,其中,樣品總砷含量按照國家標準GB 5009.11-2014《食品安全國家標準 食品中總砷及無機砷的測定》,采用原子熒光法進行測定。
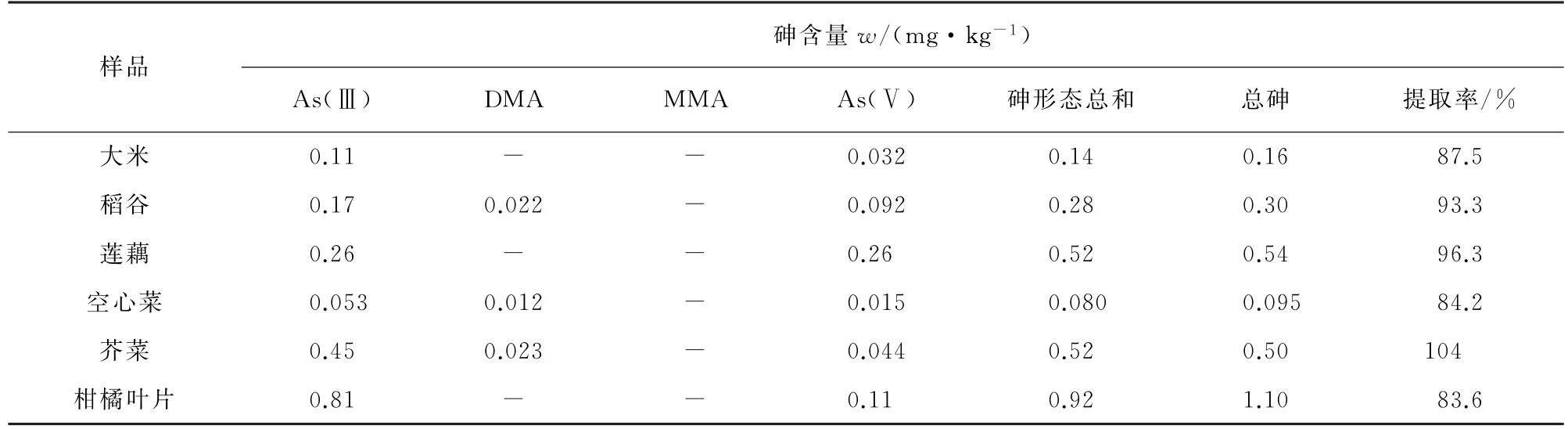
表4 樣品分析結果Tab.4 Analytical results of samples
由表4可知:5種樣品中都檢測出了As(Ⅲ)和As(Ⅴ),部分樣品檢出少量DMA,但均未檢出MMA。除了蓮藕樣品外,其他樣品中As(Ⅲ)的含量均高于As(Ⅴ)的,說明大部分植物樣品中的砷主要以毒性較強的As(Ⅲ)存在。4種砷形態總和與總砷測定結果基本一致,樣品中砷的提取率為84.2%~104%,說明HPLC-HG-AFS 不僅可以有效分離樣品中的4種砷形態,而且可以進行準確的定量分析。
本工作建立了HPLC-HG-AFS測定植物樣品中4種砷形態的方法,該方法準確、簡便、靈敏,適用于植物樣品中4種砷形態的測定。

