碳量子點/金屬有機骨架材料修飾玻碳電極用于雙酚A的電化學檢測
羌 越,陳 璐,張 靜
(常州大學 石油化工學院 食品學院,常州 213164)
雙酚A[2,2-雙(4-羥基苯基)丙烷,BPA]作為一種有機單體,可廣泛用于制造環氧樹脂,聚碳酸酯和聚苯乙烯樹脂等材料,常見于嬰兒奶瓶、食品和飲料容器以及熱敏紙等物品中,在使用過程中,BPA可能從這些塑料包裝遷移到食物中。BPA 是一種對人體有毒害作用的材料,不僅會影響機體的內分泌系統,還會增加患癌風險[1-2]。因此,開發一種簡便、高靈敏、可有效測定BPA 含量的方法對于人類健康事業刻不容緩。
電化學法是一種能夠較好地測定BPA 含量的方法,具有操作簡便、費用低、靈敏度高、抗干擾性強、線性范圍寬等優點,其關鍵步驟是化學修飾電極的制備。目前,已經有大量的新型功能性材料,如離子液體、氧化物納米材料、碳納米材料、貴金屬納米材料以及納米復合材料等,可用于制備化學修飾電極[3-9]。其中,金屬有機骨架材料(MOFs)是由無機中心離子與有機配體通過配位鍵自組裝形成的材料,其性能優異,已應用于多種領域[10-11]。當MOFs材料作為載體和催化劑修飾電極時,可用于檢測8-羥基脫氧鳥苷[12]、重金屬離子[13]、過氧化氫[14]等。本工作合成了一種具有木柴狀納米棒結構的鈰-金屬有機骨架材料(Ce-MOFs),通過靜電吸附作用將陽離子聚合物聚二甲基二烯丙基氯化銨(PDDA)修飾的碳量子點(CDs)負載于Ce-MOFs上得到PDDA-CDs/Ce-MOFs復合物,將復合物滴涂在玻碳電極(GCE)表面構建了基于PDDA-CDs/Ce-MOFs的修飾電極(PDDA-CDs/Ce-MOFs/GCE)用于牛奶樣品中BPA 含量測定的電化學方法。
1 試驗部分
1.1 儀器與試劑
CHI 660E 型電化學工作站;DF-101S 型水浴鍋;RE-201DRE-501型離心機;TG16-WS型旋轉蒸發儀;JEM-2100 型透射電子顯微鏡(TEM);SUPRA 55型掃描電子顯微鏡(SEM);玻碳電極(直徑3 mm)。
三電極體系:工作電極為PDDA-CDs/Ce-MOFs/GCE,對電極為鉑絲電極,參比電極為飽和甘汞電極(SCE)。
磷酸鹽緩沖溶液:用磷酸二氫鈉和磷酸氫二鈉配制0.1 mol·L-1的磷酸鹽緩沖溶液,pH 為7.0,用作支持電解質。
BPA、六水合硝酸鈰、1,3,5-均苯三甲酸、乙醇、PDDA、乙二胺、檸檬酸、磷酸氫二鈉、磷酸二氫鈉、氫氧化鈉、一氯代乙酸、鹽酸等試劑均為分析純;試驗用水為超純水;6種牛奶樣品均采購自當地超市。
1.2 儀器工作條件
1)富集條件 富集時間150 s,富集電位0.3 V。
2)差示脈沖伏安條件 掃描電位0.1~0.9 V,脈沖振幅50 m V,脈沖寬度50 ms。
1.3 試驗方法
1.3.1 Ce-MOFs的制備
根據文獻[15]合成Ce-MOFs,具體方法為:稱取0.105 g 1,3,5-均苯三甲酸溶解在50%(體積分數)乙醇溶液5 mL中,配制成0.1 mol·L-11,3,5-均苯三甲酸溶液。稱取0.217 g六水合硝酸鈰溶解在5 mL水中,配制成0.1 mol·L-1六水合硝酸鈰溶液。在劇烈攪拌條件下,將六水合硝酸鈰溶液逐滴加入到1,3,5-均苯三甲酸溶液中,并在60 ℃的水浴中靜置1 h。反應完成后,以10 000 r·min-1轉速離心10 min,所得白色沉淀用水洗滌3次,然后在60 ℃下干燥,即得Ce-MOFs,備用。
1.3.2 PDDA-CDs的制備
根據文獻[16]合成PDDA-CDs,具體方法為:將2.5 g檸檬酸和1.5 mL 乙二胺溶解在25 mL 水中,充分攪拌混合,將混合溶液轉移到50 mL 聚四氟乙烯襯里的高壓釜中,在150℃下反應6 h。將得到的淡黃色產物置于透析袋中,用水透析,2 h換一次水,共透析12次。透析完成后,將溶液旋蒸至近干,加丙酮進行沉淀,并用乙醇洗滌沉淀3 次,在60 ℃下干燥成粉末。將2.5 g氫氧化鈉和2.5 g一氯代乙酸溶解于50 mL 水中,加入50 mg 上述粉末,在25 ℃水浴中超聲3 h后,用0.1 mol·L-1鹽酸溶液調節其pH 至7,用透析袋透析12 h,將溶液旋蒸至原體積一半,即可得到目標CDs 溶液(2.0 g·L-1)。將2.0 mg PDDA 分散在1 mL 0.1 mol·L-1氯化鈉溶液中,得到2.0 g·L-1PDDA 溶液。將PDDA 溶液0.5 mL和2.0 g·L-1CDs溶液0.5 mL 攪拌混合,即可得到初始質量濃度為2.0 g·L-1的PDDA-CDs溶液。
1.3.3 PDDA-CDs/Ce-MOFs的制備
稱取2.0 mg Ce-MOFs均勻分散在1.0 mL 水中,得到Ce-MOFs溶液的初始質量濃度為2.0 g·L-1。加入1.0 mL的2.0 g·L-1PDDA-CDs溶液,室溫下超聲混合1 h,使PDDA-CDs通過靜電吸附作用負載在Ce-MOFs表面,以8 000 r·min-1的轉速離心10 min后,用水洗滌沉淀物數次,將其分散于水中。
1.3.4 修飾電極的制備
依次用0.3μm 和0.05μm 氧化鋁漿料拋光GCE,用水沖洗干凈后,依次在50%(體積分數)硝酸溶液、丙酮和水中超聲處理,在室溫下自然晾干。滴加2.0 g·L-1PDDA-CDs/Ce-MOFs 懸浮液4μL于處理好的電極表面,在室溫下自然晾干,得到PDDA-CDs/Ce-MOFs/GCE。同法制備 Ce-MOFs/GCE和PDDA-CDs/GCE。
1.4 樣品的測試
在20 mL支持電解質磷酸鹽緩沖溶液中滴加5 mL牛奶樣品,超聲15 min,振蕩15 min,以10 000 r·min-1轉速離心20 min,吸取1 mL 中層的乳清溶液于25 mL容量瓶中,用磷酸鹽緩沖溶液稀釋至刻度,分取20 mL 溶液至25 mL 燒杯中,根據儀器工作條件,先對其中的BPA 進行富集,平衡30 s后,采用差示脈沖伏安法對BPA 含量進行測定。
2 結果與討論
2.1 修飾材料的形貌表征
對修飾材料進行了TEM 和SEM 表征,結果見圖1。
由圖1(a)可以看出:PDDA-CDs為球形,粒徑約為3 nm,分散性較好;由圖1(b)和圖1(c)可以看出,Ce-MOFs為較均勻的木柴狀納米棒結構,這種結構的比表面積較大,有利于納米粒子和分析物的吸附;由圖1(d)可以看出,PDDA-CDs已均勻吸附在Ce-MOFs的表面,表明合成的PDDA-CDs/Ce-MOFs具有很好的復合結構。
2.2 BPA在修飾電極上的電化學響應
試驗分別采用GCE、PDDA-CDs/GCE、Ce-MOFs/GCE、PDDA-CDs/Ce-MOFs/GCE 富 集5.0μmol·L-1BPA 標準溶液后,對其進行差分脈沖伏安測試,以考察不同電極對BPA 電化學響應的效果(分別對應圖2曲線1,2,3,4),對照組考察了不富集BPA 時PDDA-CDs/Ce-MOFs/GCE的電化學行為(曲線5),響應結果見圖2。

圖1 修飾材料的TEM 和SEM 圖Fig.1 TEM and SEM images of modified materials
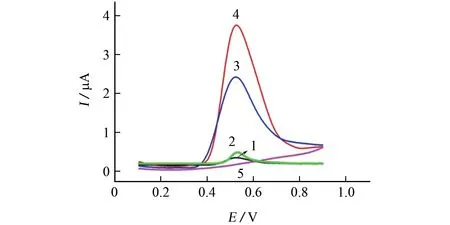
圖2 不同修飾電極對BPA 及對照組的電化學響應Fig.2 Electrochemical response of the different modified electrodes to BPA and control group
由圖2可知:BPA 在GCE 上具有微弱的電化學響應,在0.53 V 左右出現一個小而穩定的氧化峰,峰電流約為0.12μA,這是由BPA 中的羥基氧化成醌所致(曲線1);在PDDA-CDs/GCE 上,電化學響應略微提高,峰電流約為0.28μA,表明PDDACDs對BPA 的氧化有一定的催化作用(曲線2);在Ce-MOFs/GCE上,峰電流是GCE 的20倍,這可歸因于Ce-MOFs優良的電催化性能和較大的比表面積(曲線3);PDDA-CDs/Ce-MOFs/GCE對BPA 電化學響應最好,峰電流約為GCE的25倍,這可歸因于PDDA-CDs和Ce-MOFs之間的良好的協同作用(曲線4);而未富集BPA 的PDDA-CDs/Ce-MOFs/GCE的空白電流較小,沒有出現明顯的BPA 氧化峰,說明該修飾電極具有較小的背景電流和較低的干擾(曲線5)。
綜上所述,PDDA-CDs/Ce-MOFs/GCE 對于BPA 有較高的電化學響應,能夠顯著提高GCE 對BPA 電化學催化能力。
2.3 修飾電極制備條件的選擇
2.3.1 PDDA-CDs溶液的初始質量濃度
試驗考察了PDDA-CDs溶液質量濃度為1.0~3.0 g·L-1時制備的PDDA-CDs/CE-MOFs/GCE對BPA 電化學響應效果的影響,結果見圖3。
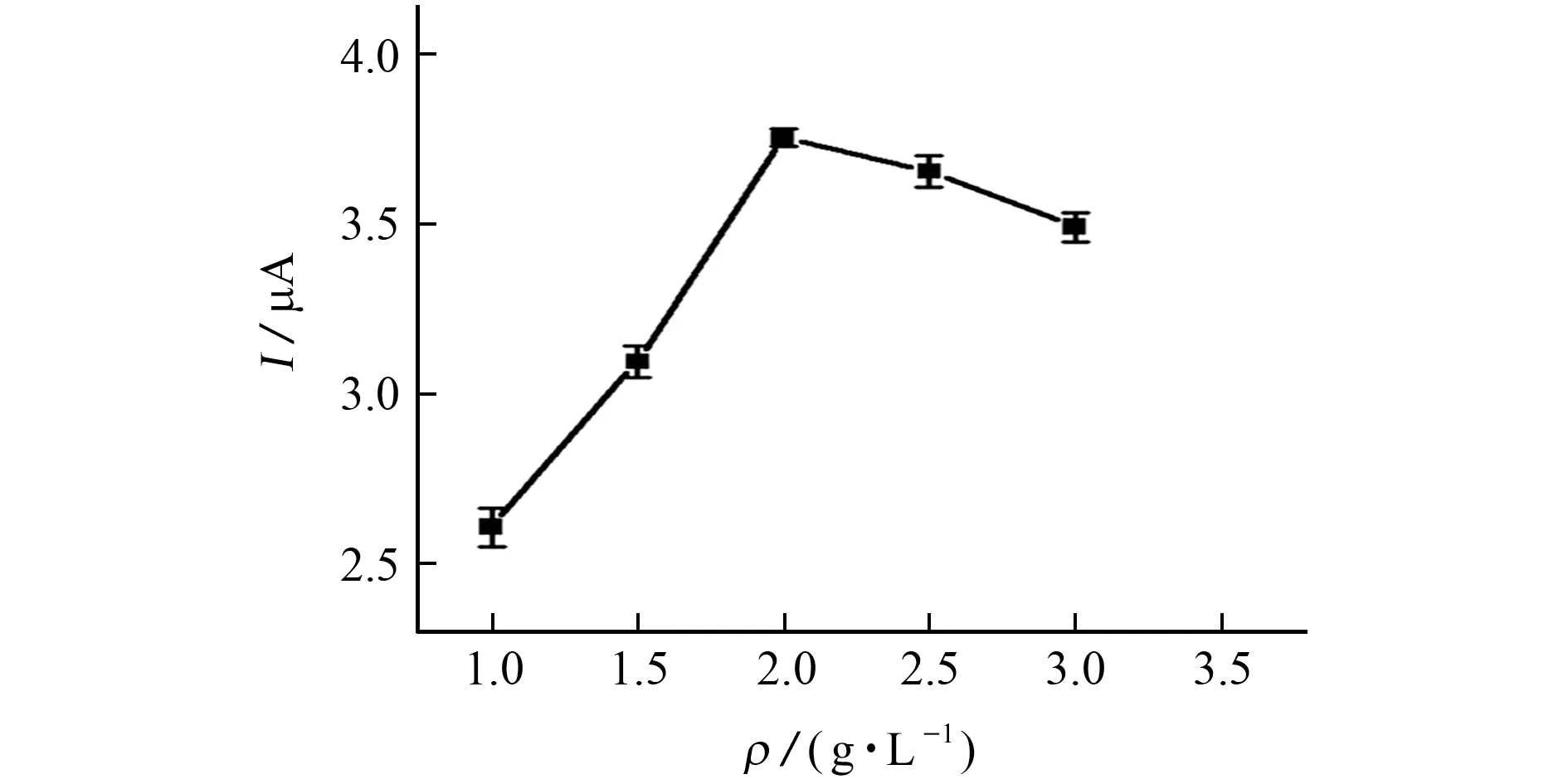
圖3 PDDA-CDs溶液的初始質量濃度對峰電流的影響Fig.3 Effect of initial mass concentration of PDDA-CDs solution on peak current
由圖3可知:當PDDA-CDs溶液初始質量濃度為1.0~2.0 g·L-1時,BPA 的氧化峰電流呈上升趨勢:而當PDDA-CDs溶液的初始質量濃度進一步增大時,響應電流下降。這可能是因為PDDA-CDs溶液的初始質量濃度增加至2.0 g·L-1時,電化學位點較多,促進了BPA 的氧化;而當其質量濃度進一步增加時,會使BPA 和電極表面之間的電子交換受阻。綜上,試驗選擇PDDA-CDs溶液的初始質量濃度為2.0 g·L-1。
2.3.2 Ce-MOFs溶液的初始質量濃度
試驗考察了Ce-MOFs溶液的初始質量濃度為1.0~3.0 g·L-1時制備的PDDA-CDs/Ce-MOFs/GCE對BPA 電化學響應效果的影響,結果見圖4。
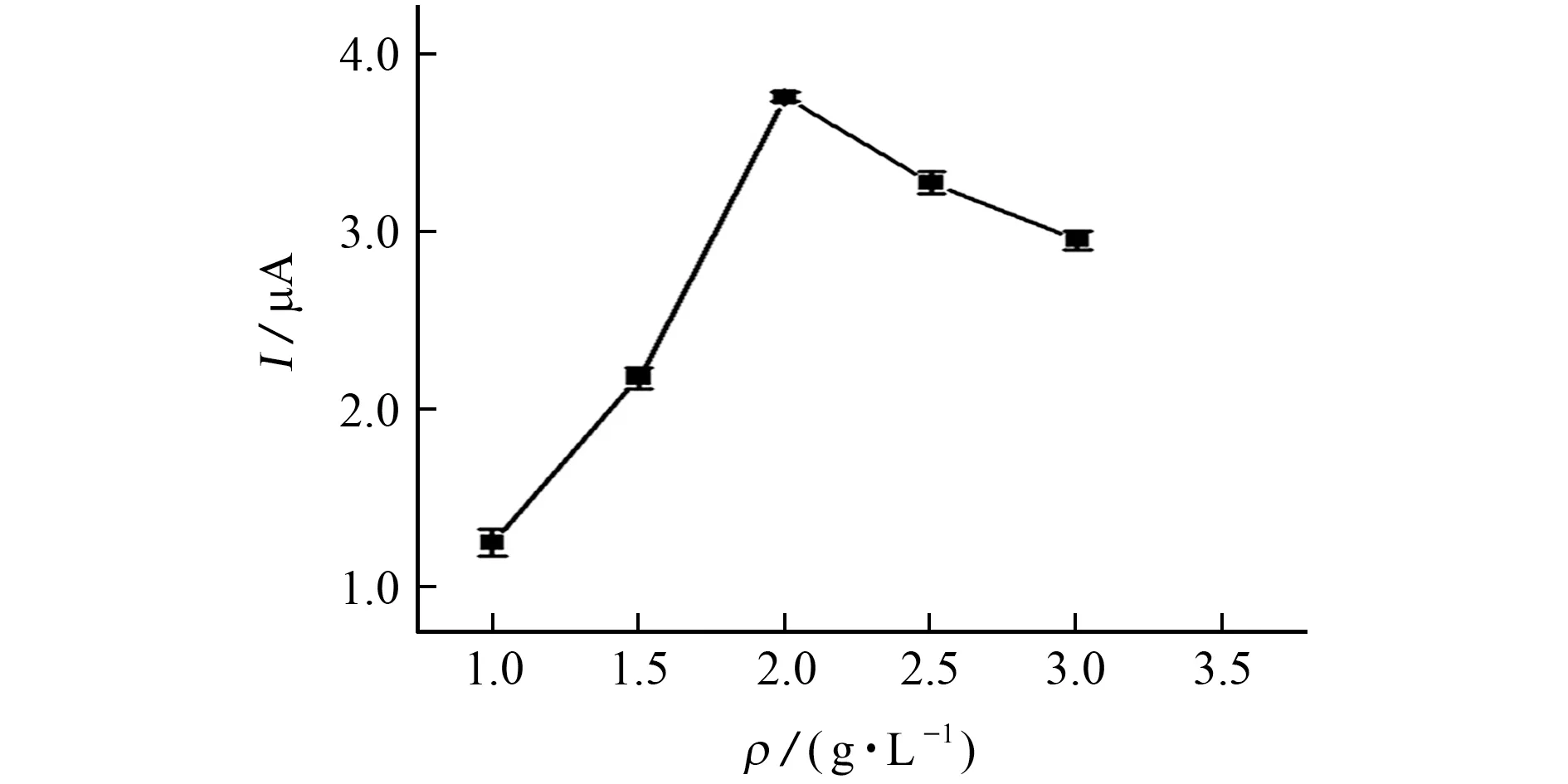
圖4 Ce-MOFs溶液的初始質量濃度對峰電流的影響Fig.4 Effect of initial mass concentration of Ce-MOFs solution on peak current
由圖4 可知:當Ce-MOFs溶液的初始質量濃度為1.0~2.0 g·L-1,修飾電極對BPA 的響應電流逐漸增加;而當Ce-MOFs溶液的初始質量濃度進一步增大時,響應電流逐漸降低。這可能是由于較高初始質量濃度的Ce-MOFs溶液阻止了BPA和電極表面之間的電子交換。因此,試驗選擇2.0 g·L-1Ce-MOFs 溶液制備PDDA-CDs/Ce-MOFs/GCE。
2.3.3 PDDA-CDs/Ce-MOFs懸浮液用量
試驗考察了PDDA-CDs/Ce-MOFs懸浮液用量為2~6μL時制備的修飾電極對BPA 電化學響應效果的影響,結果見圖5。
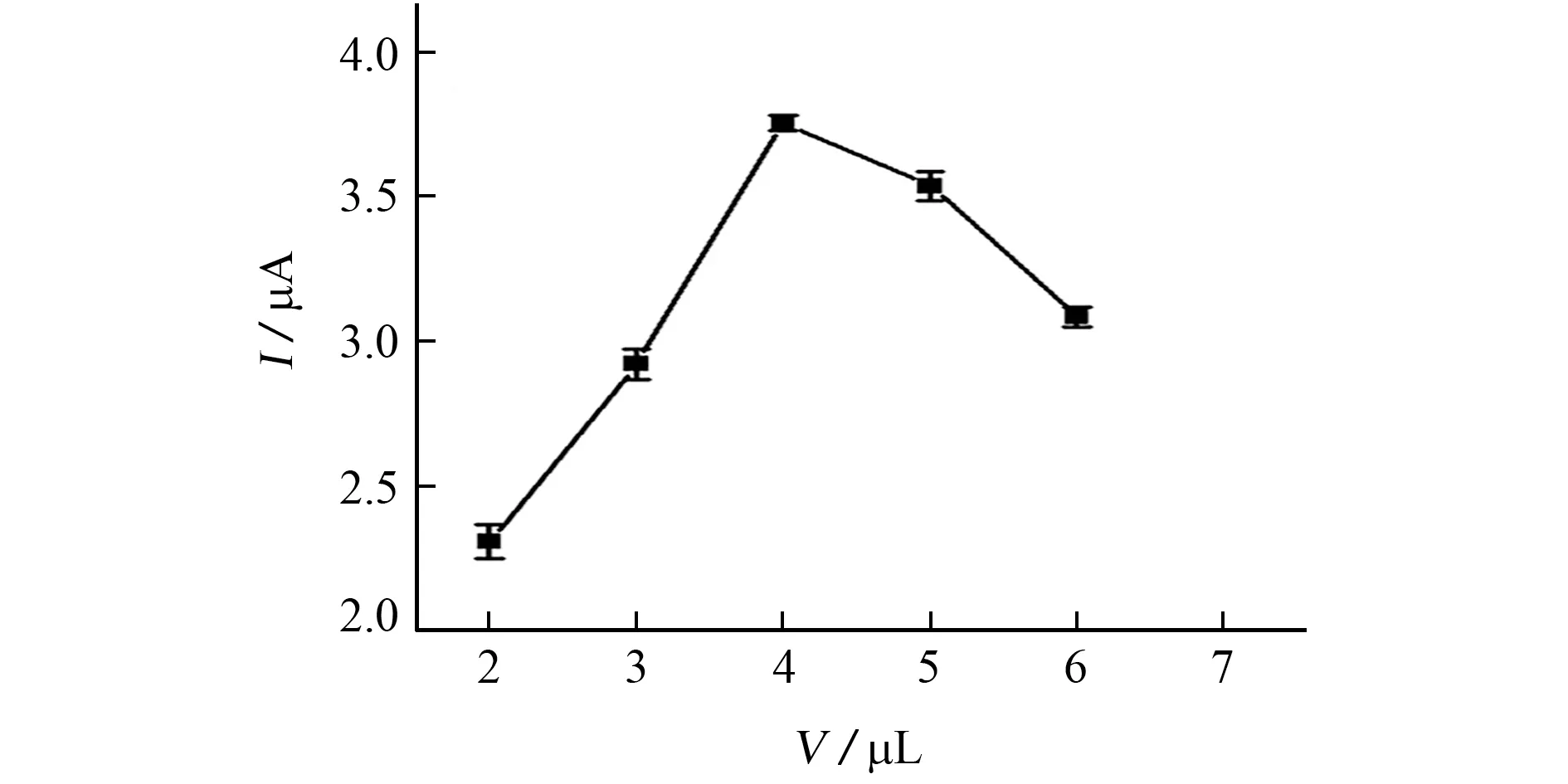
圖5 PDDA-CDs/Ce-MOFs懸浮液用量對峰電流的影響Fig.5 Effect of amount of PDDA-CDs/Ce-MOFs suspension on peak current
由圖5可知:當PDDA-CDs/Ce-MOFs懸浮液用量為4μL時,BPA 的氧化峰電流最大;而當其用量進一步增大時,修飾電極對BPA 的響應電流下降,這可能因為過量的PDDA-CDs/Ce-MOFs會在GCE表面形成較厚的修飾膜,阻礙了BPA 和電極表面的電子交換,進而影響到修飾電極的催化性能。所以,試驗選擇用4μL PDDA-CDs/Ce-MOFs懸浮液制備修飾電極。
2.4 儀器工作條件的選擇
2.4.1 富集時間
由于富集時間會影響修飾電極的靈敏度,試驗考察了富集時間為30~210 s時PDDA-CDs/Ce-MOFs/GCE對BPA 電化學響應效果的影響,結果見圖6。
由圖6可知:當富集時間為150 s時,響應電流達到最大;繼續延長富集時間,響應電流變化不大,說明修飾電極吸附的BPA 已趨于飽和。因此,試驗選擇的富集時間為150 s。
2.4.2 富集電位
試驗考察了富集電位為0~0.4 V 時PDDACDs/Ce-MOFs/GCE對BPA 電化學響應效果的影響,結果見圖7。
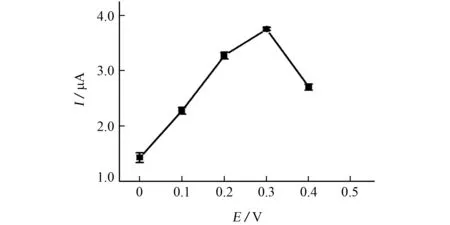
圖7 富集電位對峰電流的影響Fig.7 Effect of enrichment potential on peak current
由圖7可知:氧化峰電流在富集電位為0.3 V時達到最大;進一步增大富集電位,響應電流下降。因此,試驗選擇富集電位為0.3 V。
2.4.3 支持電解質酸度
支持電解質的酸度對BPA 的氧化電流影響較大,試驗考察了支持電解質pH 為5.0~9.0 時,PDDA-CDs/Ce-MOFs/GCE 對BPA 電化學響應效果的影響,結果見圖8。
由圖8可知:當支持電解質的pH 為7.0時,氧化峰電流達到了最大值;pH 繼續增加,峰電流開始下降。這可能是由于BPA 的pKa為9.73,當pH為7.0時,BPA 以未解離的疏水性分子形態存在,能夠有效富集在修飾電極表面,局部濃度提高,從而提高修飾電極對其的響應靈敏度。因此,試驗選擇pH 7.0的0.1 mol·L-1磷酸鹽緩沖溶液作為支持電解質。此外,試驗還考察了支持電解質酸度對于BPA 氧化峰電位的影響,結果見圖9。
由圖9可知:BPA 氧化峰電位隨著pH 的增大向負電位方向發生偏移,兩者之間呈線性關系,線性回歸方程為Epa=-0.060 70 pH+0.944 0,相關系數為0.997 2,斜率(60.7 m V/pH)非常接近理論值(59 m V/pH),說明在修飾電極上發生的BPA 氧化是等量的電子與質子參與的過程。
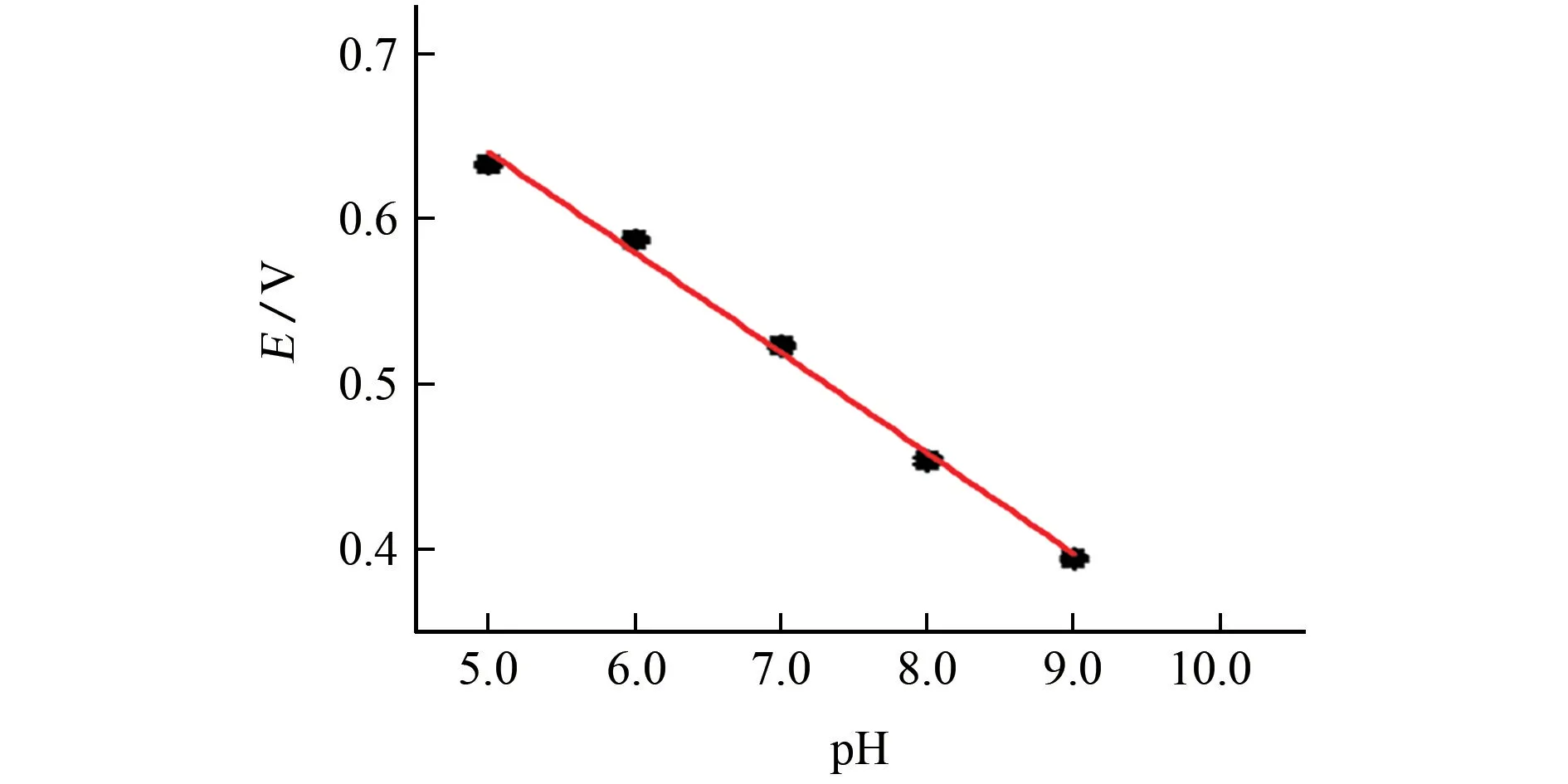
圖9 支持電解質酸度對峰電位的影響Fig.9 Effect of acidity of supporting electrolyte on peak potential
2.5 掃描速率的影響
為了進一步了解修飾電極的電化學行為,試驗采用循環伏安法考察了在掃描速率為50~200 m V·s-1時,PDDA-CDs/Ce-MOFs/GCE 對5.0μmol·L-1BPA 溶液的電化學響應,結果見圖10。
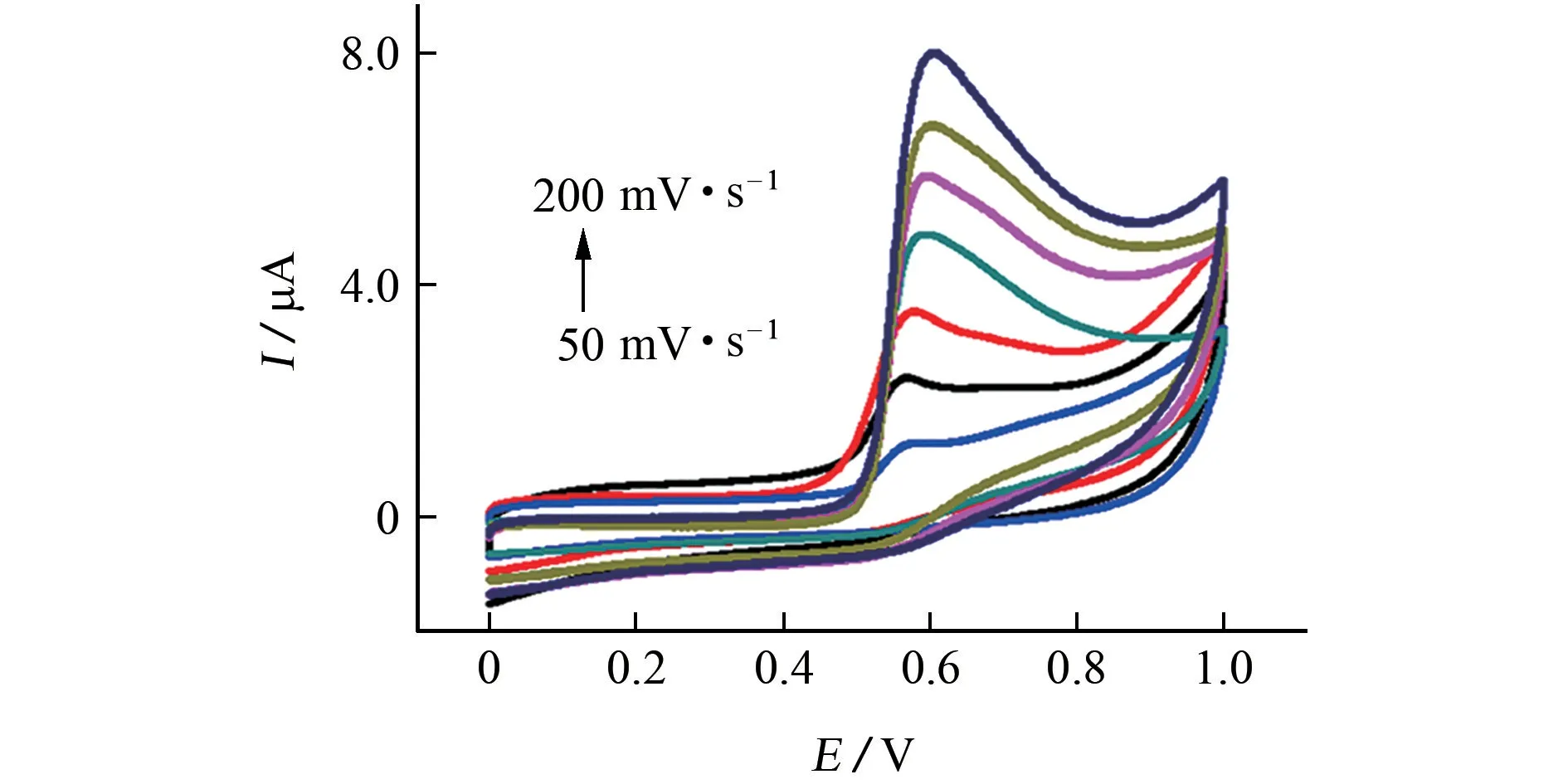
圖10 掃描速率對BPA 電化學行為的影響Fig.10 Effect of scanning rate on electrochemical behavior of BPA
由圖10可知:隨著掃描速率從50 m V·s-1增加到200 m V·s-1,氧化峰電流逐漸增加,且兩者呈很好的線性關系,線性回歸方程為Ipa=0.038 00ν+0.378 0,相關系數為0.998 3,說明BPA在修飾電極上的氧化過程是一個典型的吸附控制過程,同時說明該修飾電極可以很好催化氧化BPA;BPA 氧化峰電位隨著掃速的增大,向正電位方向偏移,且氧化峰電位與掃描速率的自然對數(lnν)之間呈線性關系,線性回歸方程為Epa=0.028 80 lnν+0.452 0,相關系數為0.999 5,依據能斯特方程公式(1):
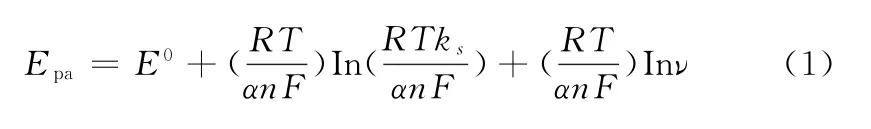
式中:E0為BPA 標準氧化還原電位;k s為標準速率常數;n為電子轉移數;ν是掃描速率;T是熱力學溫度(298 K);R為氣體常數(8.314 J·Kmol-1);F為法拉第常數(96 485 C·mol-1);α是轉移速率常數,無量綱,對于不可逆的反應,α通常取0.5。
根據氧化峰電位與掃描速率的線性方程中的斜率可以求出公式(1)中的電子轉移數n為1.84,表明BPA 在修飾電極上的電催化氧化過程是兩個電子和兩個質子參與轉移的過程,這與文獻[4]和文獻[17]的報道結果一致。
2.6 標準曲線和檢出限
按照儀器工作條件對0.01~50μmol·L-1的BPA 標準溶液系列進行測定,以BPA 的濃度為橫坐標,其對應的氧化峰電流為縱坐標繪制標準曲線。結果顯示:BPA 的濃度與其對應的氧化峰電流分別在0.01~5.0μmol·L-1和5.0~50μmol·L-1內呈線性關系,線性回歸方程分別為y=0.748 0x+0.149 9和y=0.088 30x+3.339,相關系數分別為0.998 7,0.998 3。
以3倍的信噪比(S/N)計算檢出限(3S/N),所得結果為2.2 nmol·L-1。
2.7 重復性和穩定性
按照儀器工作條件對5.0μmol·L-1BPA 標準溶液進行6次重復測定,測定值的相對標準偏差(RSD)為4.6%,表明該修飾電極擁有良好的重復性。
將制備好的修飾電極在278 K 條件保存,每7 d測試1次,7 d后和28 d后,修飾電極對BPA 的響應電流分別降為初始電流的96.8%和95.4%,表明修飾電極具有優異的穩定性。
2.8 干擾試驗
以5.0μmol·L-1BPA標準溶液為測試對象,試驗考察了一些可能存在的潛在干擾物質,如K+、Cu2+、Mg2+、Fe3+、Cl-、雙酚B、雙酚F、鄰氨基苯酚、鄰硝基苯酚和對硝基苯酚對BPA 測定結果的干擾。結果表明:50倍濃度的K+、Cl-、SO42-、鄰氨基苯酚、鄰硝基苯酚,30倍濃度的Cu2+、Fe3+、對硝基苯酚和等濃度的雙酚B、雙酚F 對修飾電極對BPA 測定結果的干擾的絕對值均小于5%。
2.9 樣品分析
按照1.4 節試驗方法對6 種牛奶樣品進行測定,每種樣品平行測定5次,結果見表1。
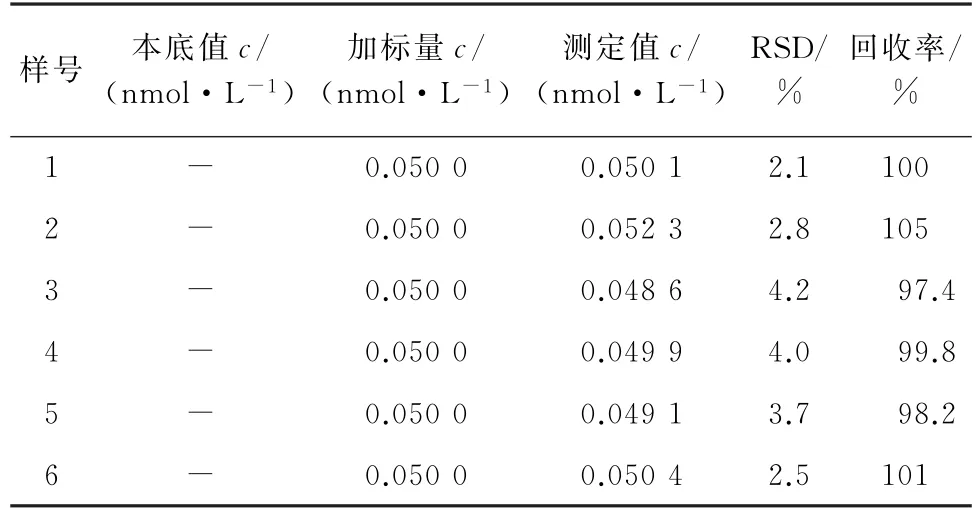
表1 樣品分析結果(n=5)Tab.1 Analytical results of samples(n=5)
由表1 可知:6 種牛奶樣品均不含BPA,BPA測定值的RSD 為2.1%~4.2%,BPA 的回收率為97.4%~105%,表明該方法具有良好的精密度和準確度,能夠滿足實際樣品中BPA 的檢測。
2.10 方法比對
將本方法與其他已報道的相關方法進行了比對,結果見表2。
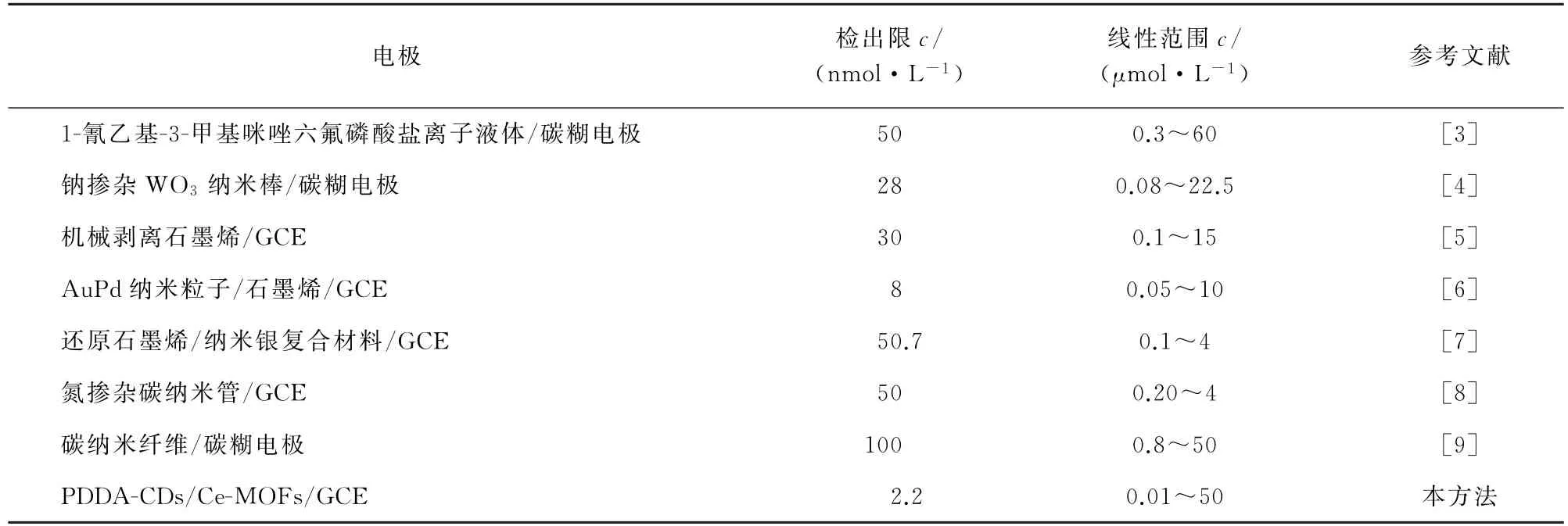
表2 方法比對Tab.2 Comparison of method
由表2可知:本方法具有較寬的線性范圍以及 較低的檢出限,說明采用PDDA-CDs/Ce-MOFs/GCE具有較好的電催化性能。
本工作合成了球形納米粒子PDDA-CDs和具有木柴狀納米棒結構的Ce-MOFs兩種復合物,通過靜電吸附作用將兩者修飾在GCE表面,構建了修飾電極測定牛奶中BPA含量的電化學方法。制備的修飾電極具有較好的電催化性能、重現性、穩定性以及抗干擾能力,可用于實際樣品中BPA含量的測定。

