基于適配體的納米金光學探針可視化法快速測定中藥材中的啶蟲脒
尤金坤,魏小紅,陳媛媛,葉淑敏,余宇燕,張紅艷
(福建中醫藥大學 藥學院,福州 350122)
啶蟲脒化學名稱為N-(N-氰基-乙亞氨基)-N-甲基-2-氯吡啶-5-甲胺,屬于氯化煙堿類化合物,是一種新型殺蟲劑,通過作用于昆蟲神經系統突觸部位的煙堿乙酰膽堿受體,從而干擾刺激的傳導,使神經系統通路堵塞,進而導致乙酰膽堿在突觸部位積累,達到殺蟲目的,被廣泛應用于蚜蟲、飛虱、薊馬等蟲害防治中[1-3]。隨著中藥材產業規模化發展,大面積集中種植導致病蟲害日漸嚴重,而啶蟲脒因殺蟲效果良好,且與傳統的殺蟲劑相比,具有毒性低的優勢,被廣泛應用到中藥材生產種植中。但啶蟲脒易殘留在植物體內,進而通過食物鏈蓄積在人體內,可能對用藥人群造成健康危害[4-5]。為了評價啶蟲脒對中藥材采收及使用安全性的影響,需對其殘留情況進行研究及評估。
目前啶蟲脒傳統的測定方法為色譜法和免疫分析法[6-9]。色譜法主要依托于大型儀器進行定量分析,如氣相色譜-串聯質譜法(GC-MS/MS)、液相色譜-串聯質譜法(LC-MS/MS)等[10-12],雖然這些檢測方法已經得到廣泛的應用,但是需要繁瑣的樣品預處理,而且所需儀器大多體積大、價格昂貴、攜帶困難,不適合現場快速檢測。免疫分析法盡管檢測快速、特異性強,但是抗體不易獲取且制備周期長。因此,發展靈敏準確、快速便捷的新型傳感器對啶蟲脒農藥殘留物的測定具有重要意義。
適配體,又被稱為“化學抗體”,具有目標物類別廣泛、穩定性好、成本低廉且易于修飾等特點,被廣泛應用于生物傳感器的生物識別探針中[13]。納米金具有許多獨特的物理和光學性質,它兼具合成方法簡單、性質穩定、生物親和性好、消光系數高、易于修飾等優點。而由納米金制備的光學探針操作方法簡單,可以快速觀察到結果,在各種化合物的鑒別和測定中得到了廣泛應用[14]。
本工作結合納米金與適配體的獨特性質,采用納米金作為光學探針,適配體作為識別元件,建立一種可視化納米金比色傳感器,以期實現對中藥材中啶蟲脒農藥殘留的現場快速測定。
1 試驗部分
1.1 儀器與試劑
Infinite M200 PRO 型多功能酶標儀;ZNCLBS型恒溫磁力攪拌器;H-7650型透射電子顯微鏡(TEM);DFY-600型高速萬能粉碎機。
氯金酸溶液:0.1 g·L-1,取1 mL 10.0 g·L-1氯金酸溶液,用水定容至100.0 mL。
檸檬酸三鈉溶液:0.01 g·mL-1,稱取0.101 6 g的檸檬酸三鈉,用水溶解并定容至10.00 mL。
啶蟲脒標準溶液:1 g·L-1,稱取0.010 3 g的啶蟲脒,用甲醇溶解并定容至10 mL容量瓶中。其他所需質量濃度均由此溶液用甲醇逐級稀釋制得。
阿特拉津、吡蟲啉、毒死蜱、甲胺磷標準溶液:100 mg·L-1。
啶蟲脒適配體序列:5′-TGTAATTTGTCTGCAGCGGTTCTTGATCGCTGACACCATATTATGAAGA-3′。
啶蟲脒適配體溶液:100μmol·L-1,使用時用水稀釋至所需濃度。
所用試劑均為分析純,試驗用水為超純水。實際樣品信息見表1。
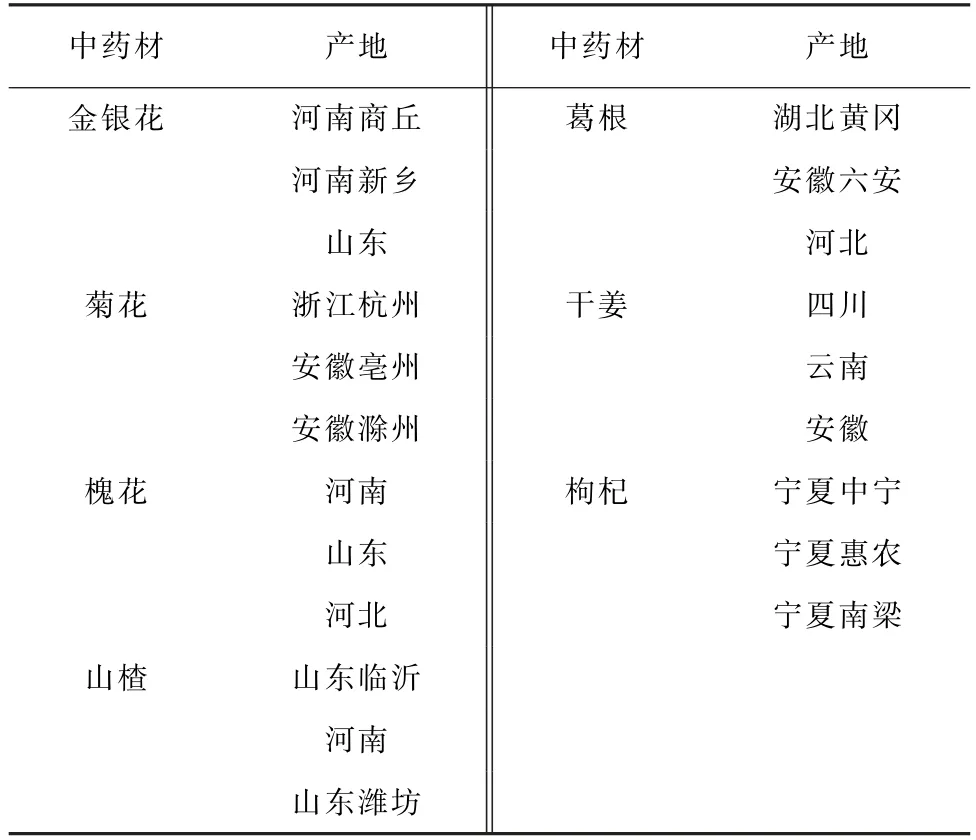
表1 實際樣品Tab.1 Real samples
1.2 試驗方法
1.2.1 納米金溶液的制備
采用檸檬酸還原法合成納米金[15]。在劇烈攪拌下將100 mL 0.1 g·L-1氯金酸溶液加熱至沸騰,迅速加入3 mL 檸檬酸三鈉溶液,保持溶液持續沸騰10 min后,停止加熱,繼續攪拌15 min。待溶液冷卻至室溫,用0.22μm 濾膜過濾,將制備好的納米金溶液置于4 ℃下避光保存。
1.2.2 樣品中啶蟲脒的測定
將中藥材樣品粉碎,過孔徑為0.154 mm 的篩網,混勻后,取1 g于10 mL 離心管中,加入6 mL甲醇,超聲提取15 min后,以3 500 r·min-1轉速離心10 min。取上清液1 mL 于2 mL 離心管中,加入100 mg無水MgSO4、50 mgN-丙基乙二胺,渦旋2 min后,以8 000 r·min-1轉速離心5 min,分離出樣品溶液。在酶標板中加入150μL 的納米金溶液和1.00 μmol·L-1啶蟲脒適配體溶液30μL,混勻后在室溫下反應15 min;在上述溶液中加入樣品溶液,室溫下反應20 min;再加入200 mmol·L-1的NaCl溶液30μL,混合均勻后靜置5 min。通過多功能酶標儀對樣品溶液進行400~700 nm 的紫外-可見吸收光譜掃描,讀取各溶液在520,650 nm 處的吸光度。
2 結果與討論
2.1 試驗原理
經檸檬酸根穩定的納米金會在靜電排斥作用下保持穩定,但在高鹽環境下,納米金之間的靜電排斥作用會被屏蔽,從而發生聚集,導致溶液顏色發生變化。當以上體系中有適配體或啶蟲脒存在時,會發生如1所示的變化。
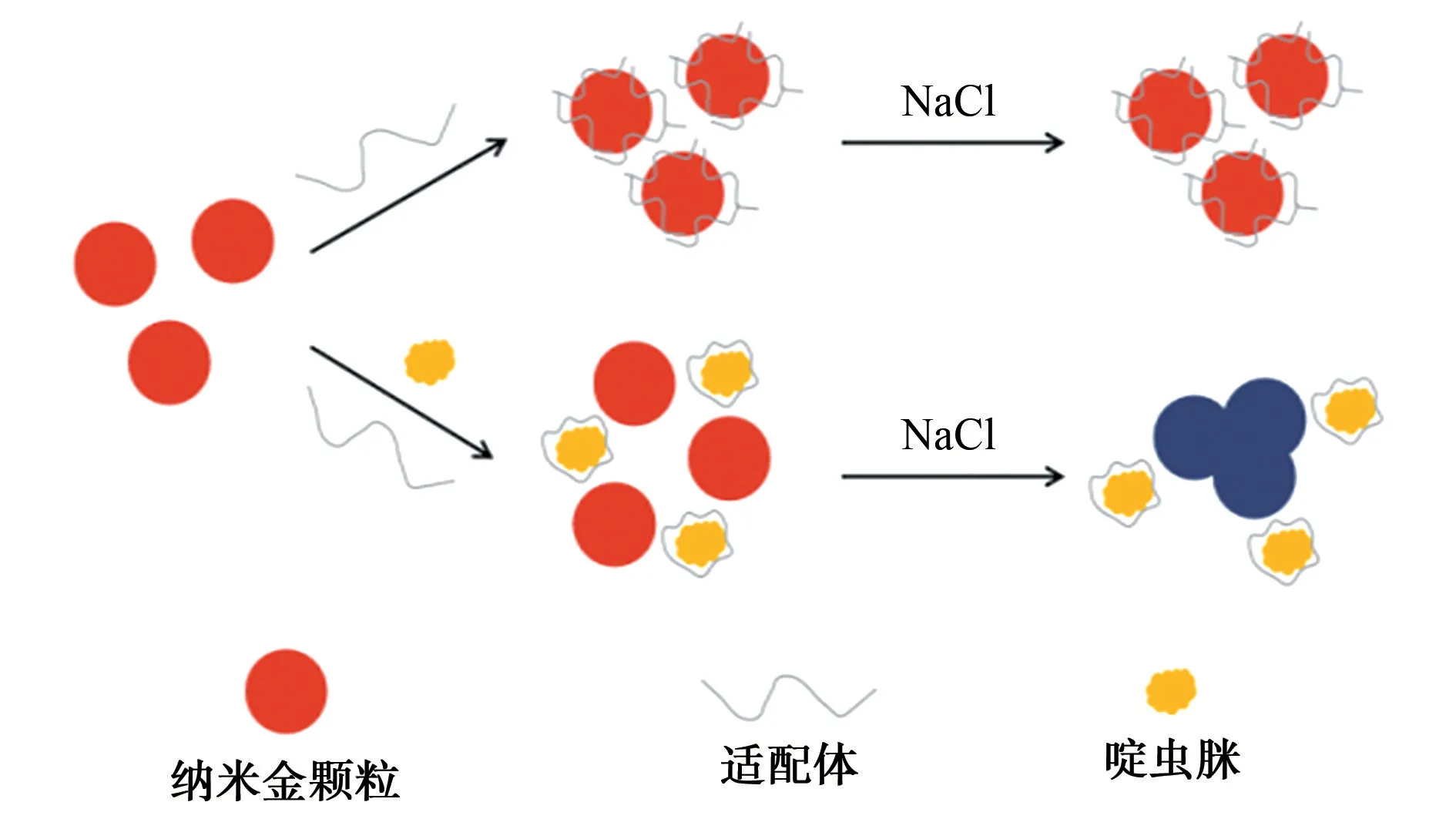
圖1 比色傳感器原理圖Fig.1 Schematic illustration of the mechanism of colorimetric sensor
如圖1所示:適配體可以通過靜電作用吸附在納米金表面,使納米金在高鹽溶液中維持分散狀態;當在納米金-適配體體系中加入啶蟲脒時,啶蟲脒與適配體發生特異性結合,將適配體從納米金表面解離下來,納米金失去保護后,將在高鹽環境下團聚,體系的顏色由紅色變為藍色。
納米金、納米金-啶蟲脒、納米金-適配體-鹽及納米金-適配體-啶蟲脒-鹽等4 種體系中納米金的紫外-可見吸收光譜變化見圖2。其中,OD 為光密度。
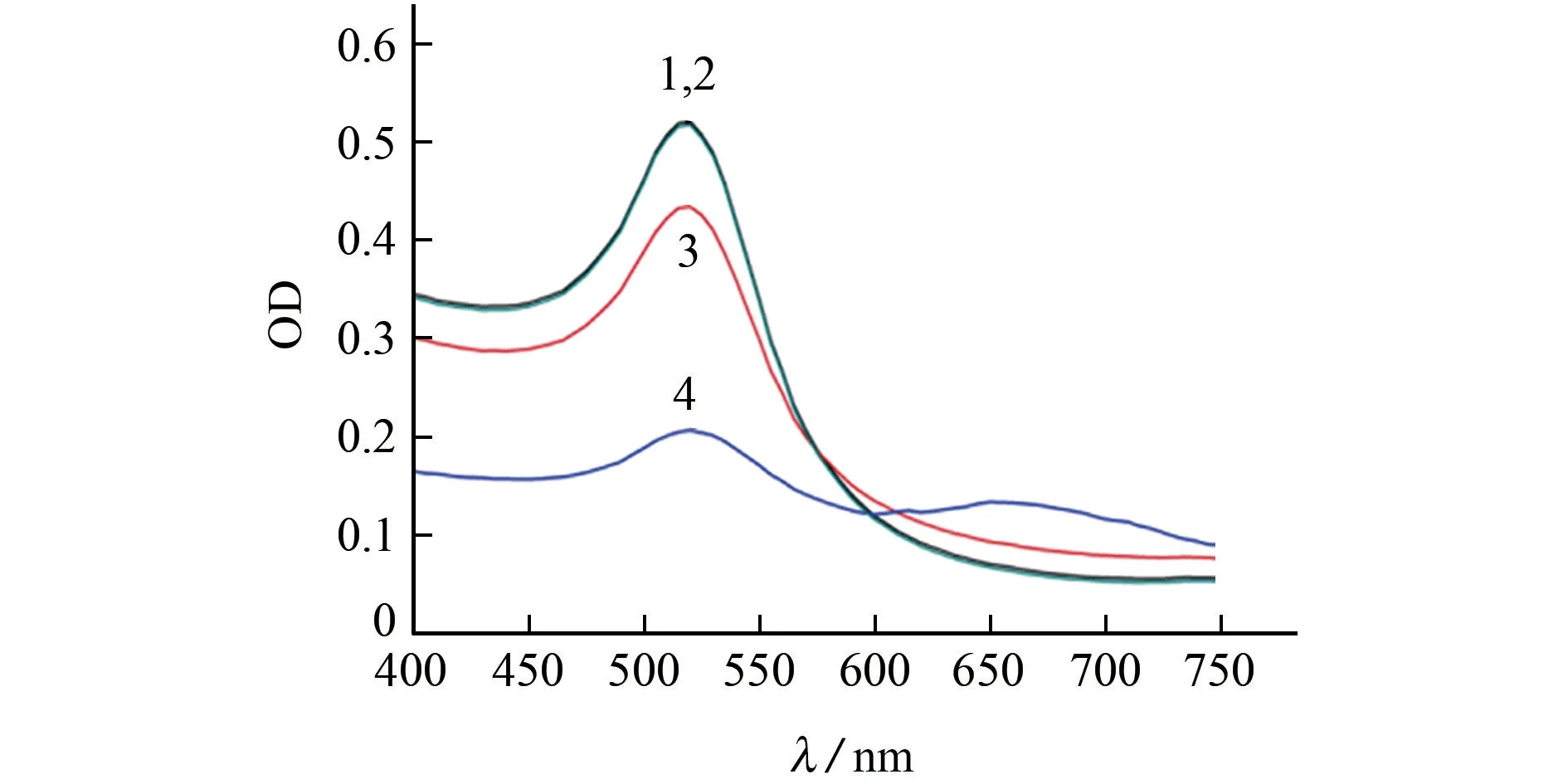
圖2 納米金在不同體系中的紫外-可見吸收光譜Fig.2 UV-Vis absorption spectrum of gold nanoparticles in different systems
由圖2可知:當納米金顆粒以分散狀態存在時,最大吸收峰在520 nm 處,溶液顏色為紅色;單獨加入啶蟲脒后,納米金的吸收光譜和顏色均沒有發生變化;加入適配體和鹽溶液后,溶液顏色沒有明顯變化,最大吸收峰仍在520 nm 處,強度沒有明顯降低,這是由于適配體上的含氮堿基會與納米金結合,從而保護納米金免受高鹽誘導,保持均勻的分散狀態;加入適配體、啶蟲脒和鹽溶液后,體系顏色變成藍色,520 nm 處的OD 值下降了超過一半,且在650 nm 處產生了新的吸收峰,這是由于適配體會與啶蟲脒產生特異性結合,而失去保護的納米金在高鹽的誘導下發生聚集的作用。
2.2 納米金的表征
對制備好的納米金溶液進行400~700 nm 內的紫外-可見吸收光譜掃描和TEM 形貌表征,結果見圖3。其中,圖3(b)中的內插圖為納米金顆粒TEM 放大圖。
由圖3 可知:納米金的特征吸收峰在520 nm處,峰形尖銳無雜峰,與文獻[16]報道的一致;納米金顆粒為圓球形,分散均勻且粒徑均一,粒徑約為18 nm。
2.3 試驗條件的選擇
2.3.1 NaCl溶液濃度
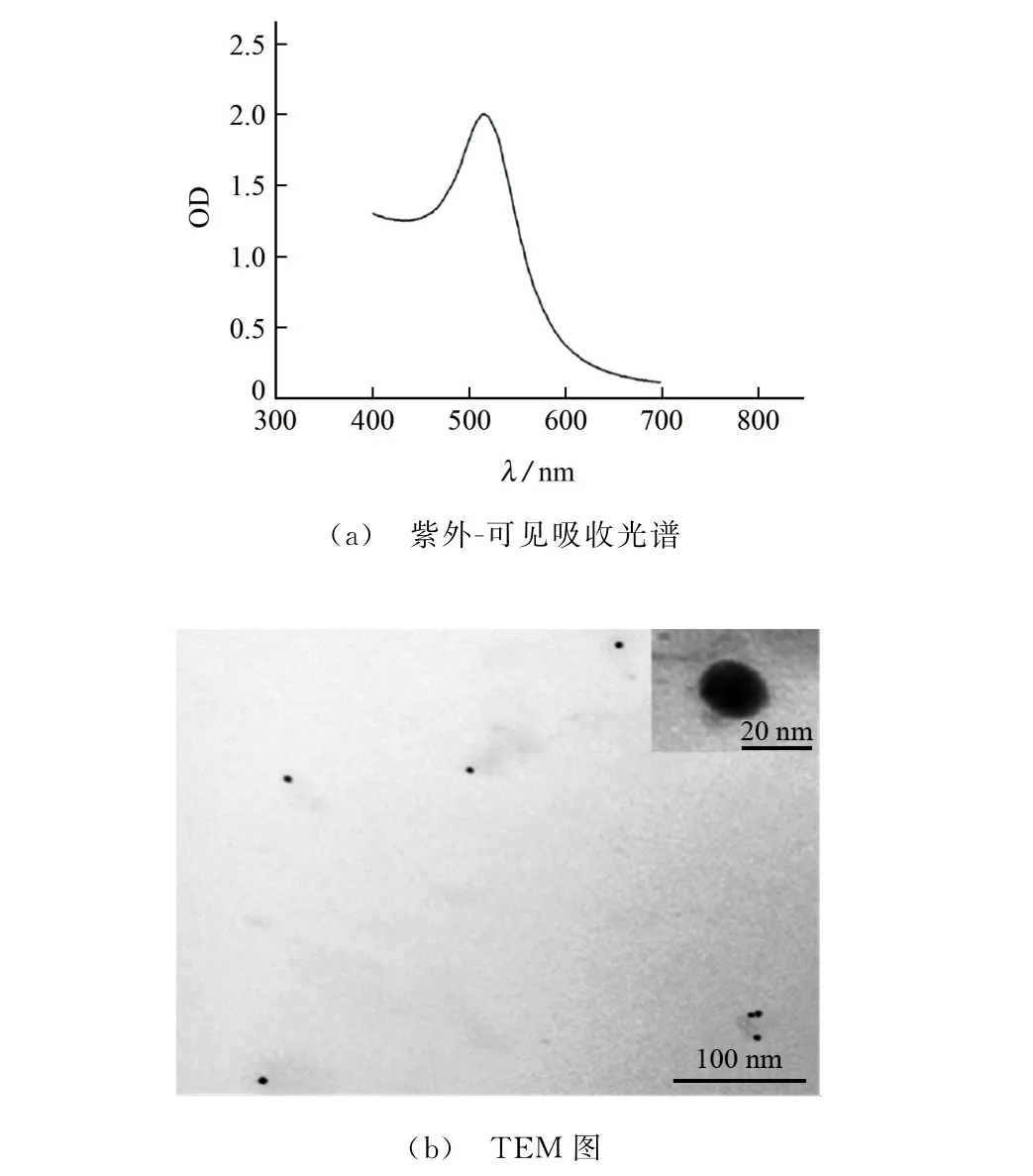
圖3 納米金的紫外-可見吸收光譜和TEM 圖Fig.3 UV-Vis absorption spectrum and TEM image of gold nanoparticles
NaCl能夠破壞納米金表面的雙電層,使納米金顆粒發生團聚[17]。隨著NaCl溶液濃度的增加,發生團聚的納米金顆粒數量增多,體系的顏色會由紅色逐漸變為藍色。納米金比色傳感器中NaCl溶液濃度會直接影響整個體系靈敏度,過高NaCl溶液濃度會使納米金在沒有啶蟲脒存在下發生團聚,過低NaCl溶液濃度則會導致納米金聚集不完全,影響結果的準確度。因此,NaCl溶液濃度的選擇至關重要。
按照1.2.2節試驗方法(其中,用水代替適配體溶液,用甲醇代替樣品溶液)考察了NaCl溶液濃度分別為0,50,100,150,200,300,350 mmol·L-1時對測定的影響,結果見圖4。
由圖4 可知:當NaCl 溶液濃度為50~350 mmol·L-1時,納米金在520 nm 處的OD 值隨著NaCl溶液濃度的增加而逐漸降低;當NaCl溶液濃度低于200 mmol·L-1時,納米金溶液為紅色;當NaCl溶液濃度為200 mmol·L-1時,體系顏色變化明顯,且520 nm 處的OD 值顯著下降。因此,最終選擇200 mmol·L-1的NaCl溶液開展后續試驗。
2.3.2 適配體溶液濃度
按1.2.2節試驗方法(其中,用甲醇替代樣品溶液)考察適配體溶液的濃度分別為0,0.25,0.50,0.75,1.00,2.00,3.00μmol·L-1時對測定的影響,結果見圖5。
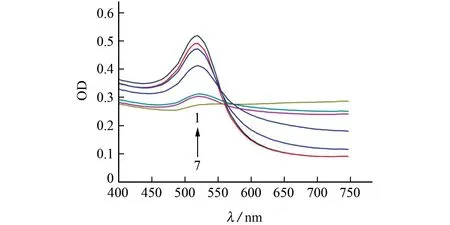
圖4 納米金在不同濃度NaCl溶液中的紫外-可見吸收光譜Fig.4 UV-Vis absorption spectrum of gold nanoparticles in the different concentrations of NaCl solution
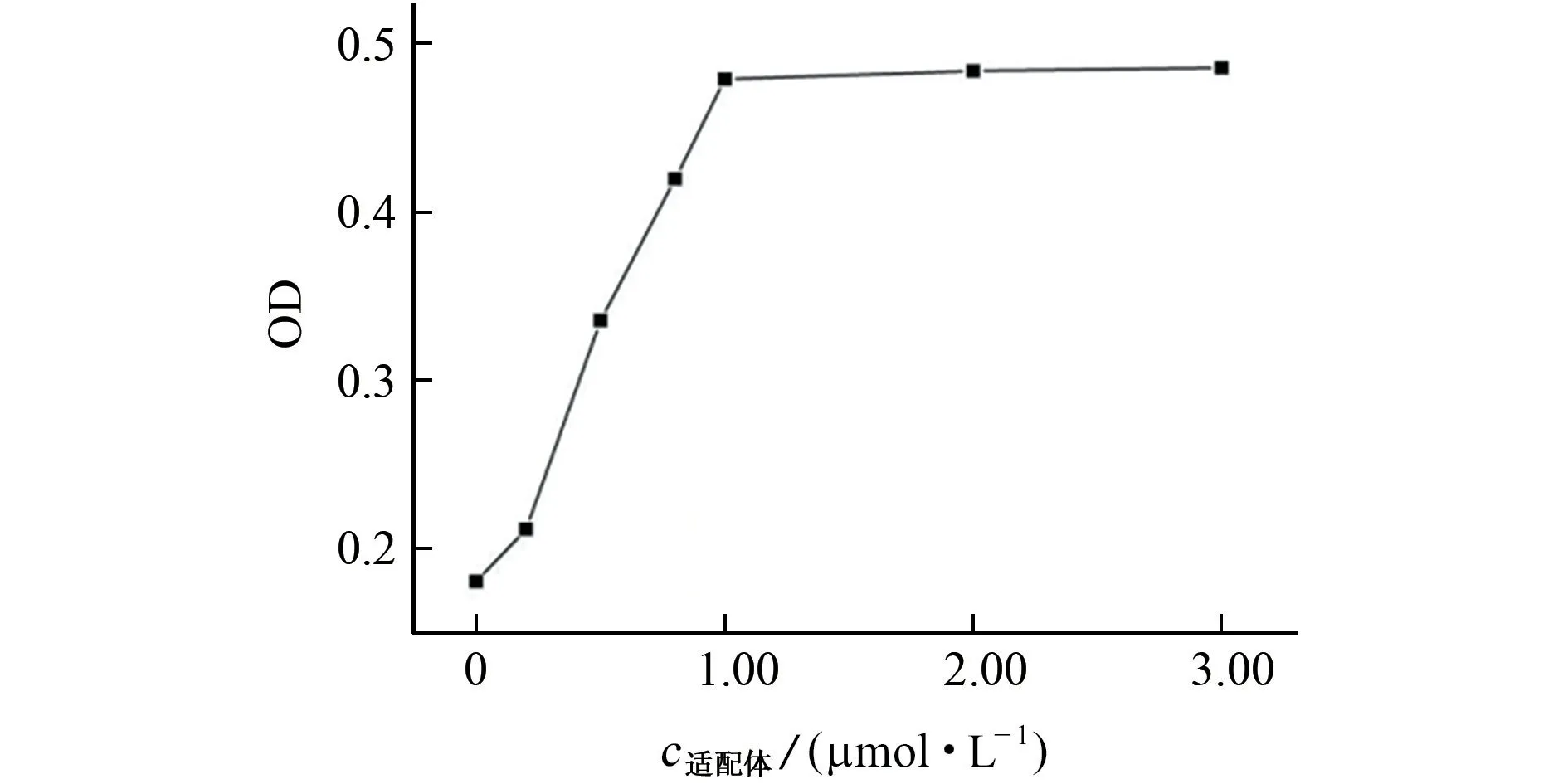
圖5 納米金在不同適配體溶液濃度下的OD值Fig.5 OD values of gold nanoparticles in the different concentrations of aptamer solution
由圖5 可知,當適配體溶液濃度小于1.00μmol·L-1時,納米金分散狀態隨著適配體溶液濃度的增加而逐漸變好;當適配體溶液濃度大于等于1.00μmol·L-1時,體系OD 值基本不再變化。因此,最終選擇1.00μmol·L-1適配體溶液開展后續試驗。
2.3.3 納米金-適配體和啶蟲脒-適配體作用時間
按照1.2.2 節試驗方法(分別用甲醇和200μmol·L-1啶蟲脒標準溶液替代樣品溶液)考察納米金-適配體作用時間分別為0,5,10,15,20,25 min,啶蟲脒-適配體反應時間分別為0,5,10,15,20,30 min時對測定的影響,520 nm 處的OD 值隨體系作用時間的變化見圖6。
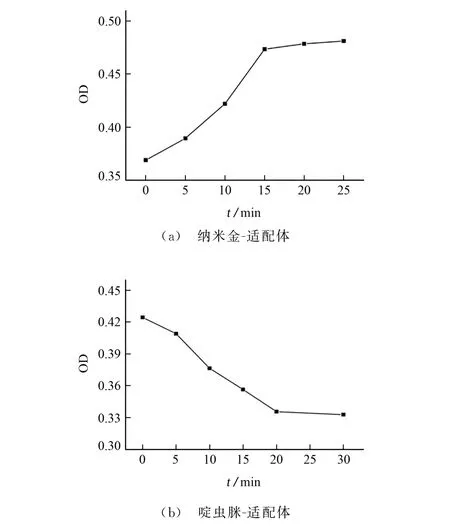
圖6 2種體系作用時間對520 nm 處OD值的影響Fig.6 Effect of reaction time of the 2 systems on OD value at 520 nm
由圖6可知:520 nm 處的OD 值隨著納米金-適配體作用時間的延長而增加,當作用時間達到15 min后,體系OD 值不再發生明顯變化,說明體系中的納米金與適配體已經結合完全,因此試驗選擇納米金-適配體的作用時間為15 min;520 nm 處的OD 值隨著啶蟲脒-適配體作用時間的延長而降低,當作用時間為20 min時,OD 值沒有明顯變化。因此,試驗選擇啶蟲脒-適配體的作用時間為20 min。
2.4 標準曲線和檢出限
按照1.2.2 節試驗方法對0,1,5,10,20,50,100,150,200,250,300μg·L-1的啶蟲脒標準溶液系列進行測定。結果顯示:隨著啶蟲脒質量濃度的增加,體系顏色逐漸由紅色向藍色轉變,在20~200μg·L-1范圍內,650 nm 和520 nm 處吸光度的比值與啶蟲脒質量濃度呈良好的線性關系,線性回歸方程為y=3.100×10-3x+3.105×10-1,相關系數為0.991 4。
按照1.2.2 節試驗方法對樣品空白重復測定8次,計算650,520 nm 處吸光度比值的標準偏差,以3倍標準偏差與標準曲線斜率的比值計算檢出限,所得結果為1.13μg·L-1。
2.5 特異性試驗
為研究體系的特異性,按照1.2.2 節試驗方法對相同質量濃度(200μg·L-1)啶蟲脒、阿特拉津、吡蟲啉、毒死蜱、甲胺磷進行測定,結果見圖7。
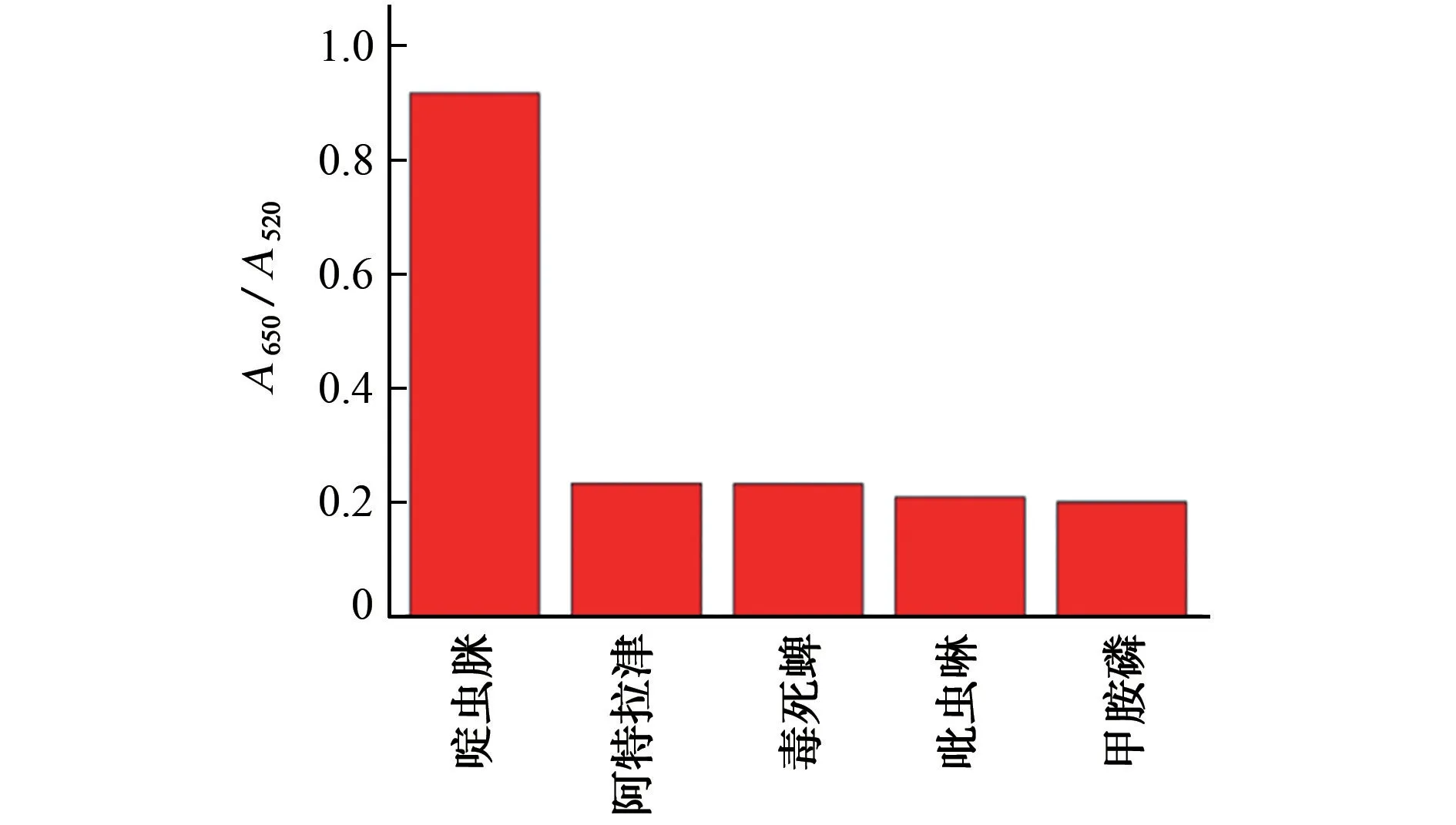
圖7 加入不同農藥后的響應值Fig.7 Response values after adding the different pesticides
由圖7可知,除了啶蟲脒,其他4種農藥的溶液顏色及其在650,520 nm 處的光吸收均未發生明顯變化,說明選擇的其他4種農藥對啶蟲脒的測定沒有顯著影響,本體系具有良好的特異性。
2.6 精密度和回收試驗
對7種空白中藥材進行3個濃度水平的加標回收試驗,每個濃度水平平行測定5次,計算回收率和測定值的相對標準偏差(RSD),結果見表2。

表2 精密度和回收試驗結果(n=5)Tab.2 Results of tests for precision and recovery(n=5)
由表2 可知,啶蟲脒的回收率為91.1%~105%,RSD 為1.1%~4.8%,表明該方法精密度和回收率良好。
2.7 樣品分析
按照1.2.2節試驗方法對21份樣品進行測定,僅在來自河南商丘的金銀花和來自寧夏惠農的枸杞中檢出了啶蟲脒,檢出質量分數分別為329.10,125.22μg·kg-1。
本工作建立了一種基于納米金-核酸適配體的可視化納米金比色傳感器用于中藥材中啶蟲脒殘留量測定的方法。該方法操作簡單、特異性高,可通過肉眼直接半定量分析樣品,具有現場檢測開發前景,為中藥材中農藥殘留檢測及藥材質量評價提供依據。

