牛血清白蛋白水熱法一步合成氮摻雜碳點熒光檢測2,4,6-三硝基甲苯
劉翠娥, 黃加玲, 王婷婷, 王小琴, 劉鳳嬌, 李順興
(閩南師范大學化學化工與環境學院,現代分離分析科學與技術福建省重點實驗室,福建漳州 363000)
碳點(Carbon Dots,CDs)因其具有可調諧的光致發光特性,優異的理化性能,光穩定性好,以及低毒性、生物相容性和生物降解性等[1-7]優點,成為熒光傳感器的研究熱點。CDs發光特性與其表面結構有關,因此探討不同來源、不同表面功能團CDs對熒光檢測性能影響機制倍受關注。2,4,6-三硝基甲苯(2,4,6-Trinitrotoluene,TNT)是人工合成的爆炸能力強、性質穩定、通用烈性炸藥。TNT可通過皮膚、肺和眼睛被人體吸收[8],從而損傷肝臟、造血系統和皮膚,并可能引起血紅蛋白變性[9]。TNT及其降解產物可對水生生物和群落產生不利影響[10-12]。TNT的使用帶來嚴重的人身安全和環境污染隱患,因此對其快速、準確、高效檢測技術的需求日益增長[13]。
近年來,已經開發出基于X射線擴散、中子分析、拉曼光譜[14]和電化學傳感[15,16]等方法。與其他技術相比,熒光法在痕量TNT檢測中具有操作簡單、低成本、便攜性、高靈敏度和選擇性好等優點[17]。基于NH2-CDs“功能單體”,乙二胺功能化CDs[18,19]已成功應用于TNT的選擇性檢測,但后修飾添加氨基活性位點法所需合成和純化過程復雜。因此,以含氮物質為前驅體,一步合成氮摻雜CDs(Nitrogen-doped CDs,N-CDs)更便捷且環境友好。Zhang等[20]通過一步微波輔助熱解乙二胺和檸檬酸,成功合成了N-CDs,在強的TNT-NH2相互作用下建立了熒光傳感平臺,對TNT檢測的線性范圍為1.0×10-8~1.5×10-6mol/L,檢測限為1.0×10-9mol/L。Cayuela等[21]報道了一種使用含氮聚合物作為前驅體,合成疏水的N-CDs,在氯仿中可與TNT通過光誘導能量轉移機制產生熒光猝滅,檢測的線性范圍為2.2×10-5~2.2×10-4mol/L,檢測限為5.3×10-6mol/L。本文以含氮豐富的牛血清白蛋白(Bovine Serum Albumin,BSA)為碳源,采用水熱法一步合成的N-CDs可定量檢測TNT,同時還可以通過比色法半定量檢測TNT。
1 實驗部分
1.1 儀器與試劑
pHS -3E型pH計(上海雷磁公司);JEM-2100型場發射透射電子顯微鏡(日本,JEOL公司);ESCALAB 250 Xi型X射線光電子能譜(XPS)儀(美國,Thermo Fisher Scientific公司);Nicolet iS10型傅立葉變換紅外(FTIR)光譜儀(美國,Thermo Fisher Scientific公司);X射線衍射(XRD)儀(日本,Rigaku公司);SPECORD?200 PLUS型紫外-可見分光光度計(德國,耶拿分析儀器股份公司);Cary Eclipse型熒光分光光度計(美國,Agilent公司)。
標準物質2,4,6-三硝基甲苯(TNT)的甲醇溶液購買于中國計量研究院;標準物質2,4-二硝基甲苯、鄰硝基甲苯、間硝基甲苯、鄰硝基苯酚的甲醇溶液,及標準物質間硝基苯酚均購買于北京坦墨質檢科技有限公司。牛血清白蛋白(BSA)、NaOH、H3PO4、H3BO3、KCl、一水合檸檬酸、無水Na2HPO4、KH2PO4均購買于西格瑪奧德里奇(上海)貿易有限公司;冰HAc(≥98%,色譜純)購買于上海阿拉丁生化科技股份有限公司;Ca(OH)2標準緩沖液購買于廈門海標科技有限公司;乙醇(分析純)購買于西隴科學股份有限公司;甲醇(色譜純)購買于德國默克公司;實驗用水為Milli-Q?系統(美國Millipore)制備的超純水(電阻率18.2 MΩ·cm)。
1.2 實驗方法
1.2.1 N-CDs的制備參考文獻報道[22],修訂N-CDs合成方法如下:將0.0300 g BSA溶于15.0 mL超純水中,并在快速混合器上快速混合后,加入15.0 mL乙醇,在冰水浴中超聲處理30 min,最后將上述混合液轉至容量為50 mL的聚四氟乙烯內襯中,裝于不銹鋼高壓釜中,在180 ℃下反應12 h,冷卻至室溫;0.22 μm濾膜過濾純化后,轉入透析袋(3 500 D)透析48 h,最后轉移至培養皿冷凍干燥,回收固體粉末樣品,在4 ℃儲存備用。
1.2.2 N-CDs對TNT的紫外-可見吸收光譜和熒光光譜檢測將0.0050 g N-CDs溶于50 mL的B-R緩沖液(pH=12)中,取500 μL上述配制的混合液,加入TNT并定容至2 mL,反應60 min后,檢測波長190~800 nm的紫外-可見吸收光譜,以及激發波長為310 nm的熒光光譜。
1.2.3 N-CDs對實際水樣檢測分析取自來水水樣,用0.22 μm濾膜過濾,備用待測。取500 μL的含0.1 g/L N-CDs的B-R緩沖液(pH=12),并用采集的水樣定容至2 mL,反應60 min后,在激發波長為310 nm進行熒光光譜檢測。同時采用加標回收驗證該方法的可行性。
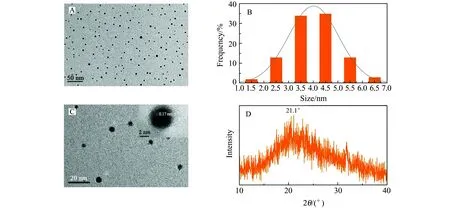
圖1 N-CDs的透射電鏡(TEM)圖(A)、粒徑分布直方圖(B)、高分辨透射電鏡(HRTEM)圖(C)和X射線衍射圖(D)Fig.1 TEM image(A),size distribution histogram(B),high resolution TEM image(C) and X-ray diffraction(XRD) pattern (D) of nitrogen-doped carbon dots(N-CDs)
2 結果與討論
2.1 N-CDs的形態與組成
由透射電鏡(TEM)(圖1A)及粒徑分布(圖1B)可知,以BSA為前驅體,采用水熱法制備的N-CDs顆粒分散好,粒徑大部分分布在3.5~4.5 nm。由TEM(圖1C)可知,N-CDs的外圍輪廓模糊,即外部碳化不完全;而從圖1C的右上方高分辨透射電鏡(HRTEM)圖顯示出清晰的晶格條紋,表明制備的N-CDs碳芯碳化完全,這與常見CDs由類似石墨的核和無定形的含氧殼層組成相符[8]。從圖1D的X射線衍射(XRD)圖可知,寬衍射峰位于2θ=21.1°,表明N-CDs以非晶型碳形式存在,與TEM圖中碳核外部碳化不完全的結果相符,且與先前的一些報道[22-24]相似。
BSA是水溶性蛋白質,分子量為66.4 kDa,由583個氨基酸組成,其中有35個半胱氨酸,形成17對二硫鍵,一個游離的巰基[25]。因此對N-CDs的C、H、O和S四種元素進行X射線光電子能譜(XPS)分析(圖2A)。結果表明,制備的N-CDs中含有C 88.86%,N 3.20%,O 7.36%及S 0.58%。XPS高分辨C 1s 光譜(圖2B)中顯示出5個峰,結合能分別為284.5 eV、284.9 eV、285.5 eV、286.5 eV和288.0 eV,這歸因于sp2雜化C-C[26,27]、C-C[28]、C-O或C-S或C-N[26,29]、C=O和C=O[30]。N 1s光譜(圖2C)在399.8 eV、400.5 eV和401.8 eV處顯示三個峰歸因于C-N-C、N-(C)3和N-H[28],證實了N-CDs的形成。O 1s光譜(圖2D):C=O(531.8 eV)、C-OH或C-O-C(532.3 eV)和N-OH(533.4 eV)[28,31]。
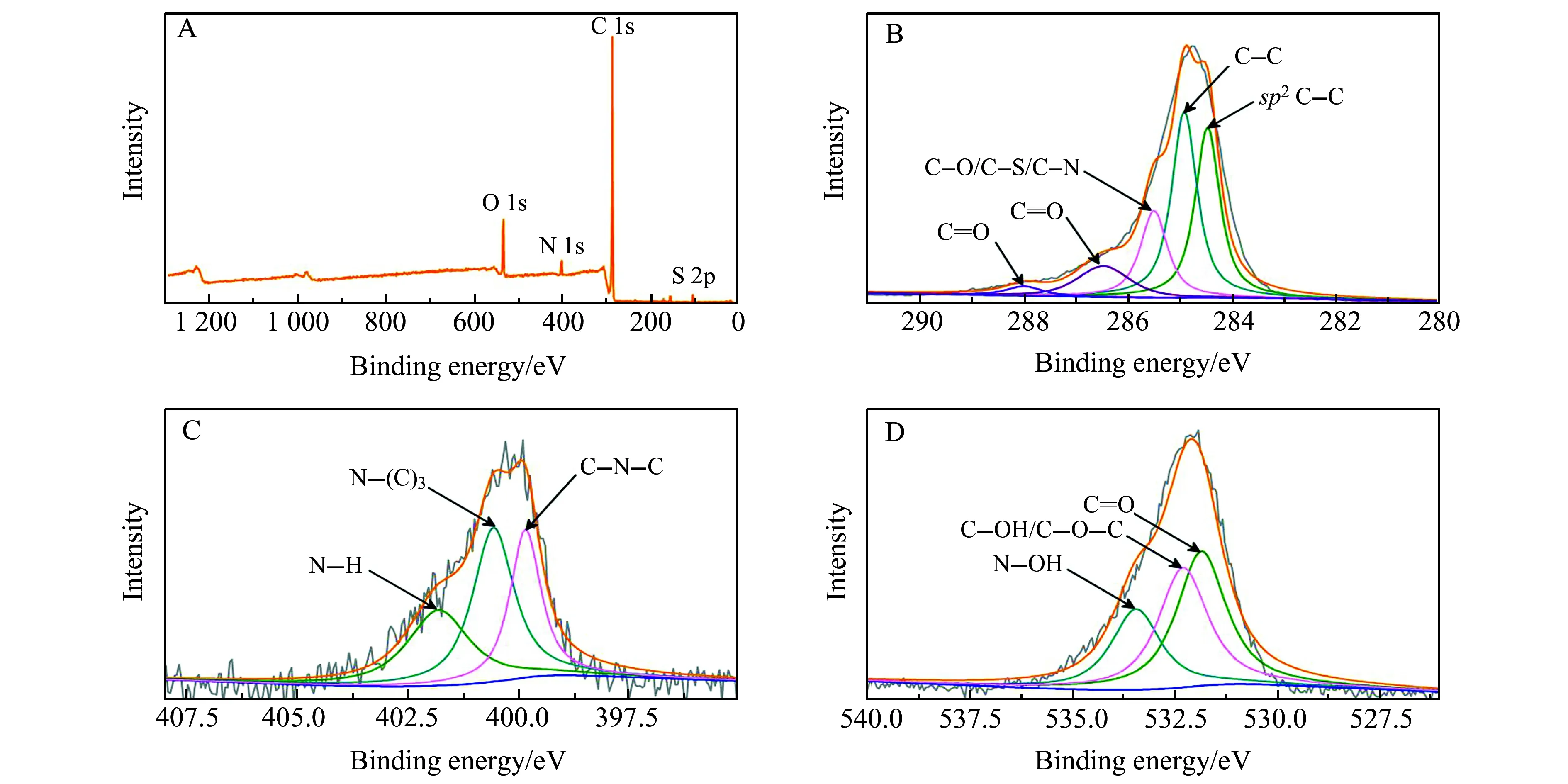
圖2 N-CDs的X射線光電子能譜(XPS)表征。(A)全譜圖,(B)C 1s譜圖,(C)N 1s譜圖,(D)O 1s譜圖Fig.2 XPS of N-CDs(A) full spectrum,(B) C1s spectrum,(C) N 1s spectrum,(D) O 1s spectrum
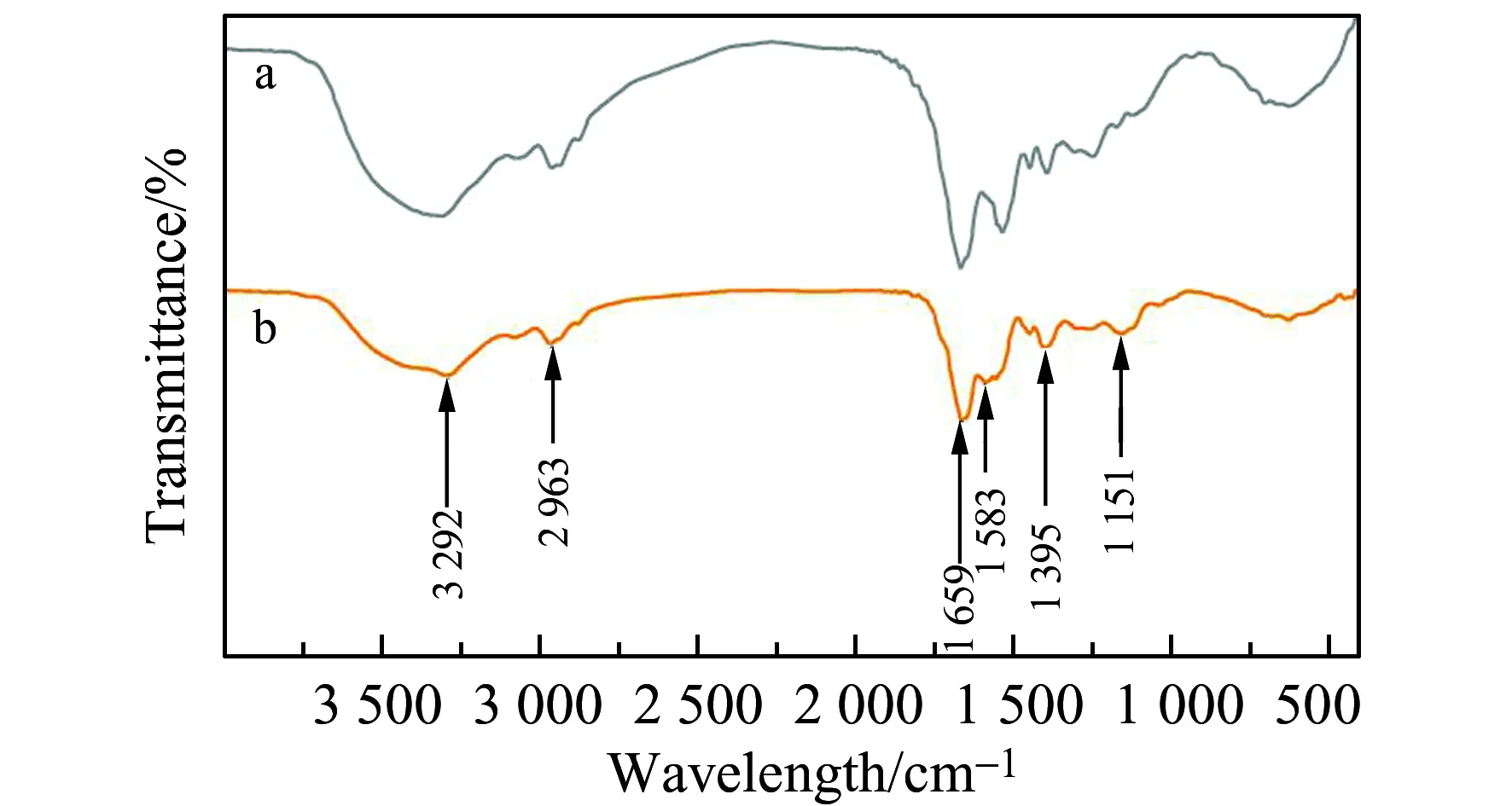
圖3 BSA(a) 和N-CDs(b)的傅立葉變換紅外光譜圖Fig.3 Fourier transform infrared(FTIR) spectra of BSA(a) and N-CDs(b)
由傅立葉變換紅外(FTIR)光譜儀測得的譜圖見圖3。分析圖譜:N-CDs(圖3曲線b)的N-H、C-H和C=N伸縮振動分別在3 292 cm-1、2 963 cm-1、1 659 cm-1處有明顯的峰[32,33],以及COO-(1 395 cm-1)和C-O-C(1 151 cm-1)[22],表明制備的N-CDs含有豐富的含氧基團。與原料BSA(圖3曲線a)對比,制備的N-CDs在C=C(1 583 cm-1)的伸縮振動峰變寬,表明在水熱制備N-CDs的過程中,BSA被碳化而形成不飽和的碳鍵,這與XPS中C 1s表征的sp2雜化C-C結果一致。
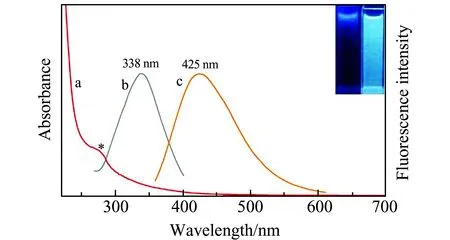
圖4 N-CDs的紫外-可見光譜(a)以及熒光激發(b)和發射(c)光譜圖 (插圖:N-CDs在254 nm(左)和365 nm(右)紫外燈照射下圖片)Fig.4 UV-Vis spectrum(a),fluorescence excitation spectrum(b) and emission spectrum (c) of N-CDs (Inset:photographs of N-CDs under 254 nm(left) and 365 nm(right) UV irradiation)
2.2 N-CDs的熒光特性
N-CDs的紫外-可見(UV-Vis)吸收光譜(圖4a)表明,在波長277 nm處有一吸收峰,是熒光N-CDs的一個典型特征[34],歸因于n-π*躍遷吸收[35],碳與雙鍵相連接的雜原子C=O、C=N、S=O上未成鍵的孤對電子向π*反鍵軌道躍遷吸收所致。N-CDs的熒光激發光譜(圖4b)和發射光譜(圖4c),在波長338 nm處激發時,425 nm處顯示出最大發射峰。插圖中顯示:254 nm紫外光照射下,N-CDs水懸浮液只呈現出微弱藍光,而365 nm紫外光照射下,呈現相對較強藍綠色熒光,表明N-CDs在水中分散性良好[36]。
N-CDs的另一個顯著特征是具有激發波長的依賴性[35]。如圖5A所示,340 nm激發時,N-CDs最大發射位于425 nm;400 nm激發時,發射峰移至468 nm。N-CDs在不同激發波長下的歸一化熒光光譜,如圖5B所示,這種變化更為明顯。
在500 μL的含0.1 g/L N-CDs的B-R緩沖溶液(pH=12)中加入不同體積的甲醇后,用超純水定容至2 mL,在激發波長310 nm的條件下,發射波長403 nm處N-CDs的熒光強度無明顯的變化,表明甲醇對N-CDs熒光強度的影響可基本忽略。同時,在不同濃度的NaCl溶液中,在激發波長320 nm的條件下,發射波長413 nm處N-CDs的B-R緩沖液(pH=12)熒光強度同樣無明顯的變化,表明N-CDs穩定,在高離子強度條件下也不會聚集[28,29]。
2.3 N-CDs對TNT的檢測
反應時間對N-CDs檢測TNT時熒光強度的影響如圖6A所示,0~5 min時,N-CDs的熒光強度急劇下降,5~60 min時,N-CDs的熒光強度依然緩慢地不斷減弱,60 min后N-CDs的熒光強度幾乎不再發生變化。因此,N-CDs對TNT的響應截止時間設為60 min。一定量的TNT加入配制的含0.1 g/L N-CDs的不同pH值B-R緩沖液,在激發波長320 nm條件下,記錄有無TNT時N-CDs的熒光強度,如圖6B所示。N-CDs的pH穩定性好,不同pH下N-CDs對TNT都有一定的熒光猝滅響應,而pH=12時,N-CDs響應最為靈敏。同時,插圖中為加入TNT反應60 min后溶液的顏色,僅有pH=12時,溶液的顏色為淺橙色,易于辨別。
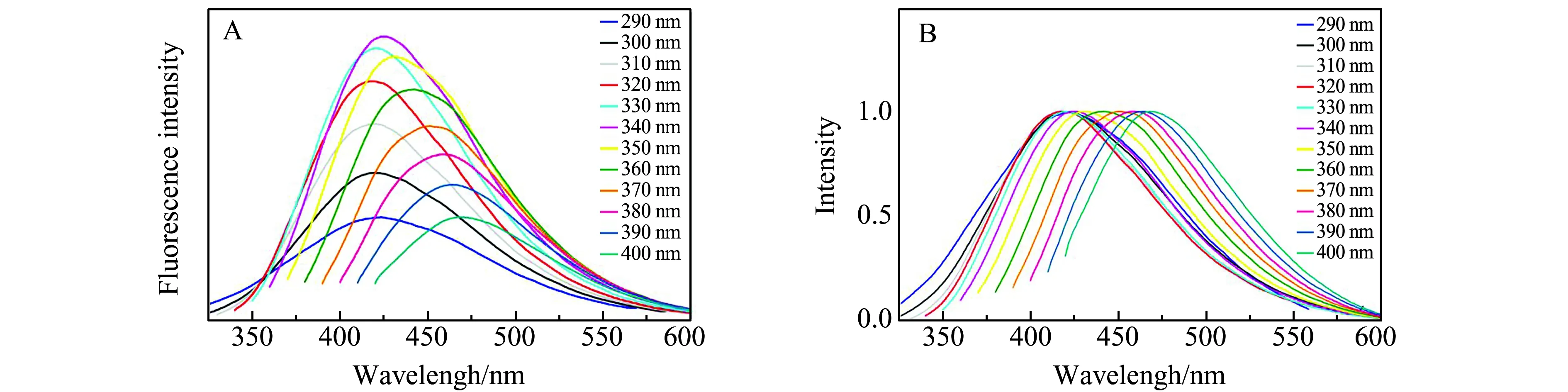
圖5 (A) N-CDs不同激發波長下熒光發射光譜;(B) N-CDs不同激發波長下歸一化熒光光譜Fig.5 (A)Fluorescence emission spectra of N-CDs excited at different wavelengths;(B) Normalized fluorescence emission spectra of N-CDs excited at different wavelengths
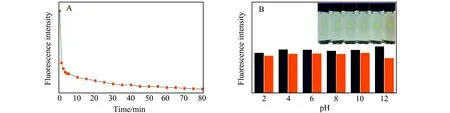
圖6 (A) 反應時間對N-CDs檢測TNT時熒光強度的影響;(B)不同pH的B-R緩沖液和有無TNT時N-CDs的熒光強度(黑色和橙色直方圖分別代表無TNT和有TNT)。插圖:不同pH的N-CDs液,檢測TNT時日光下的照片。Fig.6 (A) Effects of reaction time on the change of fluorescence intensity of N-CDs for TNT delection;(B) Intensity of N-CDs in B-R buffer with different pH and with or without TNT(black and orange histograms represent absence and presence of TNT,respectively).Inset:Photograph of N-CDs at different pH under daylight when TNT is detected.
研究不同緩沖體系對N-CDs檢測TNT的影響。等量的N-CDs分別加入pH=12的B-R、Ca(OH)2、Na2HPO4-NaOH不同緩沖液中,然后加入等量的TNT,在激發波長320 nm條件下,測試有無TNT時的熒光強度,如圖7A所示。其中,N-CDs溶液的熒光強度為F0,而檢測TNT的N-CDs溶液的熒光強度為F,N-CDs熒光強度的變化為ΔF=F0-F。由圖可知:ΔF/F0(B-R)>ΔF/F0(Ca(OH)2)>ΔF/F0(Na2HPO4-NaOH)。在B-R緩沖液中,N-CDs對TNT響應的靈敏度最佳,所以選擇pH=12的B-R緩沖體系作為N-CDs檢測TNT的溶劑環境。由不同激發波長下N-CDs檢測有無TNT時熒光強度的變化,對N-CDs檢測TNT時的激發波長進行優化,如圖7B所示。根據熒光強度的大小,以及比較ΔF/F的大小,確定310 nm為N-CDs檢測TNT的最佳激發波長。
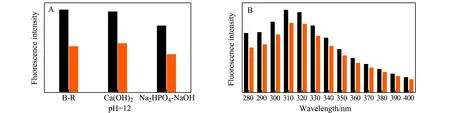
圖7 不同緩沖液下(A)和不同激發波長(B)時N-CDs與TNT作用前后的熒光強度(黑色直方圖代表N-CDs的熒光強度,橙色代表檢測TNT時N-CDs的熒光強度)Fig.7 Fluorescence intensity of N-CDs before and after reacting with TNT under different buffer systems(A) and under different excitation wavelengths(B)The black histograms represent the fluorescence intensity of N-CDs,and the orange represent the fluorescence intensity of N-CDs when detecting TNT.
綜上所述,500 μL的含0.1 g/L N-CDs的B-R緩沖液(pH=12)中,加入一定量的TNT,最終定容至2 mL,反應60 min后,以310 nm為激發波長,測定N-CDs的熒光發射光譜。隨著TNT量的不斷增加,N-CDs的熒光猝滅現象越明顯,并出現藍移現象,反應液的顏色越深,如圖8A所示。TNT加入后,溶液的顏色由起初的無色轉變為玫紅色,最后為橙色的比色響應可以肉眼捕獲,根據顏色的深淺可進行半定量分析檢測TNT。根據Stern-Volmer方程:F0/F=1+KSV·[Q]。其中F0和F分別為無TNT和有TNT存在時N-CDs的熒光強度,KSV為Stern-Volmer猝滅常數,[Q]為猝滅劑TNT的濃度。如圖8B中的插圖所示,工作曲線由(F0-F)/F和猝滅劑TNT的濃度映射關系,在2.6×10-6~8.0×10-4mol/L范圍內存在顯著的線性相關關系(R2=0.9950),檢出限(3σ/k)為5.1×10-6mol/L。
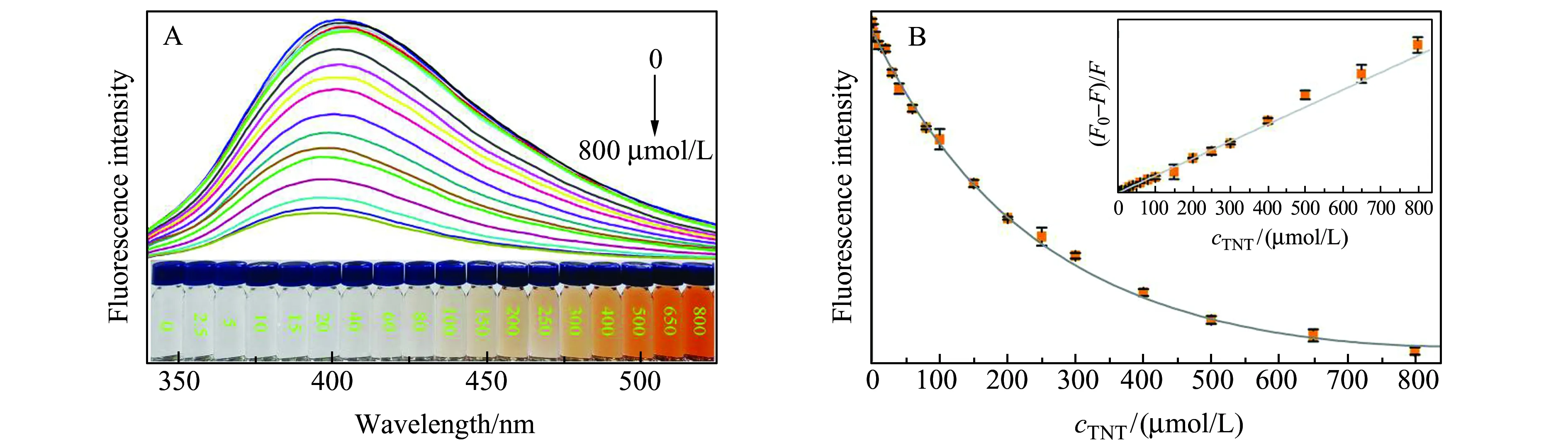
圖8 (A) B-R緩沖液(pH=12)中不同濃度TNT時N-CDs的熒光發射光譜(插圖:對應反應溶液在日光下的照片);(B)B-R緩沖液(pH=12)中不同濃度TNT時N-CDs的熒光猝滅圖(插圖:N-CDs的Stern-Volmer圖)Fig.8 (A) Fluorescence emission spectrum of N-CDs in B-R buffer(pH=12) at different concentrations of TNT(Inset:photograph of the corresponding reaction solution under daylight);(B) Fluorescence quenching spectrum of N-CDs in B-R buffer(pH=12) at different concentrations of TNT(Inset:Stern-Volmer plots of N-CDs)
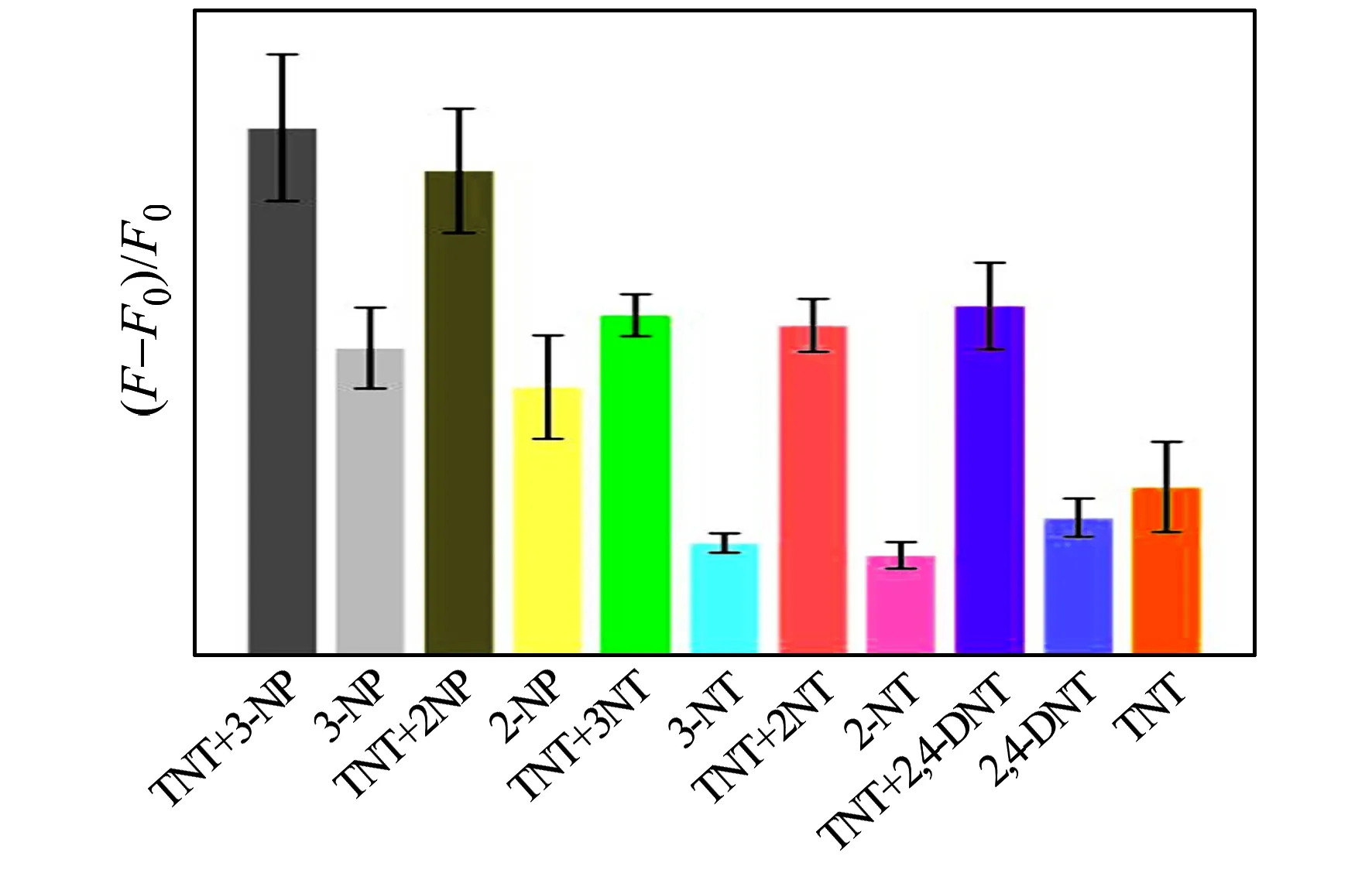
圖9 其他硝基甲苯化合物和硝基酚類化合物對N-CDs檢測TNT的干擾作用Fig.9 Interference effect of other nitrotoluene compounds and nitrophenols on the detection of TNT using N-CDs
探討TNT相似干擾物2,4-二硝基甲苯(2,4-Dinitrotoluene,2,4-DNT)、2-硝基甲苯(2-Nitrotoluene,2-NT)、3-硝基甲苯(3-Nitrotoluene,3-NT)、2-硝基苯酚(2-Nitrophenol,2-NP)、3-硝基苯酚(3-Nitrophenol,3-NP)對N-CDs的熒光猝滅的影響。于N-CDs的B-R緩沖液(pH=12)中,加入上述等濃度等體積的硝基芳香爆炸物,60 min后,以激發波長310 nm測定反應液的熒光強度。由圖9可知,通過TNT、2,4-DNT、2-NT和3-NT對N-CDs的熒光猝滅效率可知,TNT猝滅效應最佳,其次為2,4-DNT,最后為猝滅效應相近的2-NT和3-NT,可知硝基甲苯化合物對N-CDs的猝滅效應與硝基的個數有關。而將其中的硝基甲苯化合物和芳香硝基酚類化合物相比,芳香硝基酚類化合物對N-CDs的猝滅效應更好。在N-CDs檢測TNT的抗干擾實驗中,2,4-DNT、2-NT、3-NT、2-NP和3-NP都加強了TNT對N-CDs的猝滅效應,對N-CDs檢測TNT具有正向干擾性,N-CDs檢測TNT的抗干擾性不佳。N-CDs與硝基甲苯類化合物的猝滅可歸因于硝基甲苯類化合物與N-CDs氨基之間形成的Meisenheimer絡合物所致;而對于硝基苯酚類化合物,則是N-CDs氨基與酚羥基之間發生酸堿反應形成硝基酚鹽的結果[17]。
2.4 實際水樣中TNT檢測
通過測定自來水水樣中的TNT,檢驗該方法的適用性。對摻有標準TNT溶液(60、80和100 μmol/L)的樣品進行了加標回收率的測試,所獲得的樣品回收率從97.6%~99.6%,且測定的相對標準偏差(RSD)最大值為2.5%,表明該方法可用于實際水樣中TNT檢測(表1),即水樣中共存物質不干擾測定。
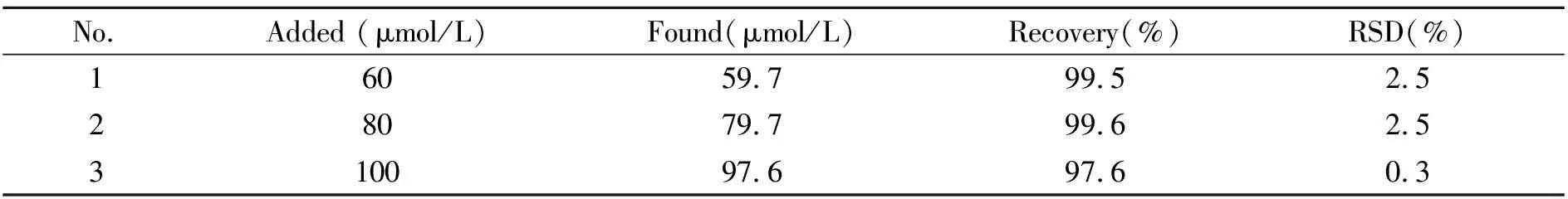
表1 水樣中TNT的檢測
3 結論
本文以含氮豐富的BSA為碳源,采用水熱法制備N-CDs,不需進一步的化學修飾,而在寬的pH范圍內保持良好的熒光強度,檢測TNT表現出良好的線性關系,同時依據反應液可肉眼捕獲的比色響應,半定量檢測TNT。但是,N-CDs對TNT檢測的選擇性不佳,且受到其他硝基芳香甲苯化合物和硝基酚類化合物的干擾,實際應用中將受到一定的限制。所以,提高N-CDs對TNT的選擇性和抗干擾性,是后續工作中值得展開探討的方向。

