多器官功能衰竭患者檢出棲稻假單胞菌1例
符曉瑩,朱雄,麥珍,王立程,王崇圳,韓麗梅,李歡,陳海
三亞市人民醫院檢驗科/中心實驗室, 海南 三亞 572000
棲稻假單胞菌(Pseudomonasoryzihabitans,P.oryzihabitans)是一類非發酵的需氧革蘭氏陰性桿菌,該菌廣泛存在于自然界,在稻葉上定植,通常存在于水、泥土和潮濕環境中,包括醫院環境中的下水道、呼吸機、含水的醫療器械和洗手盆等[1-2]。1977年,Pien[3]從1例硬膜外腦出血患者的血培養中分離發現該菌,這是棲稻假單胞菌作為致病菌首次被臨床報道。目前,棲稻假單胞菌作為條件致病菌和院內感染菌,多分離自免疫功能低下、肝臟損傷、腫瘤或慢性腎臟疾病患者[4],在軟組織感染、肺炎、心內膜炎和菌血癥等[1-2, 5-6]中常見,偶見于特殊病例如假體周圍關節感染[7]等。目前,國內外對棲稻假單胞菌感染的臨床病例報道相對較少,導致臨床醫務人員對該菌的認識不足。本文對就診于三亞市人民醫院重癥監護治療病房(intensive care unit,ICU)的1例患者血培養中分離并鑒定出的1株棲稻假單胞菌報道如下。
1 臨床資料
1.1 病例
患者男性,33歲,黎族,公司職員,家住海南省陵水黎族自治縣。該患者于2019年11月17日就診于陵水縣人民醫院,就診前半月余無明顯誘因出現雙下肢水腫,未予注意;就診前3 d出現全身乏力、氣短、尿少,伴惡心、嘔吐等癥狀,仍未予注意。就診當天以上癥狀進一步加重。生化檢查:肌酐234.0 μmol/L,血鉀6.89 mmol/L;胸部、腹部CT:左肺上葉炎癥、心包少量積液、右側胸腔積液、左側胸膜增厚、脂肪肝、肝臟形態增大、腹腔積液、雙側腎周滲出改變。縣醫院考慮患者病情極為危重,于就診當日便將其轉入三亞市人民醫院搶救,急診科以“腎功能衰竭、高鉀血癥”收入ICU。
入院查體:體溫35.8 ℃,脈搏94次/分,血壓107/83 mmHg(多巴胺維持下)。雙下肢中度水腫,雙小腿見散在色素沉著。血常規檢查:白細胞17.23×109/L,中性粒細胞比率 81.9%,血紅蛋白 137 g/L,血小板200×109/L;生化檢查:肌酐281 μmol/L,降鈣素原3.98 ng/mL,谷丙轉氨酶996 U/L,血鉀7.06 mmol/L;心肌鈣蛋白I 1.33 μg/L。患者既往體健,否認高血壓、冠心病、糖尿病等病史。
入院診斷:急性腎損傷;肺部感染;膿毒性休克;脂肪肝;肝功能不全;多器官功能障礙綜合征。
治療:入院后告病危,給予靜脈滴注亞胺培南西司他丁(泰能)1.0 g,每8 h 1次,聯合莫西沙星 0.4 g,每日1次,加強抗感染;并加強炎癥因子清除、補液抗休克以及糾酸對癥支持治療,但預后極差。患者入院立即送檢做血培養,24 h后報告陽性,涂片染色鏡檢可見革蘭陰性桿菌。回報血培養危急值時,臨床告知患者已出院。出院原因系患者家屬因自身因素主動要求。出院時患者呈昏迷狀,血壓 83/45 mmHg(去甲腎上腺素3.0 μg·kg-1·min-1、腎上腺素3.0 μg·kg-1·min-1維持下),血氧飽和度96%。雙側瞳孔等大等圓2.0 mm,對光反射稍遲鈍。
1.2 材料與方法
1.2.1 主要試劑哥倫比亞血瓊脂平板、嗜血巧克力瓊脂平板、中國藍瓊脂平板和水解酪蛋白瓊脂(Mueller-Hinton, MH)培養基購于廣州迪景微生物科技有限公司;血液增菌培養瓶購于美國 BD 醫療器械公司;質譜專用基質(一般細菌)購于生物梅里埃公司;藥敏試驗紙片購于Oxoid Limited公司;細菌基因組DNA提取試劑盒購于北京天根生化科技公司;PCR Master Mix和2000 Marker購于上海翊圣科技有限公司。質控標準菌株大腸埃希菌 ATCC 25922、銅綠假單胞菌ATCC 15442由國家衛生健康委員會臨床檢驗中心提供。
1.2.2 主要儀器全自動血培養儀(BDBACET/FX/200)購自美國 BD 醫療器械公司,迪爾細菌鑒定系統 (DL-96Ⅱ)購自珠海迪爾生物工程有限公司,全自動快速微生物質譜檢測系統(VITEK MS IVD V3.2)購自生物梅里埃公司,PE基因擴增儀(PE-9700)購自美國應用生物系統公司,高電壓電泳儀(PowerPac HV)購自美國Bio-Rad公司,紫外線透射分析儀(UV-3C)購自珠海黑馬醫學儀器有限公司。
1.2.3 細菌分離培養按照《臨床微生物檢驗標準化操作程序》《實用臨床微生物學檢驗與圖譜》等權威著作和執行標準提供的方法[8-9]進行。采集后的血培養標本立即置于全自動血培養儀中35 ℃孵育,24 h后需氧瓶報陽性,立即取出置于生物安全柜內進行分離培養。用無菌注射器抽取需氧瓶中血液標本適量,分別接種于血瓊脂平板、巧克力瓊脂平板和中國藍瓊脂平板,同時進行涂片及革蘭染色鏡檢。
1.2.4 質譜儀鑒定依據制造商說明書和《中國臨床微生物質譜應用專家共識》[10]進行質譜操作和結果判讀。分離菌在血瓊脂平板生長24 h后,用一次性無菌接種環挑取單個適量菌落,均勻涂布于靶板,用1 μL基質液封板,置室溫干燥后使用VITEK MS IVD V3.2對分離菌進行鑒定。以大腸埃希菌 ATCC 25922進行質控。
1.2.5 生化試驗分離菌在血瓊脂平板生長24 h后,挑取單個菌落溶于無菌生理鹽水,配置成0.5麥氏濃度的菌懸液,選擇迪爾96NE鑒定板,經迪爾細菌鑒定系統 DL-96Ⅱ進行生化試驗。
1.2.6 藥物敏感試驗(antimicrobial susceptibility test,AST)參考美國臨床和實驗室標準協會(Clinical and Laboratory Standards Institute,CLSI )M100抗菌藥物敏感性試驗執行標準(2019版)[11]中銅綠假單胞菌藥敏試驗標準,采用紙片擴散法進行。取0.5麥氏濃度的菌懸液均勻涂布于MH平板,每個平板貼的藥敏紙片不超過5個,并將平板置于35 ℃普通培養箱中,24 h后測量抑菌環的直徑進行結果判讀。以銅綠假單胞菌ATCC 15442進行質控。
1.2.7 16S rRNA測序分析分離菌TS383在血瓊脂平板生長48 h后,使用細菌基因組DNA提取試劑盒提取細菌基因組DNA;實驗所用16S rRNA通用引物為27F(5′-AGAGTTTGATCCTGGC-TCAG-3′)和1492R(5′-GGTTACCTTGTTACG-ACTT-3′),引物由生工生物工程(上海)股份有限公司合成。聚合酶鏈反應(polymerase chain reaction,PCR)體系為:25 μL PCR Master Mix,上、下游引物和模板DNA各2 μL,加無核酸水補足至50 μL;反應條件為:94 ℃,30 s;52℃,30 s;72 ℃,90 s,30個循環。擴增產物送北京睿博興科公司研發部進行TA克隆測序。
1.2.8 系統發育樹構建根據16S rRNA測序結果,運用在線Blast軟件進行序列比對,選擇同源性較高的假單胞菌屬部分模式菌株,以醋酸鈣不動桿菌(Acinetobactercalcoaceticus,A.calcoaceticus)ATCC 23055作為外群菌株,運用Mega 7.0軟件構建系統發育樹。所有菌株16S rRNA序列均從美國國家生物技術信息中心(National Center for Biotechnology Information,NCBI) GenBank獲取。
2 結果
2.1 細菌培養特征及生化特征
分離株TS383經35 ℃ 24 h培養,在血瓊脂平板上可見圓形、皺紋菌落,直徑1~2 mm(見圖1A);在中國藍瓊脂平板上為光滑菌落,微凸起,邊緣整齊(見圖1B);在巧克力瓊脂平板上可見明顯的異質性菌落特征(見圖1C);固體培養基上的菌落都具有典型黃色色素。進行涂片染色鏡檢,顯示為革蘭氏陰性桿菌,無芽孢,大多散在或成對排列。該菌氧化酶試驗陰性,觸酶試驗陽性,其他生化特征如表1所示。

A: Cultured on blood agar. B: China blue agar. C: Chocolate agar.

表1 分離株TS383的生化特征(DL-96Ⅱ鑒定)
2.2 質譜檢測系統鑒定
經質譜儀VITEK MS IVD V3.2鑒定,分離株TS383為棲稻假單胞菌,置信度為99.9%。
2.3 藥物敏感試驗
分離株TS383對頭孢他啶、頭孢吡肟、慶大霉素、阿米卡星、左氧氟沙星、環丙沙星、哌拉西林/他唑巴坦、亞胺培南、美羅培南均敏感,對氨曲南、氨芐西林、頭孢唑啉、頭孢呋辛耐藥。
2.4 16S rRNA測序結果
PCR產物經瓊脂糖凝膠電泳檢測為約1.5 kb的單一條帶(見圖2),與目的條帶相符。經北京睿博興科公司研發部進行TA克隆測序,將序列遞交GenBank,獲得序列號MN911431.1,并運用在線Blast軟件進行序列比對。經比對,分離株TS383與GenBank中耐冷假單胞菌(Pseudomonaspsychrotolerans,P.psychrotolerans)C36T和P.oryzihabitansNBRC 102199T(LMG 7040T)的同源性最高,分別是99.79%和99.73%。
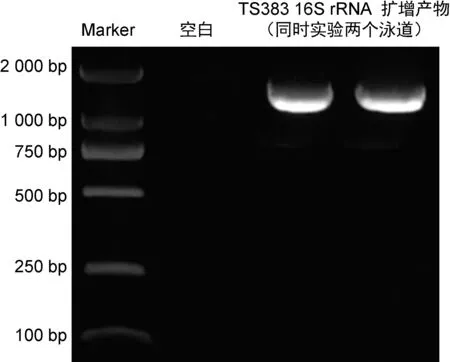
圖2 分離株TS383的16S rRNA擴增產物電泳圖
2.5 系統發育樹分析
系統發育樹如圖3所示。目前假單胞菌屬中的有效命名成員多達212個,因此只選擇16S rRNA基因序列同源性較高的部分假單胞菌構建系統發育樹。模式菌株序列從GenBank獲取,選擇A.calcoaceticusATCC 23055作為外群。使用軟件Mega 7.0比對序列,手工編輯去除不明確的核苷酸和缺口,并采用最大似然法(maximun likelihood)建樹。系統發育樹顯示,分離株TS383與P.psychrotoleransC36T以及P.oryzihabitansNBRC 102199T(LMG 7040T)進化距離最近,自展值為99%,結果可靠;且P.psychrotoleransC36T與已鑒定的5株棲稻假單胞菌歸為同一個集群,距離P.oryzihabitansNBRC 102199T(LMG 7040T)分支長度為0,距離P.oryzihabitansIAM 1568T分支長度<0.001,可見親緣關系十分相近。
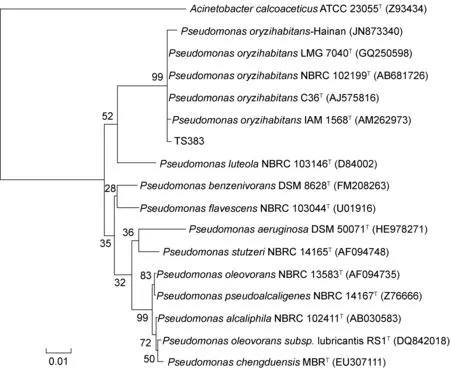
Maximum likelihood was used to build the tree based on 16S rRNA sequence analysis. The number in the node is the reliability of the bootstrap test for 1 000 times.
3 討論
3.1 命名與鑒定
由于分類學上存在爭議,棲稻假單胞菌命名經過多次修改。1985年,因該菌形態學上類似于假單胞菌并可從稻谷中大量分離得到,Kodama等[12]提出命名為棲稻假單胞菌。1987年, Holmes等[13]基于該菌與假單胞菌DNA雜交的同源性較低,提議新屬名黃色單胞菌屬,即棲稻黃色單胞菌(Flavimonasoryzihabitans,F.oryzihabitans)。1997年,Anzai等[14]通過16S rRNA系統進化分析方法,發現假單胞菌屬、黃色單胞菌屬和金色單胞菌屬同源性>93.9%,提議三者列為同一屬,并入假單胞菌屬。原核生物有效命名表(List of Prokaryotic Names with Standing in Nomenclature,LPSN)[15]上注釋該菌的正確命名為P.oryzihabitans,F.oryzihabitans為同模異名(homotypic synonym)。
棲稻假單胞菌與假單胞菌屬中大部分菌種差異最為顯著的一點是,其氧化酶試驗陰性,這值得微生物檢驗人員注意。將本報告分離的TS383株與P.oryzihabitansHainan[16]和P.oryzihabitansNBRC 102199T的生化特征進行對比,部分酶類如鳥氨酸脫羧酶、賴氨酸脫羧酶、尿素酶,部分糖類如麥芽糖、蔗糖等項目,生化反應結果都不盡相同,有時傳統的細菌鑒定儀無法準確鑒定。國外有研究者認為,棲稻假單胞菌屬于罕見致病菌,各分離株之間的表型特征差異難以鑒定到種的水平,建議采用16S rRNA測序等分子鑒定技術[5,17]。
3.2 與耐冷假單胞菌(P. psychrotolerans)的親緣關系
耐冷假單胞菌是需氧革蘭氏陰性無芽孢桿菌,菌落呈黃色,氧化酶試驗陰性、觸酶試驗陽性,生長溫度4~37 ℃,由Hauser等[18]在2004年發表有效命名。Tran等[19]在2017年對373個假單胞菌屬細菌的全基因組DNA-DNA雜交進行計算機模擬,將有效模式種的基因組兩兩比對后發現,P.psychrotoleransDSM 15758T(DSM 15758T=C36T)和P.oryzihabitansNBRC 102199T存在于同一個基因群(genospecies)中,2個菌株全基因組平均核苷酸一致性(average nucleotide identity,ANI)高達98.5%,意味著這兩種菌親緣關系密切。鑒于P.oryzihabitans發表時間早于P.psychrotolerans,本文提出P.psychrotolerans作為P.oryzihabitans的次定同物異名(junior synonym)。以上結果與本例分離株的系統發育樹中所揭示的P.psychrotoleransC36T與P.oryzihabitansNBRC 102199T(LMG 7040T)的親緣關系結果一致。本例分離株構建的系統發育樹僅基于16S rRNA序列,難免有局限性。而ANI分析基于所有直系同源蛋白編碼基因比較,克服了DNA-DNA雜交的繁復性和16S rRNA序列分析的保守性,成為目前原核生物分類的金標準[20],以ANI值的95%~96%作為分類閾值,被廣泛應用于細菌種屬的重新分類以及未知菌的鑒定。
3.3 耐藥性
本例分離株TS383的AST結果顯示對大部分抗菌藥敏感,包括頭孢他啶、頭孢吡肟、慶大霉素、阿米卡星、左氧氟沙星、環丙沙星、哌拉西林/他唑巴坦、亞胺培南、美羅培南;而對氨曲南、氨芐西林、頭孢唑啉、頭孢呋辛耐藥。這與大多數文獻報道的結果相似。需要注意的是,國內發現對3代頭孢菌素耐藥的棲稻假單胞菌分離株,其中頭孢曲松和頭孢他啶耐藥率分別達50%和37.5%[2, 6],因此治療期間應根據AST結果及時調整用藥方案。有報道指出,棲稻假單胞菌并非人體正常菌群[5],根據本例患者的個人信息、入院時的感染指征、血培養分離得到純菌落以及AST結果,推斷該患者社區感染棲稻假單胞菌的可能性大。目前,棲稻假單胞菌感染的病例報道中甚少出現多器官功能衰竭患者,本例患者臨床給予泰能聯合莫西沙星治療,但預后極差,可見感染早期使用抗菌藥物的必要性。本報道結果提示,微生物檢驗人員應關注棲稻假單胞菌的案例報道和相關研究,以獲取更多資料為臨床診治提供依據。

