老年慢性阻塞性肺疾病合并Ⅱ型呼吸衰竭患者下呼吸道銅綠假單胞菌感染的危險因素分析
柴菊愛 徐秀萍 方紅葉 郭曉霞
慢性阻塞性肺疾病(chronic obstructive pulmonary diseases,COPD)在老年人(年齡≥60歲)中的發病率約為10%~15%[1]。作為一種以持續氣流受限為特征的氣道慢性炎癥性疾病,COPD患者常因急性發作而導致Ⅱ型呼吸衰竭的發生[2]。院內銅綠假單胞菌(Pseudomonas aeruginosa,PA)感染近些年引起了臨床的高度重視。PA是革蘭陰性桿菌的一種,屬于院內感染的條件致病菌,其生存力強、易變異、易定植,具有多耐藥性,是引起ICU患者難治和死亡的重要原因[3]。老年COPD患者是PA感染的高危群體[4],但目前關于此類患者發生下呼吸道PA感染的研究主要集中在耐藥性方面,針對其危險因素的研究并不多見。本研究觀察分析老年COPD合并Ⅱ型呼吸衰竭患者下呼吸道PA感染的危險因素,并探討其耐藥性及對預后的影響,為臨床防治及病情評估提供參考。
1 對象和方法
1.1 對象 選取2014年7月至2018年7月衢州市第三醫院收治的老年COPD合并Ⅱ型呼吸衰竭患者398例為研究對象,其中男234例,女164例,年齡59~78(67.30±7.26)歲。納入標準:(1)年齡≥60歲,COPD 診斷符合《慢性阻塞性肺疾病診治指南(2013年修訂版)》[5]相關標準,且伴有Ⅱ型呼吸衰竭,入院時PaCO2≥50 mmHg,PaO2≤60 mmHg;(2)研究方案設計符合《赫爾辛基宣言》要求,所有研究對象簽署知情同意書。排除標準:(1)合并肺癌、肺結核、肺部間質性病變、支氣管哮喘、支氣管擴張等其他呼吸道疾病;(2)住院期間放棄治療自動出院或轉院者;(3)在確診PA感染前死亡而未能獲取重要檢查資料者。納入的患者住院期間每日清晨進行痰液收集實施細菌培養,PA陽性者即診斷為PA感染。依據住院期間是否發生下呼吸道PA感染分為非感染組(347例)和感染組(51例)。本研究經本院醫學倫理委員會批準。
1.2 方法
1.2.1 一般資料和實驗室檢查指標的收集 收集患者的年齡、BMI、病程、入院時 PaCO2、PaO2、氧合指數(PaO2/FiO2)、pH、性別、吸煙和飲酒史、合并基礎病(糖尿病、高血壓病、慢性腎功能不全、肺源性心臟病、冠心病、貧血、低蛋白血癥)、COPD病情分級、入院前3個月內是否使用抗生素或長期吸入糖皮質激素、入院前3個月內是否使用糖皮質激素、是否長期接受家庭氧療、近1年內慢性阻塞性肺疾病急性加重(AECOPD)是否發生≥1次、近1年內是否因病情加重住院、住院期間是否實施氣管插管、是否接受雙相持續氣道正壓(BiPAP)無創輔助通氣、住院期間是否應用碳青霉烯類抗生素、輔助通氣時間(無創+有創通氣時間)、抗生素應用時間、住院期間抗生素應用種類、住院時間、確診PA感染時血清CRP和降鈣素原(PCT)水平、入院24 h內血糖水平,其中CRP采用免疫比濁法測定,PCT采用放射免疫法測定,血糖采用日本日立7600型全自動生化檢測儀檢測。并記錄入院后28 d患者預后情況。
1.2.2 病原菌菌株鑒定及耐藥性檢測 患者每日清晨首先用清水清洗口腔3次,對于接受氣管插管者采用經人工氣道吸引分泌物至一次性無菌容器之內,之后添加等量的濃度為1%胰酶溶液(pH為7.6)后放置于35℃溫度下儲存90 min;對于非氣管插管患者痰培養方法為:首先徹底清理口腔,可用清水漱口,有假牙者需摘下,然后用力深咳,盡量將呼吸道深部的痰咳出并直接吐入專用的痰液采集器內,保證容器在使用前是無菌、密閉、干燥的,收取痰液后立即送檢。參照《全國臨床檢驗操作規程》[6]相關內容實施細菌培養,并采用法國梅里埃公司生產的VITEK2 Compact型全自動細菌分析儀進行菌種鑒定。藥敏試驗方法:取PA接種于培養皿中,采用英國OXOID公司生產的K-B紙片測定細菌耐藥性。本研究均以首次PA培養陽性結果為準。
1.3 統計學處理 采用SPSS 17.0統計軟件。計量資料以表示,兩組間比較采用兩獨立樣本t檢驗;計數資料用率表示,兩組間比較采用χ2檢驗;老年COPD合并Ⅱ型呼吸衰竭患者發生下呼吸道PA感染的危險因素采用非條件二分類logistic回歸分析(逐步分析法);并繪制Kaplan-Meier生存曲線分析兩組生存率的差異。P<0.05為差異有統計學意義。
2 結果
2.1 兩組患者一般資料和實驗室檢查指標比較 一般臨床資料的單因素分析顯示,兩組患者年齡、BMI、病程、入院時 PaCO2、PaO2、PaO2/FiO2、pH 以及性別、吸煙和飲酒史、糖尿病、高血壓病、慢性腎功能不全、冠心病、貧血、長期吸入糖皮質激素、入院前3個月內使用全身糖皮質激素、長期接受家庭氧療、BiPAP通氣、應用碳青霉烯類抗生素、入院時血清CRP≥10 mg/L的比例,比較差異均無統計學意義(均P>0.05);與非感染組比較,感染組合并有肺源性心臟病、低蛋白血癥、COPD病情分級、入院前3個月內使用抗生素或近1年內AECOPD加重≥1、因病情加重住院、氣管插管、輔助通氣時間≥14 d、抗生素應用時間≥14 d、抗生素應用種類≥3種、住院時間≥21 d、PCT≥0.5 ng/ml、血糖≥11.10 mmol/L的比例均較高,差異均有統計學意義(均P<0.05)。見表1、2。
2.2 患者發生下呼吸道PA感染的多因素logistic回歸分析 以是否發生PA感染為因變量(賦值方法:0=未發生,1=發生),以表1、2中單因素分析差異有統計學意義的指標為自變量,經過本研究多因素logistic回歸分析提示肺源性心臟病、低蛋白血癥、入院前3個月內使用抗生素、氣管插管、抗生素應用時間、確診PA感染時PCT≥0.5 ng/ml、入院時血糖≥11.10 mmol/L是老年COPD合并Ⅱ型呼吸衰竭發生下呼吸道PA感染的危險因素,見表3。
2.3 PA的耐藥性分析 培養陽性的51例患者(共51株)PA耐藥性分析顯示,PA耐藥性較高,僅對頭孢他啶和亞胺培南耐藥率低于20%,見表4。
2.4 兩組患者Kaplan-Meier生存曲線分析 入院后28 d的預后情況中,感染組死亡16例(31.37%),非感染組死亡52例(14.99%),感染組病死率明顯高于非感染組,差異有統計學意義(P<0.01)。經過Kaplan-Meier生存曲線分析顯示感染組累積生存率顯著低于非感染組(log-rank=9.395,P<0.01)。見圖 1。
3 討論
隨著臨床抗生素不合理應用及侵入性操作的增多,PA感染的病例逐年增多,并同時出現了大量耐藥菌株,給臨床感染防控工作帶來了極大的困難[7-8]。張泳等[9]對住院患者PA感染分布、耐藥狀況及預后情況進行調查顯示,呼吸科、ICU中PA感染分別占24.24%和17.42%,且總病死率為23.48%。張勇等[10]收集了634例COPD患者的痰標本并進行細菌培養時發現陽性率高達49.35%,且以革蘭陰性桿菌為主,老年患者中以PA檢出最為常見(約占22.27%),且以多重耐藥較為常見,對慶大霉素、頭孢噻肟、氨芐西林/舒巴坦等耐藥率均在70%以上。另一項研究表明,207例COPD患者中PA感染的總檢出率為10.14%(21/207)[11]。本研究結果中納入的398例COPD合并Ⅱ型呼吸衰竭患者下呼吸道PA感染率為12.81%(51/398),略高于以上報道,造成差異的原因可能與納入患者樣本量、年齡、合并基礎病、病情嚴重程度不同有關。
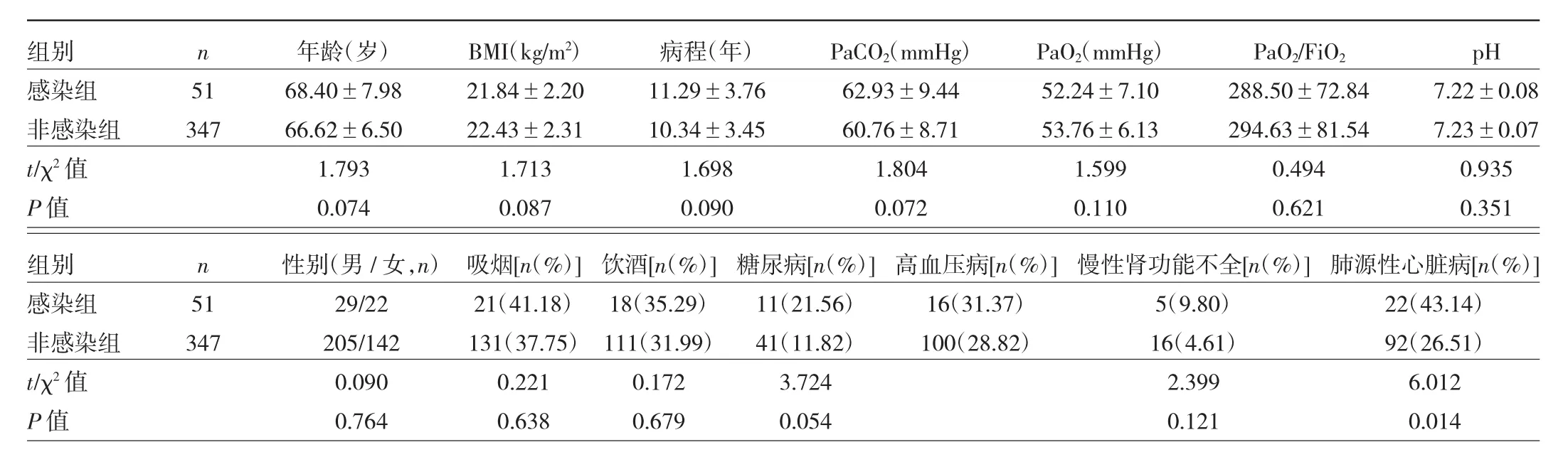
表1 兩組患者一般資料的比較
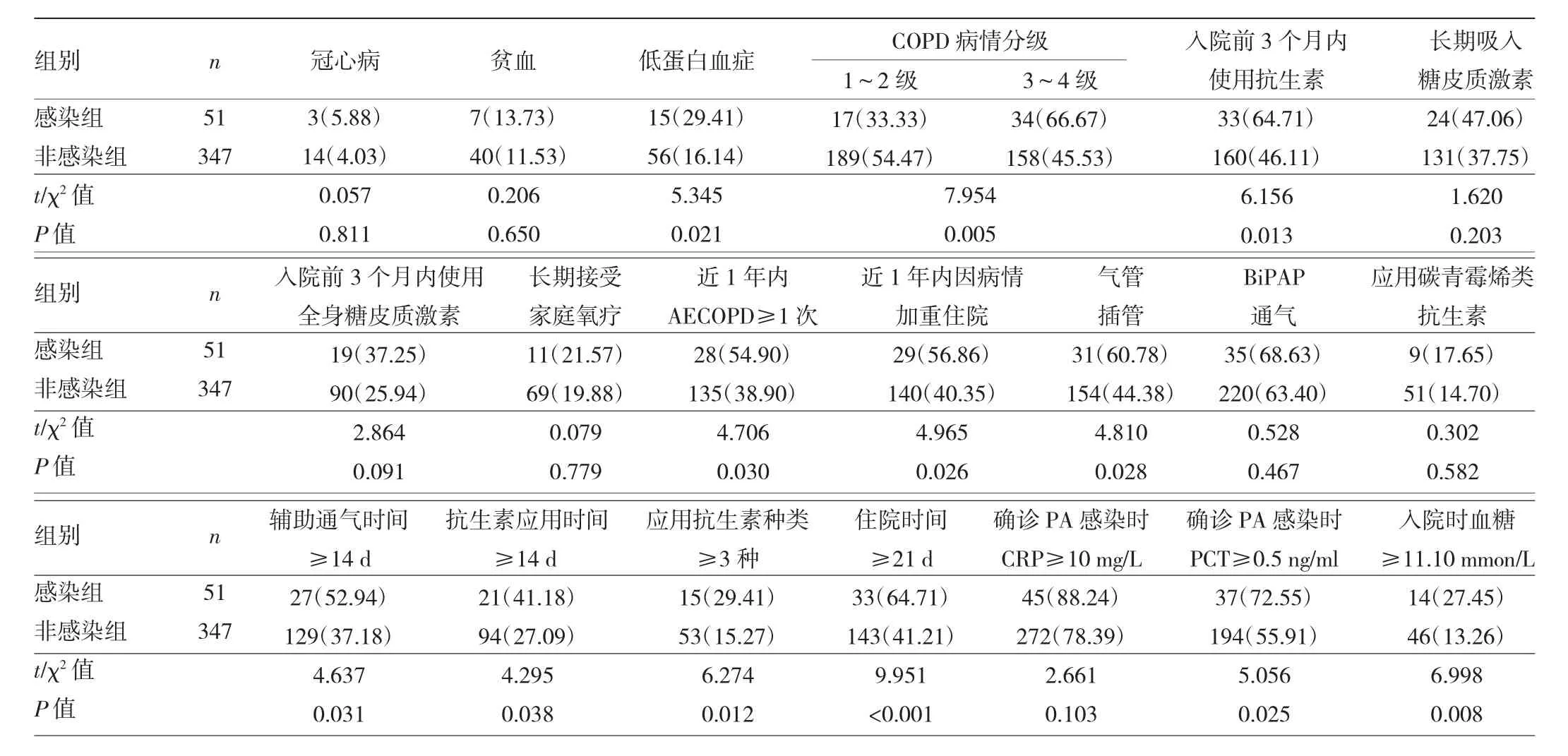
表2 兩組患者實驗室檢查指標的比較[例(%)]
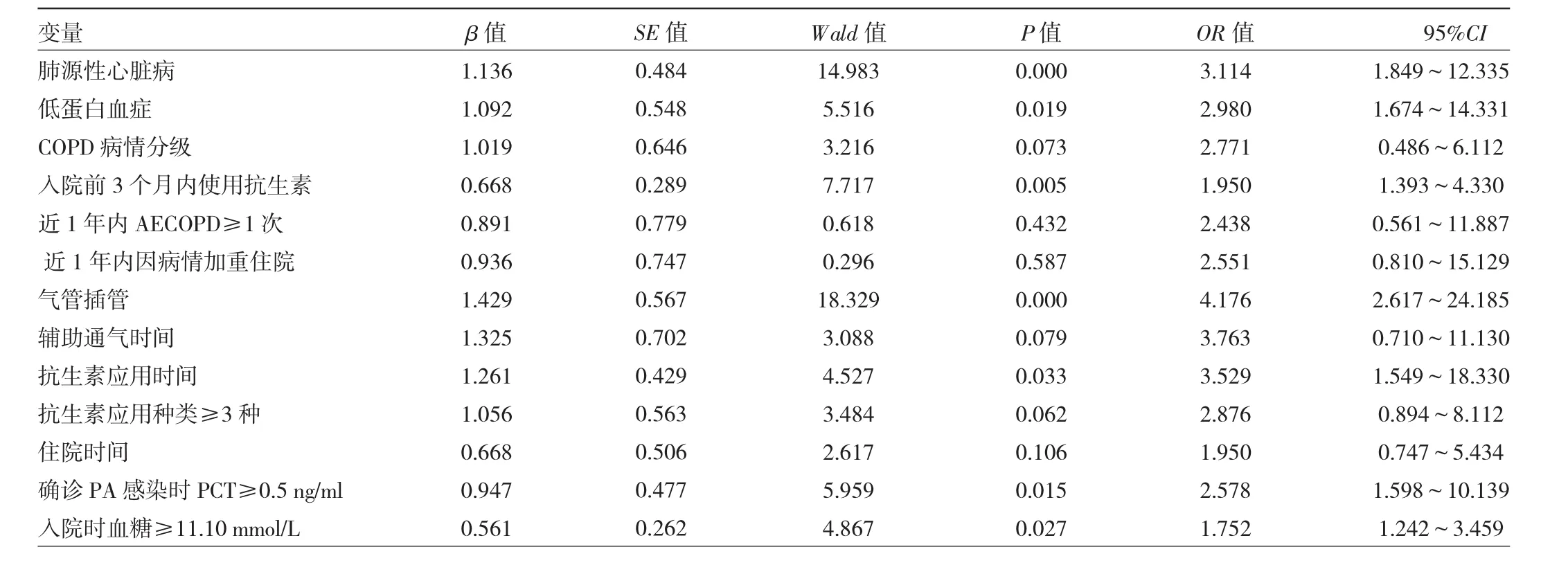
表3 患者發生下呼吸道PA感染的多因素logistic回歸分析
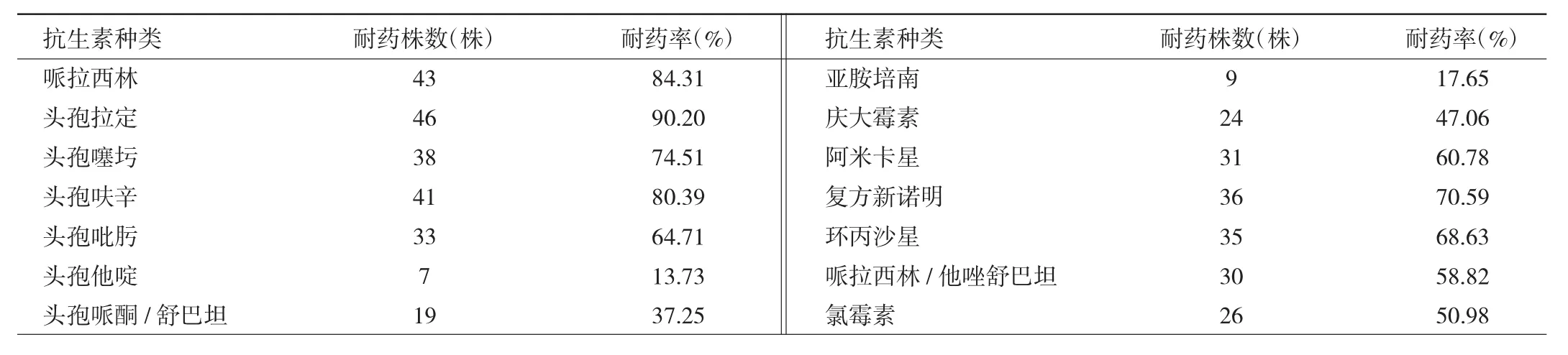
表4 PA的耐藥性分析
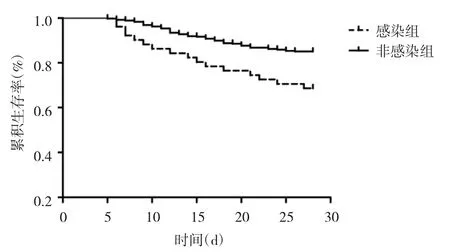
圖1 兩組Kaplan-Meier生存曲線分析
COPD合并Ⅱ型呼吸衰竭患者由于年齡偏大、免疫功能降低,呼吸道纖毛清除功能受損為PA的定植和生長提供了條件。本研究在單因素分析基礎上進行多因素logistic回歸分析顯示,肺源性心臟病、低蛋白血癥、入院前3個月內使用抗生素、氣管插管、抗生素應用時間、入院時PCT≥0.5 ng/ml、入院時血糖≥11.10 mmol/L是此類患者發生下呼吸道PA感染的危險因素。肺源性心臟病是COPD常見的基礎病之一[12],患者由于存在右心室功能異常、肺動脈高壓和肺循環淤血,因此為非發酵葡萄糖的革蘭陰性桿菌的增殖生長提供了有利的條件[13]。低白蛋白血癥在COPD中較為常見,血清白蛋白不僅是評價營養狀態的指標,亦與肺功能惡化和高病死率密切相關[14]。低白蛋白血癥能夠降低呼吸道、尿道黏膜合成分泌型IgA的能力,從而增加PA感染的風險[15]。入院前3個月內使用抗生素,尤其是使用廣譜類抗生素可能引起菌群失調,導致氣道黏膜中正常菌群結構破壞,從而誘發條件致病菌的優勢生長[16]。氣管插管屬于侵入性操作,定植于氣道黏膜中的PA可借助氣流逆行進入肺部而發感染[2,17]。長期不合理聯用抗生素是下呼吸道PA感染及多重耐藥菌株產生的獨立危險因素[18-19]。本研究單因素分析中雖然感染組抗生素應用種類≥3種、抗生素應用時間≥14 d的比例高于非感染組,但抗生素應用種類并未能進入最終的多因素logistic回歸分析,出現這種結果的原因可能與納入的樣本量、合并基礎病種類不同有關。PCT是一種評價和鑒別病毒和細菌感染、指導抗生素治療策略的參考指標[20]。血清PCT≥0.5 ng/ml則常提示細菌感染,且其水平增高常預示著COPD患者免疫能力、肺功能進一步惡化,死亡風險加大[20]。血糖增高是住院患者病死的獨立危險因素[21-22]。有研究表明,AECOPD患者中高血糖較為常見,高血糖能夠損傷機體免疫功能,造成T淋巴細胞亞群平衡紊亂[23],還能損傷氣道黏膜纖毛功能,因此可增加潛在PA感染的風險。本研究耐藥性分析結果顯示,除了對頭孢他啶和亞胺培南耐藥率低于20%之外,對哌拉西林、頭孢拉定、頭孢噻圬、頭孢呋辛、復方新諾明耐藥性均高于70%,對哌拉西林/他唑舒巴坦、環丙沙星、阿米卡星、頭孢吡肟耐藥性均高于50%,這與相關報道基本一致[13],因此應加強對COPD患者PA耐藥性的監測。根據指南《慢性阻塞性肺疾病診治指南(2013年修訂版)》[5]中的建議,應適時根據患者急性加重程度、合并基礎病、費用、本院耐藥狀況和患者治療依從性等進行評估。
綜上所述,老年COPD合并Ⅱ型呼吸衰竭患者下呼吸道PA感染與低蛋白血癥、肺源性心臟病、入院前3個月內使用抗生素、氣管插管、抗生素應用時間、高水平PCT和高血糖有關,且耐藥性與病死率較高,應當引起臨床的高度關注。在實際臨床工作中,應當積極評價患者基礎病,注意營養狀態及糾正低蛋白血癥,改善免疫功能,積極的控制血糖波動,密切監測病原學,并依據PCT、藥敏實驗結果合理指導抗生素的應用。

