胸部物理治療在體外循環先天性心臟病根治術后機械輔助通氣低齡低氧血癥患兒中的應用
王寒凝,易 敏,汪 婭,邱宏翔,周雅婷,項 明
體外循環心臟術后肺部并發癥發生率約為15%~60%,是導致病人病死率增加,住院時間延長的主要原因之一[1]。隨著心臟診療技術的不斷提高,先天性心臟病的治療越來越趨向于低齡化和低體重化,而嬰幼兒心臟術后呼吸功能的維護是手術成功的重要一環。由于心臟手術過程復雜,時間較長,采用低溫體外循環輔助,所以術后出現低氧血癥的概率較高。低氧血癥是體外循環心臟手術的嚴重并發癥,死亡率可達20%~80%[2],嚴重影響患兒的康復。體外循環術后的嬰幼兒由于肺循環血流量增多、肺組織順應性低、麻醉誘導中的高濃度氧、手術切口破壞胸廓完整性等原因,都易導致術后低氧血癥的發生[3]。胸部物理治療(chest physiotherapy,CPT)是一類非藥物、以簡單的手法或以改變病人體位、訓練病人呼吸的動作或咳嗽的技巧,也可借助器械,目的在于減輕氣道阻塞、幫助廓清氣道分泌物,改善通氣和氣體交換,增加呼吸肌功效和協調性的治療技術。該治療技術已經被驗證可以有效降低肺部感染的發生率,改善低氧血癥[4-6]。目前,關于胸部物理治療在體外循環先天性心臟病根治術后機械輔助通氣低齡低氧血癥患兒中應用的相關報道較少,且尚未檢索到有關胸部物理治療標準化流程應用于先天性心臟病患兒的研究。本研究將多種胸部物理治療技術綜合運用,結合胸部物理治療前對患兒病情的準確評估,制定個性化方案,采取集束化護理、標準化流程進行干預,取得了較好的治療效果。現報告如下。
1 對象與方法
1.1 對象 選擇2015年12月—2019年1月重慶醫科大學附屬兒童醫院胸心外科83例經體外循環行先天性心臟病根治術后機械輔助通氣低齡低氧血癥患兒為研究對象,其中2015年12月—2017年6月42例病人為對照組,2017年7月—2019年1月41例為觀察組。納入標準:①CICU中通過體外循環行先天性心臟病根治術的月齡<6個月患兒;②術后進行機械輔助通氣,且均采用同步間歇指令通氣模式(SIMV)及壓力控制模式;③患兒動脈血氣分析結果符合低氧血癥診斷標準:PaO2≤[102-(0.33×年齡)] mmHg(1 mmHg=0.133 kPa)。排除標準:①既往急性呼吸窘迫綜合征(ARDS)或其他嚴重呼吸功能障礙;②術前昏迷;③術后大量出血,需二次手術;④術后腦出血;⑤術后持續惡性心律失常;⑥術后48 h內即轉院或死亡。兩組病人性別、月齡、體重、術前/術后血紅蛋白(Hb)計數、術前/術后白細胞(WBC)計數、體外循環時間、手術時間比較差異均無統計學意義(P>0.05)。且兩組患兒機械輔助通氣期間呼吸機參數設置情況比較差異均無統計學意義(P>0.05),有可比性。見表1、表2。
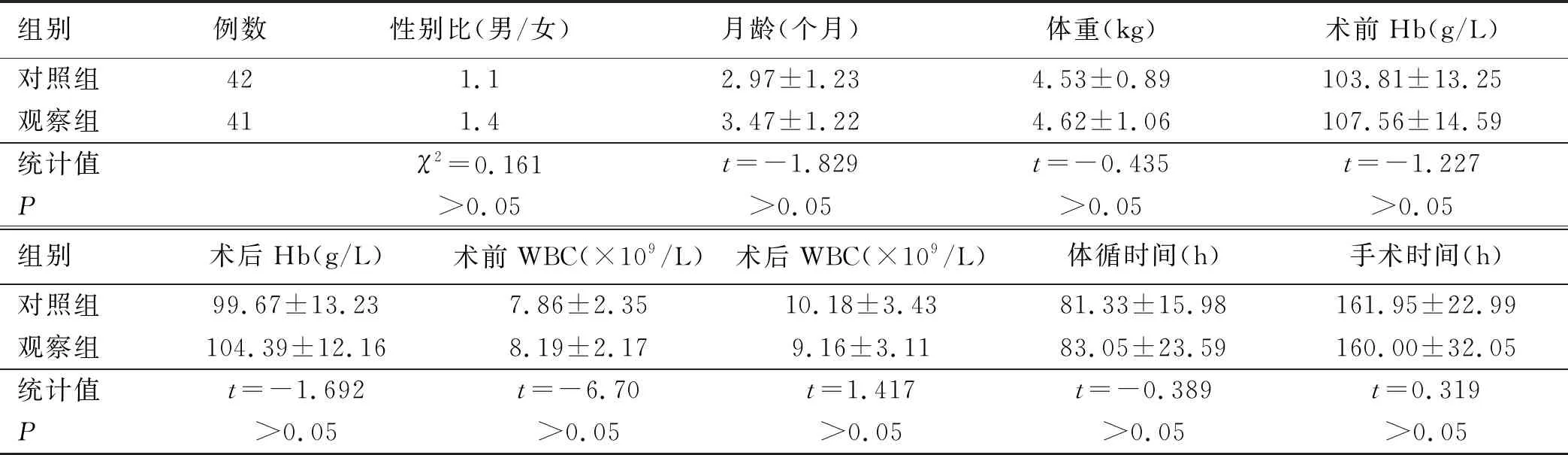
表1 兩組患兒基本情況比較
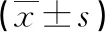
表2 兩組患兒呼吸機參數設置情況比較
1.2 干預方法
1.2.1 對照組 給予常規護理措施,包括不定時的翻身、叩擊背部、吸痰等。以上各項操作由責任護士對所負責床位患兒實施,在完成患兒日常治療及護理任務之余,適時為病人進行翻身、叩擊背部及吸痰等操作。但實施各項操作的具體方法、時機及頻次在較大程度上依賴于護士個人經驗及當班工作負荷,缺乏標準化的操作規范及流程。
1.2.2 觀察組 實施綜合胸部物理治療技術,具體如下。
1.2.2.1 成立胸部物理治療小組 共7人,其中4名主管護師,均為本科學歷,負責實施措施、收集資料;4人中1名為病區護士長,負責制訂計劃、靈活排班;1名有呼吸理療師進修學習經歷。另2名護理研究生,負責科研設計及數據分析;并邀請1名監護室醫生,由其對6名護士關于胸部物理治療技術及數據采集方法進行指導和培訓,培訓后對相關內容進行床邊考核,物理治療方法及執行順序正確、數據采集且記錄客觀方可視為合格。
1.2.2.2 設立胸部物理治療崗位 護理部主持拍攝兒童胸部物理治療技術操作示范視頻,制訂考核標準,接受培訓并通過考核者可承擔此崗位工作。
1.2.2.3 具體操作流程 首先,制定干預計劃:采用小兒CHD術后氣道管理量化評估表[7]及氣道護理干預表。見表3、表4。評估患兒病情,根據評估結果制訂每名患兒每日胸部物理治療干預計劃,計劃需結合患兒病情實時更新。

表3 小兒CHD術后氣道管理量化評估表

表4 氣道護理干預表
實施計劃:將常規護理措施融入綜合胸部物理治療中,治療順序遵循胸部物理治療標準化流程。①更換體位:2人配合,每2 h 1次。翻身時1人負責保護患兒頭頸部、固定氣管插管及頸內靜脈置管;另1人負責理順各類管道、預留足夠長度。取目標體位后,予軟枕支撐,保持體位舒適及穩定,確保各有創導管通暢、未發生移位。②叩擊背部:操作者五指合攏、呈空杯狀向肺門方向叩擊背部。也有研究者應用不同型號的小兒復蘇囊面罩,在其外部套上一次性薄膜手套,將多余部分塞進面罩中空部位,操作者用食指及中指夾住面罩上端的接孔處,其余三指扣住面罩,利用手腕力量叩擊患兒[8]。叩擊頻率約每分鐘60次,左右側背部交替叩擊各5 min,共10 min。③振動排痰:由于體位的隨意性,正逐步在臨床推廣。它能使體表機械振動的能量傳導到肺部,使墜積在氣管、支氣管、肺泡表面的痰液或黏液栓子松動及刺激咳嗽的產生將其排出[9]。國內報道,機械輔助排痰機應用于排痰困難的嬰幼兒效果是肯定的[10]。操作者施以垂直于患兒體表的力量,使排痰儀震動頭緊貼患兒背部;緩慢向肺門方向推動震動頭,左右肺交替進行,共5 min。④體位引流時,通過調整床頭高度及患兒體位,使病肺處于高位,其引流支氣管的開口向下,促使痰液借重力順體位引流排出。每次體位引流時間持續約10~15 min,引流同時配合叩擊背部及機械輔助排痰技術,效果更佳。⑤引流完成后按需清理口鼻腔分泌物,必要時進行氣管導管內吸痰。⑥抬高床頭30~45°,取頭高足低的舒適體位。
此時,一個胸部物理治療標準化流程結束。胸部物理治療結束后,對患兒進行有效的保護性約束,在保證其安全的同時兼顧患兒的舒適度。在胸部物理治療標準化流程中有其關鍵技術及質量控制要點需要特別注意。①手術當天僅抬高床頭、更換體位,暫不以其他胸部理療技術刺激患兒,以免引起傷口疼痛與血流動力學變化。②術后第1天以抬高床頭及更換體位為主,視患兒生命體征、血流動力學情況、耐受程度,酌情增加叩擊背部及機械輔助排痰、體位引流操作。③操作前評估患兒進食時間,叩擊背部及體位引流宜在餐后2 h或餐前進行。④確保患兒各管道(如氣管導管、心包或胸腔閉式引流管、尿管、腹腔引流管、深靜脈置管等)在操作前、中、后固定穩妥、保持通暢,無折疊、扭曲、滑管、脫管等意外情況。如有異常,立即通知醫生,協助處理。⑤更換體位時需避免患兒身體之下壓有電極線、深靜脈卡扣、各種管道等可能造成患兒不適或壓力性損傷的物品,保持床單清潔平整。⑥叩擊背部及機械輔助排痰時以衣物隔開皮膚,操作避開手術切口及引流管置管處,操作者可按壓切口及引流管周圍皮膚,以緩解皮膚張力增加引起的疼痛。⑦高血壓、有明顯呼吸困難伴發紺、心力衰竭屬于相對禁忌證,在充分鎮痛鎮靜的境況下可以試行體位引流。⑧治療過程中密切觀察患兒病情變化,俯臥位通氣將患兒頭偏向一側,保持氣道通暢。若患兒出現心律失常、血壓異常等并發癥或患兒煩躁不安時應立即停止操作,報告醫生并積極配合處理。⑨避免交叉感染:每個患兒治療結束后嚴格更換手套,免洗手消毒液規范洗手。接觸多重耐藥感染菌病人后以流動水清洗雙手,治療用物按規范進行終末處理。
1.3 評價指標 ①血氣指標:采用血氣分析儀,測量并記錄兩組患兒術后24 h、48 h、72 h、96 h的動脈血氧分壓(PaO2)、動脈血二氧化碳分壓(PaCO2)。②術后機械輔助通氣時間:為自手術后返回CICU上呼吸機起至脫呼吸機為止計算。③術后監護時間:為自手術后返回CICU當天至轉出CICU當天計算。④肺部并發癥發生情況:包括肺不張、肺實變等。
2 結果
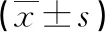
表5 兩組患兒血氣指標PaO2比較 單位:mmHg
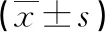
表6 兩組患兒血氣指標PaCO2比較 單位:mmHg
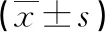
表7 兩組患兒術后機械輔助通氣時間及術后監護時間比較

表8 兩組患兒術后肺部并發癥發生情況比較 單位:例(%)
3 討論
研究認為體外循環術后參與吸氣的呼吸肌力量明顯下降,最大吸氣壓力于術后5 d下降11%,膈肌功能不佳導致病人呼吸困難程度加重,無法有效咳嗽、咳痰。且術后病人心功能不全,影響其骨骼肌氧合能力以及線粒體功能,從而影響其體力,減慢康復進程[11-12]。因此,胸部物理治療技術的綜合應用十分必要。目前我國常規的胸部物理治療技術仍然以叩擊背部為主,這高度依賴操作者的業務能力,且可能造成操作者發生腕管綜合征;并且容易導致病人血氧不足、心律失常、顱內壓增高;因此肺部并發癥預防效果不佳[13-14]。本研究針對體外循環先心病根治術后機械輔助通氣低齡低氧血癥患兒,將多種胸部物理治療技術綜合運用,結合胸部物理治療前對患兒病情的準確評估,為患兒制定個性化方案,采取集束化護理、標準化流程進行干預。本研究結果顯示:①不同干預措施下的兩組患兒術后各時間節點PaO2比較差異有統計學意義(P<0.05),觀察組患兒術后24 h PaO2低于對照組,觀察組術后48 h、72 h、96 h PaO2均高于對照組;干預措施實施后兩組患兒的PaO2均逐漸上升;不同干預措施和時間之間存在交互作用,隨著干預時間的延長,兩組患兒PaO2上升的幅度不同,以觀察組的患兒PaO2上升幅度更大。隨著干預措施的實施,觀察組患兒術后24 h、48 h、72 h、96 h PaCO2均低于對照組,且兩組比較差異有統計學意義。以上血氣分析指標的變化提示觀察組患兒術后氧合情況優于對照組,差異有統計學意義(P<0.05)。②觀察組患兒術后機械輔助通氣時間、術后監護時間均短于對照組,差異有統計學意義(P<0.05)。③胸部物理治療的主要作用是引流肺及呼吸道內分泌物,提高纖毛清除痰液的能力,改善通氣/血流比例及肺功能,增加肺容量,減少呼吸做功,從而降低肺部并發癥的發生率[15]。但本研究中兩組患兒術后肺部并發癥發生情況尚無顯著差異,可能是由于胸部物理治療標準化流程的應用較其研究干預時間短且樣本量小有關,此類指標有待進一步研究探討。值得注意的是,任素琴等[16]研究發現,危重癥患兒應用胸部物理治療技術可引起生命體征的變化。對年齡較小的兒童進行體位引流,長時間處于不舒適的體位會引起其哭吵、煩躁,有可能導致胃食管反流(GOR),從而引起血氧飽和度的降低[17],甚至發生吸入性肺炎[18]。但也有國外文獻報道,胸部物理治療時患兒處于頭低足高位并不會加劇GOR的發生[19]。因此,胸部物理治療技術應用于危重癥患兒的過程中,應密切關注患兒生命體征的變化,體位引流時護士也應格外重視患兒的舒適性,持續時間的長短也應針對患兒的病情實施個性化處理,使臨床護理工作做到更科學化、精細化的管理。
綜上所述,嬰幼兒肺炎時采用胸部物理包括霧化吸入、體位引流、叩擊、震顫、咳嗽、吸痰等治療,可有效清除氣道分泌物,改善通氣,降低呼吸道感染的發病率[20]。胸部物理治療集束化呼吸道管理在臨床上已受到越來越多醫護人員的重視,這是一種按照循證護理的證據和指南,將一系列主要關注呼吸道護理管理的治療護理措施逐步實施的過程。本研究證實,胸部物理治療技術在體外循環先天性心臟病根治術后機械輔助通氣低齡低氧血癥患兒中的應用效果確切,可有效縮短術后機械輔助通氣時間與術后監護時間,但在降低肺部并發癥發生率的療效方面,仍需進一步探討和證實。

