TiO2改性的Co-Mo耐硫變換脫氧催化劑常壓性能研究
孫倩,張新堂,趙國明,劉珊珊,尹爽,劉營春
(山東科技大學 化學與生物工程學院,山東 青島 266590)

TiO2屬于一種典型的強金屬-載體相互作用類型的載體[4-5],并在光催化領域得到了一定的應用[6-8],但是直接用作催化劑載體具有一定的局限性[9]。本實驗選擇加入TiO2作為鎂鋁尖晶石載體改性劑,充分利用鎂鋁尖晶石和TiO2兩種載體的優點,探究對催化劑性能的影響。
1 實驗部分
1.1 材料與儀器
AlOOH·nH2O、MgO、TiO(OH)2、C6H8O7·H2O、Co(NO3)2·6H2O、Ni(NO3)2·6H2O、Ce(NO3)3·6H2O、Fe(NO3)3·9H2O、氨水、C2H8N2、(NH4)6·Mo7O24·H2O、K2CO3均為分析純;田菁粉,工業級。
DJ-40型單螺桿擠條機;101-1型鼓風干燥箱;SX24-10型馬弗爐;常壓微反裝置,自制;DLIII-500智能顆粒強度測定儀;麥克ASAP2460比表面積測定儀;Rigaku Utima IV型X射線衍射儀;SP6800A氣相色譜儀。
1.2 耐硫變換脫氧催化劑的制備
將一定量的擬薄水鋁石、MgO、偏鈦酸混合,配以一定比例的造孔劑、助擠劑混捏擠成條狀,經100 ℃干燥24 h、550 ℃焙燒3 h得到載體。其中Al2O3/MgO摩爾比為1∶1,制備一系列不同TiO2含量的載體。將硝酸鈷、鉬酸銨、碳酸鉀、硝酸鎳配制成浸漬液,浸漬于載體,100 ℃干燥24 h,500 ℃焙燒3 h制得成品耐硫變換脫氧催化劑。
1.3 強度穩定性測試
隨機抽取20 g試樣,用顆粒強度測試儀測試不同TiO2含量載體的徑向破碎強度。并考察載體經過水煮處理和水熱處理后,強度的變化。
1.4 BET分析
將所需樣品研磨至無明顯顆粒感,預處理樣品抽真空4 h,BJH分析模版進行分析測試。
1.5 XRD表征
采用X射線衍射儀對催化劑進行晶相結構測定。工作電壓40 kV,工作電流100 mA,波長λ=0.154 06 nm,對樣品在 2θ為 10~80 °范圍進行掃描,掃描步長為0.02(°)/s,掃描速率為 8(°)/min。
1.6 O2/CO含量分析方法
使用氣相色譜儀對原料氣及尾氣中的O2、CO含量進行分析,5A分子篩填充柱檢測產物中的O2、CO,氦氣作為載氣,采用熱導池檢測,外標法進行定量分析。色譜條件:柱箱溫度為45 ℃,汽化室溫度為100 ℃,檢測器溫度為100 ℃,橋流100 mA,衰減1。
1.7 評價裝置及方法
在常壓微反裝置上進行催化劑硫化及活性評價,以脫氧前后氣體中O2、CO含量的變化來評價脫氧/變換活性的好壞。

圖1 催化劑產品評價裝置流程圖Fig.1 Flow chart of catalyst product evaluation device1.原料氣鋼瓶;2.高純氮氣鋼瓶;3.穩壓閥;4.轉子流量計;5.壓力表;6.水浴飽和器;7.微反裝置預熱器;8.微反裝置反應器;9.冷凝器;10.氣體干燥塔;11.氣相色譜分析系統;12.采樣六通閥;13.氣體放空
常壓脫氧劑評價條件:脫氧劑裝填量1 mL,空速3 000 h-1;原料氣組成:CO 45%,O20.5%,H2S 0.5%,其余為H2;硫化溫度280 ℃,硫化時間2 h,在210,230,250,270,290 ℃五個溫度下測定催化劑活性,先對干氣反應(水氣比:0)進行討論,最后與濕氣反應(水汽比:0.88)對比。脫氧率(%)和CO變換率(%)的計算公式如下:
(1)
(2)
其中,XO2為O2轉化率;XCO為CO變化率;yO2·in為反應前原料氣中O2百分含量;yO2·out為反應后尾氣中O2百分含量;yCO·in為反應前原料氣的CO百分含量;yCO·out為反應后尾氣中的CO百分含量。
2 結果與討論
2.1 Ti對載體強度及吸水率的影響
考察了改性劑TiO2添加量對鎂鋁尖晶石載體及其水煮處理和水熱處理后強度和吸水率的變化,結果見表1。

表1 不同TiO2含量的載體強度及吸水率Table 1 Support strength and water absorption of different TiO2 content
由表1可知,當TiO2含量為20%時,載體吸水率呈現出最大值,載體中加入少量的TiO2強度明顯下降,隨著TiO2含量的增加,載體的強度呈先上升后下降至趨于平穩,當達15%時,強度值出現最大值。當TiO2含量為75%時強度又突然增大,這是因為此載體主要相轉變為Ti的晶型,尖晶石結構發生變化時,強度突然增大。在水熱水煮處理過程中,載體物相發生變化,強度均得到明顯的提升。
2.2 載體XRD表征
對含有15%TiO2的載體在不同溫度下(450~850 ℃)焙燒處理后進行XRD表征,結果見圖2。

圖2 不同焙燒溫度的催化劑載體XRD圖(含15%TiO2)Fig.2 XRD patterns of catalyst support at different calcination temperatures(containing 15% TiO2)
通過與標準物的XRD圖對比分析,隨著焙燒溫度的增大,鎂鋁尖晶石峰越來越多,且峰強度越來越大,說明高溫條件下有利于鎂鋁尖晶石的生成。其中2θ為43.5,62.8,78.1 °處出現衍射峰歸屬于MgO,隨著焙燒溫度不斷增大,MgO衍射峰峰強度逐漸減弱,這說明溫度升高使得游離態的MgO減少,從而促進鎂鋁尖晶石的形成,且25.2,54.3 °處的TiO2衍射峰也峰逐漸增強,譜線變得尖銳,TiO2的結晶度增加,物相趨于一相。
2.3 載體BET測試
對2.2節中不同溫度焙燒后的載體進行BET測試,結果見表2。

表2 不同焙燒溫度對載體強度及孔分布的影響Table 2 Effect of different firing temperatures on the strength and pore distribution of the support
由表2可知,隨著焙燒溫度的增大,載體強度呈下降趨勢,比表面積和孔容減小,平均孔徑增大。450~750 ℃焙燒時,平均孔徑<10 nm,以小孔為主。在焙燒的過程中,TiO2-Al2O3-MgO三元復合物顆粒表面發生粘結、表面擴散和晶格擴散,使粒子變大,比表面積和孔容隨著焙燒溫度的升高而減小,高溫焙燒使得孔壁崩塌[10],一些小的孔徑逐漸消失,形成了更大的孔徑,呈現出小孔所占的比例逐漸減少,大孔比例呈增長的趨勢。這種三元復合型載體既保證了鎂鋁尖晶石載體高強度、熱穩定性好、大比表面積和適宜的孔徑分布特點,又具有TiO2結構穩定性。
2.4 Ti對催化劑脫氧性能的影響
在2.1節的載體上分別浸漬相同活性組分,進行脫氧實驗,結果見圖3。

圖3 TiO2含量對催化劑脫氧活性的影響Fig.3 Effect of TiO2 content on catalyst deoxidation activity
由圖3可知,加入TiO2對催化劑的脫氧活性有明顯的促進作用,當TiO2含量為15%時,脫氧活性呈現出最大值64.75%,隨著TiO2含量的繼續增加,脫氧活性下降至58%呈穩定趨勢。TiO2作為一種載體改性劑,可促進Mo還原成具有活性的低價Mo5+[11]。TiO2具有很強的Lewis酸性,當MoS2負載于TiO2改性的載體上,催化劑中MoS2的堆積層數和晶粒長度均趨于很小的范圍,催化劑表面的晶格缺陷或活性組分的結構都可能發生變化,從而影響催化劑的脫氧性能[12-13]。TiO2促使MoO3在鎂鋁尖晶石表面分散,使MoO3在經TiO2調變的復合載體TiO2-Al2O3-MgO上的分散閾值較鎂鋁尖晶石表面上大,而且TiO2的存在還有利于MoO3的深度還原,使活性組分Mo的還原態顯示出較高的催化活性[14]。綜合催化劑載體強度、吸水率及脫氧性能測試結果得出,當TiO2含量為15%時,脫氧率最高。
2.5 不同TiO2含量催化劑的XRD表征
對具有不同含量TiO2的鎂鋁尖晶石催化劑進行XRD表征分析,結果見圖4。

圖4 不同TiO2含量催化劑XRD圖Fig.4 XRD patterns of different TiO2 content catalysts
由圖4可知,發現42.9,62,78.3 °處均出現NiTi峰,43.1,62.1,78.6 °處出現CoTi衍射峰,這些衍射峰強度隨著TiO2含量的增加而減弱,鎂鋁尖晶石峰強度基本不受TiO2含量的影響。催化劑中均未觀察到明顯的Mo、K的衍射峰,由此得出催化劑活性組分在載體中未發生團聚,較為分散,且TiO2含量對催化劑物相的形成有一定影響。
2.6 Ce、Fe、Ni對催化劑活性的影響
此脫氧催化劑以Mo作為主要活性組分,Co在此催化劑體系中必不可少,當Co和Mo同時存在時,Co2+可以抑制Mo6+物種過度還原,促進“oxysulfo-Mo5+”相的生成,其中MoS2納米層和位于其邊緣的Co2+構成活性相Co-Mo-S,對脫氧反應起到活化促進作用,所以Co-Mo同時存在產生的協同作用更有利于脫氧過程進行[15]。
據專利CN201510316306.2報道[16],添加Ce、Fe、Ni為活性助劑對脫氧活性有影響,研究了在Co-Mo-K的基礎上添加Ce、Fe、Ni助劑對催化劑脫氧活性的影響,結果見表3。

表3 添加Fe、Ce、Ni對催化劑脫氧活性的影響Table 3 Effect of Fe,Ce,Ni addition on catalyst deoxidation activity
由表3可知,添加Ce、Fe在低溫條件下均有助于提高脫氧活性,且Ce的作用強于Fe,加入Ni的催化劑活性最高,脫氧率可達57.44%。210 ℃時,Fe對催化劑的脫氧性能具有促進作用且脫氧率較高,此狀態下的催化劑處于剛硫化完狀態,硫化形態較好,表現出的活性較高,隨著反應溫度的升高,Fe的加入反而減弱脫氧性能。氧氣存在時,硫化鐵在100~400 ℃之間處于加速氧化期,硫化鐵表面的活性中心吸附氧氣分子,表面氧氣濃度迅速增加,使硫化鐵向深度氧化階段進行,催化劑活性中心減少,溫度越高,催化劑脫氧活性越低[17-18]。綜上,Ni在提高催化劑脫氧活性方面較為優勢。
2.7 助劑Ni對催化劑活性的影響
常壓下,考察了NiO含量對催化劑活性的影響,結果見圖5。


圖5 不同Ni含量對催化劑活性的影響Fig.5 Effect of different Ni content on catalyst activitya.脫氧活性;b.變換活性
由圖5可知,加入Ni對催化劑的脫氧活性有促進作用,當NiO含量達到0.2%時,各個溫度點催化劑均表現出較高的脫氧活性;當NiO含量超過0.2%時,各溫度點催化劑脫氧活性均降低。這是因為當加入少量NiO時,對載體中鎂鋁尖晶石的覆蓋削弱了活性組分Mo和鎂鋁尖晶石的相互作用,增大了Mo的濃度,協同TiO2的相互作用更加促進Mo的分散,使結構發生變化,有利于H2和O2的反應[19],且由2.2節中催化劑載體XRD表征結果得出,載體中存在少量MgO,MgO可提高NiO的分散度[20],從而提高催化劑活性。當繼續增大NiO的含量時,負載的NiO會在載體表面發生聚集,從而弱化部分鎳相與載體之間的相互作用,導致催化劑脫氧活性降低[21]。催化劑均具有變換活性,隨著溫度的升高,變換活性不斷增大,加入Ni的變換活性略微有所提高。
由表4加NiO和不加NiO的BET測試結果表明,NiO對催化劑樣品的比表面積和孔分布影響不大,Ni不是通過改變催化劑的幾何結構而提高催化劑活性的。

表4 加Ni和不加Ni催化劑的物性比較Table 4 Comparison of physical properties with and without Ni catalyst
2.8 K對催化劑脫氧活性的影響
據文獻報道Co-Mo系催化劑中添加堿金屬可以會促使Mo5+更穩定的存在,有效提高催化活性[22-23]。以K2CO3作為K源,對不同含量的K2O對催化劑活性的影響進行研究,實驗結果見圖6。


圖6 不同K含量對催化劑活性的影響Fig.6 Effect of different K content on catalyst activitya.脫氧活性;b.變換活性
由圖6可知,加入K對催化劑的脫氧活性有明顯的促進作用,且當反應溫度為270 ℃時,催化劑脫氧活性最高。K2O含量到達9%時,脫氧活性表現出最大值。繼續增加K2O的含量,催化劑脫氧活性明顯降低,且K2O含量在9%時,催化劑變換活性最高,變換活性隨著溫度的升高而增大。縱秋云等[24]研究發現,K含量對Co-Mo系催化劑的孔分布和比表面積影響不大,所以K并不是通過改變催化劑的幾何因素促進催化劑脫氧活性升高。K同時促使Mo轉向低價態,活性中心Mo(V)數量增加,活化態的氧分子、氫分子和活性組分Mo之間的電子轉移加快,從而加速脫氧反應的進行,有利于氣體的吸附脫附[25]。同時K與TiO2在影響催化劑脫氧活性方面具有協同作用,提高催化劑的“捕硫”能力,增加催化劑表面硫濃度,降低失硫速率,能夠保持較高的耐硫脫氧活性。但K2O含量過高,易使脫氧劑活性中心覆蓋過剩的游離態的K,從而活性中心減少,達不到真正的脫氧目的。
3 硫化及工藝條件對催化劑活性的影響
3.1 干濕氣硫化對催化劑活性的影響
干濕氣硫化會對催化劑活性產生影響。由圖7可知,干氣硫化后的催化劑無論是脫氧活性還是變換活性均高于濕氣硫化的催化劑,說明在原料氣中配入水蒸氣影響催化劑的硫化程度,降低催化劑活性。當反應溫度低于250 ℃時,濕法硫化的催化劑脫氧率呈下降趨勢,隨后又升高,說明濕法硫化后的催化劑不穩定。水能夠加速催化劑中K流失速率和反硫化反應,同時還可以加速催化劑中小顆粒融結和長大,催化劑中的Co-Mo-S活性相和“缺陷”面積急劇減少[26],導致硫化效果低。
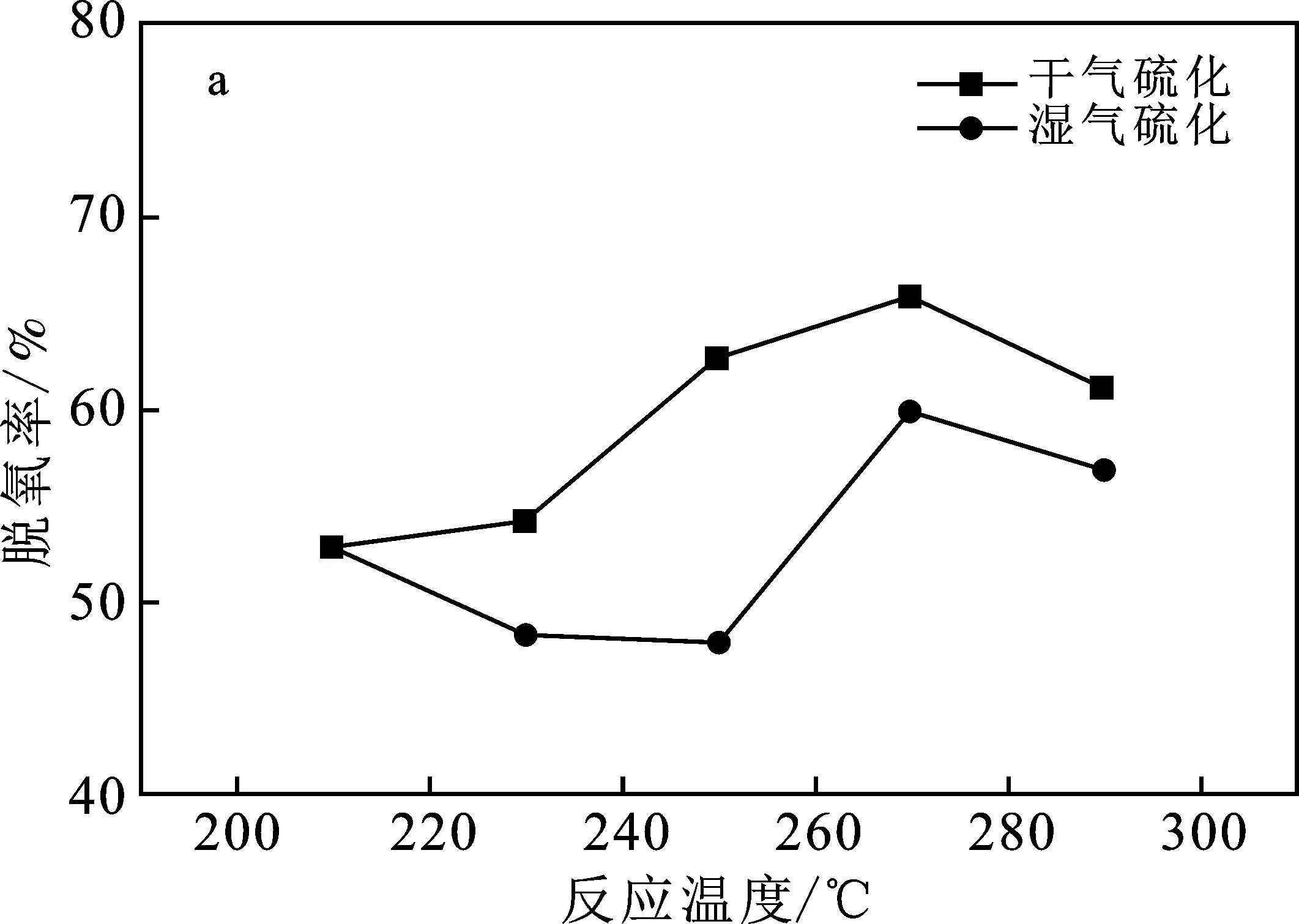

圖7 干濕氣硫化對催化劑活性的影響Fig.7 Effect of dry and wet gas sulfuration on catalyst activitya.脫氧活性;b.變換活性
3.2 硫化時間對催化劑活性的影響
硫化時間對催化劑活性產生影響見圖8。


圖8 硫化時間對催化劑活性的影響Fig.8 Effect of vulcanization time on catalyst activitya.脫氧活性;b.變換活性
由圖8可知,隨著硫化時間的延長,催化劑的脫氧、變換活性均呈遞增趨勢。當硫化時間低于2 h時,催化劑的脫氧、變換活性提升較快,到達2 h后,延長硫化時間催化劑的脫氧率、變換率趨于平緩。這是因為硫化時間越短導致氧化態的催化劑硫化不充分,生成的硫化態活性中心不足。隨著硫化時間的延長,催化劑硫化度增加,每個溫度條件下都存在一個平衡值,當達到此平衡值后,硫化時間延長,硫化度不會再提高,催化劑活性趨于穩定[27]。
3.3 反應空速對催化劑活性的影響

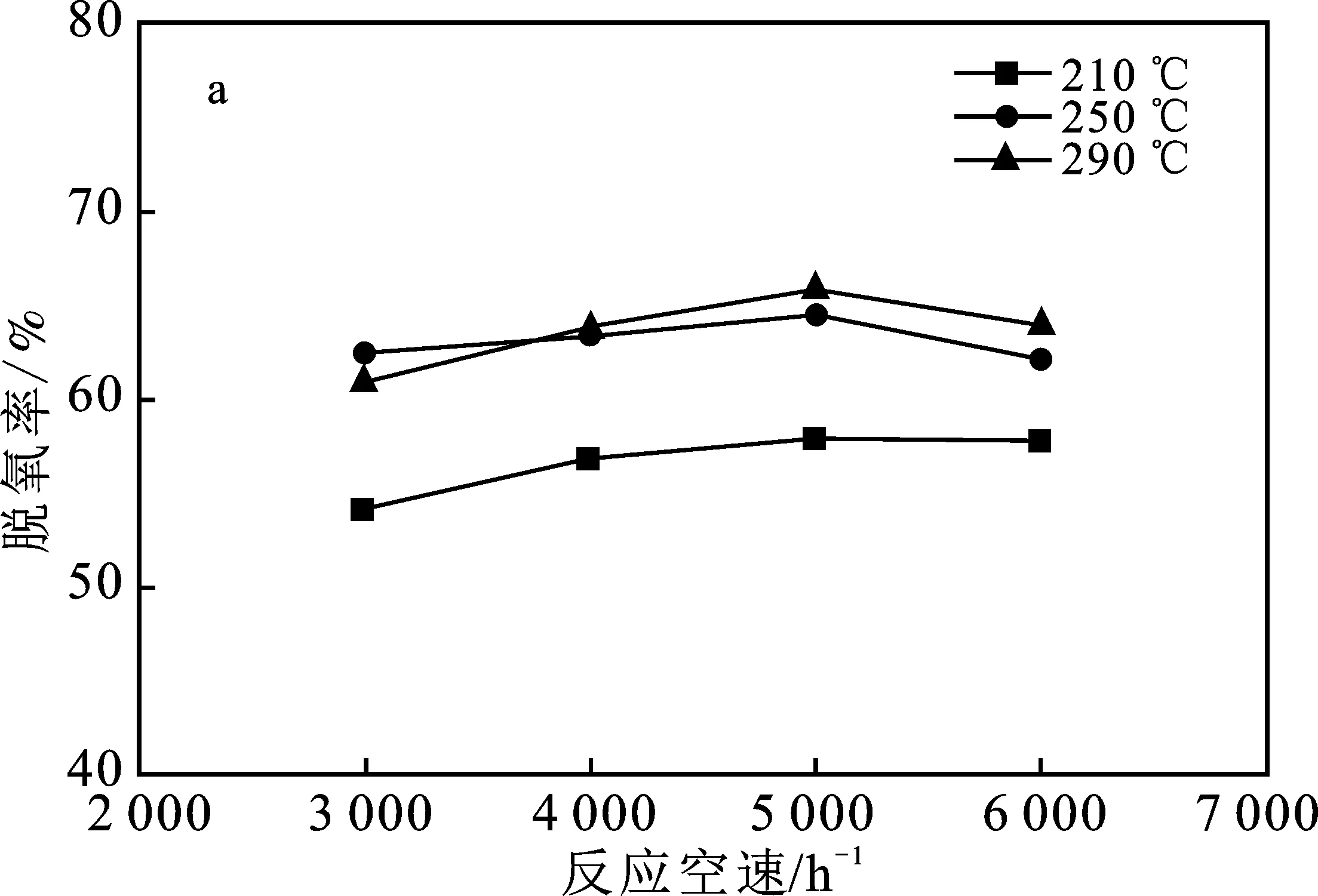

圖9 空速對催化劑活性的影響Fig.9 Effect of space velocity on catalyst activitya.脫氧活性;b.變換活性
由圖9可知,在空速低于5 000 h-1時,提高空速,催化劑的脫氧活性增大。在此范圍內提高空速有助于擴散阻力的消除,從而提高脫氧活性。但是提高空速的同時,催化劑的變換活性下降,這是因為提高空速,催化劑床層中反應氣的停留時間變短,并且本實驗只使用了1 mL的催化劑,在反應器中能轉化的CO氣體隨著空速的增加減少,導致催化劑變換活性降低。
3.4 干濕氣反應活性對比



圖10 干濕氣反應對催化劑活性的影響Fig.10 Effect of dry and wet reaction on catalyst activitya.脫氧活性;b.變換活性
3.5 催化劑熱穩定性探究
正常測試不同溫度下催化劑的脫氧活性之后,切斷原料氣,通入高純氮氣,提升反應器溫度至500 ℃,在此條件下熱沖擊5 h。再將催化劑重新硫化,測試不同溫度下的催化劑活性,結果見圖11。

圖11 催化劑熱穩定性比較Fig.11 Comparison of catalyst thermal stability
由圖11可知,催化劑經長時間熱沖擊后,脫氧活性變化不大,說明此催化劑具有較好的熱穩定性。
4 結論
(1)載體加Ti改性有助于提升催化劑脫氧活性,當含量在15%的時候,活性最高,載體強度穩定性最好。且Ti的加入影響載體的強度、吸水率和活性組分Mo的分布從而影響催化劑活性,且TiO2含量影響催化劑物相的形成。
(2)焙燒溫度越高鎂鋁尖晶石晶型越多,TiO2晶型越穩定。
(3)對比Ce、Fe、Ni3種活性助劑對脫氧活性的影響,加入Ni的催化作用較好,其中NiO含量在0.2%時,能夠保持較高的脫氧活性。
(4)助劑K的加入大大提高了脫氧活性,當 K2O 的含量在9%時,表現出較高脫氧活性和變換活性。
(5)硫化過程中使用干氣比濕氣硫化效果好,且經過2 h,催化劑硫化度達到穩定,在5 000 h-1空速以內,提高空速有助于脫氧活性提升,干氣脫氧效果比濕氣脫氧好,濕氣條件有助于催化劑變換作用,催化劑具有較好的熱穩定性。

