一測多評法同時測定表虛感冒顆粒中9 種成分
何 敏,陳瀟瀟,陳 燕*,李佳佳
(1.東南大學附屬中大醫院藥學部,江蘇 南京 210009;2.中國藥科大學藥學院,江蘇 南京 210009)
表虛感冒顆粒由桂枝、白芍、葛根、炒苦杏仁、生姜、大棗6 味藥材組成,可用于發熱惡風、有汗、頭痛項強、咳嗽痰白、鼻鳴干嘔、苔薄白、脈浮緩等感冒風寒表虛證的治療[1],該制劑收載于2015 年版《中國藥典》 一部[1],但僅以臣藥白芍所含芍藥苷為檢測指標,而文獻[2-4]也僅對其單一成分進行定量分析。中藥及其制劑有效成分繁多復雜,藥理作用相輔相承,單一成分難以有效控制其質量穩定性和療效一致性,故多指標成分測定已成為相關質量評價的發展趨勢。
按照中藥質量標志物確認原則[5],本實驗選取質量穩定、價廉易得的葛根素作為內標,采用一測多評法同時測定表虛感冒顆粒中君藥桂枝主要藥效成分肉桂酸、桂皮醛,臣藥白芍主要活性成分氧化芍藥苷、芍藥內酯苷、芍藥苷,佐藥葛根特征性成分3′-羥基葛根素、葛根素、3′-甲氧基葛根素、染料木苷的含有量,以期建立該制劑多指標成分質量控制模式,并為提高相關質量標準提供參考。
1 材料
1.1 儀器 Waters 2695 型高效液相色譜儀(美國沃特斯公司);Agilent 1200 型高效液相色譜儀(美國安捷倫公司);FA2004 型電子天平(德國賽多利斯公司);SB25-12DT 型超聲波清洗機(寧波新芝生物科技股份有限公司)。
1.2 試劑與藥物 染料木苷 (批號111709-201702,純度99.9%)、肉桂酸 (批號110786-201604,純度98.8%)、桂皮醛 (批號110710-201821,純度99.6%)、芍藥苷 (批號110736-201943,純度95.1%)、葛根素 (批號110752-201816,純度95.4%) 對照品均購于中國食品藥品檢定研究院;氧化芍藥苷(批號18031641,純度98.8%)、芍藥內酯苷(批號18040323,純度98.5%)、3′-羥基葛根素 (批號17051825,純度100.0%)、3′-甲氧基葛根素(批號17032021,純度99.7%) 對照品均購于上海同田生物技術股份有限公司。表虛感冒顆粒 (每袋裝10 g,批號20190142、20190602、20200102) 來源于遼寧華潤本溪三藥有限公司。乙腈為色譜純(德國Merck公司);其余試劑均為分析純。
2 方法與結果
2.1 色譜條件 Agilent ZORBAX SB-C18色譜柱(250 mm×4.6 mm,5 μm);流動相乙腈(A) -0.1%甲酸(B),梯度洗脫(0~9.0 min,15.0%A;9.0~20.0 min,15.0%~23.0% A;20.0~35.0 min,23.0%~34.0% A;35.0~45.0 min,34.0%~40.0% A;45.0~50.0 min,40.0%~15.0%A);體積流量0.9 mL/min;柱溫25 ℃;檢測波長230 nm (0~20.0 min,氧化芍藥苷、芍藥內酯苷、芍藥苷)[6-7]、250 nm (20.0~35.0 min,3′-羥基葛根素、葛根素、3′-甲氧基葛根素、染料木苷)[8-10]、280 nm (35.0~50.0 min,肉桂酸、桂皮醛)[11];進樣量10 μL。
2.2 對照品溶液制備 精密稱取氧化芍藥苷、芍藥內酯苷、芍藥苷、3′-羥基葛根素、葛根素、3′-甲氧基葛根素、染料木苷、肉桂酸、桂皮醛對照品適量,50% 乙醇制成質量濃度分別為0.408、1.712、2.998、1.214、3.856、0.992、0.218、0.172、1.954 mg/mL 的貯備液,分別精密吸取1.0 mL,50%乙醇定容至20 mL,即得(各成分質量濃度分別為20.4、85.6、149.9、60.7、192.8、49.6、10.9、8.6、97.7 μg/mL)。
2.3 供試品溶液制備 取顆粒適量,研細,取粉末約2.0 g,精密稱定,精密加入50%乙醇25 mL,稱定質量,超聲處理30 min,放冷,50%乙醇補足減失的質量,搖勻,濾過,即得。
2.4 陰性樣品溶液制備 按照顆粒制備工藝和處方比例,分別制備缺白芍、缺葛根、缺桂枝的陰性樣品,按“2.3” 項下方法制備,即得。
2.5 專屬性試驗 取對照品、供試品、陰性樣品溶液各10 μL,在“2.1” 項色譜條件下進樣測定,結果見圖1。由此可知,各成分色譜峰峰形對稱,分離度均大于1.5,理論塔板數按各成分計均不小于4 500,陰性無干擾,表明該方法專屬性良好。
2.6 線性關系考察 精密吸取“2.2” 項下貯備液0.1、0.2、0.5、1.0、1.5、2.0 mL,50% 乙醇定容至20 mL,制成對照品溶液Ⅰ~Ⅵ,在“2.1”項色譜條件下進樣測定。以溶液質量濃度為橫坐標(X),峰面積為縱坐標(Y) 進行回歸,結果見表1,可知各成分在各自范圍內線性關系良好。
2.7 精密度試驗 取“2.2” 項下對照品溶液,在“2.1” 項色譜條件下進樣測定6 次,測得氧化芍藥苷、芍藥內酯苷、芍藥苷、3′-羥基葛根素、葛根素、3′-甲氧基葛根素、染料木苷、肉桂酸、桂皮醛峰面積RSD 分別為1.05%、0.91%、0.61%、0.96%、0.57%、1.01%、1.10%、1.23%、0.68%,表明儀器精密度良好。
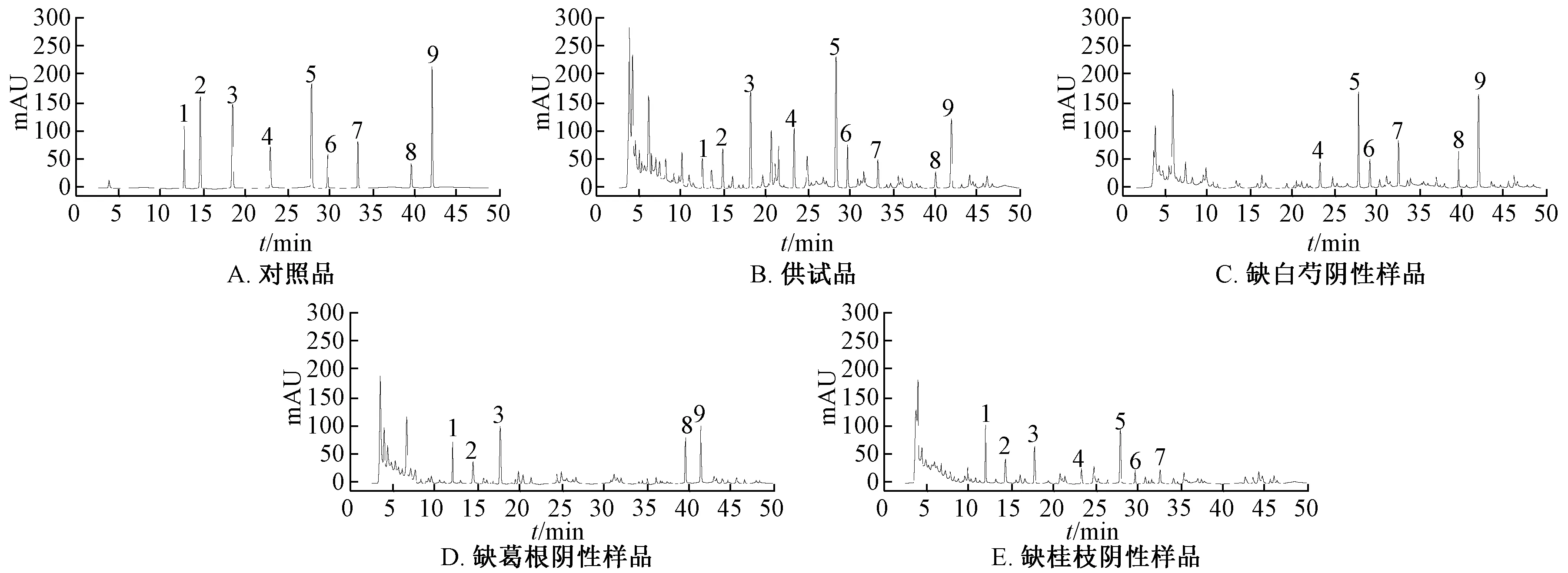
圖1 各成分HPLC 色譜圖Fig.1 HPLC chromatograms of various constituents
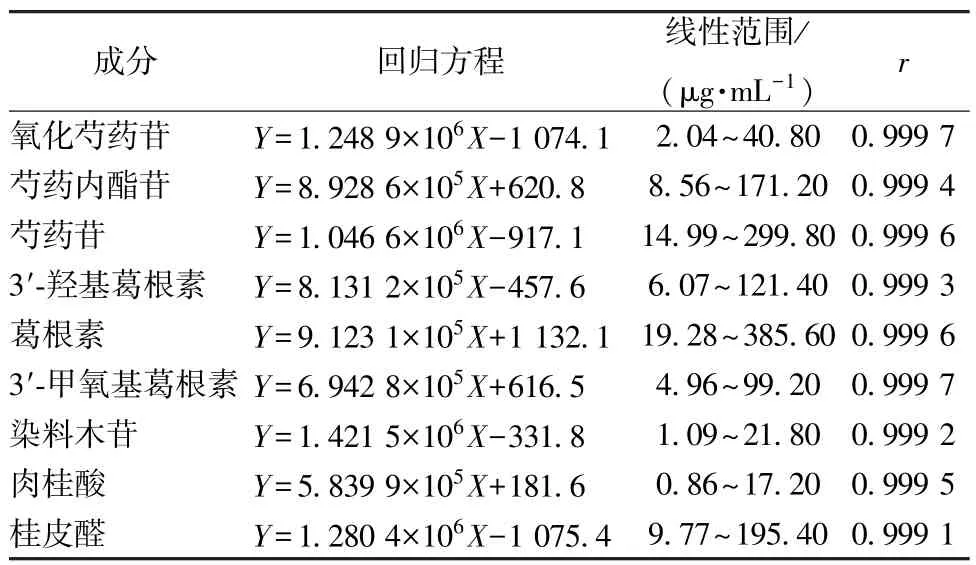
表1 各成分線性關系Tab.1 Linear relationships of various constituents
2.8 穩定性試驗 取同一份供試品溶液,分別于0、2、4、6、12、24 h 在“2.1” 項色譜條件下進樣測定,測得氧化芍藥苷、芍藥內酯苷、芍藥苷、3′-羥基葛根素、葛根素、3′-甲氧基葛根素、染料木苷、肉桂酸、桂皮醛峰面積RSD 分別為1.01%、0.92%、0.58%、0.99%、0.63%、0.98%、1.07%、1.25%、0.71%,表明溶液在24 h 內穩定性良好。
2.9 重復性試驗 取同一批顆粒,按“2.3” 項下方法平行制備6 份供試品溶液,在“2.1” 項色譜條件下進樣測定,測得氧化芍藥苷、芍藥內酯苷、芍藥苷、3′-羥基葛根素、葛根素、3′-甲氧基葛根素、染料木苷、肉桂酸、桂皮醛含有量RSD分別為1.34%、1.27%、0.95%、1.25%、0.84%、1.52%、1.78%、1.86%、0.99%,表明該方法重復性良好。
2.10 加樣回收率試驗 取各成分含有量已知的同一批顆粒9 份,研細,每份取約1.0 g,精密稱定,按照2020 年版《中國藥典》 四部要求精密加入對照品溶液 (各成分質量濃度分別為氧化芍藥苷0.212 mg/mL、芍藥內酯苷0.976 mg/mL、芍藥苷2.154 mg/mL、3′-羥基葛根素0.816 mg/mL、葛根素2.852 mg/mL、3′-甲氧基葛根素0.718 mg/mL、染料木苷0.126 mg/mL、肉桂酸0.094 mg/mL、桂皮醛1.142 mg/mL) 0.5、1.0、1.5 mL 各3 份,按“2.3” 項下方法制備供試品溶液,在“2.1”項色譜條件下進樣測定,計算回收率。結果,氧化芍藥苷、芍藥內酯苷、芍藥苷、3′-羥基葛根素、葛根素、3′-甲氧基葛根素、染料木苷、肉桂酸、桂皮醛平均加樣回收率(RSD) 分別為98.39%(1.20%)、100.01% (0.81%)、99.56% (0.78%)、99.73% (1.02%)、100.08% (0.75%)、97.99%(1.39%)、97.62% (1.54%)、96.98% (1.13%)、98.97% (0.95%)。
2.11 相對校正因子測定 精密吸取“2.6” 項下對照品溶液Ⅰ~Ⅵ,在“2.1” 項色譜條件下進樣測定,以葛根素為內標,計算其他8 種成分的相對校正因子fk/s,公式為fk/s= fk/fs=(CkAs)/(CsAk),其中Ck為其他成分含有量,Ak為其他成分峰面積,Cs為內標含有量,As為內標峰面積,結果見表2。
2.12 耐用性試驗
2.12.1 儀器、色譜柱 精密吸取“2.2” 項下對照品溶液,在“2.1” 項色譜條件下進樣測定,考察Waters 2695、Agilent 1200 型色譜儀及Agilent ZORBAX SB-C18、Topsil C18、Thermo Hypersil Gold C18色譜柱(250 mm×4.6 mm,5 μm) 對相對校正因子的影響,結果見表3,可知均無明顯影響(RSD<5%)。
2.12.2 柱溫 精密吸取“2.2” 項下對照品溶液,在“2.1” 項色譜條件下進樣測定,考察柱溫23、24、25、26、27 ℃對相對校正因子的影響,結果見表4,可知均無明顯影響(RSD<5%)。
2.12.3 體積流量 精密吸取“2.2” 項下對照品溶液,在“2.1” 項色譜條件下進樣測定,考察體積流量0.7、0.8、0.9、1.0、1.1 mL/min 對相對校正因子的影響,結果見表5,可知均無明顯影響(RSD<5%)。
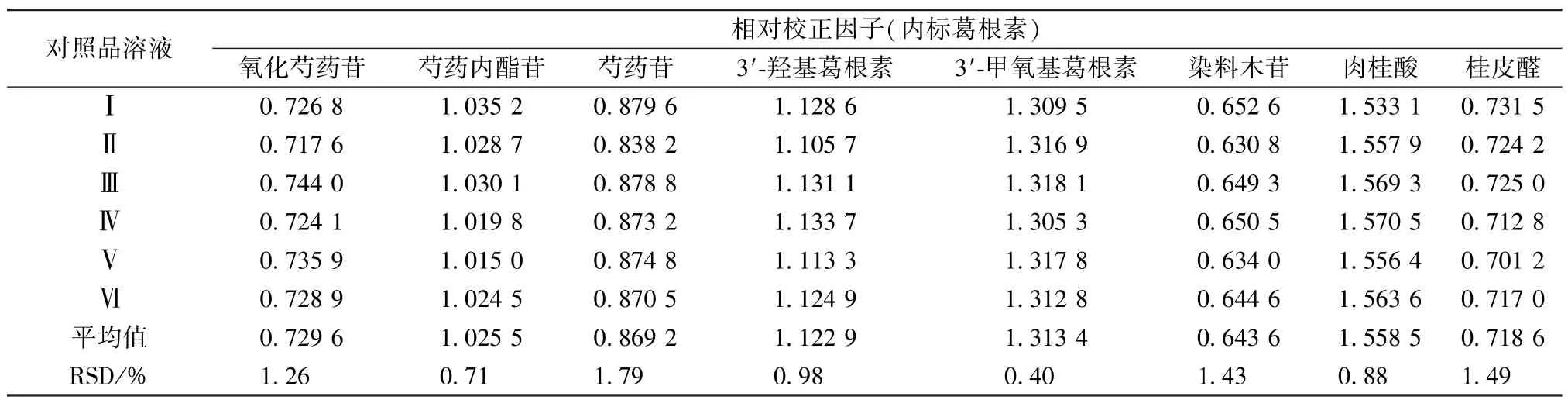
表2 各成分相對校正因子Tab.2 Relative correction factors of various constituents
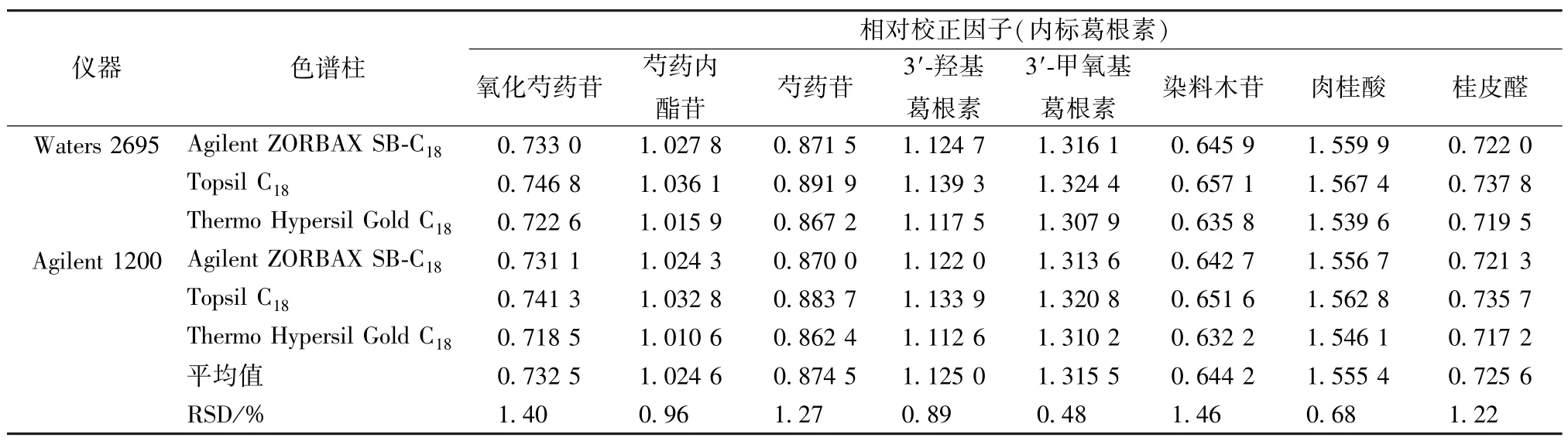
表3 不同儀器、色譜柱對相對校正因子的影響Tab.3 Effects of different instruments and columns on relative correction factors
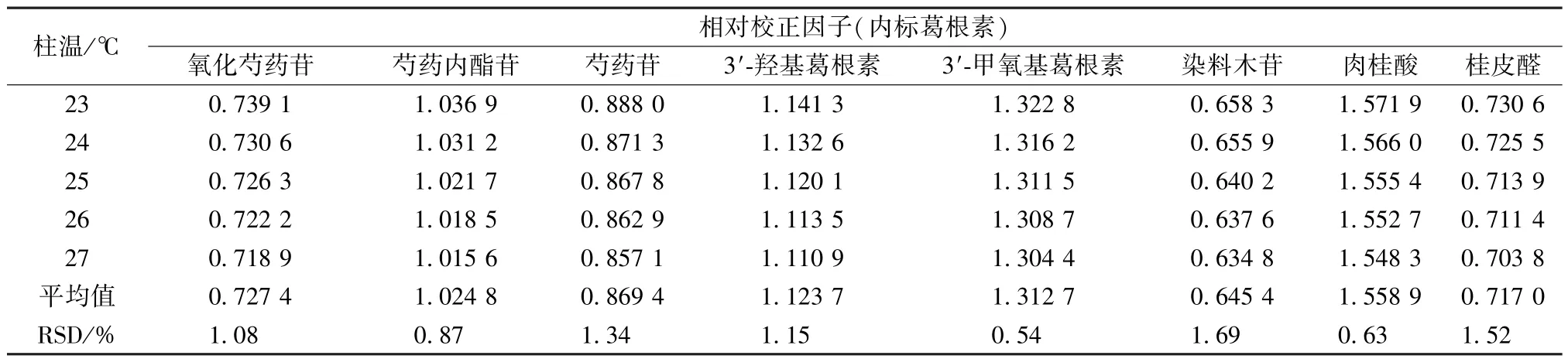
表4 不同柱溫對相對校正因子的影響Tab.4 Effects of different column temperatures on relative correction factors
2.13 色譜峰定位 精密吸取“2.2” 項下對照品溶液,在“2.1” 項色譜條件下進樣測定,考察“2.12.1” 項下儀器、色譜柱對相對保留時間的影響,結果見表6,可知均無明顯影響(RSD<5%)。
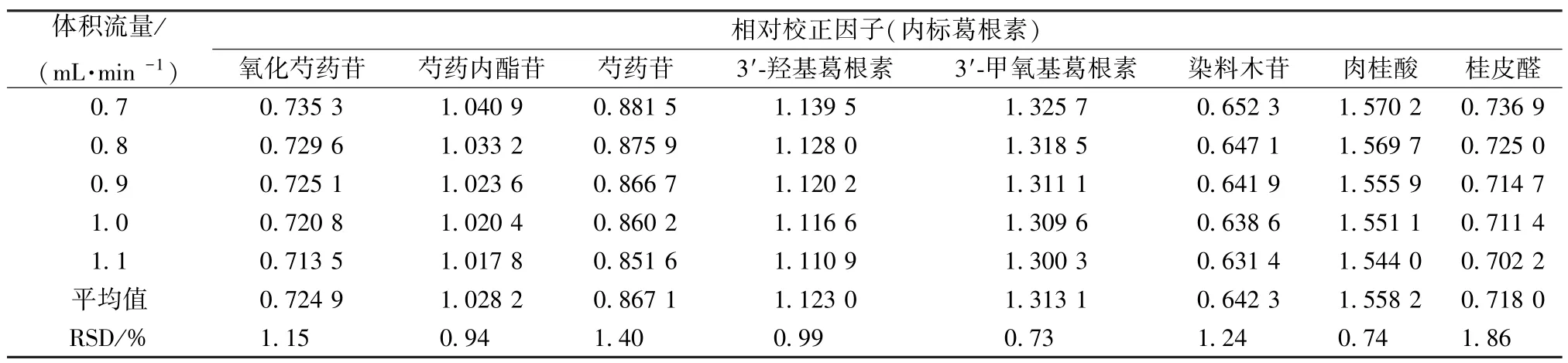
表5 不同體積流量對相對校正因子的影響Tab.5 Effects of different volumetric flow rates on relative correction factors
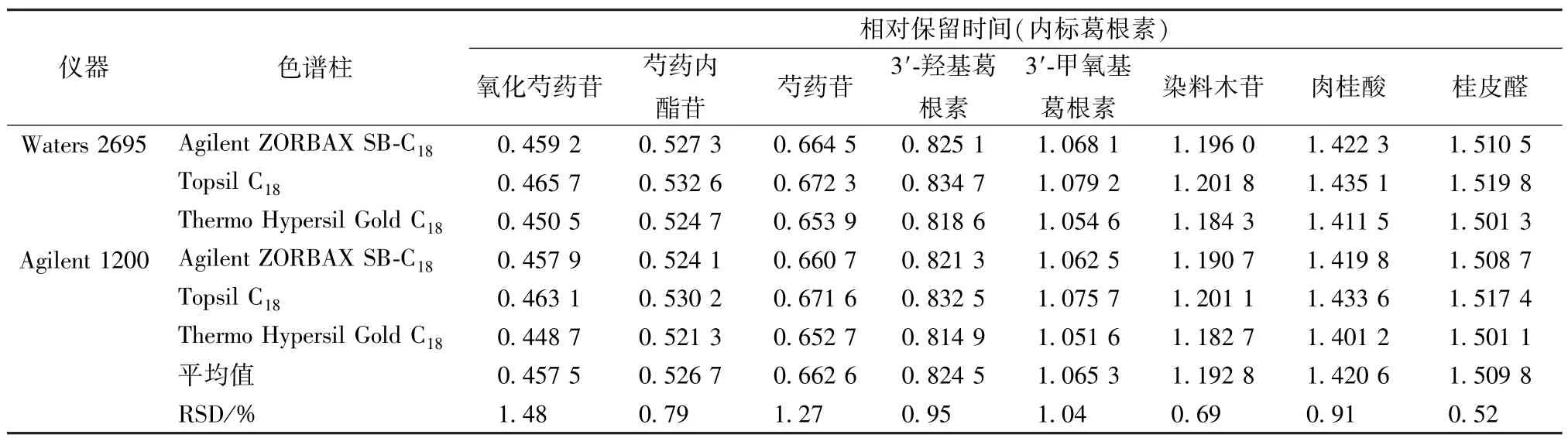
表6 不同儀器、色譜柱對相對保留時間的影響Tab.6 Effects of different instruments and columns on relative retention time
2.14 樣品含有量測定 取3 批顆粒,按“2.3”項下方法制備供試品溶液,每批3 份,在“2.1”項色譜條件下進樣測定,分別采用外標法和一測多評法計算含有量,結果見表7,可知2 種方法所得結果無明顯差異[相對平均偏差(RAD) <5.0%]。
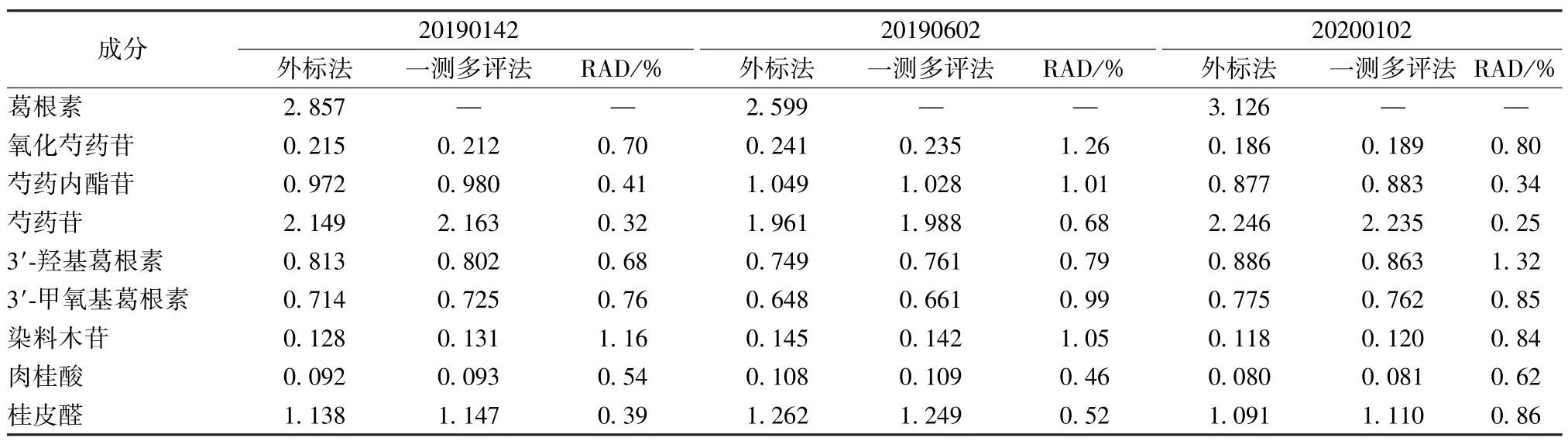
表7 各成分含有量測定結果(mg/g)Tab.7 Results of content determination of various components (mg/g)
3 討論
3.1 指標成分選擇 表虛感冒顆粒中桂枝發汗解肌,助陽化氣[12],為君藥;白芍養血調經,斂陰止汗,為臣藥;葛根解肌退熱,炒苦杏仁降氣止咳平喘,合為佐藥;大棗益氣和中,生姜發汗解表,引藥入肺,合為使藥,諸藥合用,共奏散風解肌、和營退熱之功效。肉桂酸、桂皮醛等揮發油為桂枝主要藥效成分,芍藥苷、氧化芍藥苷、芍藥內酯苷等單萜為白芍主要活性成分,3′-羥基葛根素、葛根素、3′-甲氧基葛根素、染料木苷等異黃酮為葛根主要特征成分。因此,本實驗按照中藥質量標志物確認原則,選取上述化合物作為指標成分,可更全面地評價表虛感冒顆粒整體質量。
3.2 供試品溶液制備方法選擇 本實驗首先考察了提取溶劑 (甲醇[13]、30% 乙醇[8]、50% 乙醇[6-7]、70%乙醇[9,14]),發現50%乙醇提取時各成分綜合提取率最佳。再考察了提取方式 (超聲[6-7,14]、加熱回流[8-9])、提取時間 (15、30、60 min),發現超聲提取30 min 時各成分均能提取完全,可能與表虛感冒顆粒中6 味藥材均經水煎煮后入藥有關。
3.3 含有量分析 表7 顯示,不同批次樣品之間各成分含有量存在一定差異,以氧化芍藥苷、染料木苷、肉桂酸更明顯,可能與原藥材、產地、采收季節差異及生產過程中控制參數等有關。因此,建議藥品生產企業和監管部門進一步完善表虛感冒顆粒質量控制標準,對原藥材來源和制劑生產過程加以控制,以確保該制劑質量穩定性和療效一致性。
4 結論
本實驗采用一測多評法同時測定表虛感冒顆粒中氧化芍藥苷、芍藥內酯苷、芍藥苷、3′-羥基葛根素、葛根素、3′-甲氧基葛根素、染料木苷、肉桂酸和桂皮醛的含有量,該方法簡便準確,可為全面評價該制劑質量提供有力依據。

