不同骨水泥注入量下PKP治療T12椎體壓縮性骨折的療效與有限元分析
李石頭,鮮文峰
(河南省南陽市第二人民醫院骨一科,河南南陽 473000)
近年來,隨著影像設備及醫務人員技術的不斷提高,經皮椎體后凸成形術(percutaneous kyphoplasty,PKP)治療胸腰椎壓縮性骨折成為主流的治療方案[1-2]。本研究主要探討PKP術中骨水泥注入量與療效的相關性,同時利用有限元分析技術評價骨水泥注入量與不同運動強度下的上下終板受力的關系。
1 資料與方法
1.1 一般資料
納入標準:① X線、CT及MRI證實T12骨質疏松性椎體壓縮性骨折;②骨折時間小于3周;③無腫瘤病史且影像學檢查未見轉移瘤征象;④CT確認椎體后壁完整且椎弓根完整;⑤椎體壓縮程度在2/3之內。排除標準:①脊柱具有先天性畸形,不利于形態學評估者;②椎體感染;③中途退出研究或隨訪時間不足6個月者。
共110例T12骨質疏松性椎體壓縮性骨折患者納入研究范圍。根據術中骨水泥注入量分為A(<4 mL)、B(≥4 mL)兩組。其中A組60例,男35例,女25例;年齡52~89歲,平均(68.3±12.8)歲,骨水泥注入量(3.5±0.4)mL;B組50例,男28例,女22例;年齡53~87歲,平均(69.8±11.1)歲,骨水泥注入量(4.6±0.5)mL。兩組患者基本情況一致,有可比性。
1.2 手術方法
患者取俯臥位,C臂透視定位目標椎體、標記位置。行1%鹽酸利多卡因注射液局部浸潤麻醉。于傷椎椎弓根外上緣穿刺進針,針尾保持適當外展及頭傾。穿刺過程中確保穿刺針朝向傷椎中部,同時行患椎正側位透視,直至穿刺針安全通過椎弓根進入椎體中柱前緣。拔出穿刺針芯,更換工作套管,將鉆頭手動旋轉至椎體前中1/3。將球囊經工作套管放置于椎體內,C臂透視下緩慢擴張球囊直至椎體恢復滿意高度,退出球囊。調和骨水泥,待拉絲后注入椎體內。
術后常規應用抗生素2 d,正規抗骨質疏松治療(包括口服碳酸鈣D3、骨化三醇,靜脈輸注唑來膦酸注射液)。所有患者術后第2天鼓勵佩戴胸腰椎支具下地行功能鍛煉。
1.3 觀察指標
記錄術中骨水泥輸入量,觀察患者術前、術后72 h、術后6個月VAS評分、椎體前緣高度、椎體中間高度與Cobb角。
1.4 統計學分析
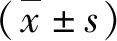
2 有限元分析
納入健康志愿者1名,男性,29歲,體重為70 kg。排除髖關節畸形、腫瘤及骨病等異常情況。對志愿者進行胸腰椎CT掃描,DICOM數據存于光盤待用。本研究涉及軟件包括醫學圖像處理軟件Mimics、有限元模型前體處理軟件Hypermesh、有限元處理軟件Abaqus及建模軟件Solidworks。
2.1 實驗步驟
骨性輪廓及內固定器械建模:將胸腰椎CT的DICOM數據導入醫學處理軟件Mimics中,根據CT閾值對髖部的骨性結構進行自動識別,實驗者使用閾值選取、區域增長、手動填充及擦除、布爾運算等方法繪制胸腰椎骨性輪廓。同時利用建模軟件Solidworks繪制骨水泥塊,根據本研究團隊臨床經驗以及納入患者的分組標準(A組<4 mL、B組≥4 mL)進行模擬,決定繪制3.5 mL及4.5 mL骨水泥塊,置于T12椎體中部,將所有模型保存備用。
材料賦值、邊界約束及載荷施加[3]:將胸腰椎骨性模型及骨水泥塊模型導入HyperMesh軟件,在該軟件中建立materials及properties,其中前縱韌帶、后縱韌帶、黃韌帶、棘間韌帶、棘上韌帶及橫韌帶等材料屬性見表1。脊柱模型遠端設定為無移動、無旋轉,以模擬患者站立位時的穩定狀態。根據Orthoload數據庫(https://orthoload.com)資料,該數據庫由Julius Wolff研究所研發,科研人員將力學測量裝置植入人工椎體內部,經過安全評估后經過手術植入人體,測量站立位、行走及各運動狀態下椎體受力情況,其認為標準體重66 kg且站立位時椎體受力474 N。本研究中受試者體重70 kg,按照比例將載荷設定為500 N。

表1 模型的材料屬性
2.2 有限元結果分析
分析相同運動狀態情況下,高、低骨水泥注入量條件下的T12椎體上下終板受力情況。
3 結果
3.1 高、低骨水泥注入量與療效的關系
術前、術后72 h、術后6個月時,兩組患者在椎體前緣高度、椎體中緣高度、Cobb角恢復方面,組間比較差異均無統計學意義(P>0.05)。兩組患者術后72 h、術后6個月VAS評分較術前均明顯改善(P<0.05);術前、術后72 h,VAS評分的組間差異無統計學意義(P>0.05),術后6個月時,B組VAS評分明顯高于A組(P<0.05),見表2。

表2 高、低骨水泥注入患者療效對標情況
3.2 高、低骨水泥注入量條件下上下終板受力情況
相同軸向載荷作用下,高骨水泥注入量模型A的應力云圖顯示,上下終板均有明顯應力集中現象,經測定上、下終板最大米塞斯應力值分別為309 MPa和263 MPa。相比較,低骨水泥注入量模型B在相同條件下應力分布相對均勻、并無異常應力集中現象。上、下終板最大米塞斯應力值分別為99 MPa和67 MPa。
4 討論
4.1 骨水泥注入量與療效的相關性
骨質疏松性椎體壓縮骨折是困擾老年人的常見疾病,保守治療需長期臥床,容易引起墜積性肺炎、壓瘡等并發癥。傳統開放性手術恢復慢、創傷大[4]。PKP手術切口小、允許早期下地功能鍛煉、止痛效果佳,已成為公認的首選治療方案[5]。
目前PKP術中最優骨水泥注入量尚未形成共識。Lu等[6]提出骨水泥注入量與PKP術后患者的疼痛緩解程度并無明顯關聯。有學者指出,疼痛多由于骨折椎體形態變化刺激疼痛感受器及肌肉受力異常所致,術中骨水泥釋放的熱量可對椎體內部疼痛感受器予以破壞,他們推測骨水泥注入量與疼痛緩解程度并無直接關聯[7]。本研究顯示,術后6個月的隨訪過程中,高骨水泥注入量患者VAS評分明顯高于低注入量組,與上述學者的研究結果差別較大。深究其原因,主要為胸腰椎為脊柱形態與力學交界處,尤其是骨質疏松性椎體壓縮性骨折的椎體多為楔形變,當患者進行功能鍛煉時,脊柱后凸畸形可引起椎體后方韌帶及椎旁肌肉痙攣、緊張,從而引起疼痛。PKP術中經球囊擴張,可有效恢復椎體前、中緣椎體高度,糾正Cobb角畸形,從而緩解軟組織緊張,據此可有效解釋術后72 h和術后6個月疼痛評分較術前均有明顯緩解。但是骨水泥高注入量患者術后椎體強度明顯增強,導致局部應力集中增加,遠期甚至可造成鄰近椎體退變加速,因此骨水泥高注入量患者VAS評分高于低注入量組。
4.2 骨水泥注入量與椎體強度的關系
多數學者認為PKP能夠恢復椎體的力學性能,但是對骨水泥的注入量仍有爭議,適量的骨水泥能夠避免椎體再骨折,但是過量注入會使得椎體強度過高,加速鄰近椎體病變,因此骨水泥注入量對病變椎體生物力學性能的作用始終是研究熱點[7]。Wang等[8]通過脊柱標本力學實驗證實,PKP術后鄰近椎體的極限強度下降約20%,外力作用下,鄰近椎體再次發生壓縮性骨折的概率明顯增加。Li等[9]指出,PKP術中不應過分強調骨水泥的充分彌散,只需達到病變椎體體積的14%即可達到止痛及恢復椎體力學性能的要求。
本研究通過有限元分析證實,隨著骨水泥注入量的增加,病變椎體上下終板的異常應力集中點明顯增加,經測定上、下終板最大米塞斯應力值分別為309 MPa和263 MPa。與低注入量患者相比,最大米塞斯應力超出300%。同時,低注入量椎體上下終板的應力分布相對均勻,可以推測低注入量的生物力學性能更佳。唐勇濤等[10]同樣利用有限元技術發現,PKP術中只需少量的骨水泥即可影響椎體的抵抗軸向壓縮的能力,如果過高的骨水泥注入量會導致椎體彈性勢能下降,過量的載荷沿脊柱縱軸完全傳遞,使得鄰近椎體的載荷分布改變,嚴重者會引起二次骨折,與本研究的結果基本吻合。
本研究同樣具備幾點不足:①研究中力學加載工況設定為靜態加載,與真實生活中日常動作往往具有動態屬性的情況存在一定差距。②研究中力學模擬僅進行單次加載,尚未進行疲勞試驗,無法對脊柱-骨水泥裝配體的遠期力學情況進行預測。③本研究為單中心研究,納入患者僅為同地區骨質疏松性胸腰椎壓縮性骨折患者,普遍性較差。今后將納入多中心數據,進一步挖掘并分析PKP的臨床療效。
綜上所述,PKP治療胸腰椎壓縮性骨折可有效緩解疼痛、恢復脊柱形態,但是骨水泥注入量與療效無明顯相關性。增加骨水泥注入量會導致椎體出現應力集中現象,從而加速椎體退變。

