參麥注射液對惡性腫瘤化療患者微循環及白細胞水平的影響
郝晶 孫岸弢 趙偉 杜福泉 高明潔

摘要?目的:探討參麥注射液對惡性腫瘤化療患者微循環及白細胞水平的影響。方法:選取2016年2月至2017年1月黑龍江中醫藥大學附屬第一醫院收治的惡性腫瘤患者61例作為研究對象,按照隨機數字表法隨機分為對照組(n=30)和觀察組(n=31)。對照組接受常規化療,觀察組在對照組基礎上給予參麥注射液進行治療。檢測2組化療前后全血T淋巴細胞亞群、血液流變學、微循環狀態及白細胞水平,統計2組化療后緩解率。結果:化療4個周期后,對照組全血CD3+、CD4+、NK及觀察組CD8+較化療前降低,且觀察組全血CD8+低于對照組(P<0.01);觀察組全血CD3+、CD4+、NK及CD4+/CD8+較化療前升高,且觀察組高于對照組(P<0.01);2組全血血漿黏度、血沉、纖維蛋白原、紅細胞壓積及形態、管周狀態、流態、綜合積分較化療前降低,且觀察組低于對照組(P<0.01)。化療1~4周期后,對照組全血白細胞計數較化療前逐漸降低,觀察組較化療前先降低后升高,且化療4個周期后觀察組高于對照組(P<0.01)。化療4個周期后,觀察組ORR高于對照組(64.52% vs 33.33%,P<0.05)。結論:參麥注射液可改善惡性腫瘤化療患者微循環狀態,并能抑制化療所致的白細胞減少。
關鍵詞?惡性腫瘤;化學療法;參麥注射液;微循環;免疫;血液流變學;白細胞水平
Abstract?Objective:To explore the effects of Shenmai Injection on microcirculation and leukocyte levels of patients with malignant tumor receiving chemotherapy. Methods:A total of 61 patients with malignant tumor admitted to First Affiliated Hospital, Heilongjiang University of Chinese Medicine were selected as the research objects and were randomly divided into a control group (n=30) and an observation group (n=31) according to random number table method. The control group received conventional chemotherapy, and the observation group was treated with Shenmai Injection on the basis of the control group. The whole blood T-lymphocyte subsets, hemorheology, microcirculation status and leukocyte levels in 2 groups of patients were detected before and after chemotherapy, and the remission rate in 2 groups were statistically analyzed after chemotherapy. Results:The whole blood CD3+, CD4+ and NK proportion in control group and CD8+ proportion in observation group after 4 cycles of chemotherapy were lower than those before chemotherapy (P<0.01), the whole blood CD8+ proportion in observation group was lower than that in control group (P<0.01); the whole blood CD3+, CD4+, NK proportion and CD4+/CD8+ in observation group were higher than those before chemotherapy, and observation group were higher than control group (P<0.01); the whole blood plasma viscosity, erythrocyte sedimentation rate, fibrinogen, hematocrit and morphology, peritubular state, fluid state, and comprehensive integral in the 2 groups were lower than those before chemotherapy, and the observation group were lower than the control group (P<0.01). After 1~4 cycles of chemotherapy, the total white blood cell count of the control group gradually decreased compared with that before chemotherapy, and the observation group first decreased and then increased. The observation group was lower than before chemotherapy and then increased, and the observation group was higher than the control group after 4 cycles of chemotherapy (P<0.01). After 4 cycles of chemotherapy, the ORR of the observation group was higher than that of the control group (64.52% vs 33.33%, P<0.05). Conclusion:Shenmai Injection could improve microcirculation status of patients with malignant tumor receiving chemotherapy, and inhibit the reduction of leukocyte caused by chemotherapy.
Keywords?Malignant tumor; Chemotherapy; Shenmai Injection; Microcirculation; Immune; Hemorheology; Leukocyte levels
中圖分類號:R273文獻標識碼:Adoi:10.3969/j.issn.1673-7202.2020.21.017
惡性腫瘤患者普遍存在血液高黏、高凝、白細胞減少等情況,是威脅人類健康的重要疾病之一[1]。臨床治療方法主要有手術、放化療,其中化療是惡性腫瘤的重要治療方法,能夠延長患者生存時間,但化療過程中易產生多種并發癥,常見的有骨髓抑制、心臟毒性等,其延長了化療周期,對患者的生活質量及身體健康帶來嚴重危害[2-3]。參麥注射液能夠促進白細胞生成,抑制腫瘤生長,調節患者免疫功能,是一種能增強抗癌療效,并減少化療毒性的藥物[4-5]。因此本研究旨在探討惡性腫瘤患者在化療過程中使用參麥注射液的療效,以觀察其對患者微循環及白細胞水平的影響。
1?資料與方法
1.1?一般資料?選取2016年2月至2017年1月于黑龍江中醫藥大學附屬第一醫院就診的惡性腫瘤患者61例作為研究對象,按照隨機數字表法隨機分為對照組(n=30)和觀察組(n=31),對照組男18例,女12例;年齡36~76歲,平均年齡(53.64±6.04)歲;按國際抗癌聯盟(UICC)腫瘤分期標準:Ⅲ期13例,Ⅳ期17例;其中淋巴瘤8例,多發性骨髓瘤6例,急性白血病5例,骨髓增生異常綜合征-RAEB 11例。觀察組男20例,女11例;年齡40~78歲,平均年齡(54.28±6.25)歲;腫瘤分期:Ⅲ期15例,Ⅳ期16例;其中淋巴瘤5例,多發性骨髓瘤8例,急性白血病4例,骨髓增生異常綜合征-RAEB 14例。2組患者基線比較,差異無統計學意義(P>0.05),具有可比性。本研究經本院醫學倫理委員會審批后(倫理審批號:HL201756)。
1.2?診斷標準?西醫符合《中國常見惡性腫瘤診治規范》[6]中關于惡性腫瘤的相關診斷標準;中醫符合《中藥新藥臨床研究指導原則(試行)》[7]中的氣虛血瘀、氣陰兩虛等型。
1.3?納入標準?臨床分期為Ⅲ~Ⅳ期者;Karnofsky評分在60分以上者;預計生存期大于6個月者;經病理學或細胞學診斷為淋巴瘤、多發性骨髓瘤、急性白血病、骨髓增生異常綜合征-RAEB者;自愿參與本研究,且患者與家屬均對本研究知情并同意者。
1.4?排除標準?腫瘤診治經過記錄不清,資料不完整者;肝腎功能不全者;服用其他中藥,影響評價結果者;對本研究所用藥物過敏者;妊娠或哺乳期婦女;合并心腦血管、造血系統等原發性疾病者等。
1.5?脫落與剔除標準?正在參加其他藥物臨床實驗者;治療過程中病情驟然加重,或有嚴重不良反應及并發癥者;治療后失訪者等。
1.6?治療方法?2組均接受常規化療:霍奇金淋巴瘤:ABVD方案,多柔比星(汕頭經濟特區明治醫藥有限公司,國藥準字H44024477)25 mg/m2,博萊霉素(日本化藥株式會社,進口藥品注冊證號:20090885)10 mg/m2,長春堿(Maybe Pharma Pty Ltd,進口藥品注冊證號:H20050134)6 mg/m2,達卡巴嗪(上海瀚香生物科技有限公司,國藥準字H20044281)375 mg/m2,第1~15天;非霍奇金淋巴瘤:RCHOP方案,利妥昔單抗(上海羅氏制藥有限公司,國藥準字J20170034)375 mg/m2,環磷酰胺(江蘇盛迪醫藥有限公司,國藥準字H32020856)750 mg/m2,多柔比星(汕頭經濟特區明治醫藥有限公司,國藥準字H44024477)50 mg/m2,長春新堿(廣東嶺南制藥有限公司,國藥準字H20065057)1.4 mg/m2,第1天,潑尼松(天津力生制藥股份有限公司,國藥準字H12020123)100 mg/m2,第1~5天;多發性骨髓瘤:PAD方案,硼替佐米(齊魯制藥有限公司,國藥準字H20183102)1.3 mg/m2,第1、4、8天,多柔比星(汕頭經濟特區明治醫藥有限公司,國藥準字H44024477)9 mg/m2,第1~4天,地塞米松(廣東白云山天心制藥股份有限公司,國藥準字H44022090)30 mg/m2,第1~4天;急性髓系白血病:誘導化療DA方案:阿糖胞苷(輝瑞制藥有限公司,進口藥品注冊證號:H20160230)100 mg/m2,第1~7天,柔紅霉素(深圳萬樂藥業有限公司,國藥準字H44024361)45 mg/m2,第1~3天;骨髓增生異常綜合征-RAEB:地西他濱方案(江蘇豪森藥業集團有限公司,國藥準字H20130067)25 mg/m2,第1~5天。觀察組在常規化療基礎上靜脈滴注參麥注射液(正大青春寶藥業有限公司,國藥準字Z33020021)50 mL+5% 500 mL葡萄糖溶液,1次/d,21 d為1個周期,治療4個周期。
1.7?觀察指標?1)分別于化療前、化療4個周期后,采集2組靜脈血4 mL,1部分取全血,另1部分經抗凝處理后,3 500 r/min,離心半徑為13.50 cm,離心10 min取血漿,于-70 ℃保存備用。采用Beckman Couhere流式細胞儀檢測2組全血CD3+、CD4+、CD8+及NK細胞比例,并計算CD4+/CD8+。2)采用黏度計(北京普利生有限公司)檢測2組血漿纖維蛋白原水平、血漿紅細胞壓積、血漿黏度及血沉水平。3)采用WXH-7型微循環檢測分析系統,在18~25 ℃下對患者的左手無名指甲襞進行檢測,觀察血管形態、流態、管周等狀態,應用田氏加權積分法評價各項積分及綜合總分。4)采用Mindray BC-1800型全自動快速血球分析儀檢測2組全血白細胞計數。5)統計2組化療4個周期后臨床總緩解率(ORR)。
1.8?療效判定標準?評價療效參照WHO實體瘤療效標準[8],其中完全緩解(CR)為所有靶病灶消失,且≥1個月未復發;部分緩解(PR)為靶病灶最長經之和與基線狀態比較減少≥50%,且復發時間≥1個月;疾病穩定(SD)為靶病灶最長經之和與基線狀態比較減少<50%,或≥25%,且無新病灶出現;疾病發展(PD)為靶病灶最長經之和與基線狀態比較≥50%,或出現新病灶。
1.9?統計學方法?采用SPSS 21.0統計軟件進行數據分析,計數資料以百分比(%)表示,采用χ2檢驗;計量資料以(±s)表示,采用t檢驗,計量資料多組間比較采用F檢驗,以P<0.05為差異有統計學意義。
2?結果
2.1?2組細胞免疫狀態比較?化療4個周期后,對照組全血CD3+、CD4+、NK比例及觀察組CD8+比例較化療前降低(P<0.01),且觀察組全血CD8+比例低于對照組(P<0.01);化療4個周期后,觀察組全血CD3+、CD4+、NK比例及CD4+/CD8+較化療前升高(P<0.01),且觀察組高于對照組(P<0.01)。見表1。
2.2?2組血液流變學變化情況?化療4個周期后,2組全血血漿黏度、血沉、纖維蛋白原水平及紅細胞壓積較化療前均降低,且觀察組低于對照組(P<0.01)。見表2。
2.3?2組微循環功能改善情況比較?化療4個周期后,2組形態積分、管周狀態積分、流態積分、綜合積分較化療前降低(P<0.01),且觀察組低于對照組(P<0.01),見表3。
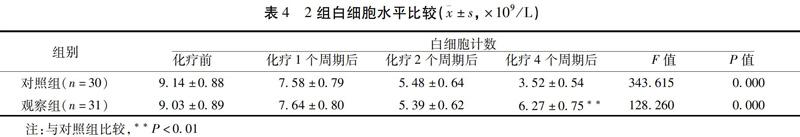
2.4?2組白細胞水平比較?化療1~4周期后,對照組全血白細胞計數較化療前逐漸降低(P<0.01),觀察組較化療前先降低后升高(P<0.01),且化療4個周期后,觀察組高于對照組(P<0.01)。見表4。
2.5?2組臨床療效比較?化療4個周期后觀察組CR 7例,PR 13例,SD 7例,PD 4例,ORR為64.52%(20/31);對照組CR 2例,PR 9例,SD 13例,PD 7例,ORR為33.33%(10/30),觀察組高于對照組(χ2=4.749,P=0.029)。
3?討論
致癌因子的積累、免疫力下降等多種因素均會引起惡性腫瘤產生,多數惡性腫瘤確診時已是晚期,其血液存在高凝、高黏等狀態,血液流變學也會存在異常,使患者失去手術機會[9]。通過化療可改善惡性腫瘤患者的臨床癥狀,延長其生存時間,但化療藥物不僅對腫瘤細胞有抑制、殺滅的作用,還會影響人體的正常細胞,使化療過程中出現貧血、白細胞減少、血小板減少等不良反應,進而損害機體的免疫功能,導致大多數患者不能耐受化療而影響治療效果,嚴重威脅患者的生命安全[10]。因此急需找到既可延長患者生存期,又能減輕化療不良反應的藥物及方法。
中醫學認為正氣不足為腫瘤形成的關鍵因素,《黃帝內經》曰:“邪之所湊,其氣必虛,正氣存內,邪不可干”,認為腫瘤的形成與正氣不足有關;《醫宗必讀》:“積之成也,正氣不足,而后邪氣距之”,認為正氣虛弱,外邪入侵而致氣血瘀滯,邪濁交結,最終發展為腫瘤。“正氣”是機體的抵抗力,“邪氣”即為腫瘤細胞,因此治療中應遵循“扶正為根本,祛邪為目的”的原則[11]。中醫可通過調理臟腑、補氣益血等方法祛除邪氣,增強機體免疫功能,進而控制腫瘤的復發,在改善患者生命質量、延長生存時間等方面有著重要意義[12]。參麥注射液是以《癥因脈治》中的生脈飲為基礎,由相同劑量的紅參和麥冬提純后混合而制成,其中補氣常用藥紅參有補脾益肺、生津安神、益氣攝血、補元氣等功效;補陰常用藥麥冬有清心除煩、養陰潤肺、益胃生津等功效,二者共奏養陰生津、益血安神、運脾化濕之功效。現代藥理研究表明,參麥注射的有效成為人參、麥冬皂甙及微量多糖,能夠使巨噬細胞炎性反應遞質胺釋放量降低,減輕對機體的損傷,增強機體體液免疫及細胞免疫應答,提高患者的抗腫瘤能力;此外,參麥注射液能刺激造血器官生成白細胞、血紅蛋白,預防化療所致骨髓抑制及白細胞減少[13-14]。本研究結果顯示,化療4個周期后,觀察組全血CD3+、CD4+、NK、CD4+/CD8+比例均高于對照組,而全血CD8+比例低于對照組;化療1~4周期后,對照組全血白細胞計數較化療前逐漸降低,觀察組較化療前先降低后升高,且化療4個周期后觀察組顯著高于對照組,提示參麥注射液可提高惡性腫瘤化療患者的免疫功能,抑制化療所致的白細胞減少。
有研究稱,惡性腫瘤患者伴有高黏滯血癥及血液流變學異常,高黏度血液有利于癌細胞著床,促進癌細胞生長和轉移,還可以導致微循環障礙,使血液流速緩慢,黏附于血管壁上極易形成癌栓;腫瘤細胞促進血小板在其表面聚集、變形,導致腫瘤細胞表面被掩蓋而不易被殺死[15]。因此治療惡性腫瘤的過程需要改善患者微循環狀態、降低血液黏度。現代藥理研究表明,人參多糖可抑制腫瘤細胞進入分裂期,抑制腫瘤的生長,人參皂苷可通過增加內皮活性物質釋放,抑制細胞黏附分子及細胞因子表達,進而增加血流量,降低血液黏稠度;麥冬多糖可明顯降低血液高切黏度、低切黏度、血漿黏度,改善血液流變學,麥冬皂苷可強心利尿、擴張血管,降低血液黏稠度,改善微循環,增加血液流動性[16]。本研究結果顯示,化療4個周期后,觀察組血漿黏度、血沉、纖維蛋白原水平、紅細胞壓積及形態、管周狀態、流態、綜合積分均低于對照組,而ORR明顯高于對照組,提示參麥注射液可改善惡性腫瘤化療患者微循環狀態,降低血液黏稠度,提高化療效果。
綜上所述,參麥注射液可改善惡性腫瘤化療患者微循環狀態,降低血液黏稠度,提高其免疫功能,抑制化療所致的白細胞減少,提高化療效果,值得臨床推廣應用。

