SM22α在腫瘤發(fā)生發(fā)展中作用的研究進(jìn)展
郭惠珊,宋楠,席豪,王榕,陳寧,呂品
1河北醫(yī)科大學(xué)醫(yī)學(xué)與健康研究院心血管醫(yī)學(xué)研究中心,石家莊050017;2河北醫(yī)科大學(xué)基礎(chǔ)醫(yī)學(xué)院細(xì)胞生物學(xué)教研室
平滑肌22 alpha蛋白(SM22α)又稱轉(zhuǎn)凝蛋白(transgelin),于1987年從雞胃平滑肌中分離得到,因其相對(duì)分子質(zhì)量為22 kD而得名,其cDNA和蛋白質(zhì)的一級(jí)結(jié)構(gòu)在進(jìn)化上高度保守。小鼠SM22α基因定位于9號(hào)染色體,全長(zhǎng)6 271 bp,由5個(gè)外顯子和4個(gè)內(nèi)含子組成,編碼一個(gè)由201個(gè)氨基酸殘基組成的蛋白質(zhì)分子。SM22α是鈣調(diào)蛋白家族的一種肌動(dòng)蛋白結(jié)合蛋白,包含一個(gè)氨基末端CH結(jié)構(gòu)域和一個(gè)羧基末端鈣調(diào)蛋白樣重復(fù)基序(CLR),通過直接結(jié)合肌動(dòng)蛋白微絲結(jié)構(gòu)影響細(xì)胞骨架的重塑。以往研究主要集中于SM22α在血管重構(gòu)中的作用,生理水平的SM22α通過調(diào)控血管平滑肌細(xì)胞(VSMC)表型轉(zhuǎn)化[1~3]、增殖、遷移、氧化應(yīng)激[4]、炎癥[5, 6]和糖代謝[7]等,在維持血管穩(wěn)態(tài)中起關(guān)鍵作用。現(xiàn)就SM22α的結(jié)構(gòu)特征及其在腫瘤發(fā)生發(fā)展中的作用進(jìn)行綜述。
1 SM22α的表達(dá)特點(diǎn)
1.1 SM22α的表達(dá)具有時(shí)空和組織特異性 SM22α在脊椎動(dòng)物胚胎發(fā)育階段即在平滑肌組織(E9.5)中開始表達(dá),并在心肌(E8.5~E12.5)和骨骼肌(E9.5~E12.5)組織中出現(xiàn)一過性表達(dá)。胚胎后期及出生后成熟組織中SM22α主要在平滑肌組織特異性表達(dá),如子宮、膀胱、胃、前列腺等,是一種重要的平滑肌標(biāo)志物。此外,SM22α亦可在血管內(nèi)皮、心臟、脊髓、腎上腺等非平滑肌組織表達(dá)。
1.2 SM22α表達(dá)具有細(xì)胞表型特異性 已知SM22α在收縮型VSMC高表達(dá),而在合成型VSMC中表達(dá)急劇下降,故其具有分化表型特異性[1,8]。在腫瘤細(xì)胞去分化過程中,SM22α表達(dá)亦發(fā)生顯著變化,但與平滑肌細(xì)胞不同的是,不同類型腫瘤細(xì)胞SM22α表達(dá)變化有差異。如SM22α在前列腺癌[9]、結(jié)腸癌[10~12]、宮頸癌、非小細(xì)胞肺癌和膀胱癌[13]等腫瘤中低表達(dá)甚至不表達(dá),而在胃癌、食管癌、胰腺癌、腎細(xì)胞癌等組織中高表達(dá),在乳腺癌[14,15]中有雙重作用。Li等[16]指出,高表達(dá)的SM22α主要見于富含平滑肌的組織而非腫瘤細(xì)胞層,這可能與胃的解剖學(xué)結(jié)構(gòu)有關(guān)。基于食管與胃的結(jié)構(gòu)和功能密切相關(guān),食管鱗癌與胃癌可能有相似的SM22α表達(dá)特點(diǎn)。SM22α在間充質(zhì)細(xì)胞中表達(dá),而在上皮細(xì)胞的表達(dá)量極低,當(dāng)腫瘤細(xì)胞經(jīng)歷上皮細(xì)胞向細(xì)胞間充質(zhì)轉(zhuǎn)化(EMT)時(shí),也就意味著SM22α在間充質(zhì)細(xì)胞的重新表達(dá)。
2 SM22α在腫瘤發(fā)生發(fā)展中的作用
SM22α的發(fā)現(xiàn)已有30余年歷史,但直到2000年左右,人們才對(duì)其功能有初步認(rèn)識(shí)。其首要功能是肌動(dòng)蛋白結(jié)合蛋白,這一特性賦予了它在個(gè)體發(fā)育、細(xì)胞黏附、運(yùn)動(dòng)等方面強(qiáng)大的生物學(xué)功能[17],其介導(dǎo)的細(xì)胞骨架調(diào)控網(wǎng)絡(luò)為細(xì)胞的穩(wěn)態(tài)調(diào)節(jié)和損傷后修復(fù)提供了不可或缺的微環(huán)境(圖1)。生理?xiàng)l件下,SM22α缺失并不影響血管等平滑肌組織的正常發(fā)育和功能,這就意味著SM22α功能可能被其同源蛋白Calponin或平滑肌22β(SM22β)所補(bǔ)償。然而,病理狀態(tài)時(shí),SM22α的功能是不可替代的。SM22α在動(dòng)脈粥樣硬化斑塊[6, 18]、血管成形術(shù)后再狹窄[6]、血管鈣化[19]、主動(dòng)脈夾層[20]和主動(dòng)脈瘤[21]等血管損傷性疾病中表達(dá)急劇下調(diào),且下調(diào)水平與血管損傷程度呈正相關(guān)。因此,SM22α表達(dá)降低不僅是鑒定平滑肌細(xì)胞去分化的一個(gè)特異性標(biāo)志物[1],還直接參與血管損傷。近年來(lái),有關(guān)SM22α在血管損傷修復(fù)中的作用,國(guó)內(nèi)外實(shí)驗(yàn)室展開了大量研究。SM22α可作為伴侶分子或支架蛋白,以actin結(jié)合依賴或非依賴的方式,于不同的亞細(xì)胞間隔區(qū)募集或整合信號(hào)分子,決定信號(hào)轉(zhuǎn)導(dǎo)方向和應(yīng)答性質(zhì),參與調(diào)控VSMC表型轉(zhuǎn)化[1]、增殖、遷移、氧化應(yīng)激[4]、炎癥[5]、收縮[22]、葡萄糖代謝[7]和轉(zhuǎn)運(yùn)[3]、血管新生內(nèi)膜形成[4]、血管肥厚[4]、平滑肌細(xì)胞向成骨細(xì)胞轉(zhuǎn)化等生物學(xué)過程,維持血管穩(wěn)態(tài)。此外,衰老的哺乳動(dòng)物細(xì)胞中,SM22α表達(dá)上調(diào),且慢性氧化應(yīng)激狀態(tài)下,過表達(dá)SM22α誘導(dǎo)人成纖維細(xì)胞復(fù)制性衰老,提示高水平SM22α在衰老中的潛在作用。成年大鼠腎小球腎炎發(fā)生時(shí),足細(xì)胞持續(xù)高表達(dá)SM22α可加重腎小球硬化病變的進(jìn)程。這些發(fā)現(xiàn)啟示我們,SM22α可在特定的病理?xiàng)l件下發(fā)揮作用,適宜的SM22α表達(dá)水平/模式有助于損傷修復(fù)微環(huán)境的構(gòu)建。但目前的主要研究對(duì)象仍然是血管,SM22α在腫瘤發(fā)生發(fā)展中的作用,特別是機(jī)制研究,仍處于起步階段。
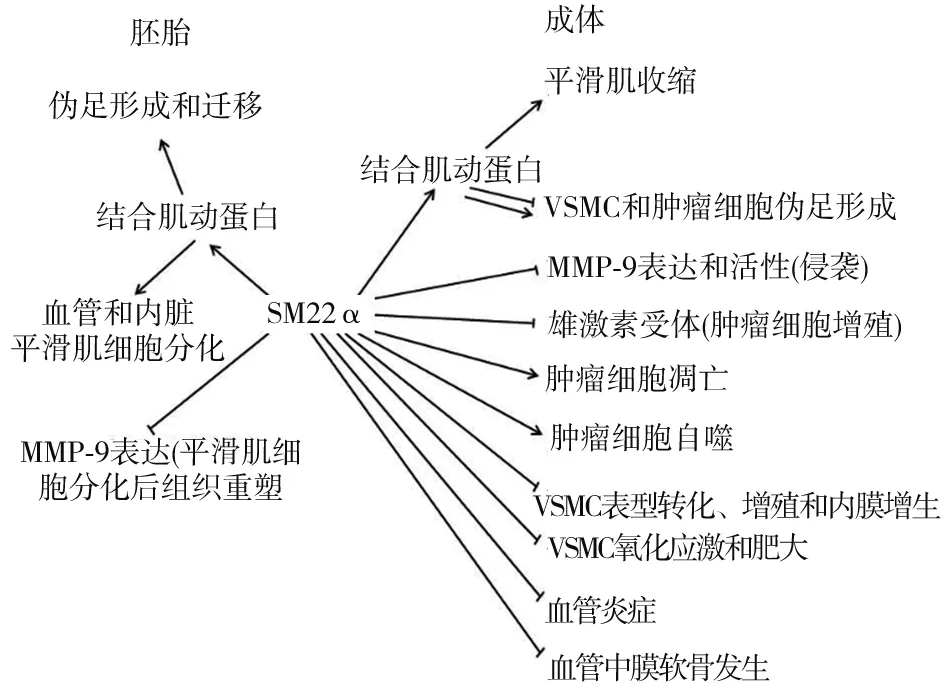
圖1 SM22α的生物學(xué)功能
2.1 SM22α在腫瘤細(xì)胞骨架動(dòng)力學(xué)中的作用 以細(xì)胞骨架重塑為基礎(chǔ)的細(xì)胞增殖、遷移、趨化和黏附等生命活動(dòng)是腫瘤發(fā)生發(fā)展的重要病理生理學(xué)基礎(chǔ)。國(guó)內(nèi)外大量研究表明,作為細(xì)胞骨架相關(guān)蛋白,SM22α可通過CLR基序直接或間接與肌動(dòng)蛋白結(jié)合,參與VSMC F-actin的聚合/解聚,且該過程與SM22α的表達(dá)和表觀遺傳學(xué)修飾有關(guān)[3]。Matsui等[23]研究表明,在A7r5平滑肌細(xì)胞中,SM22α通過CH結(jié)構(gòu)域和EF-hand參與肌動(dòng)蛋白復(fù)合物的形成,間接作用于肌動(dòng)蛋白和偽足形成,而CLR基序與肌動(dòng)蛋白相互作用不顯著。Prasad等[24]通過基因芯片GO分析發(fā)現(xiàn),SM22α在前列腺癌組織中表達(dá)下調(diào),并且SM22α在調(diào)節(jié)其他actin結(jié)合蛋白基因(tropomyosin、smoothelin、dystonin、actinin和vinculin)表達(dá)活性中起關(guān)鍵作用。Thompson等[25]指出,在REF52成纖維細(xì)胞中,應(yīng)用小干擾RNA(siRNA)敲低SM22α,可見SM22α敲低組在血清饑餓的刺激下,更易引發(fā)細(xì)胞偽足形成、運(yùn)動(dòng)和侵襲;在人前列腺癌細(xì)胞PC3中,過表達(dá)SM22α,細(xì)胞的運(yùn)動(dòng)和侵襲能力顯著下降,進(jìn)一步印證了SM22α功能的特異性和重要性。這些結(jié)果提示,SM22α表達(dá)下調(diào)影響細(xì)胞骨架動(dòng)力學(xué)和調(diào)控網(wǎng)絡(luò),導(dǎo)致細(xì)胞內(nèi)外環(huán)境失衡和細(xì)胞功能紊亂,是腫瘤細(xì)胞惡性發(fā)展的關(guān)鍵環(huán)節(jié)。
2.2 SM22α在細(xì)胞侵襲和轉(zhuǎn)移中的作用 腫瘤的侵襲和轉(zhuǎn)移是治療失敗的主要原因。Yang等[15]指出,在兩種乳腺癌細(xì)胞(BT-549, MDAMB-231)、Ⅰ~Ⅲ期原發(fā)性乳腺癌及無(wú)轉(zhuǎn)移的臨床標(biāo)本中,SM22α具有抑癌作用,低表達(dá)的SM22α促進(jìn)人乳腺癌細(xì)胞遷移能力,而過表達(dá)SM22α抑制乳腺癌細(xì)胞的肺轉(zhuǎn)移。低表達(dá)SM22α使線粒體質(zhì)量新分布,過氧化物還原酶表達(dá)下調(diào),促進(jìn)活性氧(ROS)生成和核因子-κB (NF-κB)活化,進(jìn)而導(dǎo)致轉(zhuǎn)移相關(guān)基因如趨化因子受體4(CXCR4)、基質(zhì)金屬蛋白酶-1 (MMP-1)和MMP-2表達(dá)上調(diào),提示SM22α可能通過激活ROS/NF-κB信號(hào)通路促進(jìn)乳腺癌轉(zhuǎn)移。Sayar等[26]研究亦證實(shí),與非致瘤性乳腺細(xì)胞相比,乳腺癌細(xì)胞中SM22α基因啟動(dòng)子區(qū)高度甲基化導(dǎo)致其表達(dá)下調(diào),敲低SM22α增加細(xì)胞的侵襲與遷移能力。然而,Liu等[27]發(fā)現(xiàn),在乳腺癌細(xì)胞MCF-7/S和MDA-MB-231中,高表達(dá)SM22α可增強(qiáng)乳腺癌細(xì)胞的遷移能力,促進(jìn)裸鼠體內(nèi)腫瘤形成及肺部轉(zhuǎn)移。進(jìn)一步研究表明,過表達(dá)SM22α通過下調(diào)人第10號(hào)染色體缺失的磷酸酶及張力蛋白同源的基因(PTEN)表達(dá),激活PI3K/Akt/GSK-3通路,調(diào)控細(xì)胞周期、遷移、分化、凋亡等。Aikins等[14]在研究SM22α與血管生成擬態(tài)(VM)關(guān)系時(shí)亦發(fā)現(xiàn),在人乳腺癌細(xì)胞MDA-MB-231中敲低SM22α,細(xì)胞增殖和VM形成受抑,IL-8和CXCR2的表達(dá)下調(diào)[28]。SM22α對(duì)乳腺癌細(xì)胞系侵襲和轉(zhuǎn)移作用的差異可能與這些細(xì)胞系不同核型、突變狀態(tài)和蛋白質(zhì)組特征等有關(guān)[29]。Zhao等[12]發(fā)現(xiàn),過表達(dá)SM22α削弱了人結(jié)直腸癌細(xì)胞HCTL16的侵襲和轉(zhuǎn)移能力。進(jìn)一步研究表明,過表達(dá)SM22α抑制細(xì)胞外信號(hào)調(diào)節(jié)激酶(ERK)的磷酸化和MMP-9的表達(dá),可能通過ERK/MMP-9信號(hào)通路調(diào)節(jié)結(jié)直腸癌侵襲和遷移能力。此外,SM22α還參與膀胱癌、食管鱗癌等多種腫瘤的侵襲和轉(zhuǎn)移,具體發(fā)揮抑癌作用還是促癌作用與激活不同信號(hào)通路及不同調(diào)控分子參與有關(guān)。
2.3 SM22α在腫瘤細(xì)胞增殖和凋亡中的作用 腫瘤的發(fā)生與細(xì)胞的無(wú)限增殖和異常凋亡有關(guān),是兩者平衡失調(diào)的結(jié)果。本課題組的研究表明,過表達(dá)SM22α抑制VSMC增殖和血管新生內(nèi)膜形成,但對(duì)VSMC凋亡幾乎無(wú)影響。然而,SM22α參與結(jié)直腸癌[12]、膀胱癌[13]、前列腺癌[9]等腫瘤細(xì)胞增殖和凋亡的調(diào)控,且具有不同的調(diào)控模式。Tsui等[13]發(fā)現(xiàn),在人膀胱癌細(xì)胞HT1376和人膀胱癌組織中,敲低SM22α可促進(jìn)膀胱癌細(xì)胞增殖,而過表達(dá)SM22α抑制膀胱癌細(xì)胞增殖,該過程與p53和PTEN有關(guān)。Zhang等[9]研究發(fā)現(xiàn),SM22α以p53依賴的方式誘導(dǎo)細(xì)胞凋亡,過表達(dá)SM22α促進(jìn)人前列腺癌細(xì)胞LNCaP中p53表達(dá)及p53從胞核向胞質(zhì)轉(zhuǎn)位,胞質(zhì)中積累的p53引發(fā)凋亡相關(guān)基因B細(xì)胞淋巴瘤/白血病-2蛋白(Bcl-2)表達(dá)下調(diào),Bcl-2相關(guān)X蛋白(Bax)表達(dá)上調(diào),進(jìn)而觸發(fā)Caspase-3表達(dá)誘導(dǎo)細(xì)胞凋亡。
微小RNA(miRNA)通過調(diào)控靶基因表達(dá)發(fā)揮癌基因或抑癌基因的功能,參與腫瘤的發(fā)生、發(fā)展、侵襲和轉(zhuǎn)移過程。Tang等[30]發(fā)現(xiàn),食管鱗癌組織和細(xì)胞中miR-133b表達(dá)低于癌旁組織,經(jīng)TargetScan和miRDB在線軟件預(yù)測(cè)和雙熒光素酶報(bào)告基因證實(shí),SM22α是miR-133b的靶基因,過表達(dá)miR-133b使SM22α表達(dá)顯著下調(diào)。miR-133b通過調(diào)控SM22α表達(dá),在食管鱗癌細(xì)胞增殖中發(fā)揮重要作用。
2.4 SM22α在細(xì)胞外基質(zhì)(ECM)降解中的作用 ECM是腫瘤細(xì)胞侵襲和轉(zhuǎn)移過程中的天然組織屏障,而MMP是降解ECM的一種重要的蛋白水解酶,幾乎能降解多糖以外的所有ECM成分,增強(qiáng)癌細(xì)胞的侵襲能力。SM22α是一個(gè)新型的MMP-9基因抑制因子。在人纖維肉瘤細(xì)胞HT1080中,過表達(dá)SM22α顯著抑制MMP-9表達(dá),反之,敲低SM22α顯著增強(qiáng)MMP-9的表達(dá)活性。免疫組化結(jié)果同樣顯示,與野生型相比,SM22α基因敲除鼠子宮MMP-9水平明顯升高。進(jìn)一步研究結(jié)果表明,SM22α的CH結(jié)構(gòu)域通過靶向ERK信號(hào)通路,抑制癌基因蛋白c-Fos與MMP-9啟動(dòng)子區(qū)AP-1結(jié)合位點(diǎn)的相互作用,進(jìn)而抑制MMP-9的表達(dá)活性,該結(jié)果為其他惡性腫瘤組織中SM22α和MMP-9表達(dá)的負(fù)相關(guān)性提供了進(jìn)一步證據(jù),同時(shí)也提示SM22α能以actin結(jié)合非依賴的方式調(diào)控基因表達(dá),進(jìn)一步豐富了SM22α的生物學(xué)功能,體現(xiàn)了其功能的多樣性。
2.5 SM22α在細(xì)胞自噬中的作用 自噬是將細(xì)胞內(nèi)受損、變性或衰老的蛋白質(zhì)和細(xì)胞器運(yùn)輸?shù)饺苊阁w進(jìn)行消化降解的過程。自噬和腫瘤的關(guān)系復(fù)雜,在腫瘤發(fā)生的早期階段,自噬可抑制腫瘤細(xì)胞形成;在腫瘤的發(fā)展階段,細(xì)胞可通過適度的自噬促進(jìn)腫瘤存活,過度的自噬亦可誘導(dǎo)腫瘤細(xì)胞自噬性死亡。Xie等[11]研究發(fā)現(xiàn),SM22α在結(jié)直腸癌組織和結(jié)腸癌細(xì)胞(HCT116、HT29)中表達(dá)急劇下調(diào),且與結(jié)直腸癌低自噬活性相關(guān)。在SM22α低表達(dá)的惡性結(jié)腸癌樣本中,p62表達(dá)均升高,而過表達(dá)SM22α顯著抑制結(jié)直腸癌細(xì)胞株p62表達(dá),該結(jié)果初步證實(shí)SM22α可能參與腫瘤細(xì)胞自噬活性的調(diào)節(jié)。
2.6 SM22 α在腫瘤耐藥中的作用 腫瘤耐藥是惡性腫瘤化療失敗的主要原因。體內(nèi)外研究發(fā)現(xiàn),腫瘤耐藥與靶基因突變、靶基因擴(kuò)增、DNA損傷修復(fù)能力、藥物進(jìn)入腫瘤細(xì)胞內(nèi)濃度減少等諸多因素有關(guān),提示腫瘤耐藥分子機(jī)制的復(fù)雜性。SM22α在以紫杉醇為誘導(dǎo)劑的人乳腺癌耐藥細(xì)胞MCF-7/PTX中異常高表達(dá),促進(jìn)MCF-7/PTX發(fā)生EMT,使細(xì)胞間連接缺失,增加腫瘤細(xì)胞的增殖和侵襲能力。siRNA敲低SM22α,改變MCF-7/PTX中EMT標(biāo)志因子表達(dá),進(jìn)而抑制MCF-7/PTX細(xì)胞耐藥和侵襲轉(zhuǎn)移。另有研究表明,SM22α通過增加Akt、GSK-3β磷酸化水平和減少PTEN的表達(dá),激活GSK-3β/PI3K/Akt通路,參與紫杉醇耐藥,其中PI3K/Akt通路參與乳腺癌細(xì)胞的遷移和侵襲[27]。
綜上所述,SM22α主要表達(dá)于成體平滑肌細(xì)胞,雖然在其他特定組織表達(dá)量低,但對(duì)細(xì)胞功能和狀態(tài)的維持必不可少,其表達(dá)的時(shí)空秩序性和表型特異性更提示了該蛋白功能的復(fù)雜性。目前,對(duì)SM22α與腫瘤關(guān)系的研究,主要側(cè)重于SM22α的表達(dá)與腫瘤發(fā)生的相關(guān)性,表達(dá)與腫瘤病理分型分期及預(yù)后的關(guān)系尚不明確,作用機(jī)制的研究亦鮮有報(bào)道。深入探尋細(xì)胞骨架相關(guān)蛋白在惡性腫瘤發(fā)生發(fā)展中的作用和分子機(jī)制,將對(duì)惡性腫瘤的精準(zhǔn)醫(yī)療和個(gè)體化醫(yī)療產(chǎn)生深遠(yuǎn)影響。

