人類白細胞抗原B27核酸檢測國家參考品的建立
胡澤斌 高飛 孫楠 孫彬裕 李麗莉 孫晶 曲守方 黃杰
人類白細胞抗原(human leukocyte antigen,HLA)B27 抗原的表達與強直性脊椎炎有高度相關性,超過90%的強直性脊椎炎患者其HLA-B27 抗原表達為陽性,普通人群中僅5%~10%的為陽性[1-3]。迄今已有70 多種HLA-B27 亞型被發現和鑒定,在中國人群中B2705 和B2704 亞型分布最廣并且與強直性脊椎炎密切相關[4-6]。隨著基因檢測技術的發展和相關試劑盒的研發上市,基于聚合酶鏈反應(polymerase chain reaction,PCR)的HLA-B27 核酸檢測已成為臨床上的常用檢測手段[7-9]。然而目前,我國尚無針對HLA-B27 核酸檢測試劑盒的國家參考品,無法對此類試劑盒進行統一的質量評估。為確保HLA-B27 核酸檢測臨床測定結果可靠,為臨床診斷提供有力證據,中國食品藥品檢定研究院體外診斷試劑檢定所非傳染病診斷試劑室計劃研制一套能夠進行HLA-B27 核酸檢測性能評價的國家參考品。
1 材料與方法
1.1 材料
1.1.1 主要試劑
人外周血淋巴細胞分離液、環孢霉素A 和二甲基亞砜,由北京索萊寶科技有限公司提供;基因組DNA 提取試劑盒(磁珠法),HLA 高分辨基因分型建庫試劑盒,Qubit?ssDNA Assay Kit(Invitrogen),MGISEQ-2000RS 高通量測序試劑套裝,由深圳華大智造科技有限公司提供;人類白細胞抗原B 位點基因高分辨分型試劑盒(測序法)由北京博奧晶典生物技術有限公司提供;人類白細胞抗原B27 核酸檢測試劑盒(熒光PCR 法)由江蘇默樂生物科技股份有限公司提供;SeCore HLA B 位點測序分型試劑盒(測序法)由北京旌準醫療科技有限公司提供;人類白細胞抗原B*27 基因分型試劑盒(SSP 法和熒光PCR 法)由江蘇偉禾生物科技有限公司提供。
1.1.2 主要儀器
MGISEQ-2000RS 測序儀由深圳華大智造科技有限公司提供;基因擴增儀S1000(Bio-Rad)、基因分析儀3730xL(ThermoFisher)由北京博奧晶典生物技術有限公司提供;SLAN-96P 全自動醫用PCR分析系統由江蘇默樂生物科技股份有限公司提供;ABI 3130/3130XL DNA 測序儀/基因分析儀由北京旌準醫療科技有限公司提供;ABI GeneAmp-PCR System 9700、ABIReal-Time PCR Systems 7500由江蘇偉禾生物科技有限公司提供。
1.2 方法
1.2.1 樣本收集
招募自愿參與本項目的外周血捐獻者,并簽署了知情同意書。自2018年2月至2019年2月,共收集到HLA-B2704 陽性樣本2 例、HLA-B2705陽性樣本3 例、HLA-B27 陰性樣本8 例。采集志愿者10 mL 新鮮外周血,放入一次性肝素鈉/鋰或枸櫞酸鈉抗凝管采血管中,2~8℃保存運輸至實驗室。核淋巴細胞,加入病毒液制備完全轉化液,進行細胞轉化與細胞培養、凍存。建立細胞系后進行種子細胞系擴大培養。
1.2.2 國家參考品的制備與驗證
將采集的志愿者外周血進行永生化細胞系的建立[10-11],按基因組DNA 提取試劑盒操作步驟,提取10 例成功建系的細胞基因組DNA,使用安捷倫NanoDorp 測定其OD260/OD280 值檢驗純度,利用瓊脂糖凝膠電泳膠檢驗DNA 的完整性。使用Qubit Fluorometer3.0 對10 例DNA 樣本進行定量后稀釋至20 ng/μL 的濃度,采用高通量測序(next generation sequencing,NGS)技術對每個樣本驗證。驗證合格的DNA 樣本進行分裝并貼上標簽。
1.2.3 國家參考品的協作標定
分別使用4 家協作標定單位的HLA-B27 檢測試劑盒對國家參考品進行協作標定,按照試劑盒說明書進行操作。測序法每個樣本測定1 次,PCR法每個樣本測定3 次。按照說明書的檢測限要求將參考品樣本稀釋之后進行再次檢測。
1.2.4 國家參考品穩定性和均勻性驗證
隨機選取五套國家參考品,在-20℃與25℃之間反復凍融3 次(每隔1 天一次)之后,分別使用測序法、PCR 法、SSP 法的HLA-B27 檢測試劑盒對參考品進行穩定性驗證。另外隨機取出三套國家參考品,使用測序法的HLA-B27 檢測試劑盒對參考品進行均勻性驗證。
2 結果
2.1 國家參考品的制備及驗證
每套HLA-B27 國家參考品包括10 例基因組DNA 樣本(3 例HLA-B2705 陽性、7 例HLA-B27 陰性)。瓊脂糖凝膠電泳結果顯示01-10 號樣本的DNA 條帶完整銳利,且分子量在23 kb 左右,見圖1。
01-10 號樣本的OD260/OD280 值均在1.80~2.15 之間,表明DNA 的純度較高符合檢測需求經NGS 測序技術對每個樣本的HLA-B 位點進行4 位高分辨基因分型檢測,HLA-B 位點的分型結果均與建系之前的外周血基因組DNA 的分型信息一致,最后按照30 μL 體積進行分裝,貼標簽,見表1。
2.2 國家參考品的協作標定
實驗室邀請4 家協作標定單位(分別用A、B、C、D 代表),采用PCR-基因測序分型法(sequence based genotyping,SBT)、熒光PCR 法、和PCR--序列特異性引物法(sequence specific primer,SSP)對國家參考品進行了驗證,見表2。
2.3 國家參考品的穩定性和均勻性驗證
使用A 單位的HLA-B 位點基因高分辨分型試劑盒(SBT 法)對3 套參考品和2 套反復凍融3 次后的參考品進行檢測,使用C 單位和D 單位的HLA-B27 核酸檢測試劑盒(PCR 法和SSP 法)對3 套反復凍融3 次后的參考品進行檢測。見表3。
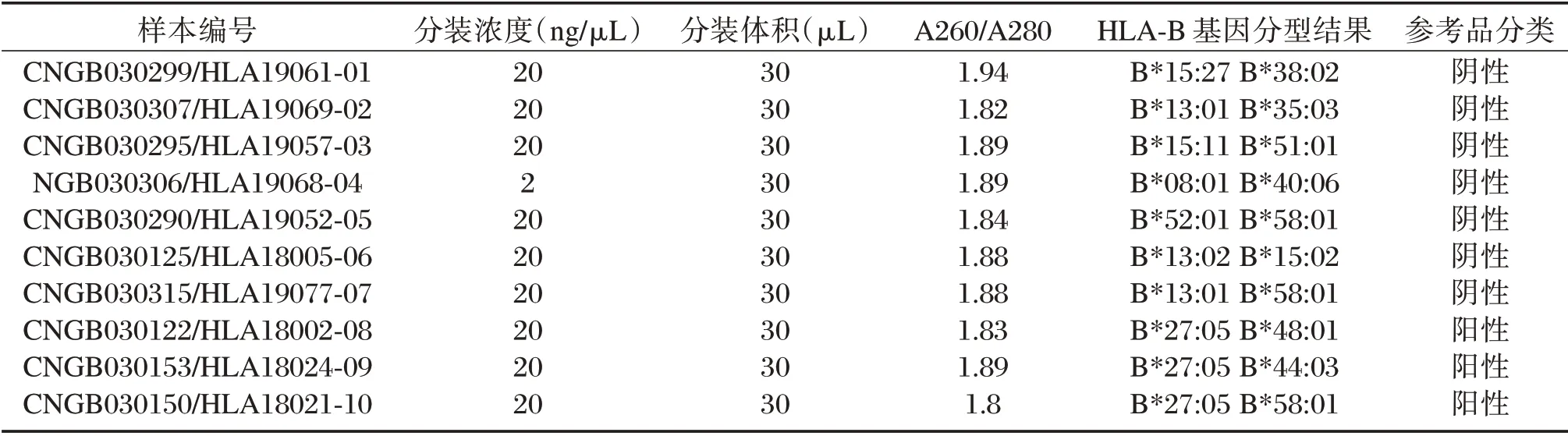
表1 10 例DNA 樣本的驗證結果Table 1 Verification results of genomic DNA from 10 Samples
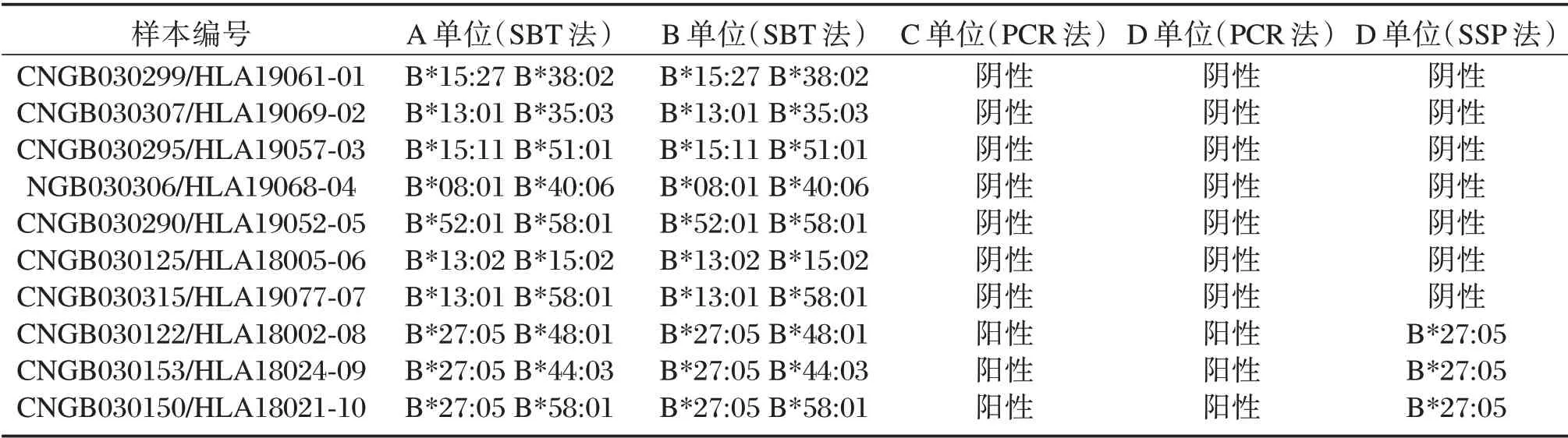
表2 4 家協作標定單位的驗證結果Table 2 Verification results of references by detection kits from 4 manufacturers
3 討論
大量研究數據表明,基于PCR 方法學的HLA-B27 核酸檢測已經成為臨床輔助診斷強直性脊柱炎的常用方法[12-14],而試劑盒的質量是保障臨床診斷準確的關鍵因素。然而不同企業不同方法學的試劑盒在檢測原理、原材料、生產工藝等方面均有所差異,在質量控制和性能評價中使用各自的企業參考品,導致不同試劑盒的檢驗結果缺乏可比性,建立標準化的國家參考品可以對不同試劑盒的質量進行統一評價。
標準物質是指具有一種或多種足夠均勻并且穩定的具有準確特性量值的測量標準,量值準確性、足夠均勻性和良好穩定性是標準物質的三大重要特性[15-17]。本研究通過4 家實驗室采用熒光PCR 法、PCR-SSP 法以及PCR-SBT 測序法的HLA-B27 檢測試劑對參考品進行協作標定,其中A 單位和B 單位兩家實驗室均使用世界衛生組織推薦的HLA 分型方法金標準即PCR-SBT 測序法,對10 例國家參考品(每一例均含2 條染色體)進行4 位基因分型,結果完全一致;C 單位和D 單位兩家實驗室使用熒光PCR 法、PCR-SSP 法的不同檢測試劑,對10 例國家參考品B27 的陰陽性結果進行判斷,結果完全一致,以上數據充分保障了國家參考品的定值準確。
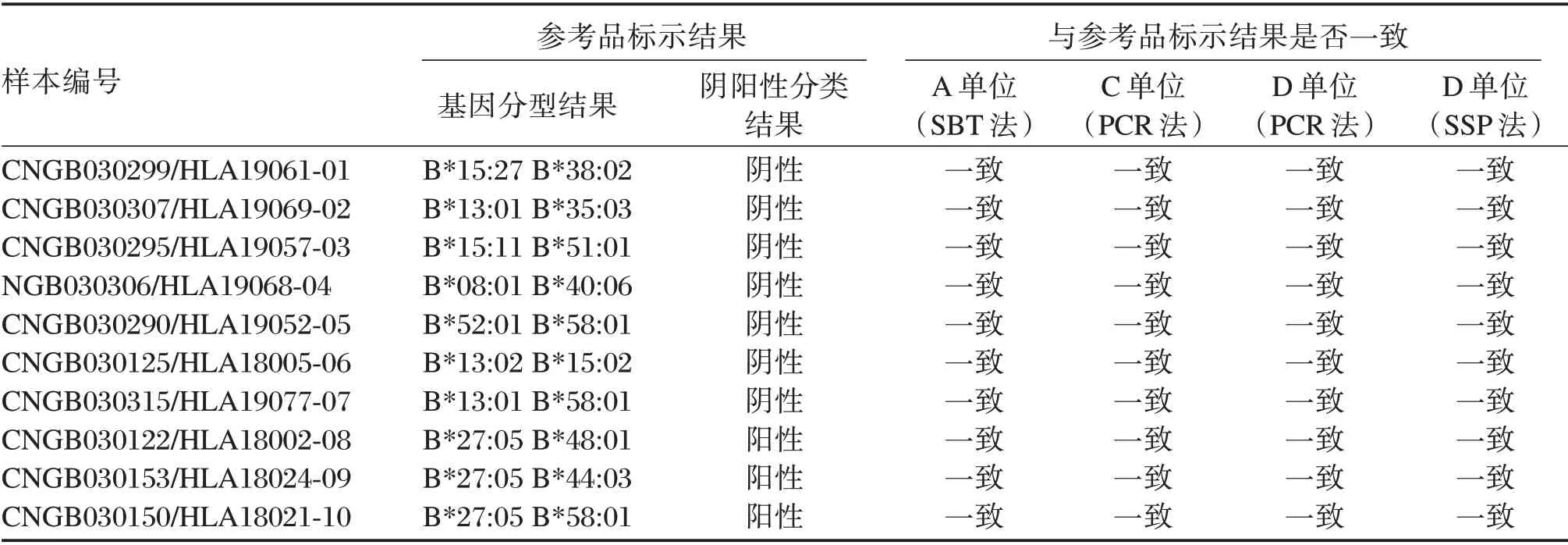
表3 國家參考品穩定性和均勻性的驗證結果Table 3 Verification results of stability and homogeneity for references
本參考品是細胞系提取的基因組DNA 樣本,常規在在-20℃以下保存,且要求干冰或-20℃冷鏈運輸,用戶不宜反復凍融后使用。DNA 樣本自身的均勻性和穩定性是良好的。本研究通過3 家實驗室采用PCR 法、PCR-SSP 法以及PCR-SBT 測序法,對3套國家參考品、以及5 套在-20℃與25℃之間反復凍融3 次之后的國家參考品進行驗證,結果顯示A 單位、C 單位和D 單位的驗證結果均與-20℃保存的國家參考品的標示結果完全一致,表明國家參考品在反復凍融3 次之后依然穩定和均勻。此外,本參考品銷售半年以來,多家用戶使用后反饋良好,也表明了其穩定性和均勻性良好;本實驗室既往研制的多套DNA 參考品的穩定性和均勻性實驗結果以及售后反饋,均表明DNA 參考品一直非常穩定[18];同時還將對該國家參考品進行長期穩定性研究以及期間核查,以確保長期放置后依然滿足要求。
由于測序法的HLA-B 核酸檢測試劑盒應對待測樣本報告出HLA-B 的4 位基因分型信息,國家參考品在對此類試劑盒進行性能評價時,10 例參考品均作為陽性參考品可對試劑盒的準確性指標進行評價,10 例參考品稀釋后可對試劑盒的檢測限指標進行評價;其他方法學的HLA-B 核酸檢測試劑盒主要包括:熒光PCR 法、PCR-SSP 法、PCR-序列特異性寡核苷酸探針法(sequence specific oligonucleotide,SSO)、PCR 熔解曲線法,此類試劑盒一般針對B27 的常見亞型如B2705 和B2704 設計特異性引物,對待測樣本報告陰性或陽性的結果。7 例B27 陰性國家參考品可對試劑盒的特異性指標進行評價,3 例B27 陽性國家參考品可對試劑盒的準確性和檢測限指標進行評價。
綜上所述,本實驗室成功建立了人類白細胞抗原B27 核酸檢測國家參考品,該參考品的準確性、均一性和穩定性均符合要求,可用于人類白細胞抗原B27 核酸檢測試劑盒的質量評價。