基于手持技術測定溶液反應的平衡常數
眭蘇奇 劉立雄 錢揚義 程俊

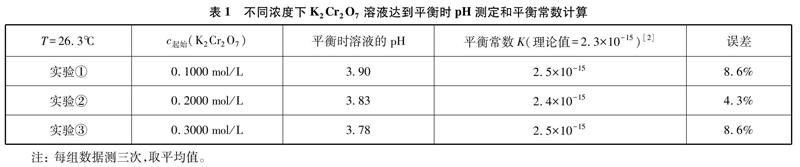
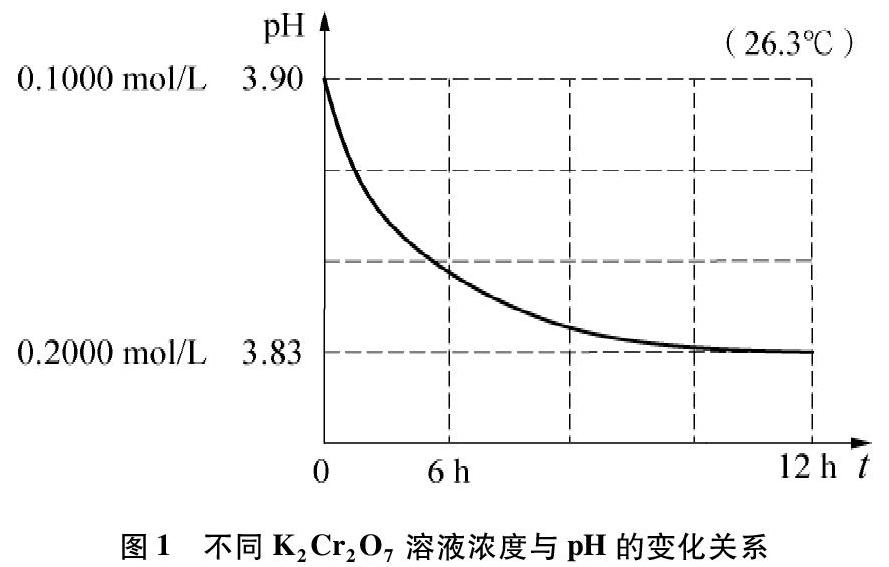
摘要:運用手持技術定量測定不同濃度K2Cr2O7溶液達到化學平衡(Cr2O2-7+H2O2CrO2-4+2H+)時溶液的pH,計算該反應的平衡常數,同時又測量同一濃度K2Cr2O7溶液在不同溫度下達到平衡時溶液的pH變化關系,得出化學平衡常數只與溫度有關,與濃度等其他物理量無關的結論。揭示現行教材存在的一些局限與不足,突破化學平衡常數教學上某些誤區和疑點,讓學生從源頭上理解化學平衡常數的含義和本質,充分發揮其教學功能和價值。通過實驗探究,培養學生收集、分析、處理數據的能力,促進自身學科核心素養的發展。
關鍵詞:溶液反應; 化學平衡常數測定; pH傳感器; 實驗探究
文章編號:1005-6629(2020)09-0063-04
中圖分類號:G633.8
文獻標識碼:B
1?研究背景分析
1.1?化學平衡常數在平衡原理教學中的地位、功能與價值
“化學平衡常數”(以下也可用K表示)是化學平衡理論體系的核心之一,是學習電離平衡、水解平衡等的必備基礎知識,對深入理解其他平衡具有重要的理論指導意義[1]。特別是通過這個章節的學習,既是對之前所學勒夏特列原理的延伸和補充,也是對之后要學的電離平衡常數、水解平衡常數和溶度積常數的一種示范和鋪墊,可以繼續發揮化學平衡常數的功能與價值。
通過深入學習化學平衡常數,首先可以增進學生對化學反應的限度的理解,其次可以增進學生對平衡移動規律的理解,還可以為學生提供分析其他平衡移動問題的新的思路和方法。因此,學生通過借助化學平衡常數認識到“不同條件下化學平衡狀態、移動和限度是不同的”,在改變一個或多個外因情況下,可以利用化學平衡常數進行定量表征和比較,對化學平衡的認識由定性水平上升到定量水平,還可以讓學生關注到體系和環境中多個要素之間的關系,對化學平衡狀態、移動和限度的認識由孤立(單一因素作用)認識發展到系統(多因素共同作用)認識,為學生找到了進行理性分析的思維“支架”,對于突破學生認識障礙點、發展學生對化學平衡狀態、移動和限度的認識,實現認識方式的轉變具有重要意義。
1.2?化學平衡常數在現行教材呈現形式上存在的一些局限與不足
現行幾套教材對化學平衡常數這一重要概念的呈現可能在實證研究方面存在一些局限與不足。這幾套教材在這個重要概念的呈現上沒有設計相應的定量實驗,這可能是由于傳統實驗儀器和手段還無法開展此類精度要求較高的定量實驗或是利用傳統實驗儀器和手段設計的實驗較為復雜、操作難度較大,不利于中學階段開展,因此基本上都是以給出實驗數據的方式呈現給學生,本身說服力就不夠,而且有些版本的教材將運算的結果也直接呈現給學生,這樣不僅會減弱學生探究的熱情和興趣,而且會增大學生對這個問題的理解難度。試想有了不勞而獲的數據和結論,還有誰會再花大力氣去認真鉆研呢?對于這個較為抽象的概念,由于缺乏實證素材,只能直接“空降”硬塞給學生,可能學生在教師反復提醒下“記住”了這個結論(而不是真正理解),帶著這樣的疑惑在之后電離平衡常數、水解平衡常數和溶度積常數的學習中遇到較復雜的化學平衡問題,稍不留神就可能會出現這樣或那樣的錯誤了。
1.3?化學平衡常數在常規教法過程中存在的誤區與疑點
教師在教學過程中由于教材的局限和實證素材的缺乏,很多一線教師的常規教法是直接把定義和結論告訴學生,教學重點也僅僅鎖定在表達和計算上,雖然看似簡單高效學生學起來感覺并不難,但卻普遍存在較大的疑惑。主要是集中在改變某種單一組分的濃度或是等倍數改變所有組分濃度(即改變壓強)不影響K值,學生在理解上有障礙,例如通常有一部分學生會錯誤認為增大反應物的濃度,反應正向移動,消耗了反應物使得反應物濃度減少,同時產生了生成物使得生成物濃度增加,K值應該增大。很明顯,這部分學生并沒有真正理解勒夏特列原理,尤其是對原理中“減弱”二字理解并不到位;還有一部分學生雖然能理解“減弱”二字的含義,但對于反應物、生成物濃度都增加時,K值保持不變還是會心存疑惑。所以若把化學平衡常數與平衡移動規律內在聯系割裂開來,反而會讓學生產生認識誤區與疑點。因此筆者認為化學平衡常數的教學重點,是通過定量實驗測定化學平衡常數,讓學生從源頭上理解化學平衡常數的含義和本質,這樣才能在教學中充分發揮化學平衡常數的功能和價值。
從圖2和表3可以看出,隨著溶液溫度升高,溶液pH降低,K值越來越大,反應向正方向移動,還可以根據圖像和數據預測正反應為吸熱反應,因為此反應可看成Cr2O2-7的水解,水解為吸熱反應,這也為下階段水解學習積累實證素材。合理選擇教學媒體(手持技術),同步呈現真實實驗,表征可逆反應的微觀過程,可以實時顯示出微粒(H+)濃度的改變隨時間或其他變量改變的曲線圖,呈現化學平衡的動態特征。同時幫助學生澄清模糊概念,建立科學的動態平衡觀,能有效幫助學生理解化學平衡常數,強化學生對化學平衡常數與各種關系的連結能力[3],例如“Cr2O2-7+H2O2CrO2-4+2H+”平衡各種曲線圖,可以鍛煉學生理清和處理各種微粒數量關系的能力。以往化學平衡的曲線圖多數只出現在考試題中,學生普遍都會感到陌生和突兀,難度大,而運用手持技術后這些曲線變得真實而熟悉,“搭臺階降難度”,在自己動手操作和處理實驗數據時,可以進一步加深對化學平衡中各種微觀粒子的代數關系和化學平衡常數本質的理解,既提升學生的“證據推理與模型認識”“科學探究與創新意識”等學科素養,又提高學生的應試解題能力,一舉多得。
3?研究展望
從現行教材中化學實驗來看,主要以演示、驗證、定性實驗為主,可能難以培養學生自主地、定量地搜集和處理信息的能力以及進行研究性學習的能力;使用的實驗儀器、裝置等甚至是上百年沒有變動,雖然經典可靠穩定性強,但也存在精確度差、缺乏自動采集、處理大量數據的功能以及很難與多媒體計算機連接等不足,與當今科技高速發展的數字化信息時代有些不相符。
手持技術的出現極大程度地改變了這種實驗現狀,這種由數據采集器、傳感器、終端設備及配套的軟件并能與計算機連接的實驗技術,具有自動記錄數據、實時的圖線繪制等功能,能讓學生從數據讀取、記錄和圖像繪制的繁雜枯燥的勞動中解脫出來,讓學生可以迅速建立實驗現象與圖像的聯系,更好地提升學生對數據、圖像中呈現信息的獲取、解釋和預測能力,有助于學生通過對圖像變化趨勢的觀察與理解及時實驗條件做出適當的調整或建立新的實驗假設,并在每一次修訂實驗方案或控制探究變量的過程中不斷思考自己的預測與實驗事實不吻合的具體原因,從而引導他們更深層次的學習[4]。
將手持技術引入中學化學實證探究教學中不僅可以增加化學實驗的科學技術含量和時代氣息,還可以提高學生對科學實驗的興趣,讓學生從中學到其他方面的知識和技術,更加有利于開闊學生的視野,提高他們從事創新活動和探索的信心。因此將化學實證探究教學與手持技術結合起來是合理、有效的。
參考文獻:
[1]李振雯, 秦浩正. 氯氣與水反應實驗的設計及相關教學探討[J]. 化學教學, 2018, (4):69.
[2]宋心琦, 何少華主編. 普通高中課程標準實驗教科書教師教學用書·化學反應原理(第3版)[M]. 北京:人民教育出版社, 2007:46.
[3]葉靜怡. “化學平衡”迷思概念的轉變教學研究[J]. 化學教學, 2010, (6):31.
[4]錢揚義, 鄧峰. 數字化化學探究實驗室的建設與學生探究能力的培養[J]. 中國電化教育, 2006, (11):50.

