體外膜肺氧合心肺復蘇后不同目標體溫管理對患者腦功能的影響
潘飛艷 童洪杰 張曉玲 陳琨
[摘要] 目的 探討體外膜肺氧合心肺復蘇后不同的目標體溫管理對患者腦功能預后的影響。 方法 納入2014年5月~2020年1月我院收住行體外心肺復蘇的患者60例,將患者隨機分為兩組,其中A組30例,B組30例。A組患者的體溫控制在32.0℃~34.0℃;B組患者的體溫控制在34.1℃~36.0℃。通過分析比較出院時患者的存活情況、CPC評分以及并發癥來評估兩組患者之間的差異。 結果 60例患者中A組存活患者12例,B組存活患者10 例,兩組患者存活情況比較差異無統計學意義(P>0.05)。A組患者CPC評分良好12例,B組患者CPC評分良好7例,兩組患者CPC評分比較差異無統計學意義(P>0.05)。兩組患者在并發癥方面比較差異無統計學意義(P>0.05)。結論 與目標體溫控制在34.1℃~36.0℃相比較,體外膜肺氧合心肺復蘇后的患者目標體溫控制在32.0℃~34.0℃對患者的腦功能預后并無更多益處。
[關鍵詞] 體外膜肺氧合;心肺復蘇;亞低溫;腦保護
[中圖分類號] R459.7 ? ? ? ? ?[文獻標識碼] B ? ? ? ? ?[文章編號] 1673-9701(2020)21-0116-04
Impacts of different objective body temperatures management on cerebral function in patients after extracorporeal membrane oxygenation cardiopulmonary resuscitation
PAN Feiyan TONG Hongjie ZHANG Xiaoling CHEN Kun
Department of Critical Care Medicine, Jinhua Municipal Central Hospital in Zhejiang Province, Jinhua 321000, China
[Abstract] Objective To investigate the impacts of different objective body temperatures management on the prognosis of patients cerebral function after extracorporeal membrane oxygenation(ECMO) and cardiopulmonary resuscitation. Methods Sixty patients admitted to our hospital for extracorporeal cardiopulmonary resuscitation from May 2014 to January 2020 were included. The patients were randomly divided into two groups, including group A(n=30) and group B(n=30). The patients body temperatures controlled at 32.0℃-34.0℃ were divided into group A, while the patients body temperatures controlled at 34.1℃-36.0℃ were divided into group B. The difference between the two groups was evaluated by analyzing and comparing the survival condition of patients at discharge, cerebral performance category(CPC) score and complication. Results Among the sixty patients, there were twelve survivors in group A, ten survivors in group B, and there was no statistical difference in survival between the two groups(P>0.05). Twelve patients with high CPC scores in group A, and seven patients with high CPC scores in group B, and there was no statistical difference in CPC scores between the two groups(P>0.05). There was no difference of complication between the two groups(P>0.05). Conclusion Compared with the objective body temperatures control at 34.1℃-36.0℃, those at 32.0℃-34.0℃ after ECMO cardiopulmonary resuscitation have no more benefits to the prognosis of the cerebral function of patients.
[Key words] Extracorporeal membrane oxygenation; Cardiopulmonary resuscitation; Mild low temperature; Cerebral salvage
據不完全統計,我國每天約有1500人死于心跳驟停[1]。在心跳驟停的搶救過程中,中樞神經系統是最容易受損傷的也是最難恢復的一個部分,因此,臨床工作者們不僅關注患者的存活情況,更關注患者的神經系統預后。大量的研究表明[2,3],亞低溫治療可以改善心跳驟停患者的中樞神經系統預后。2015年最新的心肺復蘇指南也推薦將復蘇后的患者采用32℃~36℃的亞低溫進行治療[4]。體外心肺復蘇(Extracorporeal cardiopulmonary resuscitation,ECPR)是近年來較新穎的搶救心跳驟停患者的手段,該方法通過改善患者的循環給患者的重要臟器提供了有效灌注,其中包括腦組織[5]。相較于傳統的心肺復蘇,這類患者的腦組織代謝是增加的[6],因此如何設定該類患者的體溫管理目標以達到腦保護的目的是值得去思考的問題。本研究擬對體外膜肺氧合心肺復蘇后的患者采用不同的目標體溫管理,探索不同的目標體溫對患者中樞神經系統預后的影響。現報道如下。
1 資料與方法
1.1 一般資料
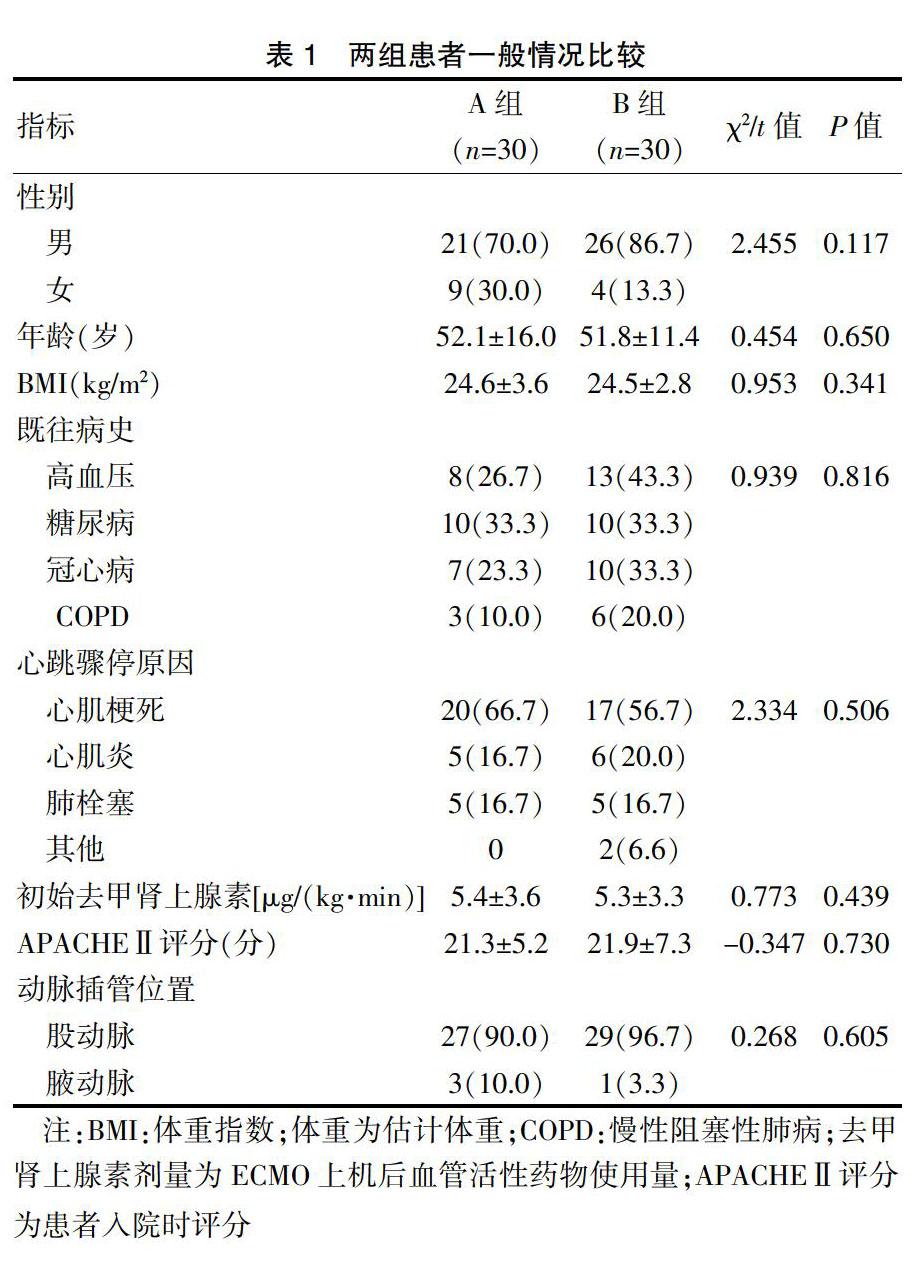
2014年5月~2020年1月我院收住的ECPR患者60例被納入本項研究。納入標準[7]:(1)ECPR后循環恢復者;(2)無亞低溫治療的禁忌證者;(3)臨床資料完整者。排除標準[8]:(1)嚴重的凝血功能障礙者;(2)嚴重的顱腦外傷者;(3)家屬不愿意參與研究者。本研究獲得患者及其家屬的知情同意,并經我院醫學倫理委員會批準。納入的患者按隨機數字表法分為兩組,其中A組30例,B組30例,兩組患者在性別構成、年齡、體重指數(BMI)、既往病史、心跳驟停原因、初始去甲腎上腺素劑量、APACHEⅡ評分、動脈插管位置等方面比較均無統計學差異(P>0.05),具有可比性,見表1。
表1 ? 兩組患者一般情況比較
注:BMI:體重指數;體重為估計體重;COPD:慢性阻塞性肺病;去甲腎上腺素劑量為ECMO上機后血管活性藥物使用量;APACHEⅡ評分為患者入院時評分
1.2 方法
本研究為前瞻性隨機對照性研究。通過調節體外膜肺氧合(Extracorporeal membrane oxygenation,ECMO)水溫箱的溫度、亞低溫治療儀以及冬眠合劑實現體溫管理目標。A組:患者體溫控制在32.0℃~34.0℃,B組:患者體溫控制在34.1℃~36.0℃。兩組患者的亞低溫時間均維持24 h。復溫流程為撤除亞低溫治療儀,上調水溫箱溫度,使體溫恢復到36.0℃以上,復溫時每小時體溫上升不超過0.25℃[9]。通過分析比較出院時患者的存活情況及格拉斯哥-匹茲堡腦功能表現評分(Cerebral performance categories scale,CPC)來評估兩組患者之間的差異,CPC評分1~2分認為是腦功能良好。
1.3 評價標準
格拉斯哥-匹茲堡腦功能表現評分[10]:1分:腦功能完好,神志清醒,有正常生活和工作能力,可能有輕度的心理功能缺陷、輕度語言障礙、不影響功能的輕度偏癱或輕微顱神經功能異常;2分:中度腦功能殘障,神志清醒,可在特定的環境中部分時間工作或獨立完成日常活動,可能存在偏癱、癲癇發作、共濟失調、構音障礙、永久性記憶或心理改變;3分:嚴重腦功能殘障,清醒,但需要他人的日常幫助,保留有限的認知功能,或可以行動,但嚴重記憶紊亂,或癡呆,或癱瘓而僅依賴眼睛交流;4分:昏迷及植物性狀態,無知覺,對環境無意識,無認知,不存在與周圍環境的語言或心理相互作用;5分:腦死亡。
1.4 觀察指標
觀察并比較兩組患者在ECMO上機完成后初始去甲腎上腺素的使用劑量、入院后APACHEⅡ評分[6]以及患者ECMO動脈導管的插管位置(股動脈、腋動脈)的分布情況;觀察兩組患者的存活和死亡例數、兩組CPC評分[10]處于1~2分和3~5分的患者例數以及兩組患者并發癥的發生情況(包括:下肢缺血、血流感染、腎損傷的發生比例)。
1.5 統計學方法
采用SPSS22.0統計學軟件進行分析,計量資料以均數±標準差(x±s)表示,組間比較采用獨立樣本的t檢驗;計數資料采用χ2檢驗,理論頻數<5時采用校正χ2檢驗,當理論頻數<1時采用Fisher's精確概率法;P<0.05為差異有統計學意義。
2 結果
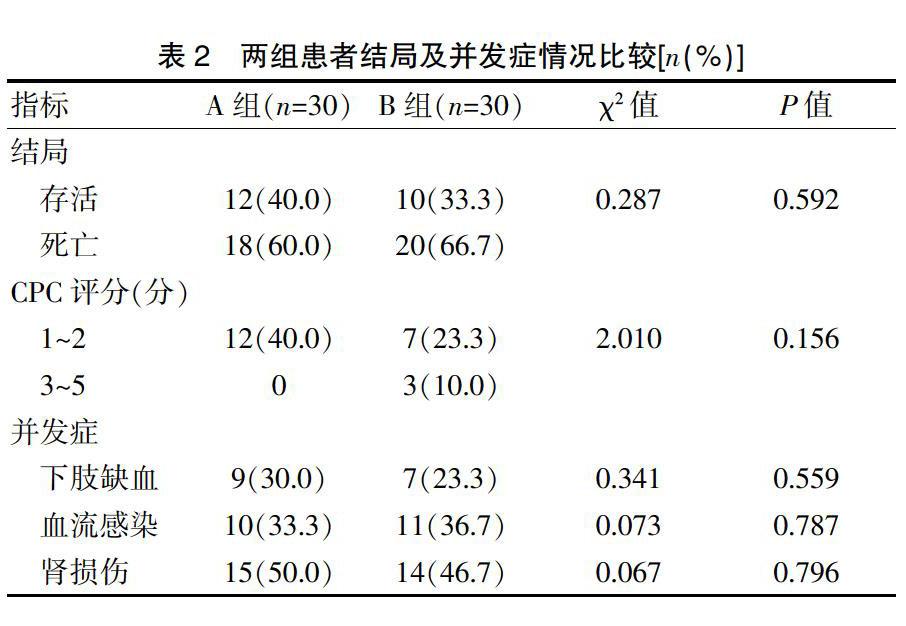
出院時A組存活患者12例,B組存活患者10例,A組患者CPC評分良好12例,B組患者CPC評分良好7例,兩組患者存活情況及CPC評分比較差異無統計學意義(P>0.05);兩組患者在并發癥(下肢缺血、血流感染、腎損傷)方面比較差異無統計學意義(P>0.05),見表2。
3 討論
心跳驟停后患者腦功能的恢復一直以來是臨床工作者們關心的內容。盡管ECPR搶救了更多心跳驟停的患者,但是存活至出院且中樞神經系統結局良好的患者比例仍然不高,尤其是在院外心跳驟停的患者,這個比例更低[7,11]。亞低溫被證明是能夠改善心跳驟停患者腦功能的方法。然而,針對這類患者目標體溫的設定是一個沒有解決的問題。國內的成人體外膜肺氧合循環輔助專家共識建議ECPR患者可以聯合使用亞低溫治療,但沒有明確指出該類患者的目標體溫應控制在哪個水平[12]。通過本研究發現,將ECPR患者的目標體溫控制在32.0℃~34.0℃,與34.1℃~36.0℃相比較對患者的腦功能預后并無更多益處。
亞低溫是指位于32.0℃~35.0℃之間的溫度。亞低溫有助于減少神經系統的代謝、降低炎癥反應、減少缺血再灌注損傷進而起到減少中樞神經系統的損傷[13],因此,該方法常用于心跳驟停患者的復蘇成功后的腦保護。Bernard SA等[14]的早期研究表明對于心肺復蘇后恢復自主循環的患者采用33℃的低溫2 h有利于改善該類患者的神經系統結局。發表在新英格蘭雜志上的早期研究[15]對137例心跳驟停患者采用32℃~34℃的亞低溫治療,結果表明相較于未采用亞低溫的患者,這部分患者6個月的神經系統預后更為良好,存活率更高。但近期另一項研究[16]表明,將院外心跳驟停的患者體溫控制在33℃與控制在36℃相比較,對中樞神經系統的影響并無統計學差異。相反,體溫控制過低可能會帶來更多的風險。因此,2015年以后心肺復蘇指南也將原來的目標體溫改為32℃~36℃。然而,以上研究均是針對傳統心肺復蘇后的患者開展的,對于ECPR患者這類研究很少。Seok KY等[17]的研究納入16例ECPR患者,在ECPR復蘇成功后通過導管將患者的核心體溫控制在34.5℃~35.0℃,研究結果表明,該方法有利于改善患者的神經系統預后,但該研究納入患者例數較少,且為觀察性研究,無對照,因此,證據等級較低。另外一項關于ECPR患者使用選擇性低體溫的研究(NCT03345706)正在開展,該研究通過比較將該類患者體溫控制在25℃~29℃與控制在33℃~34℃對患者預后的影響,以尋找該類患者的體溫管理目標。但該研究仍在招募患者,研究尚未完成,結果未知。此外,Wang CH等[18]的研究將ECPR患者的體溫控制在深低溫范圍(24℃~30℃)12 h發現患者的腦功能恢復較好。然而,這僅屬于個案報道,尚需要大規模的研究來得出結論。
本研究首次發現,將ECPR患者的目標體溫控制在32.0℃~34.0℃,相比較于34.1℃~36.0℃并沒有給神經系統預后帶來更多的益處。這擴張了我們對ECPR患者目標體溫管理的認知。與傳統的CPR不同,ECPR后的患者腦組織得到了更好的灌注,但在復蘇后的早期,這對于脆弱的腦細胞可能是有害的,因此我們構想這類患者可能需要將體溫控制在更低的水平以減少腦細胞的代謝,減少氧消耗。然而,研究結果表明,更低的體溫對于患者的神經系統預后并未起到改善作用。低體溫雖然能改善神經系統預后,但更低的體溫同時也會帶來更多的并發癥,如呼吸抑制、凝血功能障礙等[19]。Cashen K等[20]的研究發現接受亞低溫治療的患者在ECMO運行的最初7 d更容易發生腦出血(P=0.012),但由于ECMO支持的患者在治療過程中進行抗凝,運行期間出血的發生率可達到50%,因此并不能認為亞低溫是引起患者腦出血的唯一因素。但事實證明,對于這類患者目標體溫不是越低越好。
本研究存在以下不足:首先未記錄冬眠合劑和鎮靜藥物的劑量。其次,未詳細記錄亞低溫帶來的并發癥,對于這方面的研究而言是非常重要的。
綜上所述,將ECPR患者的目標體溫控制在32.0℃~34.0℃,相比較于34.1℃~36.0℃并沒有給神經系統預后帶來更多的益處。
[參考文獻]
[1] Zhang S. Sudden cardiac death in China:Current status and future perspectives[J]. Europace,2015,17(Suppl 2):ii14-18.
[2] Kagawa E,Dote K,Kato M,et al. Do lower target temperatures or prolonged cooling provide improved outcomes for comatose survivors of cardiac arrest treated with hypothermia?[J]. J Am Heart Assoc,2015,4(9):e002123.
[3] Fukuda T. Targeted temperature management for adult out-of-hospital cardiac arrest:Current concepts and clinical applications[J]. J Intensive Care,2016,4:30.
[4] Kwon OY. The changes in cardiopulmonary resuscitation guidelines:From 2000 to the present[J]. J Exerc Rehabil,2019,15(6):738-746.
[5] Zhao Y,Xing J,Du Z,et al. Extracorporeal cardiopulmonary resuscitation for adult patients who underwent post-cardiac surgery[J]. Eur J Med Res,2015,20:83.
[6] Kim WY,Choi DH,Kim YJ,et al. Extracorporeal cardiopulmonary resuscitation among patients with out-of-hospital cardiac arrest[J]. Clinical & Experimental Emergency Medicine,2016,3(3):132-138.
[7] MacLaren G,Masoumi A,Brodie D. ECPR for out-of-hospital cardiac arrest:More evidence is needed[J]. Crit Care,2020,24(1):7.
[8] Kurisu K,Yenari MA. Therapeutic hypothermia for ischemic stroke; pathophysiology and future promise[J]. Neuropharmacology,2018,134(Pt B):302-309.
[9] Silverman MG,Scirica BM. Cardiac arrest and therapeutic hypothermia[J]. Trends Cardiovasc Med,2016,26(4):337-344.
[10] Ahn C,Kim W,Cho Y,et al. Efficacy of extracorporeal cardiopulmonary resuscitation compared to conventional cardiopulmonary resuscitation for adult cardiac arrest patients:A systematic review and meta-analysis[J]. Scientific Reports,2016,6:34208.
[11] Wang J,Ma Q,Zhang H,et al. Predictors of survival and neurologic outcome for adults with extracorporeal cardiopulmonary resuscitation:A systemic review and meta-analysis[J]. Medicine,2018,97(48):e13257.
[12] 中國醫師協會體外生命支持專業委員會. 成人體外膜氧合循環輔助專家共識[J]. 中華醫學雜志,2018,98(12):886-894.
[13] Chen X, Zhen Z, Na J,et al. Associations of therapeutic hypothermia with clinical outcomes in patients receiving ECPR after cardiac arrest:Systematic review with meta-analysis[J]. Scand J Trauma Resusc Emerg Med,2020,28(1):3.
[14] Bernard SA,Gray TW,Buist MD,et al. Treatment of comatose survivors of out-of-hospital cardiac arrest with induced hypothermia[J]. N Engl J Med,2002,346(8):557-563.
[15] Hypothermia after Cardiac Arrest Study G. Mild therapeutic hypothermia to improvethe ?neurologic outcome after cardiac arrest[J]. N Engl J Med,2002,346:549-556.
[16] Dragancea I,Horn J,Kuiper M,et al. Neurological prognostication after cardiac arrest and targeted temperature management 33℃ versus 36℃:Results from a randomised controlled clinical trial[J]. Resuscitation,2015,93:164-170.
[17] Seok KY,Jik LY,Ki-Bum W,et al. Extracorporeal cardiopulmonary resuscitation with therapeutic hypothermia for prolonged refractory in-hospital cardiac arrest[J]. Korean Circulation Journal,2017,47(6):939-948.
[18] Wang CH,Lin YT,Chou HW,et al. Novel approach for independent control of brain hypothermia and systemic normothermia:Cerebral selective deep hypothermia for refractory cardiac arrest[J]. J Neurointerv Surg,2017,9(8):e32.
[19] Assis FR,Narasimhan B,Ziai W,et al. From systemic to selective brain cooling-Methods in review[J]. Brain Circ,2019,5(4):179-186.
[20] Cashen K,Reeder RW,Shanti C,et al. Is therapeutic hypothermia during neonatal extracorporeal membrane oxygenation associated with intracranial hemorrhage?[J]. Perfusion,2018,33(5):354-362.
(收稿日期:2020-01-14)

