基于石墨烯和功能核酸的Ag+熒光檢測方法
吳雪琪 張立佩 曹陽 文曉剛 周小紅
(1. 上海師范大學環境與地理科學學院,上海 200234;2. 清華大學環境學院環境模擬與污染控制國家重點實驗室,北京 100084;3. 嘉興學院南湖學院,嘉興 314001)
近年來,銀作為一種抗菌劑在醫院得到廣泛的使用,特別是在傷口敷料、外用制劑和醫療器械(氣管內呼吸管、骨假體等)中。然而,長期接觸銀和銀化合物會導致銀質沉淀癥及其他癥狀,如頭痛、胃痛、疲勞、皮膚刺激或更嚴重的神經、腎臟或肝臟并發癥。膠體銀還可能干擾某些藥物的吸收,如培那西拉敏、喹諾酮類、四環素和甲狀腺素。由于人類對銀的接觸越來越普遍,因此需要開發一種簡單快速的方法來監測水源和體內的銀[1-2]。
大量研究表明,在分子水平上某些重金屬離子可與特定的基因序列發生作用,使其空間結構發生改變[3],而這種結構和性能的關系使重金屬離子,如Ag+、Hg2+的快速、特異識別有了一條便捷的途徑。上述能夠發生特異結構變化的DNA或RNA鏈,被稱為功能核酸[4],它們通過3種類型的傳感方式實現重金屬離子的檢測:第一種是利用DNA,基因錯配特異性結合重金屬離子實現檢測[5]。本課題組報道了基于Hg2+與T堿基錯配形成T-Hg2+-T復合物的倏逝波定量檢測Hg2+的研究,對Hg2+的檢測限為2.1 nmol/L[6];第二種是與鳥嘌呤(G)-四聯體發生特異性反應,G-四聯體是由ssDNA(單鏈DNA)中的多個G-4面互相重疊而產生,重金屬離子可進入G-四聯體的中心,從而影響其與其他離子結合[7-8];第三種是基于金屬依賴性的核酸酶DNAzyme,即在特定重金屬離子的存在下,DNAzyme催化發生水解斷裂反應,不可逆地將帶有熒光標記的核酸片段剪斷,從而實現檢測[9]。目前依據這些傳感設計思路已經用于多種重金屬的單指標甚至多指標的同時測定。最常見的傳感策略是基于熒光體(供體)和猝滅劑(受體)之間的能量共振轉移(FRET)[10]。然而,傳統的基于熒光生物傳感的方法需要在DNA鏈上修飾兩種或更多的猝滅劑以降低背景信號。因此,尋找不含標記物或含有較少標記物的熒光染料或猝滅材料是適配體的發展方向。
近幾年,納米技術取得飛速發展,納米材料也成為很有發展前景的生物分析材料。石墨烯是一種單層碳原子通過sp2雜化形成二維蜂窩狀點陣結構的二維碳納米材料[11-12],這種特殊的單層碳原子結構決定石墨烯材料具有特別的物理和化學性質[13-14]。同時石墨烯特殊的結構決定其可與生物大分子尤其是DNA分子相互作用,從而為構建新型化學和生物傳感器奠定了基礎。研究發現,單鏈DNA和雙鏈DNA在石墨烯上具有不一樣的結合能力,而且石墨烯可以作為優異的能量或電子受體猝滅發光材料的熒光[15-16],由此可以選擇性的吸附和猝滅有熒光標記的單鏈(ss-)DNA探針。其作為猝滅劑的優點包括無需標記到DNA上,長距離熒光猝滅效應,低背景噪聲等[17]。因此如果能以石墨烯作為新的信號傳導基體,無疑將為目標物的快速、高靈敏和高通量檢測提供新的思路。
本實驗利用石墨烯對單鏈DNA和雙鏈DNA不一樣的連接能力,以及其優異的熒光猝滅能力,結合適配體錯配原理,設計開發了C-Ag+-C和石墨烯的新型熒光傳感器用于快速和高靈敏檢測Ag+。
1 材料與方法
1.1 材料
1.1.1 材料及來源 硝酸銀(AgNO3),氫氧化鈉(NaOH):分析純,北京化工廠(北京);氧化石墨烯(GO):先豐納米科技有限公司(南京);熒光基團FAM修飾的Ag+適配體:DNA探針(SSO-FAM,5'-FAM-CTC TCT TCT CTT CAT TTT TCA ACA CAA CAC AC-3',該 探 針 設 計 參 考 了Ono等[18],Wen等[19]的研究),上海生工生物科技有限公司(上海);HEPES:4-羥乙基哌嗪乙磺酸;N-(2-羥乙基)哌嗪-N’-2-乙烷磺酸,1M溶液,Mediatech公司(美國);SDS:十二烷基硫酸鈉,≥95.0%,拜爾迪生物技術有限公司(北京)。
1.1.2 儀器 F-7000熒光分光光度計(Hitachi,日本);pH計(梅特勒-托利多儀器有限公司,中國);CF16RX II離 心 機(Hitachi,日 本);MTC-100恒溫混勻儀(南京戶川電子,中國);超純水:Barnstead,NANOpure Dlamond,≥18.2MΩ。
1.1.3 溶液配制 0.5 g/L的GO溶液:稱取0.25 g GO,用超純水定容至500 mL,以200 W的功率超聲4 h以上(控制溫度不超過40℃)(溶液在使用前需再超聲10 min)。
1 μmol/L的SSO-FAM溶液:先將引物以12 000 r/min離心2 min,加入35 μL的超純水定容,配成100 μmol/L的儲備液,使用時再稀釋到合適濃度。
100 μmol/L和1 μmol/L的AgNO3溶液:準確稱取AgNO3粉末1.698 7 g,加少量超純水溶解,定容至10 mL,混合均勻,濃度即為100 mol/L。
1 mol/L的NaNO3溶液:稱取NaNO3粉末8.499 g,取少量水溶解,定容至100 mL濃度即為1 mol/L。
1 mol/L的HEPES溶液:購得。
1.2 方法
1.2.1 可行性分析 分別測試SSO-FAM體系,SSOFAM-GO體系,以及在SSO-FAM-GO體系下加入不同濃度Ag+的熒光強度。
1.2.2 GO超聲時間優化 GO溶液對SSO的猝滅效率有至關重要的作用,影響Ag+檢測的信噪比,是實現Ag+檢測的關鍵因素。本實驗將不同濃度的GO溶液在超聲0 min、10 min和30 min后加入SSOFAM溶液中,測定其熒光強度,并計算熒光猝滅效率。
1.2.3 SSO-FAM和GO反應時間優化 SSO-FAM和GO的反應時間會的熒光信號產生影響,將終濃度為10 nmol/L的SSO-FAM溶液和10 mg/L的GO溶液的反應時間設置為0 min、10 min、20 min、30 min、40 min,檢測熒光強度,觀察反應時間對GO熒光猝滅效率的影響。
1.2.4 SSO-FAM與GO溶液反應用量的優化 選取3組不同比例的SSO-FAM溶液和GO溶液,第1組為終濃度10 nmol/L的SSO-FAM溶液和10 mg/L的GO溶液,第2組為終濃度20 nmol/L的SSO-FAM溶液和10 mg/L的GO溶液,第3組為終濃度20 nmol/L的SSO-FAM溶液和20 mg/L的GO溶液,將不同濃度的Ag+加入上述3組溶液中,測定熒光強度。
1.2.5 Ag+的檢測方法 將20 μL 1 μmol/L的DNA探針溶液與0-800 nmol/L不同濃度梯度的Ag+溶液混合均勻,將10 μL 1 mol/L HEPES溶液和50 μL 1 mol/L的NaNO3溶液加入上述溶液中,定容體積為1 mL,pH 7.10,37℃下避光反應20 min,生成C-Ag+-C的復合物。然后再加入終濃度為20 mg/L的GO,混合反應10 min,以494 nm的激發波長檢測熒光信號。
1.2.6 其他金屬離子的干擾測定 保持反應條件不變,將1 μmol/L Cd2+、Pb2+、Hg2+等金屬離子作為干擾離子加入樣品中,檢測各金屬離子的熒光強度。
1.2.7 Ag+的加標回收試驗 使用熒光分光光度計檢測200-500 nmol/L不同濃度梯度的Ag+溶液的熒光強度,根據樣品濃度與測得的熒光強度建立Ag+標準曲線;使用飲用水配制樣品溶液,并將一定濃度的Ag+加入樣品中,檢測加入Ag+后樣品的熒光強度,結果與標準曲線的熒光信號對照,計算樣品加標回收率。
2 結果
2.1 可行性分析
為了證明該傳感器設計的合理性,我們考察了各體系的熒光光譜。如圖1所示,當體系中不存在Ag+時,SSO修飾的FAM熒光被一定量的石墨烯完全猝滅,表明單鏈DNA與石墨烯之間存在π-π作用力;當Ag+存在時,該體系表現出較強的熒光,說明Ag+能夠與兩個胞嘧啶堿基結合,使SSO折疊成為穩定的分子內C-Ag+-C雙鏈結構,減弱了與石墨烯之間的作用力,從而使該體系的熒光得到恢復,并且加入濃度越高,熒光恢復強度越大,由此證明Ag+檢測的可行性。
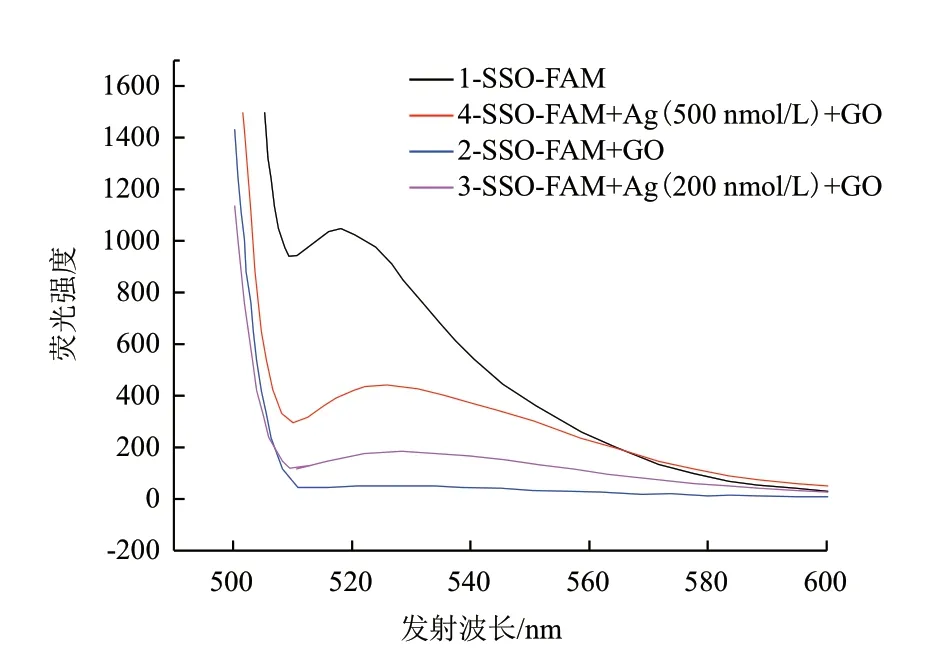
圖1 不同條件下SGI的熒光強度
2.2 GO超聲時間優化結果
實驗對比了不同濃度的GO溶液在不同超聲時間下對SSO-FAM的猝滅效率的影響。結果如圖2所示。未經超聲處理的GO溶液,即使增加溶液的濃度到30 mg/L時,其猝滅效率依然低于30%;當GO經過分別10 min和30 min超聲處理后,10 mg/L的GO添加量就可達到95%的猝滅效率,說明GO在使用前需要進行10 min以上的超聲處理。
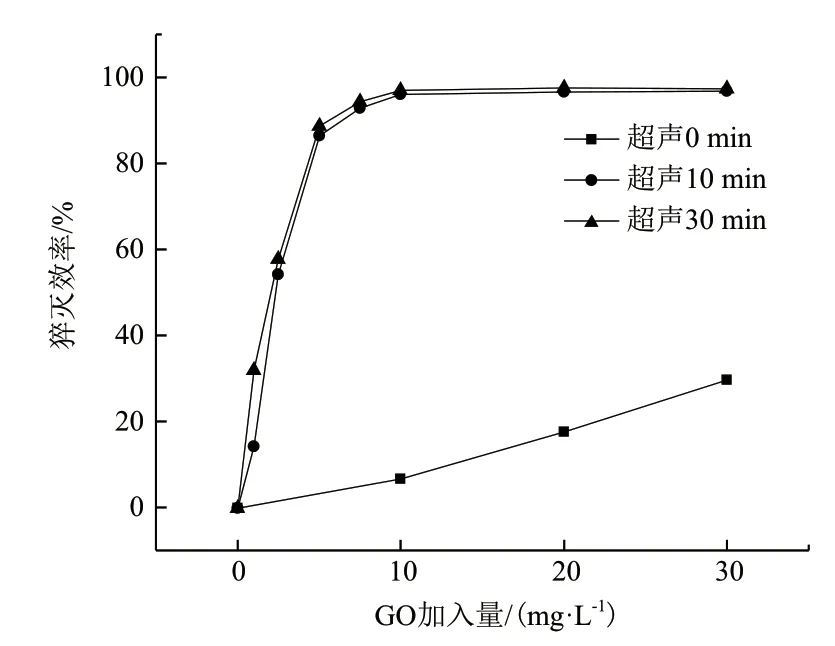
圖2 GO超聲時間對其熒光猝滅效率的影響
2.3 SSO-FAM和GO反應時間優化結果
將 10 nmol/L的DNA探針溶液和10 mg/L的氧化石墨烯溶液設置0-40 min的反應時間,觀察熒光猝滅效果,結果如圖3所示。實驗結果表明,DNA探針溶液和氧化石墨烯溶液的熒光強度隨著反應時間的增加而下降,20 min后熒光強度出現回升,40 min與10 min處的熒光強度基本相同,說明Ag+與SSO錯配反應充分。因此,本實驗的反應時間設定為10 min。
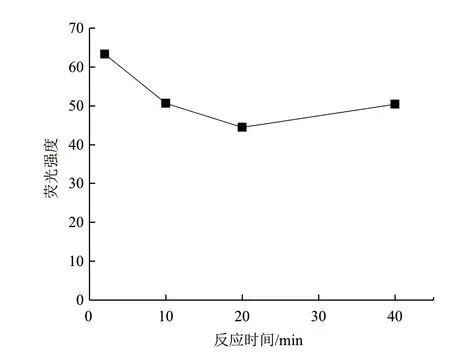
圖3 反應時間對GO熒光猝滅效率的影響
2.4 SSO-FAM與GO溶液反應用量的優化結果
考察了3組比例不同的DNA探針溶液和石墨烯溶液對Ag+熒光測試的影響,結果如圖4所示。其中,曲線1為10 nmol/L的DNA探針溶液和10 mg/L的石墨烯溶液的混合溶液。在加入的Ag+濃度低于100 nmol/L時,檢測出的熒光強度出現下降,加入的Ag+濃度超過100 nmol/L時,樣品的測試值出現上升,但穩定性差,并且上升緩慢;曲線2為20 nmol/L的DNA探針溶液和10 mg/L的石墨烯溶液的混合溶液,在加入的Ag+濃度低于200 nmol/L時,測試出的熒光強度不斷下降,這是由于石墨烯的用量不足未能將熒光完全猝滅,當添加的Ag+濃度超過200 nmol/L后,檢測出的熒光強度隨著Ag+濃度上升;曲線3為終濃度20 nmol/L的DNA探針溶液和20 mg/L的石墨烯溶液的混合溶液,熒光強度從50 nmol/L開始出現逐漸上升的趨勢,當Ag+濃度大于800 nmol/L后,檢測出的熒光強度逐漸趨于穩定。根據3組實驗的實驗結果,曲線3的樣品信噪比低,且檢測的線性范圍最寬,因此實驗選用20 nmol/L的DNA探針溶液和20 mg/L的石墨烯溶液作為最佳比例的反應用量。
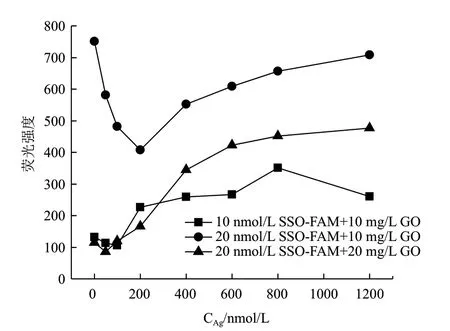
圖4 SSO濃度對Ag+檢測的影響
2.5 Ag+的檢測結果
在最優的條件下,熒光增強強度與Ag+濃度在150 nmol/L-400 nmol/L濃度范圍呈線性相關(圖5),校正曲線方程為F= 0.917 3CAg-80.006,相關系數為0.991,按照IUPAC定義的檢出限(LOD)計算方法求得檢出限(3 σ)為23 nmol/L。
2.6 其他金屬離子的干擾測定
為了驗證本方法適用于復雜水體中的Ag+濃度的測試,通過實驗測試了幾種常見的金屬離子在本方法下的熒光強度響應。將1 μmol/L的Fe3+、Zn2+、Mg2+、Pb2+、Co2+、Ni2+、Cd2+、Hg2+、Ca2+、Mn2+和Cu2+加入DNA探針與石墨烯的混合體系中,保持其他的方法不變,檢測不同金屬離子的熒光強度,結果如圖6所示。200 nmol/L的Ag+的樣品熒光強度為240,其他金屬離子的熒光強度都低于50,不足Ag+的1/10。結果顯示,本方法對于Ag+具有特異性,適用于復雜水體。
2.7 樣品Ag+加標檢測
進一步將該探針用于自來水中Ag+的檢測,該樣品中未檢測出Ag+,向這些樣品中加入300 nmol/L的Ag+,其回收率為96.6%,證明該方法對于實際樣品分析具有一定的指導意義。
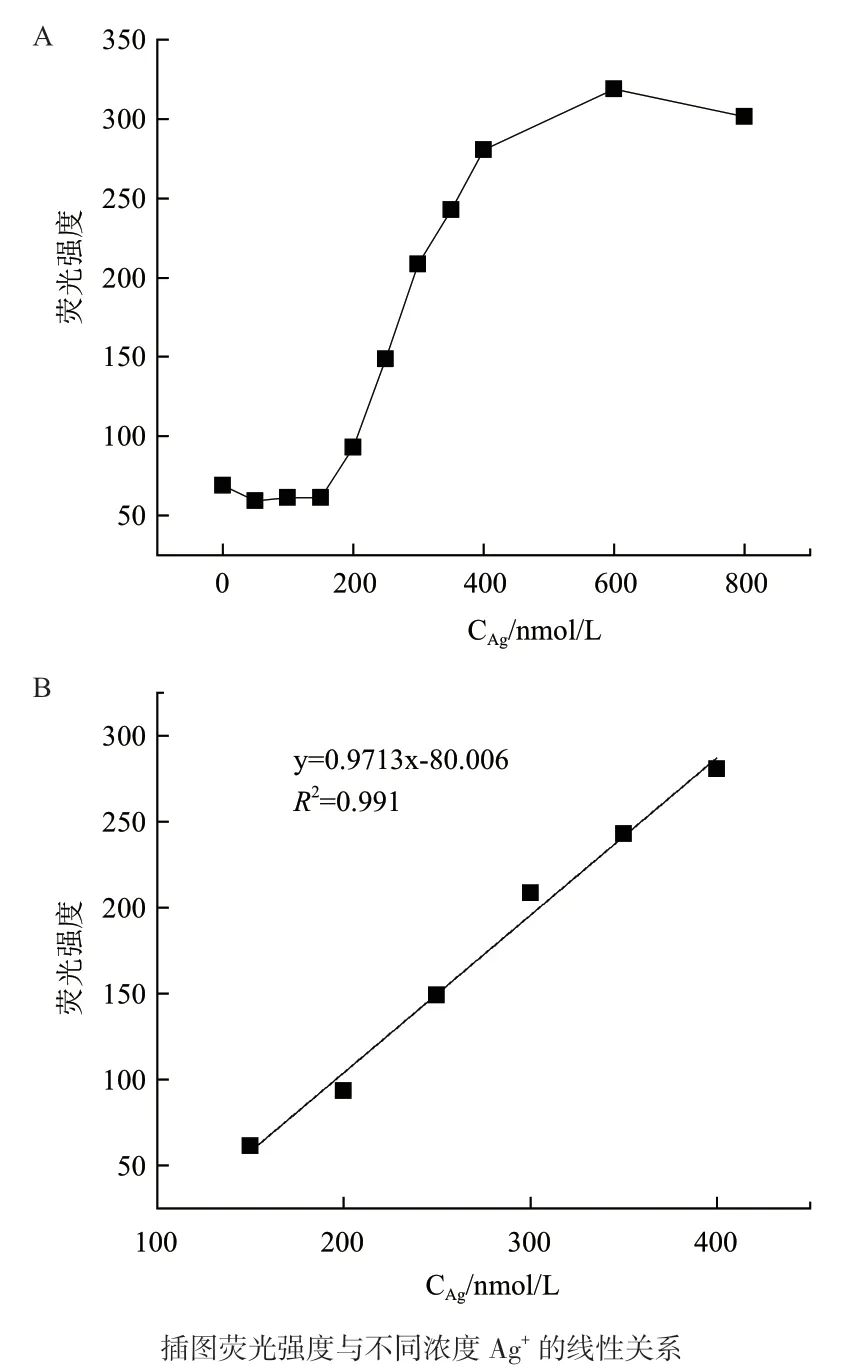
圖5 不同濃度Ag+對應的熒光強度
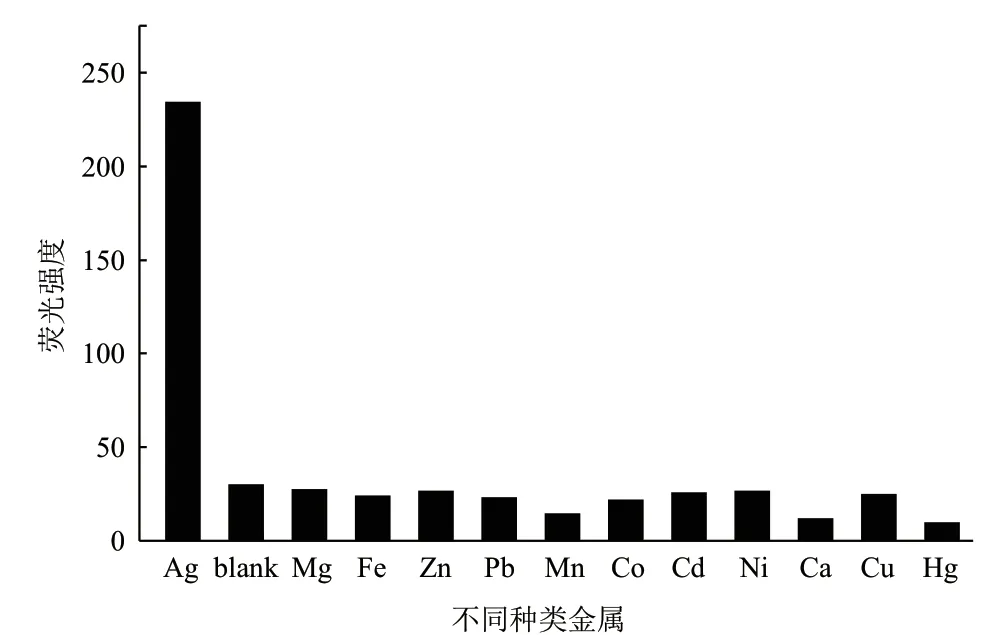
圖6 選擇性分析
3 討論
有些核酸探針的信號單元同時包括了染料分子和納米材料,這類探針稱為核酸-染料/納米探針[23]。該探針多數是通過染料分子和納米材料之間的FRET效應實現的。以石墨烯納米材料為例,如Yang課題組首先利用石墨烯對單鏈DNA和雙鏈DNA吸附能力的不同,實現了DNA分子的檢測[16]。檢測機理如下:染料標記的單鏈DNA探針可以通過π-π作用力與石墨烯結合,從而拉近染料和石墨烯之間的距離,導致二者發生能量共振轉移,染料熒光發生猝滅,當目標物DNA存在時,可以與探針分子雜交形成雙鏈DNA,從而減弱了核酸與石墨烯之間的作用力,阻礙了能量共振轉移的發生,體系熒光得以恢復[24]。本研究傳感原理,如圖7所示,重金屬離子可與特定的基因序列發生作用[25],當體系中無Ag+存在時,由于堿基與石墨烯之間的π-π作用力,單鏈DNA與石墨烯形成石墨烯/單鏈DNA復合物,此時FAM與石墨烯之間發生共振能量轉移或電子轉移,其熒光猝滅。當體系中加入Ag+時,由于Ag+能夠選擇性的與兩個胞嘧啶堿基結合,使得DNA發生構型變化折疊成為穩定的分子內C-Ag+-C雙鏈結構[26],由于空間位阻的存在,此時加入的石墨烯不會與產物發生相互作用,因此FAM的熒光不能被有效猝滅,因此可以通過傳感器的熒光增強程度對體系中加入的Ag+進行定量檢測[27]。
將本研究結果與利用納米材料和富C堿基DNA探針檢測Ag+的部分已報道研究進行對比,結果如表1所示。可以看出,本實驗方法的線性范圍和檢出限與其他方法相比各有優劣,與同樣使用氧化石墨烯的方法相比,本研究所建立的核酸傳感器對Ag+的檢測線性范圍更大。
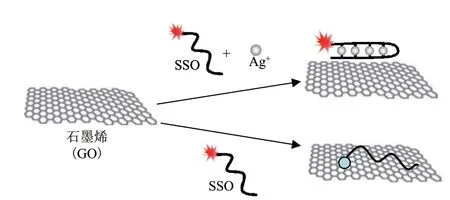
圖7 利用GO和SSO-FAM檢測Ag+的原理示意圖
4 結論
本實驗基于核酸適配體錯配反應的原理,利用SSO-FAM和GO建立了一種對Ag+檢測的方法。使用本方法,在150-400 nmol/L范圍內Ag+濃度和熒光強度檢測值呈線性關系,Ag+的檢測限可達23nmol/L。該方法在飲用水的實驗樣品中Ag+加標檢測的回收率達到96.6%,對飲用水中Ag+含量的檢測具有一定的指導意義。但是該方法線性范圍較窄,并未達到預期結果,在方法設計和實際檢測方面還有待進一步的改進。
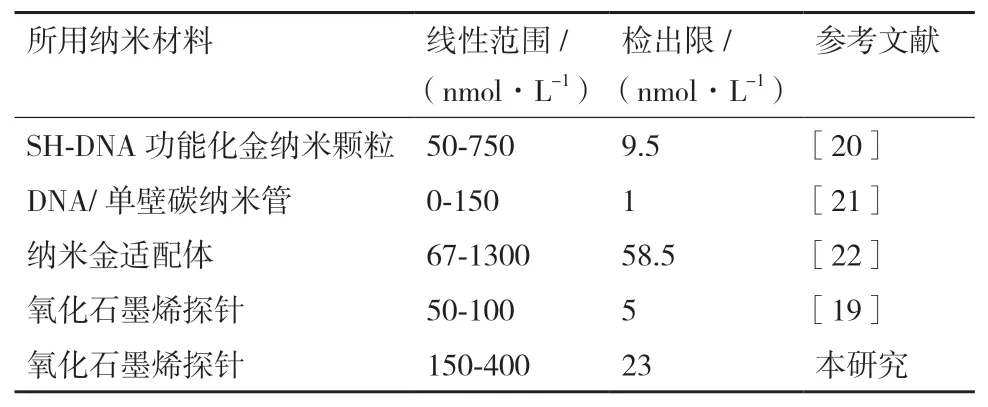
表1 本研究方法與其他方法的性能對比

