不同入路枕部頭皮神經阻滯在乙狀竇后入路開顱手術中的應用
王洪萌, 李敏捷, 林 婷, 林 群
近年來,隨著快速康復理念在臨床中的推廣,神經外科開顱術后的疼痛問題得到越來越多臨床醫生的關注,頭皮神經阻滯作為圍術期多模式鎮痛管理的重要組成部分在開顱術后鎮痛中得到廣泛應用[1]。本研究就不同入路的枕部頭皮神經阻滯在乙狀竇后入路開顱手術圍術期的鎮痛效果進行比較研究。
1 對象與方法
1.1對象 選擇2017年8月—2019年7月筆者醫院神經外科經乙狀竇后入路行聽神經瘤、巖骨背側腦膜瘤、膽脂瘤等橋小腦角區病變的神經外科顯微手術患者40例,根據美國麻醉醫師協會(American Society of Anesthesiologists,ASA)標準,所有患者術前病情評估為ASA Ⅰ~Ⅲ級。將患者以1∶1的比例根據隨機數字表法分成經典入路組(C組,n=20)和頭下斜肌入路組(O組,n=20)。術前所有患者在麻醉評估時,均行0~10 cm標尺的視覺模擬評分(visual analogue scale,VAS)法、術后疼痛緩解的圖像表現及Ramsay鎮靜評分的宣教。如果患者存在以下情況則在排除之列:不能理解和無法完成VAS和Ramsay鎮靜評分,對局麻藥過敏,阻滯部位有明顯感染,高血壓及術后需留置氣管導管行機械通氣的患者。
本研究經福建醫科大學附屬第一醫院倫理委員會審批通過,患者簽署知情同意書。
1.2方法
1.2.1麻醉方法 患者入室后連接多功能監護儀(Datex Ohmeda s/5型),常規監測無創血壓(blood pressure,BP)、血氧飽和度(saturation of pulse blood oxygen,SpO2)、心電圖(electrocardiograph,ECG)及腦電雙頻指數(bispectral index,BIS)。開放外周靜脈連接輸液,隨后在局麻下行橈動脈并監測有創動脈血壓(artery blood pressure,ABP)。所有患者誘導前均予靜脈輸注乳酸林格氏液10 mL/kg,以預防麻醉誘導所致的血容量相對不足而引起的低血壓,隨后推注舒芬太尼(0.2 μg/kg)、順式阿曲庫銨(0.5 mg/kg)、丙泊酚(1.5~2.5 mg/kg)行麻醉誘導,當BIS值達40~60時,行氣管插管;氣管插管后行機械通氣,潮氣量8~10 mL/kg,呼吸頻率13 min-1,維持呼氣末二氧化碳分壓(partial pressure of end gas carbon dioxide,PetCO2)在30~40 mmHg(1 mmHg=133.3 Pa)。插管完成后,兩組患者根據分組情況分別行彩色多普勒超聲(SKK24-S6 XK9/1,美國索諾聲公司)引導下不同入路的枕部頭皮神經阻滯,所有患者均采用0.5%羅哌卡因+腎上腺素(1∶200 000)行神經阻滯。
1.2.2阻滯方法 (1)經典方法:在上項線水平觸及枕動脈搏動,消毒皮膚后,將線陣高頻探頭橫向置于枕動脈搏動點,枕大神經緊靠枕動脈,超聲影像上可以看到圓形或者卵圓形低回聲類似血管組織影,但其不易被探頭壓扁,神經定位完成后,用神經刺激針采用平面內穿刺方法穿刺,當針尖接近神經時,仔細回抽后,注入4 mL局麻藥,注射完畢,拔除針尖并壓迫穿刺部位防止血腫形成(圖1A);向側方、稍下方移動針尖,在胸鎖乳突肌的表面可以直接阻滯枕小神經和若干枕大神經淺支,同樣在仔細回抽后注入4 mL局麻藥(圖1B)。(2)頭下斜肌入路法:皮膚消毒后,將線性高頻超聲探頭置于頭下斜肌長軸方向,頭下斜肌可在超聲影像中顯影,頭半棘肌就在其上方,枕大神經就在兩者之間。神經定位完成后,使用神經刺激針在超聲引導下采用平面內穿刺法穿刺,當針尖接近神經時仔細回抽后注入4 mL局麻藥,之后拔除針尖并壓迫穿刺部位防止血腫形成(圖2A);向側下方移動探頭,定位于胸鎖乳突肌后緣中點,枕小神經表現為低回聲橢圓形結構,行走于胸鎖乳突肌和頭夾肌之間的筋膜層,同樣采用平面內穿刺法,仔細回抽后注入4 mL局麻藥(圖2B)。
1.2.3麻醉維持 患者均予持續輸注瑞芬太尼(10 μg·kg-1·h-1)和順式阿曲庫銨(0.5 mg·kg-1·h-1),同時吸入七氟醚維持麻醉。術中根據BIS值調節吸入濃度,以維持整個術中BIS值40~60。如果血流動力學指標心率(heart rate, HR)、平均動脈壓(mean arterial pressure, MAP)升高>20%,則間斷給予舒芬太尼0.05 μg/kg;若下降<20%,則間斷給予去甲腎上腺素0.05~0.1 μg/kg調整血壓。
1.3觀察指標 記錄阻滯和切皮的時間,記錄切皮前(T0),切皮時(T1),切皮后5(T2),10(T3),15(T4),30(T5),60(T6),90(T7),120(T8),150(T9),180 min(T10)的MAP,HR,BIS及呼氣末七氟醚濃度的肺泡最低有效濃度(minimum alveolar concentration, MAC)值。記錄麻醉過程中追加的舒芬太尼用量,記錄麻醉時間(術前插管到術后拔管的時間)和手術時間。術后由對小組分配不知情的研究人員記錄拔管后1,2,4,8,12 h的VAS評分和Ramsay鎮靜評分(Ramsay sedation scale, RSS)。記錄神經阻滯和局麻藥的并發癥。

2 結 果
2.1一般資料 兩組患者之間的性別、年齡、ASA分級、體質量指數(body mass index, BMI)、手術時間、麻醉時間及手術類型差別均無統計學意義(P<0.05)。C組中有5例患者術中切皮做入路分離時需追加舒芬太尼,兩組比較差別有顯著性(P<0.05,表1)。
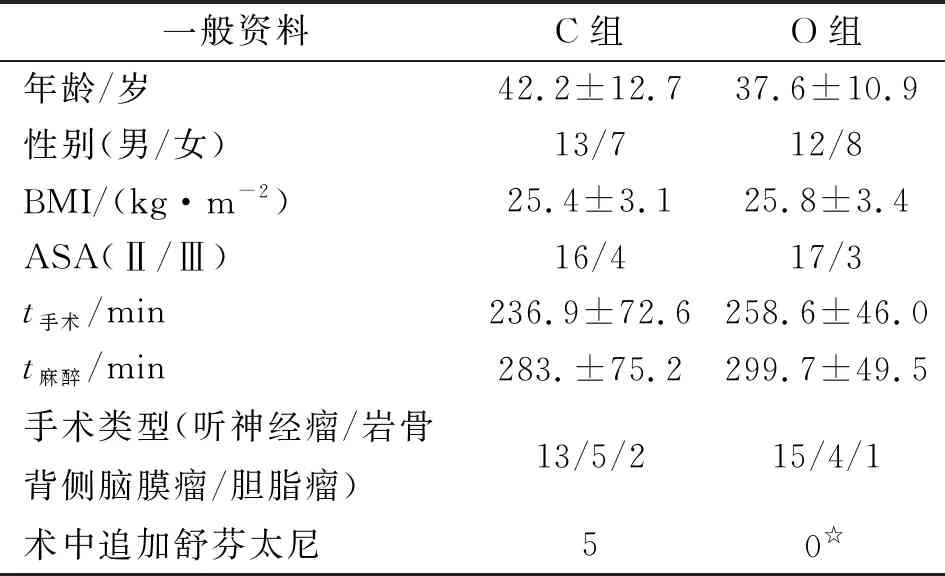
表1 患者一般資料及術中情況的比較
2.2術中血流動力學及MAC 兩組患者的HR和MAP在術中各時點不管是組內還是組間比較均無明顯差異(P<0.05),雖然C組在切皮時心率和血壓較O組有短暫的升高,但兩組的變化相似(表2)。
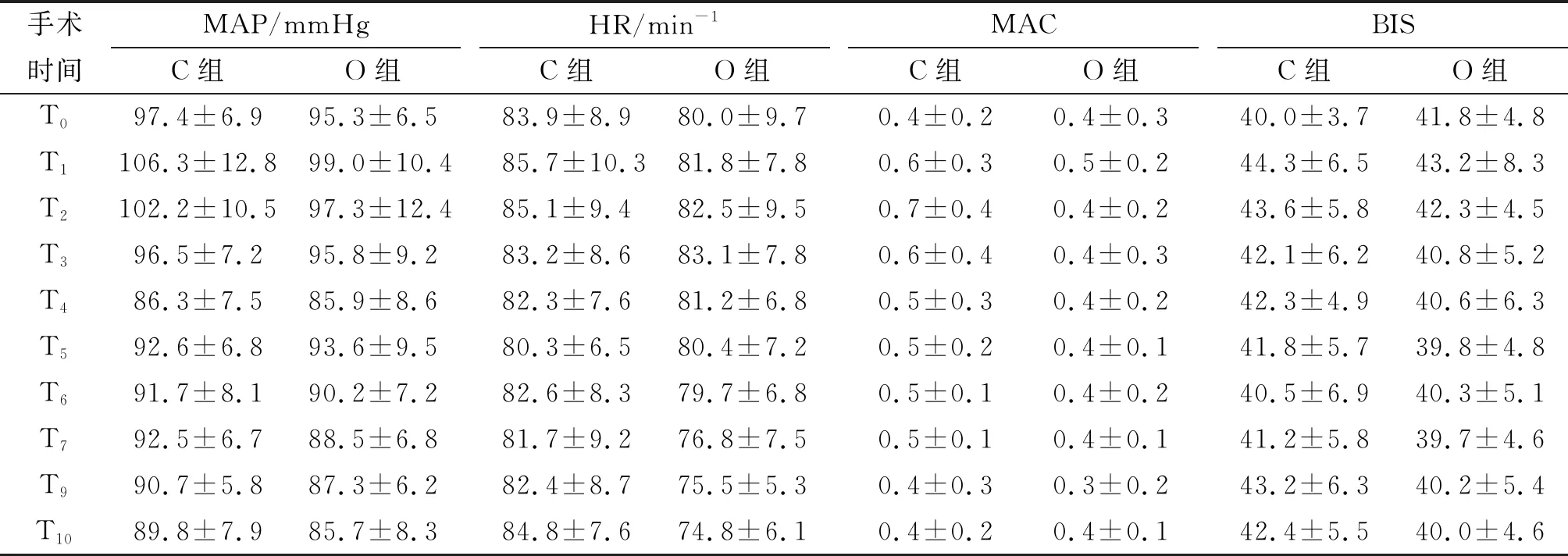
表2 兩組患者術中血流動力學指標、MAC和BIS的比較
2.3疼痛及鎮靜評分 兩組患者術后各時點的VAS評分較術后2 h均逐漸增高(P<0.05),且術后8,12 h C組VAS評分明顯高于O組(P<0.05);兩組患者術后4,8,12 h的Ramsay評分較術后1 h顯著降低(P<0.05),且C組明顯低于O組(表3)。

表3 兩組患者術后VAS和RSS評分
3 討 論
研究表明,近87%的開顱患者術后第一個24 h均遭受不同程度的疼痛[2]。枕后幕下入路的開顱手術較幕上入路常導致更多頸后肌肉的牽拉和損傷,因此圍術期往往需要更多的阿片類藥物來緩解疼痛[3]。然而過量阿片類藥物的應用可能導致嘔吐及通氣不足所致的高碳酸血癥,進一步導致顱高壓的發生從而影響預后[4-5]。經典入路的枕大、枕小神經阻滯能有效減少枕后開顱患者圍術期阿片類藥物的用量,促進血流動力學的平穩且有助于患者快速平穩的術后恢復[6-7]。隨著彩色多普勒超聲在臨床麻醉中的應用,臨床醫師可以在枕后三角的頭下斜肌平面阻滯近心段的枕大、枕小神經,而且也能取得完善的阻滯效果[8]。因此,本研究選擇行乙狀竇后入路聽神經瘤切除術的患者進行兩種入路神經阻滯的對比應用研究。
本研究結果表明,兩種入路的枕大、枕小神經阻滯,在術后<4 h的鎮痛效果沒有明顯差異,但術后8,12 h枕后三角頭下斜肌入路的阻滯方法能提供更好的鎮痛效果。經典入路的枕大、枕小神經,其實就是指傳統頭皮神經阻滯中的枕后兩支。以往研究也表明,頭皮神經阻滯在術后2~6 h能明顯降低患者的疼痛評分,但12 h后并不能起到這種作用[9]。頭皮神經阻滯較快消退的原因主要在于頭皮組織具有豐富的血運,從而導致局麻藥更快被吸收[10]。而在枕后三角,枕大神經行走在頭下斜肌和頭半棘肌間的筋膜中,枕小神經行走在頭夾肌和胸鎖乳突肌間的筋膜間隙中,因此局麻藥能維持更長時間的阻滯作用[11-12]。Kavitha等的研究發現,經上顎的顎大孔能阻滯三叉神經的眼支和上頜支,聯合經典的枕大、枕小神經阻滯能提供與傳統頭皮阻滯(框上、滑車上、耳顳神經阻滯)相似的圍術期鎮痛效果;數據還表明,經顎大孔阻滯能提供更好、更長時間的術后鎮痛,并減少了術中阿片類藥物的補充劑量[13]。這也從側面支持并解釋本研究的結果。
本研究結果還表明,C組中有5例患者術中切皮做入路分離時需追加舒芬太尼,而O組均不需追加舒芬太尼。既往研究表明,手術部位是術后疼痛唯一可靠的確定因素:幕下開顱手術往往比幕上手術更痛苦,術后需要更高的阿片累積劑量,可能是因為手術引起的頸部肌肉群的拉伸和創傷[2]。而乙狀竇入路手術在切口的下部分常將側頸部的淺層肌肉(胸鎖乳突肌和斜方肌)和中間肌層(頭夾肌、頭最長肌和頭半棘肌)與切口一并切開和牽拉。枕后三角的頭下斜肌平面阻滯能在寰樞關節后外側阻滯第二頸椎(C2)脊神經后支的感覺分支枕大神經;在同一水平的胸鎖乳突肌和頭夾肌間阻滯C2脊神經腹側支的感覺分支枕小神經,因此跟經典入路的頭皮神經阻滯相比,頭下斜肌入路能對切口下部分的肌肉起到快速而完善的阻滯效果[14]。
O組枕大、枕小神經阻滯的并發癥常有局麻藥毒性反應、局部血腫、神經損傷、椎動脈內注射及枕骨大孔或椎管內注射等[14],但O組和C組都未發現這些并發癥。頭下斜肌入路的枕大神經阻滯目前比較常用于頭頸部疼痛的治療,本研究也證實其能很好地運用于枕后幕下開顱手術圍術期的疼痛管理。但本研究存在一定的局限性,包括樣本量小,選擇的開顱手術類型比較局限等。
筆者認為,頭下斜肌入路的枕大、枕小神經阻滯能為枕后入路開顱手術提供更長時間的術后鎮痛,并能減少術中頭皮切開時舒芬太尼的用量。因此,在行經乙狀竇后入路的聽神經瘤、巖骨背側腦膜瘤、膽脂瘤等橋小腦角區病變的神經外科顯微手術時,可優先選擇頭下斜肌入路的枕大、枕小神經阻滯作為枕部頭皮神經阻滯的方式。

