新輔助化療聯合手術治療ⅢA-N2期非小細胞肺癌臨床療效觀察
魏玉磊,劉騰飛,韓媛媛,袁偉,王宇琛,鄭茂東,董躍華,張振明
河北北方學院附屬第一醫院,河北張家口075000
非小細胞肺癌是臨床最為常見的肺癌類型,臨床首選外科治療[1]。但是很多患者確診時已處于疾病晚期,單純外科手術治療容易復發轉移,遠期預后較差。ⅢA-N2期非小細胞肺癌是一組范圍廣泛的疾病,占到初診的非小細胞肺癌的30%~40%,其治療方案及和預后存在較大差異,治療模式一直存在爭議[4]。美國國立綜合癌癥網絡(NCCN)2015年第1版推薦[2]該類患者(T1~3N2M0,ⅢA)的治療方法為新輔助化療/化放療輔以手術切除。本研究觀察了新輔助化療聯合手術治療ⅢA-N2期非小細胞肺癌的臨床療效,現將結果報告如下。
1 資料與方法
1.1 臨床資料 選取河北北方學院附屬第一醫院2015年1月~2017年12月收治的ⅢA-N2期非小細胞肺癌患者77例,即術前臨床分期為cT1~3N2M0。納入標準:①術前經病理學或細胞學檢查確診的非小細胞肺癌;②初治患者;③可手術切除的;④系統查體排除轉移可能;⑤預計生存時間超過6個月;⑥重要臟器功能無嚴重異常;⑦患者體力狀況評分為0~2分;⑧堅持隨訪;⑨簽署知情同意書,并經醫院倫理委員會審核通過。排除標準:①入院前接受過任何抗腫瘤相關治療;②有遠處轉移者;③合并嚴重的全身疾病。77例患者依據治療方式的不同分為觀察組(40例)、對照組(37例)。觀察組男22例、女18例,年齡(61.4±10.5)歲,鱗癌16例、腺癌20例、其他4例;對照組男21例、女16例,年齡(60.9±10.2)歲,鱗癌15例、腺癌19例、其他3例;兩組患者的一般資料具有可比性(P均>0.05)。
1.2 新輔助化療聯合手術方案 觀察組治療方案:新輔助化療聯合手術治療。患者行TP方案(紫杉醇+卡鉑)或GP方案(吉西他濱+順鉑)或PP方案(培美曲塞+順鉑)化療,3周后重復,共化療2次。化療的同時給予輔助用藥(地塞米松、胃復安和恩丹司瓊等)治療。化療結束后3~5周時,進行化療效果評估(頭腹CT、胸部強化CT及骨ECT等),若病情無明顯進展或轉移,行手術治療。若患者病情明顯進展或轉移,改為其他方法治療。對照組治療方案:手術治療。全部患者手術方式均為開放手術后外側入路,肺葉或全肺切除或姑息手術,加系統肺門和縱膈淋巴結清掃(縱膈淋巴結清掃站數≥3,并至少清掃1站肺內淋巴結)。兩組患者術后給予常規輔助化療4~6個周期,具體根據患者身體情況調整。對切緣陽性的患者同時輔以放療。術后標本送病理科進行檢查,確定病理分型和分期,并確定淋巴結的數量及轉移情況。
1.3 觀察組新輔助化療療效評價、腫瘤降期和不良反應觀察 ①根據實體瘤評價標準[3](RECIST1.1)對觀察組患者進行新輔助化療療效評價,分為完全緩解(CR)、部分緩解(PR)、疾病穩定(SD)、疾病進展(PD),計算客觀緩解率(ORR)。CR為病灶瘤體消失,PR為病灶直徑縮小≥30%,SD為病灶直徑縮小<30%或增大<20%,PD為病灶直徑增大≥20%。ORR=(CR+PR)/觀察組人數。②新輔助化療前依據強化CT所見病灶大小確定臨床T分期、N分期,術后根據病理結果確定病理T分期、N分期,對比臨床分期和病理分期變化情況,確定降期人數,計算T降期率、N降期率。T降期率=T分期降期人數/觀察組人數×100%。N降期率=N分期降期人數/觀察組人數×100%。③觀察并記錄觀察組患者新輔助化療的不良反應,包括白細胞減少、血紅蛋白減少、血小板減少、惡心嘔吐、腹瀉,依據WHO化療不良反應標準分為0~Ⅳ級。
1.4 兩組手術指標、術后并發癥、淋巴結轉移情況觀察 記錄并比較兩組手術時間、術中出血量、R0切除率(切除后顯微鏡下無殘留)等手術指標,記錄并比較兩組術后肺部感染、胸腔積液、肺不張、肺部感染等并發癥情況,記錄并比較兩組術后清掃淋巴結總數量、轉移淋巴結數量、病人轉移率、淋巴結轉移率。病人轉移率=淋巴結轉移患者數/患者總數×100%。淋巴結轉移率=轉移淋巴結數量/清掃淋巴結總數量×100%。
1.5 兩組癌組織中Ki-67陽性表達率測算 采用免疫組化SP法。取術后癌組織病理,常規進行免疫組化染色,200倍顯微鏡下隨機選取10個視野觀察,Ki-67陽性表達細胞在顯微鏡下表現為細胞核中出現棕黃色顆粒,Ki-67陽性表達細胞比例>20%判定為Ki-67陽性表達,計算Ki-67陽性表達率。Ki-67陽性表達率=Ki-67陽性表達細胞/細胞總數×100%。
1.6 兩組術后隨訪及生存分析 兩組患者術后均通過門診復查或電話隨訪,隨訪時間3~42個月,平均隨訪時間23.2個月,截至2018年12月31日。以總生存期(OS)和無進展生存期(PFS)作為研究終點,采用Kaplan-Meier法對兩組患者進行生存分析。
2 結果
2.1 觀察組新輔助化療療效、腫瘤降期和不良反應情況 觀察組40例患者接受新輔助化療2個周期后,CR 3例,PR 18例,SD 17例,PD 2例,ORR為52.5%,T降期率為35%,N降期率為42.5%,說明新輔助化療可以使腫瘤和淋巴結減小,使腫瘤分期降期。40例患者中出現PD 2例,放棄手術給予其他治療,38例患者接受手術治療。40例患者中,不良反應以Ⅰ、Ⅱ級為主,8例出現Ⅲ級不良反應,但經過治療后,基本恢復,未影響下一步治療,提示本研究中的新輔助化療方案不良反應較小,具有良好的安全性。觀察組新輔助化療的不良反應情況見表1。
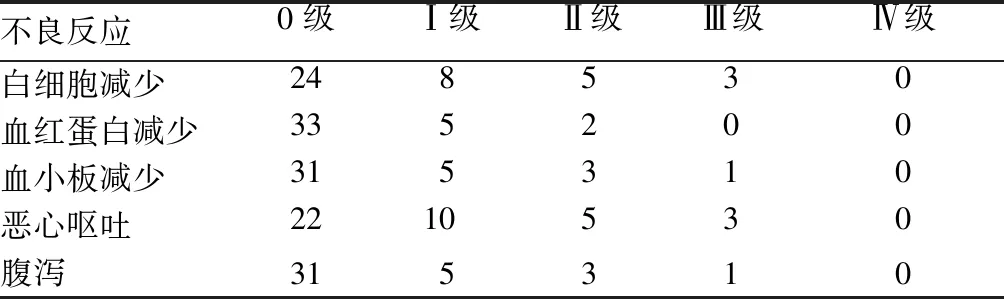
表1 觀察組新輔助化療的不良反應情況(例)
2.2 兩組手術指標、術后并發癥、淋巴結轉移情況比較 觀察組手術時間(163±62)min、術中出血量(237±102)mL、R0切除率86.8%(33/38)、術后并發癥8例,對照組手術時間(175±65)min、術中出血量(244±106)mL、R0切除率67.6%(25/37)、術后并發癥6例,其中兩組R0切除率相比,P<0.05,說明新輔助化療聯合手術治療基本是安全的,且具有更高的RO切除率。
觀察組38例患者清掃淋巴結總數量為755個、轉移淋巴結數量為135個、淋巴結轉移率為17.9%、病人轉移率為89.5%,對照組37例患者清掃淋巴結總數量為800個、轉移淋巴結數量為176個、淋巴結轉移率為22.0%、病人轉移率為100%,其中兩組轉移淋巴結數量、淋巴結轉移率、病人轉移率相比,P均<0.05。
2.3 兩組癌組織中Ki-67陽性表達率比較 觀察組癌組織中Ki-67陽性表達率為42.1%(16/38),對照組為67.6%(25/37),兩組相比,P<0.05。
2.4 兩組生存情況比較 觀察組術后1、2、3年的總生存率分別為89.5%、76.1%、57.4%,中位OS是36.5個月;對照組術后1、2、3年的總生存率分別為86.5%、56.1%、20.1%,中位OS是26.4個月;兩組相比,P均<0.05。
觀察組術后1、2、3年的無進展生存率分別為76.3%、43.4%、18.6%,中位PFS是21.2個月;對照組術后1、2、3年的無進展生存率分別為54.1%、24.0%、6.0%,中位PFS是15.1個月;兩組相比,P均<0.05。
3 討論
ⅢA-N2期非小細胞肺癌是一組范圍廣泛的疾病。美國胸內科醫師協會(ACCP)臨床診療指南根據N2狀態將其分成4類[5],其中ⅢA1期是指手術后進行病理檢查時發現N2淋巴結陽性病例;ⅢA2期是指術中發現切除最后病理證實的單站N2陽性;ⅢA3期是指術前影像學、縱膈鏡或淋巴結活檢確診的單站或多站N2腫大淋巴結,最終術后病理證實;ⅢA4期是指巨塊或固定融合的多站N2陽性淋巴結。由于ⅢA-N2期非小細胞肺癌包含廣闊,尚無具體治療指南,其治療方案多由治療者臨床經驗決定,造成其預后差異巨大。ⅢA-N2期非小細胞肺癌單純手術治療難以達到理想治療目的,術后具有較高復發和轉移風險,其最合理的治療模式仍在探索中[5~7],許多研究開始引入新輔助化療治療ⅢA-N2期患者。新輔助化療治療多種晚期腫瘤具有以下特點:①新輔助化療能夠縮小原發病灶,降低腫瘤的臨床與病理分期;②增加腫瘤與正常組織以及轉移淋巴結和血管及周圍組織間隙,從而提高手術切除率;③通過減少和消滅微轉移灶而提高長期生存率;④能夠評價機體對化療藥物敏感性和后續最佳化療藥物選擇提供幫助。
國內外研究[2,8,9]顯示,肺癌新輔助化療的臨床有效率為25%~74%,病理降期率為19%~67%。本研究顯示,新輔助化療的ORR是52.5%,T降期率是37.5%,N降期率是40%,與以往研究結果相仿。觀察組40例ⅢA-N2期非小細胞肺癌患者進行新輔助化療,其中2例因新輔助化療效果不佳而出現PD,其余38例患者進行手術治療,觀察組R0切除率是86.8%,對照組為67.6%,兩組具有明顯差異,而其他手術指標兩組近似,說明新輔助化療可以提高R0切除率。但少部分化療不敏感患者可能造成疾病進展,需引起特別關注,治療前應告知患者及家屬。
縱隔淋巴結轉移是腫瘤患者制定治療方案和預測預后的重要的因素之一[10~12],也是TNM分期系統的重要組成部分。在非小細胞肺癌中,淋巴結轉移患者有較高的疾病復發風險。張善淵等[13]研究顯示,淋巴結轉移率和非小細胞肺癌預后密切相關,低淋巴結轉移率組5年總體生存率為64.1%,高淋巴結轉移率組5年總體生存率為36.7%,顯示淋巴結轉移率是ⅢA-N2期非小細胞肺癌預后的獨立危險因素。在本研究中,觀察組患者轉移淋巴結數量較少,同時具有更低的病人轉移率和淋巴結轉移率,說明新輔助化療一方面減少了轉移淋巴結的數量,另一方面降低了淋巴結轉移概率,減少了轉移風險。
研究[14]顯示,分子標志物Ki-67是與細胞增殖密切相關的核抗原,是目前應用最為廣泛的增殖細胞標記物,廣泛應用于新輔助化療的微觀療效評估。本研究結果顯示,觀察組術后病理標本中Ki-67陽性表達率較對照組明顯降低,說明腫瘤組織經過新輔助化療后,細胞增殖活性被抑制,腫瘤的生長明顯降低。
唐翠萍等[15]研究顯示,新輔助化療組患者與對照組相比具有更低的復發率和更高的中位PFS。本研究顯示,和對照組比較,觀察組具有更高的中位OS和中位PFS,觀察組術后1、2、3 年的總生存率、無進展生存率也更高。Kaplan-Meier生存分析結果顯示,觀察組患者具有更好的OS和PFS,說明新輔助化療能夠改善患者預后和延長生存期。
綜上所述,新輔助化療聯合手術治療ⅢA-N2期非小細胞肺癌是安全有效的,有助于降低術前臨床分期、抑制腫瘤增殖、提高R0切除率、減少淋巴結轉移,進而改善患者預后,最終使患者獲益。

