血脂代謝對COPD頻繁急性加重表型的影響
劉偉良,吳 東,黃 丹,毛偉堅,李 文* (.廣東醫科大學,廣東湛江 540;.廣東醫科大學附屬醫院,廣東湛江 5400;.廣東省茂名市中醫院,廣東茂名 55000)
慢性阻塞性肺疾病(COPD)的特征是持續的氣流受限,通常呈漸進性,并與氣道和肺部對有害顆粒或氣體的慢性炎癥反應增強有關[1]。因為COPD存在持續氣流受限及慢性炎癥,使COPD患者肺功能受到不同程度的損害,所以容易累及全身器官,產生不同的并發癥。一項針對我國人群的研究表明,COPD合并代謝綜合征的總體患病率高達20%[2]。最近的研究表明,脂質代謝的改變在COPD的發病機制中發揮重要作用[3]。在重度和極重度COPD患者中的膽固醇和低密度脂蛋白升高,而高密度脂蛋白降低[4]。目前已經發現促炎癥消退脂類介質如消退素D1(Resolvin D1),可通過控制慢性炎癥減少肺氣腫的發生[5]。脂質代謝途徑和分子在COPD中明顯改變,這些改變反過來調節特定細胞的功能,例如炎癥介質或抗炎介質的產生、免疫調節或細胞死亡,最終影響COPD的發展[6]。COPD急性加重不但加快病情進展,而且增加家庭及經濟負擔。然而,血脂代謝與頻繁急性加重表型的相互作用的研究甚少。因此,本文研究COPD患者的血脂代謝異常對頻繁急性加重表型的影響,旨在對COPD患者的臨床治療提供理論依據。
1 資料和方法
1.1 一般資料
選取廣東醫科大學附屬醫院及茂名市中醫院2017年1月至2020年1月COPD患者146例,均符合以下納排標準。納入標準:(1) 診斷符合COPD全球倡議(GOLD)[7];(2)年齡>40歲;(3)對象意識清楚,無認知障礙。排除標準:(1)支氣管哮喘患者;(2)支氣管擴張、肺結核、彌漫性泛細支氣管炎、閉塞性細支氣管炎、間質性肺病、或近6個月接受肺部手術者;(3)近5 a內新發腫瘤或腫瘤病史,無論有無治療、復發或轉移;(4)正在參與其他臨床試驗或使用試驗藥物者;(5)妊娠或哺乳期婦女;(6)伴嚴重心、肝、腎、血液等疾病的患者;(7)伴有高膽固醇血癥的患者。146例中,男133例,女23例;年齡52~79歲,平均(67.7±7.1)歲;有吸煙史115例;急性加重次數0~10次,平均(1.5±1.6)次;體質指數(BMI)為(20.1±3.6) kg/m2。根據COPD患者過去1 a急性加重次數分為頻繁急性加重表型組與非頻繁急性加重表型組,并將急性加重次數≥2次的患者納入頻繁急性加重表型組(65例),急性加重次數<2次的患者納入非急性加重表型組(81例)。
1.2 方法
1.2.1 病例收集 采用整群抽樣法,通過病例管理系統篩選,收集146例COPD患者臨床資料包括年齡、性別、BMI、文化程度、吸煙史、COPD評估測試量表(CAT)、改良英國醫學研究理事會呼吸困難指數(mMRC)、COPD綜合評估、FEV1%pred、用藥情況及急性加重次數等。其中急性加重次數是通過詢問患者過去1 a內發作時的治療情況而確定,若為住院或使用任何抗生素和/或皮質類固醇激素,則認為急性加重[8]。
1.2.2 診斷及相關定義 COPD診斷標準為吸入支氣管擴張劑后FEV1/FVC<70%,除外其他疾病。急性加重是指導致需要進一步治療的呼吸道癥狀的急性惡化,可分為輕度(僅使用短效支氣管擴張劑治療)、中度(使用短效支氣管擴張劑+抗生素和/或口服皮質類固醇激素治療)和重度 (患者需要住院或急診治療)[7]。
1.2.3 生化指標檢測 所有COPD患者取空腹外周靜脈血3 mL,真空采血管抗凝,充分離心后(無凝塊與纖維),采用羅氏cobas 8000全自動生化分析儀測定COPD患者血脂代謝相關指標,包括總膽固醇(TC,3.1~5.7 mmol/L)、甘油三酯(TG,0.4~2.0 mmol/L)、低密度脂蛋白(LDL,1.80~3.36 mmol/L)、高密度脂蛋白(HDL,1.16~1.55 mmol/L)。
1.5 統計學處理
應用SPSS22.0進行統計學處理,計量資料以±s表示,組間比較采用t檢驗;計數資料采用χ2檢驗,采用二元Logistics回歸方程進行相關性分析。P<0.05為差異有統計學意義。
2 結果
2.1 臨床資料的比較
頻繁急性加重表型組的FEV1%pred低于非頻繁急性加重組(P<0.01),CAT、mMRC、綜合評估高于非頻繁急性加重表型組(P<0.01)。兩組間年齡、性別、吸煙史、文化程度、BMI、藥物史的差異無統計學意義(P>0.05)。見表1。
2.2 血脂水平的比較
頻繁急性加重表型組的TC、LDL低于非頻繁急性加重組(P<0.01或0.05),頻繁急性加重表型組的TG、HDL與非頻繁急性加重組比較,差異無統計學意義(P>0.05)。見表2。
2.3 血脂代謝、綜合評估與頻繁急性加重表型的相關性分析
COPD患者的TC、COPD綜合評估對頻繁急性加重表型有顯著影響,且TC為保護因素(P<0.05)、綜合評估為危險因素(P<0.01)。患者FEV1%pred、LDL 對頻繁急性加重表型無顯著影響。見表3。
3 討論
COPD急性加重是對患者產生重大影響的重要事件,并可能導致住院或死亡。一些經常發作的患者,現在被認為是一個獨特的臨床亞群,即“頻繁急性加重表型”[9]。頻繁急性加重表型是一種加重易感性表型,其特征是不論肺功能嚴重程度如何,患者均容易出現急性加重,且可以通過詢問患者過去1 a內急性加重次數來確定這種易于加重的特殊表型,在3 a內相對穩定[8]。有研究認為,COPD患者過去1 a內急性加重次數可作為COPD急性加重的獨立危險因素[8]。
2011年版GOLD指南更新提出的“ABCD”評估工具,即COPD患者綜合評估,打破了傳統的肺功能分級的評估模式,而GOLD 2017指南中新版綜合評估將肺功能分級與ABCD分組相互獨立開來,強調了疾病癥狀與急性加重風險在指導治療中的重要性。綜合評估包括癥狀評估與急性加重風險評估,有研究表明,CAT評分可用來監測COPD的急性發作,急性加重期患者的CAT評分較穩定期患者評分增加約4.7分[10]。而我們的研究結果顯示頻繁急性發作表型的CAT評分明顯高于非頻繁急性加重表型,但其預測頻繁急性發作表型發生的效能需進一步研究。綜合評估中急性加重風險評估主要根據COPD患者的急性加重病史進行判斷,在過去1 a中急性加重次數≥2次或上1年因急性加重住院≥1 次,表明具有高風險。然而,由于急性加重的診斷依靠臨床癥狀,缺乏客觀標準,且患者對疾病認知不足,個體主觀感受差異大,容易出現不向醫生報告急性加重情況,因此需要發現頻繁急性加重的診斷的生物標志物[11]。
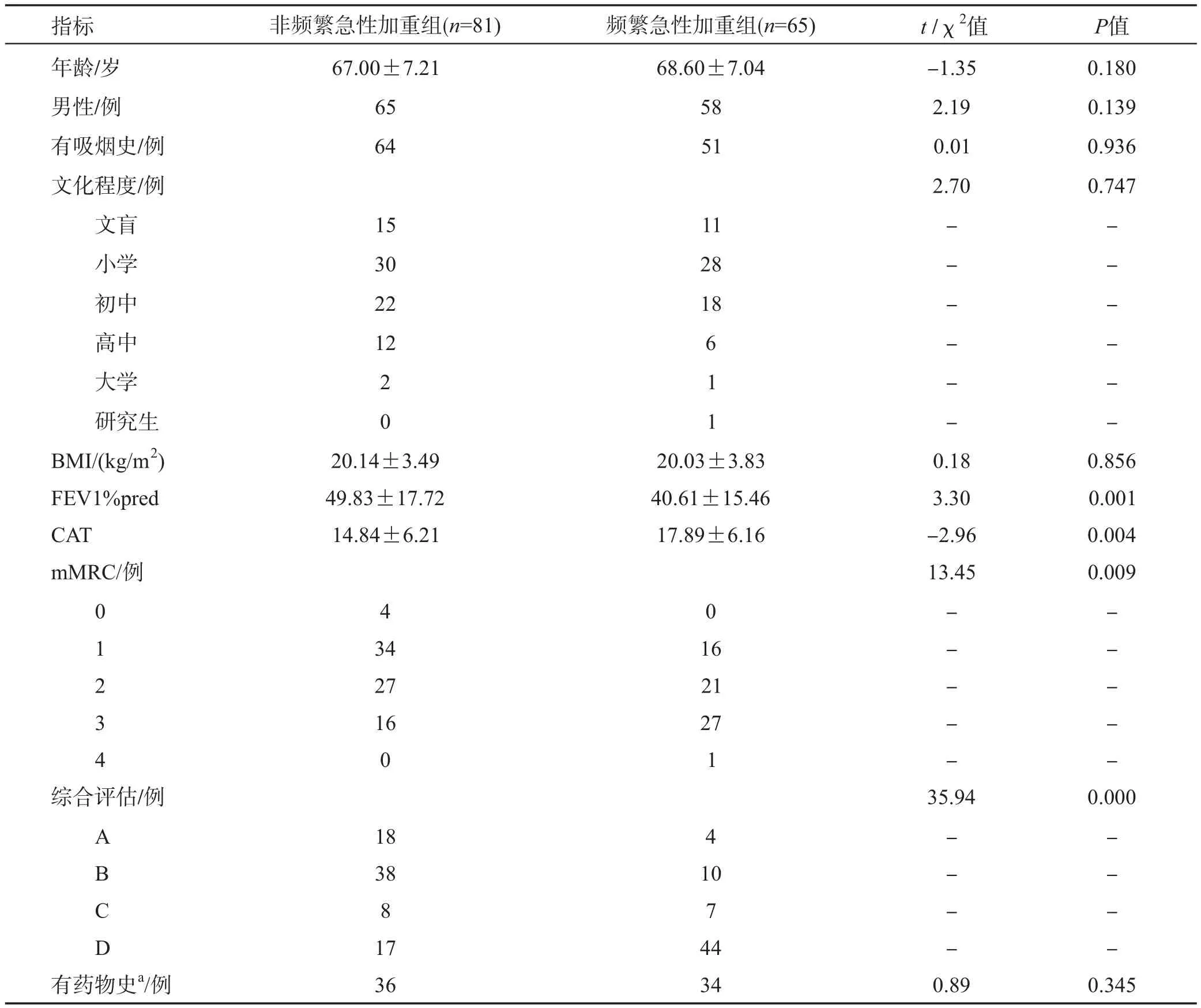
表1 各臨床指標在非頻繁急性加重組和頻繁急性加重組間的差異比較
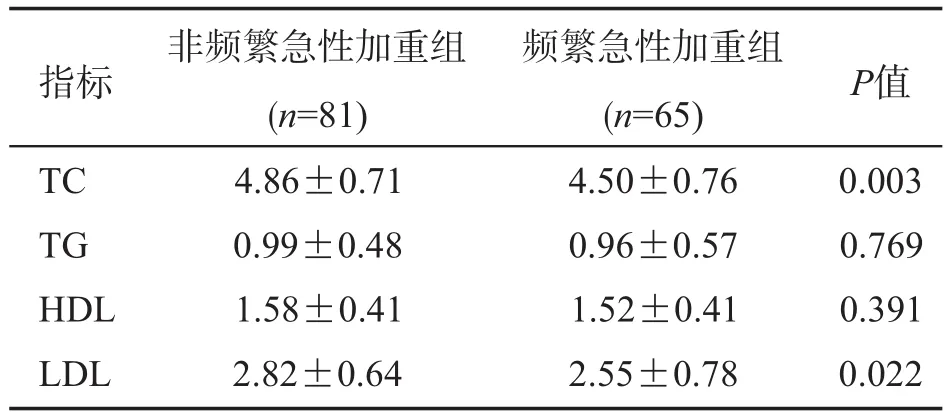
表2 血脂指標在非頻繁急性加重表型組和頻繁急性加重表型組中的差異比較
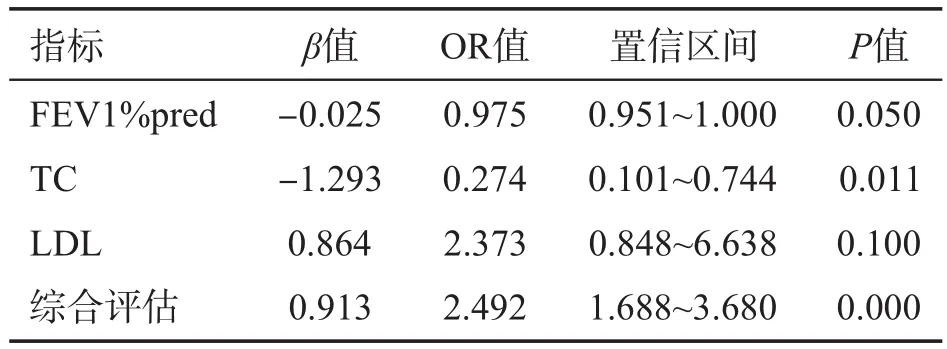
表3 頻繁急性加重表型影響因素相關性分析
血脂代謝異常通常認為是心腦血管疾病的重要危險因素,大約有50%的COPD患者死于心腦血管疾病,但一些研究認為,在各種慢性病狀態中可以觀察到傳統的心血管危險因素與該疾病患者的臨床結果之間存在矛盾關聯。這種矛盾關聯被稱為“逆流行病學”,是指生存結果與傳統心血管危險因素(例如肥胖、高血壓和高膽固醇)之間的自相矛盾和違反常理的流行病學關聯[12]。我們的研究發現,頻繁急性加重表型組的血清膽固醇水平明顯低于非頻繁急性加重表型組,對頻繁急性加重表型的發生有顯著影響。血清膽固醇是一種保護因素,與頻繁急性加重表型的發生呈負相關。由此看來,針對一般人群的膽固醇最佳控制目標可能不適合頻繁急性加重表型COPD患者等特殊人群。然而,目前COPD頻繁急性加重表型的血脂代謝異常的機制尚未十分明確。
近年來,越來越多的研究發現COPD不僅是一種肺部疾病,而且常伴隨許多肺外表現,例如心血管疾病、營養不良、代謝紊亂等[13]。COPD患者中血脂代謝異常的比例逐漸升高[14]。相較于頻繁急性加重表型患者,非頻繁急性加重表型患者的血脂水平更高,其可能的機制為:(1)血脂異常是營養不良的表現形式之一[15],原因是能量消耗增加且攝入減少,可以反映COPD晚期階段的分解代謝狀態;(2)脂肪組織通過釋放多種脂肪因子參與全身性炎癥的發展,具有促炎和抗炎活性的脂肪因子(包括瘦素和脂聯素)調節異常,可能會導致COPD全身性炎癥的發展[16];(3)肺表面活性物質最近被認為在COPD的發病機制中起著重要作用,如維持肺泡結構,由于膽固醇是肺表面活性物質的一種成分,因此有研究認為低膽固醇水平會損害這種功能[17];(4)有研究表明,血清脂蛋白與感染性藥物結合可能有改善內毒素的作用,從而降低AECOPD的嚴重程度。反過來說,高膽固醇水平可能影響COPD患者的長期生存,減少急性發作的次數[17];(5)三磷酸腺苷結合盒轉運體A1(ABCA1)是介導肺組織細胞膽固醇外流的重要途徑,有研究發現,ABCA1抑制COPD患者的氣道平滑肌細胞的增殖和遷移,同時抑制氣道平滑肌細胞釋放IL-6、IL-8、TNF-α等細胞因子[18]。因此,ABCA1通過膽固醇外流方式調節肺部炎癥的同時可能會引起血清膽固醇的升高。
總而言之,COPD是一種異質性疾病,具有不同的發病機制和表型。高脂血癥常常認為是心腦血管疾病的危險因素,但我們的研究發現,血清膽固醇與頻繁急性加重表型的發生呈負相關,因此應從基礎科學到臨床實踐中努力闡明COPD與血脂異常之間的關系。 本研究存在以下不足:一是回顧性研究存在局限性且無法控制的混雜因素會影響結果;二是急性加重次數的評估存在主觀性,容易產生信息偏倚導致結果誤差。上述不足有待日后的研究加以改進。

