碘量法測定青霉素及頭孢菌素中間體7-ACA的條件研究及探討
周 茁,曹衛宇,奚世超
(上海化工研究院有限公司 上海 200062)
青霉素及頭孢屬于β-內酰胺類抗生素,7-ACA是頭孢菌素的中間體,此類抗生素具有殺菌活性強、毒副作用小等特點,在動物飼養過程中的應用非常普遍[1-3]。隨著其在臨床上的應用研究和毒理學研究的深入,由其殘留引起的安全問題已不容忽視,故β-內酰胺類藥物在不同介質中的痕量檢測引起了廣泛的關注。降解后的抗生素藥渣經測定抗生素含量低于國家標準要求后,可資源化利用生產肥料。對不同介質中青霉素及7-ACA殘留的分析方法有傳統的微生物法[4]、HPLC-UV法[5-6]、HPLC-FD法[7-8]及LC-MS/MS法[9-10],其中高效液相色譜法最大的優點是測定結果準確度高,但每次檢測的開機費用較昂貴。《中華人民共和國獸藥典》(1990年版)采用碘量法測定青霉素含量,即青霉素經堿水解生成青霉噻唑酸后與碘作用,根據碘的消耗量測得青霉素含量。該方法不僅適用于青霉素含量的測定,也適用于與青霉素結構類似的頭孢類藥物的測定,其最大的優點是采用常規的檢測儀器及設備即可獲得令人滿意的測定結果。為此,探索了碘量法測定青霉素及7-ACA的相關條件,并驗證該方法的精密度及準確度,以期為藥渣中抗生素的檢測提供科學的依據和可靠的方法。
1 試驗部分
1.1 反應原理
7-ACA及青霉素母核6-APA不能直接與碘反應,必須經堿水解后打開內酰胺環,才能與碘反應;待6-APA和7-ACA與碘反應完全以后,用標準的硫代硫酸鈉溶液滴定過量的碘液,由消耗的標準硫代硫酸鈉溶液的體積求出7-ACA和青霉素的含量。6-APA碘量法反應方程式如式(1)、式(2)和式(5)所示,7-ACA碘量法反應方程式如式(3)、式(4)和式(5)所示。
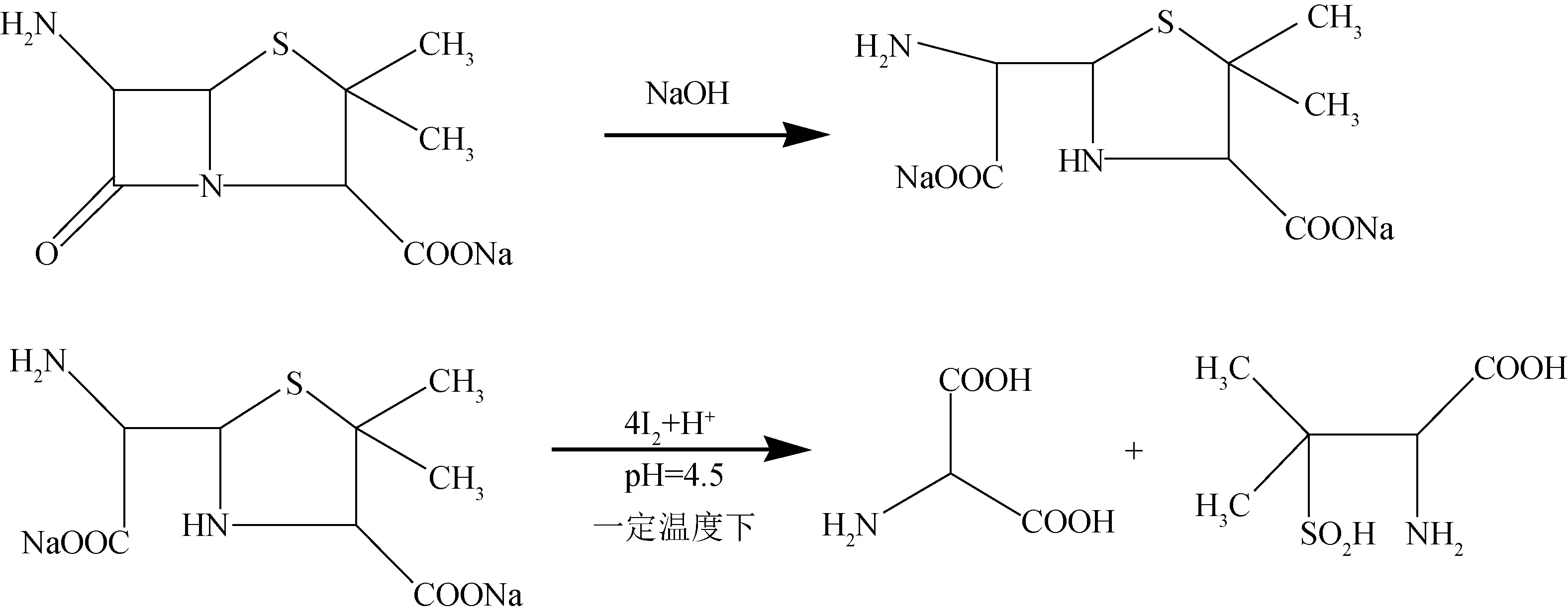
(1)
(2)
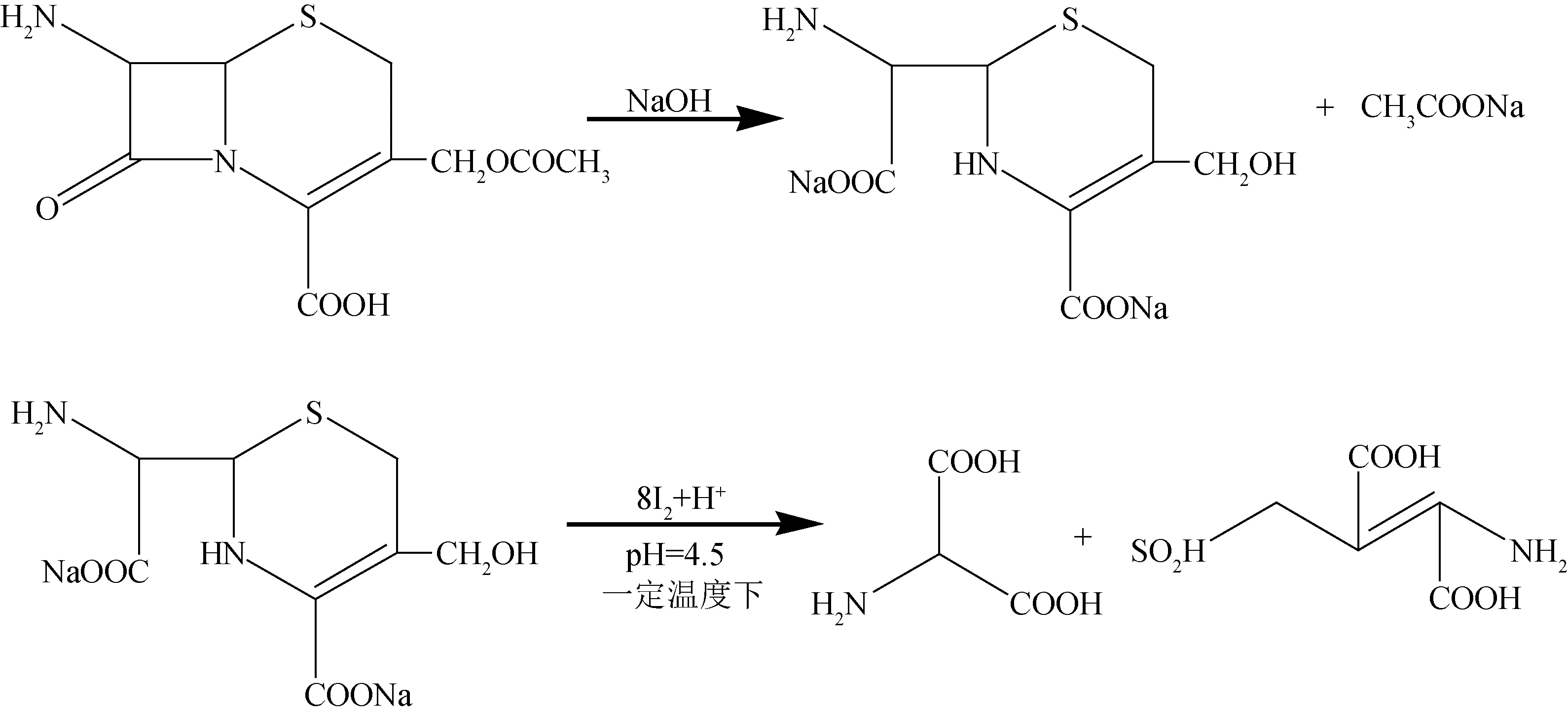
(3)
(4)
2Na2S2O3+I2=Na2S4O6+2NaI
(5)
1.2 主要儀器與試劑
主要儀器:分析天平、容量瓶、碘量瓶、滴定管、移液管等。
主要試劑:青霉素G原藥(芐青霉素鈉),內蒙古常盛制藥有限公司標品;7-ACA原藥,伊犁川寧制藥有限公司標品;0.009 748 mo/L碘液、0.011 72 mol/L硫代硫酸鈉標準溶液、淀粉指示劑、1 mol/L HCl溶液、1 mol/L NaOH溶液、醋酸-醋酸鈉緩沖液(pH=4.5)。
1.3 試驗步驟
(1)精密稱取供試樣品約100 mg于250 mL容量瓶中,加去離子水稀釋至刻度。
(2)用移液管吸取一定體積(V0)的試樣溶液于碘量瓶中,加入一定量的1 mol/L NaOH溶液,放置一定時間后加入與1 mol/L NaOH溶液等體積的1 mol/L HCl溶液、5 mL醋酸-醋酸鈉緩沖液和一定量的0.009 748 mol/L碘液于碘量瓶中并密塞,在常溫下暗處放置一定時間后,用0.011 72 mol/L硫代硫酸鈉標準溶液滴定,至近終點時加入淀粉指示劑,繼續滴定至藍色消失。
(3)另取與V0等體積的去離子水置于碘量瓶中,加5 mL醋酸-醋酸鈉緩沖液和一定量的0.009 748 mol/L碘液,用0.011 72 mol/L硫代硫酸鈉滴定,作為空白。
1.4 計算公式
青霉素和7-ACA質量分數按式(6)和式(7)計算:
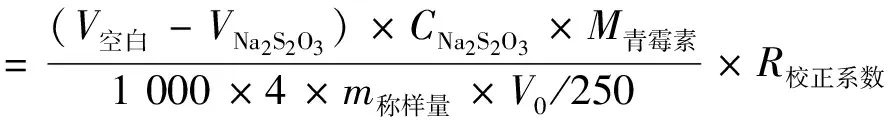
(6)
(7)
式中:V空白——對照空白消耗Na2S2O3的體積,mL;
VNa2S2O3——樣品消耗Na2S2O3的體積,mL;
CNa2S2O3——硫代硫酸鈉標準溶液物質的量濃度,mol/L;
M青霉素——青霉素的分子量;
M7-ACA——7-ACA的分子量;
m稱樣量——樣品質量,g;
R校正系數——實際含量與測定含量之比;
V0——吸取試樣的體積,mL。
2 結果與討論
2.1 不同測定條件對7-ACA含量測定結果的影響
當采用碘量法測定青霉素含量時,在常溫下吸取一定量的試樣溶液,加入1 mL的1 mol/L NaOH溶液,放置0.5 h,再加入與1 mol/L NaOH溶液等體積的1 mol/L鹽酸溶液、5 mL醋酸-醋酸鈉緩沖液和10 mL碘液后放置0.5 h,測得的青霉素質量分數為91.25%。考慮到青霉素原藥中本身含有一定的雜質,測定值與實際值接近,所以無需對青霉素的測試條件進行優化,故青霉素計算公式中的校正系數為1。采用碘量法分析測定7-ACA時,其分子結構中的內酰胺環[11]完全打開是保證分析結果準確的必要條件。由于7-ACA中的內酰胺環比青霉素中的內酰胺環結構更為穩定,要求既要確保7-ACA中的內酰胺環完全打開,又要保證7-ACA中其他結構不發生變化,因此需考察堿解開環時間、堿解開環反應溫度、NaOH加入量以及已開環7-ACA的碘氧化反應時間等因素對測定結果的影響。
2.1.1 堿解開環時間對7-ACA含量測定結果的影響
如圖1所示,加入1 mol/L NaOH溶液后,7-ACA含量的測定結果隨堿解開環時間延長呈現先增大后減小的趨勢。其原因可能是隨著堿解時間的延長,7-ACA的內酰胺環不斷被打開,碘與開環的內酰胺環發生氧化反應,但放置時間過長會引起碘揮發,導致測定結果偏低。因此,最佳堿解開環時間為1 h。
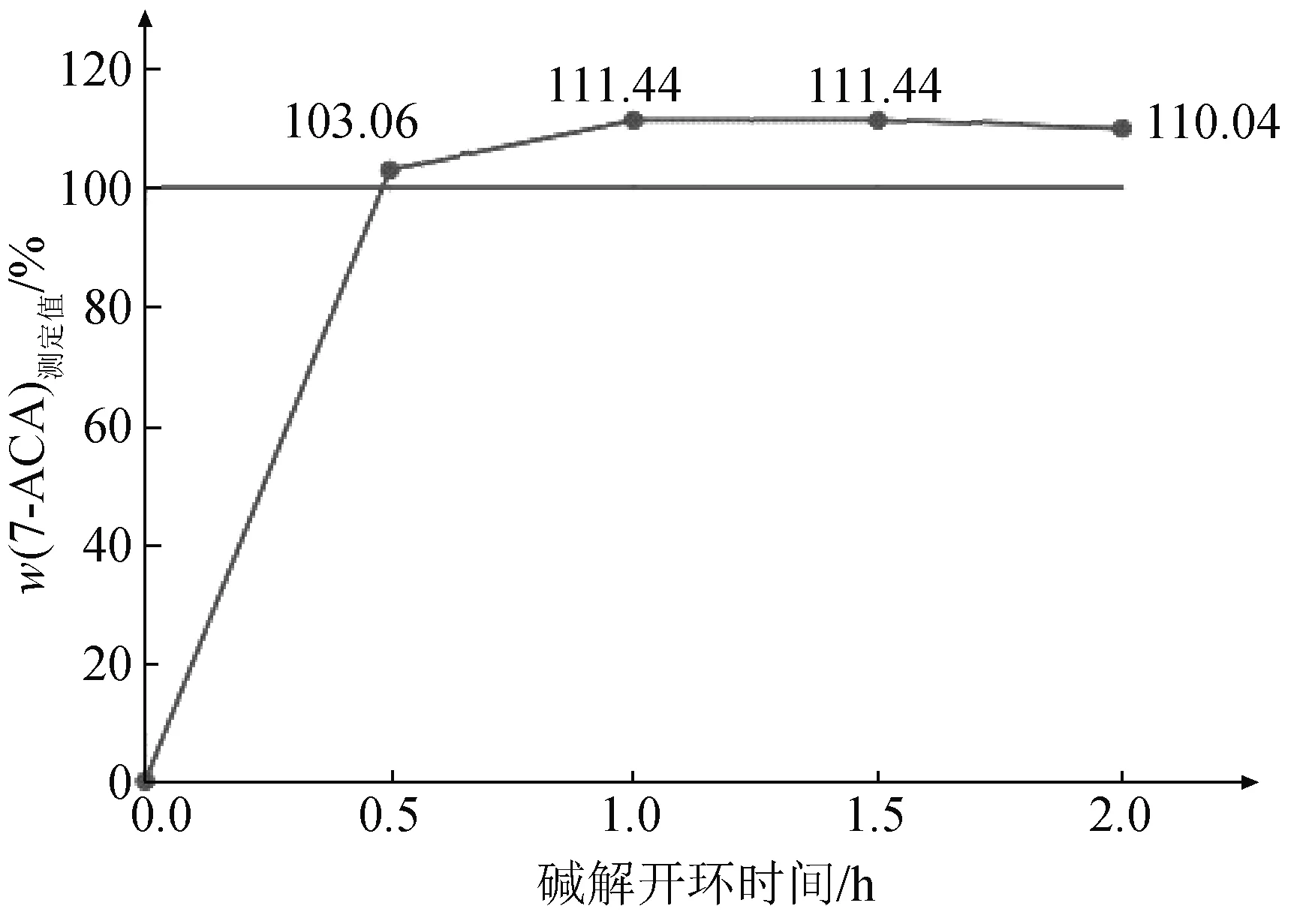
圖1 堿解開環時間對7-ACA含量測定結果的影響
2.1.2 堿解開環反應溫度對7-ACA含量測定結果的影響
如圖2所示,7-ACA含量的測定結果隨堿解開環反應溫度的升高而降低。其原因是溫度過高會導致碘的揮發,同時也會導致7-ACA中被氧化的結構發生降解。因此,最佳堿解開環反應溫度應在30 ℃以內。
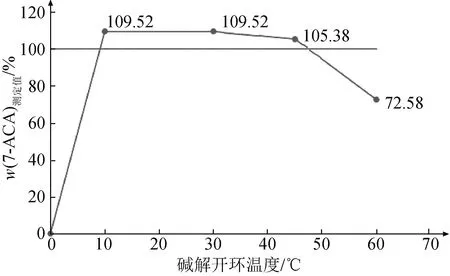
圖2 堿解開環反應溫度對7-ACA含量測定結果的影響
2.1.3 NaOH加入量對7-ACA含量測定結果的影響
如圖3所示,7-ACA含量的測定結果隨1 mol/L NaOH溶液加入量的增加呈現先增大后減小的趨勢,表明適度增加NaOH的加入量有利于堿解開環反應,但NaOH溶液加入量過多反而會抑制堿解開環反應的進行。因此,1 mol/L NaOH溶液加入量以8 mL為宜。
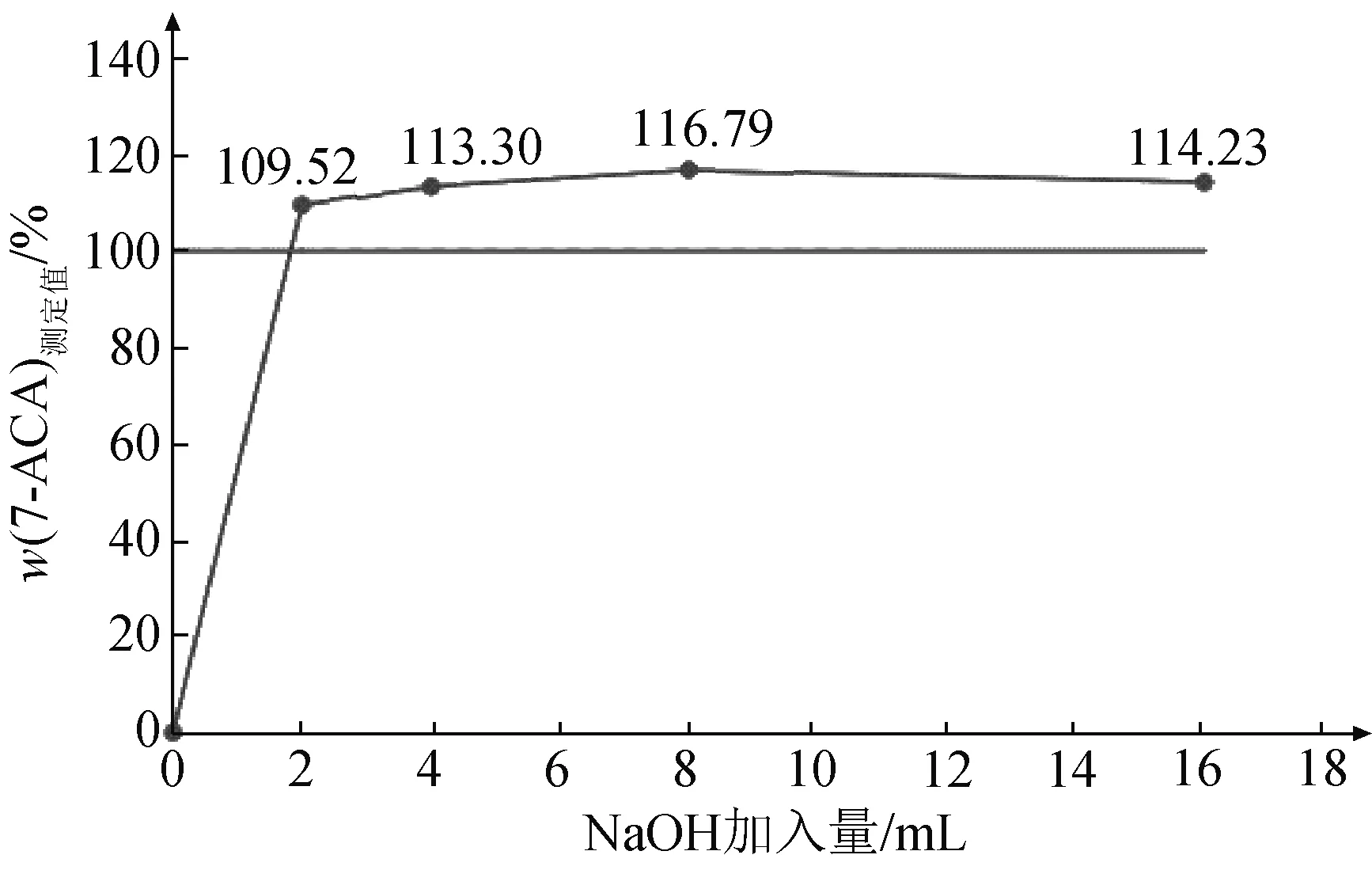
圖3 NaOH加入量對7-ACA含量測定結果的影響
2.1.4 碘氧化反應時間對7-ACA含量測定結果的影響
如表1所示,在其他條件一定的情況下,加入碘0.5 h后,碘已與開環后的7-ACA充分反應,繼續延長反應時間對測定結果影響不大。因此,加入碘后最佳的放置時間為0.5 h。
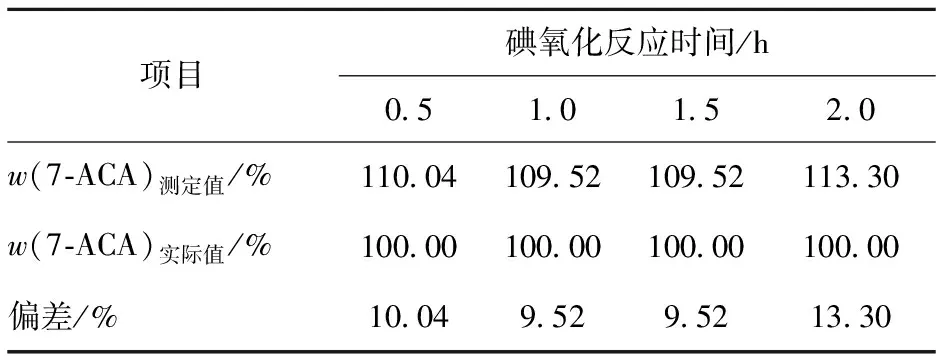
表1 碘氧化反應時間對7-ACA含量測定結果的影響
綜上所述,測定7-ACA的最佳條件為:稱取0.1 g左右的7-ACA定容至250 mL容量瓶中;吸取一定量的試樣溶液,先加入8 mL的1 mol/L NaOH溶液于常溫下放置1.0 h,然后依次加入與1 mol/L NaOH溶液等體積的1 mol/L HCl溶液、5 mL醋酸-醋酸鈉緩沖液和10 mL碘液,繼續放置0.5 h后用0.011 72 mol/L硫代硫酸鈉標準溶液滴定。在此最佳條件下測得7-ACA的質量分數為116.79%,其實際值為100.00%,故R校正系數=1/1.17。
2.2 回收率試驗
精密配制青霉素G、青霉素V和7-ACA溶液,質量濃度分別為0.60、0.80和1.00 g/L,采用碘量法測定各樣品溶液,每個樣品進行2次平行測定并計算回收率,試驗結果如表2所示。
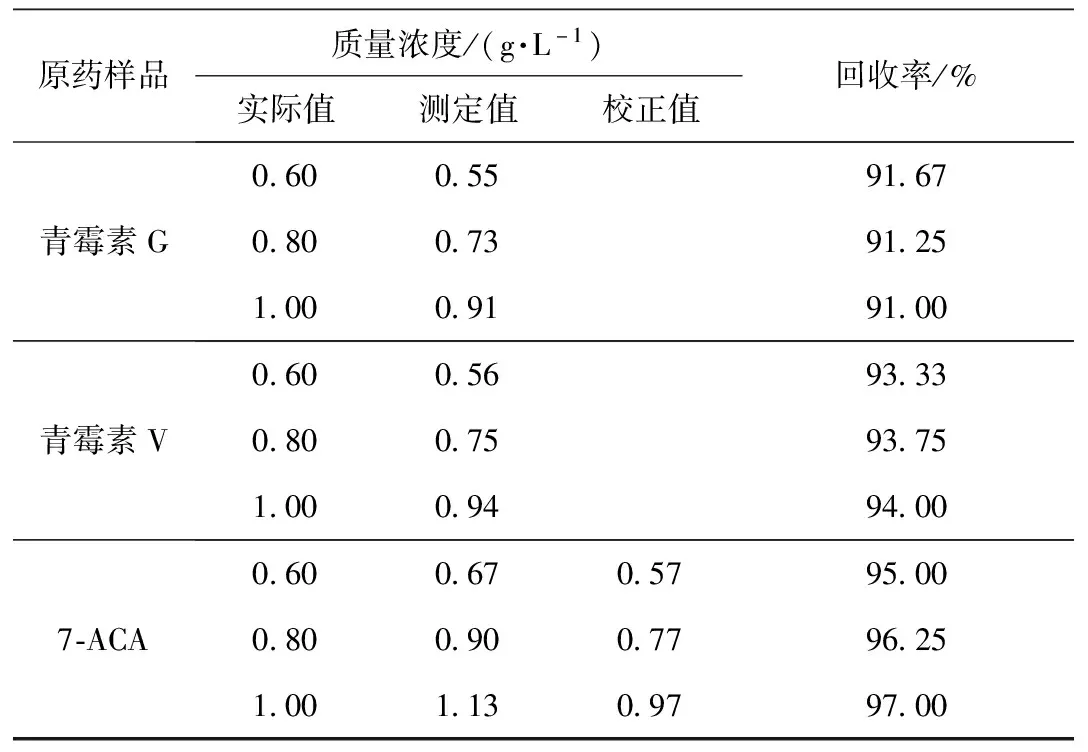
表2 回收率試驗結果
試驗結果表明,采用碘量法測定不同質量濃度的青霉素G、青霉素V及7-ACA,測定結果準確度良好,均接近實際值。
2.3 精密度試驗
分別稱取一定質量的青霉素G和7-ACA溶于水中,按上述碘量法進行4次平行測定,結果(表3)表明該方法精密度良好、重現性較高。
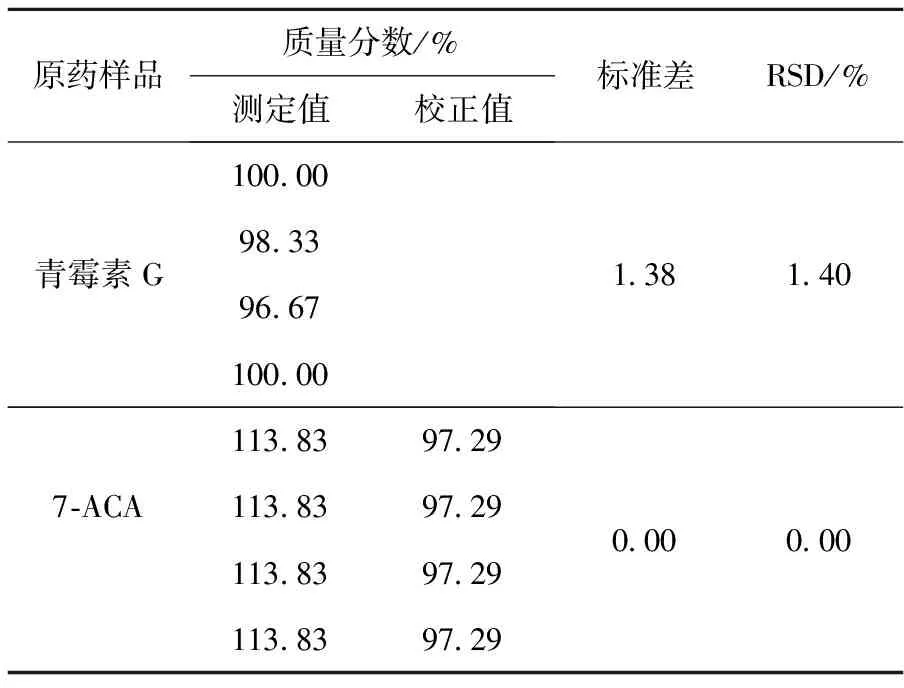
表3 精密度試驗結果
3 結語
通過試驗,對碘量法測定青霉素及7-ACA的測定條件進行了探索。測定7-ACA的最優條件:在一定量的試樣溶液中加入8 mL的1 mol/L NaOH溶液并于常溫下放置1.0 h,然后加入與1 mol/L NaOH溶液等體積的1 mol/L鹽酸溶液、5 mL醋酸-醋酸鈉緩沖液和10 mL碘液,繼續放置0.5 h后用0.011 72 mol/L標準硫代硫酸鈉溶液滴定。測定青霉素的最優條件:在一定量的試樣溶液中加入1 mL的1 mol/L NaOH溶液并于常溫下放置0.5 h,然后加入與1 mol/L NaOH溶液等體積的1 mol/L鹽酸溶液、5 mL醋酸-醋酸鈉緩沖液和10 mL碘液,繼續放置0.5 h后用0.011 72 mol/L標準硫代硫酸鈉溶液滴定。在最優試驗條件下采用碘量法對青霉素及7-ACA進行測定時,藥物回收率及精密度均良好。
——硫代硫酸鈉

