直腸癌全直腸系膜切除術術后吻合口狹窄的病因分析及外科診治
隨著腹腔鏡和雙吻合器的應用,保留肛門的直腸癌低位前切除和超低位前切除得到廣泛開展,直腸癌病人行根治性手術的同時要求保留肛門的愿望愈發強烈,但術后并發癥隨之發生,如吻合口狹窄(AS)、吻合口漏、吻合口出血、直腸陰道瘺等。直腸癌全直腸系膜切除術(total mesorectal excision,TME)術后AS降低了保肛術后病人的生活質量,輕者排便不暢、便頻,重者發生腸梗阻甚至威脅生命,對此必須引起足夠的重視[1]。AS定義為:(1)吻合口腸壁增厚、瘢痕狹窄長度>1 cm、且直徑為12 mm的結腸鏡不能通過的吻合口;(2)常伴有排氣、排糞時左側腹部脹痛、排糞次數增多、糞便變細和排糞困難等癥狀;(3)肛門指診、結腸鏡、經肛門造影和直腸磁共振等提示吻合口狹窄[2-3]。AS發生率為2.5%~19%[1]。我們對直腸癌TME術后AS進行分類診治,取得滿意療效。現報道如下。
對象與方法
一、對象
2011年~2018年我院收治的512例直腸癌TME術后AS病人 30例,發生率為5.9%,男21 例,女9 例,年齡26~84歲,平均年齡(61.5±14.5)歲。術前均行電子結腸鏡檢查病理活檢確診為直腸腺癌,腫瘤直徑(3.7±1.69)cm,腫瘤遠端距肛緣距離(7.2±2.2)cm。根據術后病理進行TNM 臨床分期:Ⅱ期14例、Ⅲ期14例,Ⅳ2例。11例行長療程新輔助放化療。全組病人均行TME,其中腹腔鏡輔助下12例,常規開腹手術18例;術中行乙狀結腸-直腸吻合術21例,乙狀結腸-肛管吻合術9例;同時行回腸保護性造口術11例,橫結腸保護性造口術3例,吻和口距肛緣距離(3.6±2.9)cm。1例術后5天出現盆腔感染,術后2天出現切口感染;2例術后7~8天出現吻合口漏,行回腸保護性造口術;1例術后出現腸梗阻,經保守治療好轉。直腸或肛管吻合口狹窄時間4~60個月,平均(18.6±15.2)個月,主要臨床表現為排便困難、肛門疼痛或墜脹,伴腹痛、腹脹。行腹腔螺旋CT、電子結腸鏡或鋇灌腸檢查均明確診斷,證實吻合口直徑均<12 mm,吻合口狹窄環直徑(1.0±0.1)cm。見表1。
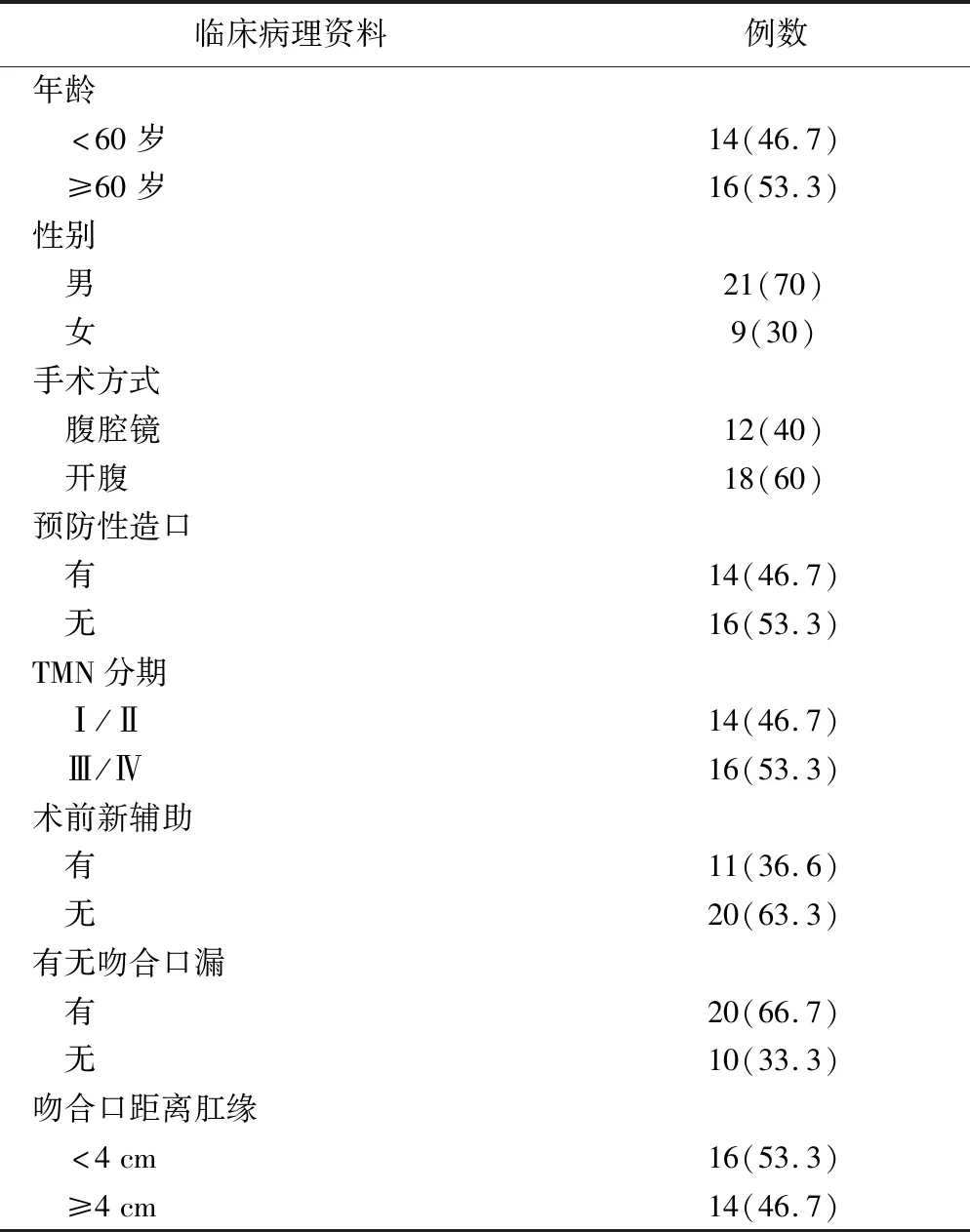
表1 30例吻合口狹窄病人臨床病理特征[例(%)]
二、方法
TME術后AS病人30例,行乙狀結腸-直腸吻合術21例,乙狀結腸-肛管吻合術9例;同時行回腸保護性造口術11例,橫結腸保護性造口術3例,AS時間4~60個月,平均(18.6±15.2)個月。根據AS特點,其中20例行吻合口狹窄環切開術,6例行吻合口狹窄擴張術,3 例行經肛門直腸吻合口狹窄環切除、橫結腸雙腔造口術,1例因腸梗阻初始選擇置入裸支架緩解梗阻,支架取出再次出現狹窄,后行乙狀結腸單腔造口術。
采用電話、門診或者住院方式進行隨訪,30例病人均獲得隨訪,均無再狹窄發生,無排便困難,術后2年內每3個月復查1次直腸指檢、血清癌胚抗原(CEA)、血糖類蛋白(CA19-9)、胸部X線片、腹部超聲;2年后每6個月復查1次,至術后5年。術后每年復查1次結腸鏡、胸腹盆增強CT。
結 果
30例AS病人經治療后癥狀均得到明顯緩解。20例吻合口狹窄環切開術及6例行吻合口狹窄擴張術病人術后每天經肛門行人工吻合口擴肛2~3次,每次3~5分鐘,復查腸鏡均未見再次狹窄。3例行經肛門直腸吻合口狹窄環切除、橫結腸雙腔造口術后3~6個月內還納腸造口,均能排除稀便。1例因腸梗阻初始選擇置入裸支架緩解梗阻,1個月后因支架取出再次出現狹窄,后行乙狀結腸單腔造口術,術后3個月后行造口還納術,并行定期手指擴肛治療,未再出現狹窄表現。
討 論
AS是直腸癌術后較為常見的并發癥,吻合口漏、盆腔感染、新輔助放化療、近端腸造口等均被認為是AS的高危因素,其根本原因在于吻合口一期愈合失敗后的肉芽組織廣泛增生和纖維化瘢痕形成。本組資料顯示,AS原因包括以下幾個方面:(1)保護性腸造口術: 由于保護性腸造口術后吻合口的廢用,以及術后沒有及時擴肛,本組14例保護性腸造口術后發生吻合口狹窄,其原因可能是吻合口肌肉組織被纖維結締組織所替代,導致吻合口狹窄[4]。(2)吻合口感染和吻合口漏:本組AS有20例行直腸癌TME術后發生吻合口感染和吻合口漏,造成吻合口周圍組織感染壞死,形成慢性炎癥,吻合口纖維組織廣泛增生。(3)腫瘤復發:包括盆腔腫瘤轉移或者吻合口復發,本組1例為腫瘤盆腔復發壓迫吻合口。(4)新輔助放化療:本組11例術前行新輔助放化療后造成吻合口狹窄。由于放療導致腸管受到放射性照射,腸管肌纖維變性,纖維組織增生,腸管僵硬、蠕動變弱[5-6]。(5)性別:男性病人發生吻合口狹窄的發生率高于女性,這可能與男性骨盆狹窄、骨盆腔相對較深、術野顯露不佳、操作解剖及吻合困難所致[7]。(6)吻合口缺血:傳統直腸癌根治術要求在腸系膜下動脈根部予以結扎及全直腸系膜切除,其結果是吻合口的血流低灌注,導致纖維組織增生。我們團隊術中裸化腸系膜下動脈,在完全清掃淋巴結的基礎上,于直腸上動脈根部離斷血管,盡量保留左結腸動脈,可能有利于吻合口血供的維持。(7)腫瘤位置過低:吻合口越接近肛門,直腸游離的范圍越大,若吻合口上方結腸保留過短或游離不充分,吻合口有張力加重血運障礙,組織缺氧致纖維組織增生導致吻合口狹窄。同時吻合口越低,發生吻合口漏的可能性越大。吻合口漏發生后,導致盆腔感染; 此時如果行腸造口,又使直腸吻合口處于廢用狀態,缺少糞便的物理刺激作用,更易造成直腸狹窄[8]。(8)吻合技術影響:直腸癌切除術后吻合口狹窄原因較多,主要包括吻合器型號選擇不當、吻合口張力大、吻合口缺血、吻合口腸管厚度,以及直腸內括約肌的痙攣和外括約肌的持續收縮,造成吻合口處于一種持續的收縮狀態,極易產生狹窄,吻合口擠壓過緊或釘合不全,產生乏氧,導致吻合口纖維組織過度增生,嚴重時造成直腸黏膜全層割裂,出現黏膜回縮,使其下層直接暴露于腸腔,更易形成瘢痕。
直腸癌病人手術前需具備良好的全身狀況,做好腸道準備,這對于減少吻合口瘺的發生具有重要作用。手術技巧方面,吻合口處理滿意的標準是吻合口的“空、松、通”,同時確保吻合口血運良好。術中充分游離結腸至脾區降低吻合口張力,盡量選用大號吻合器[9]。乙狀結腸系膜切除時注意避免切斷邊緣動脈弓。對于乙狀結腸冗長者,可保留左結腸動脈,以確保吻合口血運。另外在使用直線型切割閉合器時應使切割線在同一平面上。吻合時盡量將兩次切割交界處切除。保護性腸造口者吻合口處于廢用狀態,易引起吻合口狹窄,術后定期行直腸指檢并擴張吻合口,可減少吻合口狹窄。
直腸癌病人術后出現AS,首先要排除腫瘤在吻合口局部復發。對較輕的AS,可反復規律的經肛門手指或球囊擴張,效果較好[10-11]。球囊擴張失敗或經球囊擴張3次以上仍出現狹窄,可考慮行金屬支架置入術,但存在穿孔及移位等風險,且直腸刺激癥狀明顯,適用于中重度狹窄者短期解除腸梗阻[12]。對于多次球囊擴張或支架置入失敗的難治性AS,采用內鏡下電灼擴張術療效良好,但存在狹窄復發風險[13]。在上述治療效果不佳的情況下,手術仍然是直腸癌術后AS治療的重要方法[3]。大多數低位AS可以經肛手術治療,對于低位的膜性狹窄,可采取完整切除狹窄組織的方法;對低位長度較短的管狀狹窄,采取縱行放射狀切開狹窄部位方法[14]。但兩者術后均應規律擴張吻合口以保證手術效果。對于位置較高及狹窄長度較長的AS,需要開腹手術。對于梗阻癥狀嚴重且一般狀況差、無法耐受手術或反復多次處理仍無法緩解的病人,可考慮先行腸造口術。直腸癌術后腹腔粘連嚴重、結構不清,開腹切除狹窄區容易損傷輸尿管等周圍組織,導致骶前大出血等嚴重并發癥。尤其是行新輔助放療的病人,其手術難度及風險高,切勿強行分離、切除吻合口,必要時可由經驗豐富的胃腸外科醫師行結腸造口術[15]。我們團隊收治AS病人狹窄多為管狀及彌漫性狹窄,通常不能用手指擴肛或球囊擴張術緩解,故行外科手術治療。

