基于實時熒光RT-PCR的新型冠狀病毒的不同標本類型核酸檢測
周剛 李超 鄭國棟 柳洪濤 周榮榮 王洪濤 王剛平
新型冠狀病毒(Severe Acute Respiratory SyndromeCoronavirus-2,SARS-CoV-2)感染正席卷全球多個國家爆發(fā)流行,感染人數(shù)不斷攀升[1]。截止到2020年3月26日,SARS-CoV-2 在我國確診人數(shù)已超過8 萬余人,全球其他國家感染人數(shù)已達37 萬余人并不斷持續(xù)上升,對全球公共衛(wèi)生安全構成了巨大威脅[2]。SARS-CoV-2 的傳染源有SARS-CoV-2 感染患者及無癥狀感染者[3],尤其是無癥狀感染者的存在可導致疑似感染者及密切接觸者數(shù)量大量增加,加速疫情的蔓延。新型冠狀病毒肺炎的診斷基于流行病學史、臨床表現(xiàn)及影像學表現(xiàn),而病毒的核酸檢測可為其診斷提供直接證據(jù)[4-5],促進患者的隔離、治療和評估,同時還能為疫情防控中心及時切斷傳播途徑、有效控制傳染源提供指導,保障疫情的防控。根據(jù)新型冠狀病毒肺炎診療方案(試行第七版),可采用基因測序、實時熒光聚合酶鏈反應(Real-Time Polymerase Chain Reaction,RT-PCR)對SARS-CoV-2 感染者進行病毒核酸檢測進而確診患者,而RT-PCR技術因其操作簡單、耗時短、成本低而在臨床上得到廣泛應用[6]。本研究采用實時熒光RT-PCR 法對疑似SARS-CoV-2 感染患者進行了SARS-CoV-2核酸檢測,及時對疑似患者進行快速有效的診斷,為疫情防控提供支持與指導。
1 材料與方法
1.1 樣本來源
收集2020年1月至2020年2月送至本中心的2 258例疑似SARS-CoV-2 感染患者標本共3 284人份,其中,男性1380例(61.12%),女性878例(38.88%);年齡范圍為6 個月~91 歲,平均年齡為(35.49±16.13)歲。將符合《新型冠狀病毒肺炎診療方案(試行第七版)》疑似病例描述的疑似感染者標本均納入本研究中,采樣失敗或者流行病學史不明確、臨床表現(xiàn)不符合者均剔除。
1.2 試劑和儀器
病毒核酸提取試劑盒、病毒核酸提取儀Smart 32、熒光定量RT-PCR 試劑均為中山大學達安基因股份有限公司提供;陽性標本復核試劑由上海伯杰醫(yī)療科技有限公司提供;PowerMicrobiome?RNA Isolation Kit 由德國Qiagen 公司提供,Applied Biosystems?QuantStudio?1&3&5(以下簡稱Q5)實時定量PCR 儀由美國賽默飛世爾科技公司提供。
1.3 標本前處理與病毒RNA 提取
提前將水浴箱預熱至56℃,在生物安全柜內用75%乙醇對裝有標本的密封袋進行噴灑消毒,用吸水紙擦拭后放入浴鍋中的試管架上,標本蓋擱置重物防止試管架浮動。每隔10 min 將標本輕輕搖勻1 次,滅活時間為45 min[7-8]。將滅活好的標本從水浴鍋中取出,在生物安全柜內對密封袋進行消毒,打開密封袋后,即時用75%酒精消毒。
咽拭子/痰液:取出樣本后混勻,參照病毒核酸提取試劑盒說明書進行操作,加入20 μL 蛋白酶K,吸取離心后的標本懸液上清200 μL,加入到預混的深孔板,于生物安全柜靜置10 min 后,置于病毒核酸提取儀Smart 32 上提取病毒核酸。程序運行結束后,吸取核酸轉置于1.5 mL 離心管,直接用于實時熒光RT-PCR。由于RNA 容易降解,短暫存放可置于-20℃冷凍,長時間保存需置于-70℃或以下。
糞便標本:將送檢標本取黃豆粒大小(約0.25g)置于1.5 mL 離心管中,采用PowerMicrobiome?RNA Isolation Kit 糞便RNA 提取試劑盒提取糞便中的核酸,嚴格按照說明書進行操作。
1.4 PCR 擴增
采用新型冠狀病毒2019-nCoV 核酸檢測試劑盒(熒光PCR 法)針對ORF1ab基因和核殼蛋白N基因進行PCR 擴增,使用儀器為Q5 實時定量PCR儀,擴增程序如下:50℃15 min;95℃15 min;94℃15 s;55℃45 s,45 個循環(huán);結果判讀:如果檢測標本在FAM 和VIC 通道無擴增曲線或Ct 值>40,且Cy5 通道有擴增曲線,可判樣品未檢測到2019 新型冠狀病毒(2019-nCoV)RNA;如果檢測標本在FAM 和VIC 通道Ct 值≤40,且有明顯的擴增曲線,可判樣品為2019 新型冠狀病毒(2019-nCoV)陽性;如果檢測標本僅在FAM 或VIC 單一通道Ct 值≤40,另一通道無擴增曲線,結果需復檢,復檢結果一致可判樣品為2019 新型冠狀病毒(2019-nCoV)陽性,復檢均為陰性可判斷為未檢測到2019 新型冠狀病毒(2019-nCoV)RNA。
1.5 統(tǒng)計學分析
采用SPSS19.0 軟件進行數(shù)據(jù)處理,計數(shù)資料用n(%)表示,計數(shù)資料組間比較采用χ2檢驗,P<0.05 為差異有統(tǒng)計學意義。
2 結果
2.1 疑似SARS-CoV-2 感染者檢測結果
共收集2 258例疑似SARS-CoV-2 感染者標本3 284 人份,其中1 539例為單份樣本;824例為雙份標本,921例為三份標本;因921 人份樣本中只檢測出1 份陽性,故不納入統(tǒng)計;將單一樣本類型與兩種樣本類型陽性檢出率進行統(tǒng)計分析,差異有統(tǒng)計學意義(P<0.05),增加樣本類型可以提高陽性檢出率3 284 人份樣本中共檢出陽性樣本79 人份;其中包括男性疑似感染者13例,女性7例,性別陽性檢出率差異無統(tǒng)計學意義(P>0.05),見表1。
此外,在對20例疑似感染者重新采樣復檢時發(fā)現(xiàn),有4例疑似感染者檢測結果出現(xiàn)三次陰陽互轉的現(xiàn)象,還有1例疑似感染者多次口咽拭子、鼻咽拭子核酸檢測結果均呈陰性,而痰液標本檢測結果呈陽性的現(xiàn)象。
2.2 不同樣本類型核酸檢測結果
采用實時熒光PCR 方法檢測,結果顯示,在四種樣本類型中,鼻咽拭子與痰液標本檢測結果差異無統(tǒng)計學意義(P>0.05),而其他三種樣本類型與其它樣本類型檢測結果的差異有統(tǒng)計學意義(P<0.05),其中口咽拭子陽性檢出率最低,鼻咽拭子、痰液標本相對口咽拭子較高,而糞便標本陽性檢出率最高(本組糞便的樣本量較小)。詳見表2。
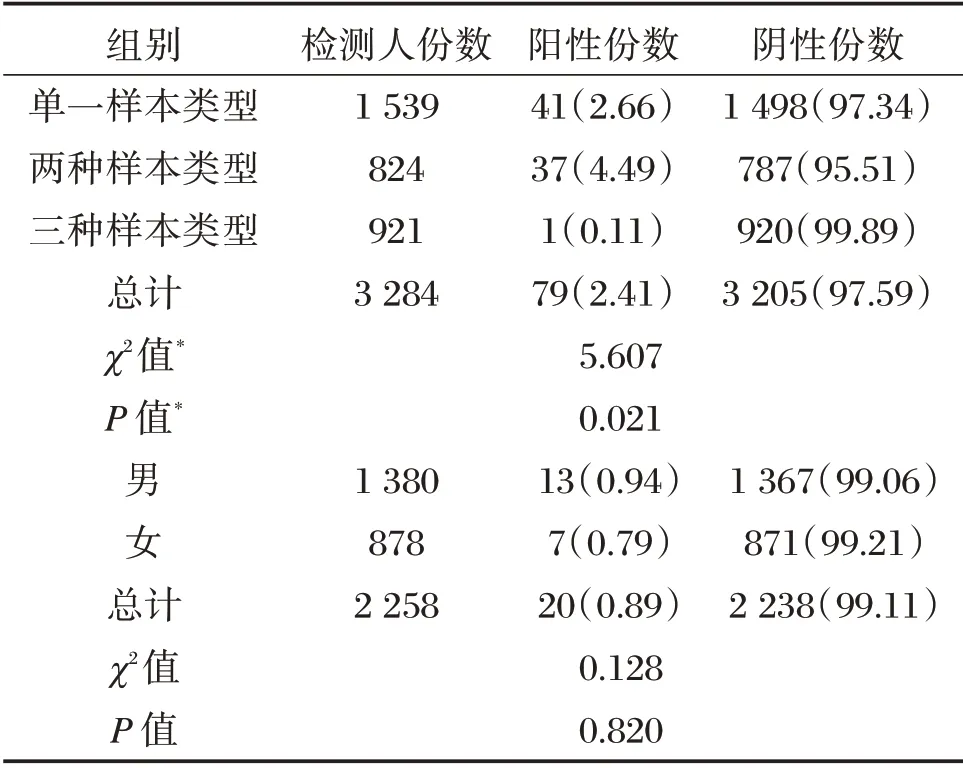
表1 疑似SARS-CoV-2 感染者核酸檢測結果及男女陽性檢出率比較[n(%)]Table1 Nucleic acid detection results of SARS-CoV-2 suspected patients and the positive rate in Male and Female groups[n(%)]
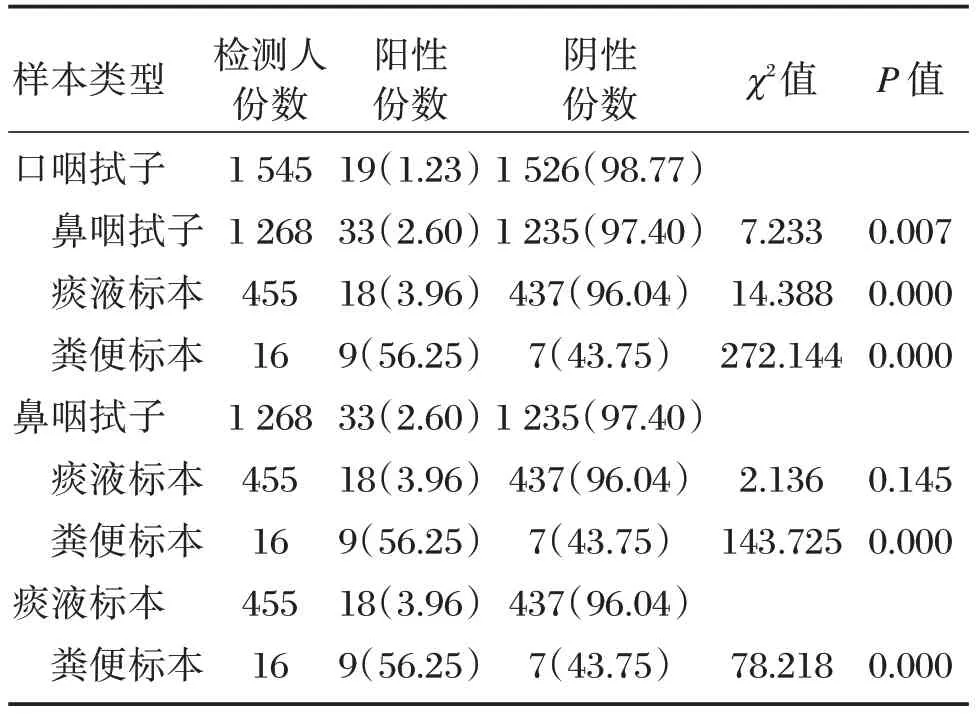
表2 疑似SARS-CoV-2 感染者不同類型標本核酸檢測結果比較[n(%)]Table2 Comparison of nucleic acid detection results of SARS-CoV-2 suspected patients[n(%)]
2.3 同一疑似感染者、同一時間不同標本類型病毒核酸檢測結果
303 人次同一時間同時取口咽拭子、鼻咽拭子及痰液標本采用實時熒光RT-PCR 的方法進行病毒檢測,3 種樣本類型中僅痰液標本檢出1 人份陽性,3 種標本相比,陽性檢出率差異無統(tǒng)計學意義(P>0.05);4 人次同一時間同時取口咽拭子、鼻咽拭子及糞便標本進行檢測,未檢出陽性樣本;280人次同一時間同時取口咽拭子和鼻咽拭子標本進行檢測,兩者陽性檢出率差異無統(tǒng)計學意義(P>0.05);132 人次同一時間同時取鼻咽拭子和痰液標本進行檢測,兩者陽性檢出率差異無統(tǒng)計學意義(P>0.05);見表3。

表3 同一疑似感染者、同一時間不同標本類型核酸檢測結果[n(%)]Table3 SARS-CoV-2 nucleic acid detection results at the same time in the same suspected patient with different sample types[n(%)]
3 討論
目前,全球疫情仍處于嚴峻的形勢。且SARSCoV-2 感染尚未有特效治療方法,及早發(fā)現(xiàn)感染者仍為疫情防控的關鍵。病毒的核酸檢測可快速診斷SARS-CoV-2 感染,為臨床治療提供依據(jù)、為防控隔離提供指導,阻止疫情擴散。
本研究針對疑似SARS-CoV-2 感染者的口咽拭子、鼻咽拭子、痰液標本及糞便標本的檢出陽性檢出率與其他研究者陽性檢出率差異比較大[9],主要原因為疫情發(fā)病地域不同,疫情與非疫情區(qū);單一樣本類型與兩種樣本類型陽性檢出率的統(tǒng)計結果提示,對高度可疑的病人,臨床有必要增加標本類型,提高陽性檢出率。此外,本研究中性別陽性檢出率差異無統(tǒng)計學意義,該統(tǒng)計結果也與Rui Liu 等[9]的結果不一致,在國內其他研究中也有報道重癥患者中男性多于女性[10],這可能與本研究來自非疫情區(qū),陽性樣本數(shù)過少有關。
本研究還觀察到4例疑似感染者檢測結果出現(xiàn)三次陰陽互轉的現(xiàn)象,還有1例疑似感染者多次口咽拭子、鼻咽拭子核酸檢測結果均呈陰性,而痰液標本檢測結果呈陽性的現(xiàn)象。疫情爆發(fā)后,有研究針對SARS-CoV-2 核酸檢測假陰性問題進行過探討,造成假陰性的原因有很多,標本采集、檢測方法、產(chǎn)品穩(wěn)定性等因素都可能影響檢測結果[11-12];有報道稱拭子樣本采用目前現(xiàn)有的RT-PCR 試劑盒,陽性檢出率預估值為30%~50%[13]。因此,在確診SARS-CoV-2 感染的過程中應綜合分析疑似患者的流行病學史、臨床癥狀以及影像學證據(jù),必要時多次、多樣本類型綜合檢測以避免假陰性結果。
目前SARS-CoV-2 核酸檢測最常用的標本類型為口/鼻咽拭子,有研究顯示口咽拭子陽性檢出率最低,與本研究結論一致[14]。SARS-CoV-2 最早確認的傳播途徑是飛沫傳播和接觸傳播,隨著對SARS-CoV-2 病毒的研究與核酸檢測的科技攻關,且有研究首次在確診病例糞便中檢測到了SARSCoV-2 病毒[15],使得糞便標本在臨床患者篩查中成為重要的樣本類型;本研究中糞便樣本取樣不多,大多數(shù)為初次/多次檢測陽性者,故糞便樣本陽性檢出率高達56.25%,與吳冰珊等[16]的研究結論一致。
臨床反饋及研究都顯示單一的咽拭子樣本進行病毒核酸檢測時會出現(xiàn)時陰時陽的現(xiàn)象,或出現(xiàn)咽拭子多次檢測陰性而糞便核酸檢測陽性的情況。因此,本研究對同一疑似感染者、同一時間不同標本類型病毒核酸檢測結果進行統(tǒng)計分析,結果顯示與王云等的結論一致[17],多樣本類型的一致性可為臨床提供更清晰明確的指導。
目前,SARS-CoV-2 仍屬于未知病毒,人類對其在體內的活動過程尚未完全清晰掌握,仍需要更多的研究來支持與指導臨床工作。本研究提示多種標本類型的聯(lián)合檢測可能提高檢出率,為防控切斷傳播途徑,尤其是無癥狀感染者的傳播提供更準確的判斷。

