HMGB1和TLR4在高血壓合并頸動(dòng)脈硬化患者外周血中的表達(dá)及作用
蔡飛,劉建勇,滕云飛,李海濤
華中科技大學(xué)同濟(jì)醫(yī)學(xué)院附屬協(xié)和醫(yī)院,武漢430022
原發(fā)性高血壓是臨床常見的一種慢性疾病,是誘發(fā)頸動(dòng)脈硬化的獨(dú)立危險(xiǎn)因素[1,2]。目前研究認(rèn)為,慢性炎癥反應(yīng)參與高血壓的病理過程[3],并可能促進(jìn)了頸動(dòng)脈硬化的發(fā)生。高遷移率族蛋白 B1(HMGB1)是一種非組蛋白染色體蛋白質(zhì),廣泛存在于真核細(xì)胞的核內(nèi)。機(jī)體受損時(shí),HMGB1通過機(jī)體釋放壞死細(xì)胞或通過炎性細(xì)胞分泌轉(zhuǎn)移至細(xì)胞外,作為炎癥介質(zhì),啟動(dòng)機(jī)體的免疫應(yīng)答[4,5]。HMGB1能激活靶細(xì)胞的Toll樣受體4(TLR4),可通過細(xì)胞遷移、增殖及活化來促進(jìn)炎癥反應(yīng)的發(fā)生,其促炎作用可導(dǎo)致下游相關(guān)炎癥因子如IL-6、IL-17以及TNFα等的釋放[6]。已有研究發(fā)現(xiàn),HMGB1/TLR4軸激活參與了原發(fā)性高血壓的病理過程[7]。為此,本研究檢測(cè)高血壓合并頸動(dòng)脈硬化患者的外周血HMGB1、TLR4表達(dá)水平,并分析二者與相關(guān)炎癥因子表達(dá)的關(guān)系。
1 資料與方法
1.1 臨床資料 收集本院2018年1月~2019年5月臨床確診的高血壓患者186例,根據(jù)頸動(dòng)脈超聲結(jié)果分為兩組。單純高血壓組74例,男40例、女34例,年齡(62.3±8.2)歲;高血壓合并頸動(dòng)脈硬化組79例,男40例、女39例,年齡(64.6±7.5)歲。納入標(biāo)準(zhǔn):①符合2010版中國(guó)高血壓防治指南原發(fā)性高血壓的診斷標(biāo)準(zhǔn);②同意接受頸動(dòng)脈超聲檢查;③無自身免疫性疾病、感染等明確與炎癥因子相關(guān)的疾病;④患者知情并同意該研究方案。排除標(biāo)準(zhǔn):①不符合上述診斷標(biāo)準(zhǔn)和納入標(biāo)準(zhǔn)者;②各種繼發(fā)性高血壓;③類風(fēng)濕關(guān)節(jié)炎、系統(tǒng)性紅斑狼疫等結(jié)締組織病以及急慢性感染性疾病正接受抗炎治療患者。選擇同期健康體檢無任何器官功能障礙者90例為對(duì)照組,男47例、女43例,年齡(60.6±9.1)歲。以上三組性別和年齡比較均無統(tǒng)計(jì)學(xué)差異(P均>0.05)。
1.2 頸動(dòng)脈超聲檢查 患者仰臥位,探頭沿頸動(dòng)脈走向自下向上作連續(xù)縱橫切面掃查,測(cè)量頸動(dòng)脈內(nèi)-中膜厚度(IMT),測(cè)量工作由兩位臨床工作超過10年的超聲科醫(yī)師完成。IMT < 1.00 mm為正常,1.00~1.20 mm為頸動(dòng)脈內(nèi)膜增厚,>1.20 mm為存在頸動(dòng)脈粥樣硬化斑塊。
1.3 血清HMGB1、TLR4 、IL-17、IL-6水平檢測(cè) 三組取空腹12 h后靜脈血5 mL,采用酶聯(lián)免疫吸附試驗(yàn)檢測(cè)血清HMGB1和TLR4水平,ELISA法檢測(cè)各組血清IL-17、IL-6水平;所有檢測(cè)操作嚴(yán)格按照試劑盒說明書進(jìn)行。
1.4 外周血單核細(xì)胞HMGB1和TLR4 蛋白水平測(cè)定 從每個(gè)樣本中分別取 100 μL抗凝全血,分別加入 20 μL PE 標(biāo)記抗體,充分混勻后室溫孵育 40 min。用標(biāo)本處理儀進(jìn)行細(xì)胞固定和破膜,3 000 r/min 離心5 min,棄上清液。用 3 mL Stain buffer(pH7.4的磷酸緩沖液加2%小牛血清和 0.1% 疊氮鈉) 緩慢沖洗2遍,加入 500 mL Stain buffer,輕輕搖勻呈細(xì)胞懸液,上流式細(xì)胞儀測(cè)定各組外周血單核細(xì)胞 HMGB1和TLR4蛋白表達(dá)水平。

2 結(jié)果
2.1 三組IMT變化 對(duì)照組、單純高血壓組、高血壓合并頸動(dòng)脈硬化組患者IMT分別為(0.87±0.07)、(0.98±0.06)、(1.23±0.14)mm。高血壓合并頸動(dòng)脈硬化組患者IMT均大于單純高血壓組和對(duì)照組,單純高血壓組IMT亦大于對(duì)照者(P均<0. 05)。
2.2 三組血清HMGB1、TLR4、IL-17、IL-6水平變化 三組血清HMGB1、TLR4、IL-17、IL-6水平比較差異有統(tǒng)計(jì)學(xué)意義(P均<0.05)。見表1。
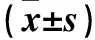
表1 三組血清HMGB1、TLR4、IL-17、IL-6水平比較
注:與正常對(duì)照組相比;*P<0.05;與單純高血壓組相比,#P<0.05。
2.3 三組外周血單核細(xì)胞HMGB1、TLR4表達(dá)變化 三組外周血單核細(xì)胞均能檢測(cè)到HMGB1和TLR4蛋白表達(dá),高血壓合并頸動(dòng)脈硬化組患者單核細(xì)胞HMGB1和TLR4表達(dá)均高于單純高血壓組和對(duì)照組,單純高血壓組單核細(xì)胞HMGB1和TLR4表達(dá)亦高于對(duì)照者(P均<0. 05)。見圖1。
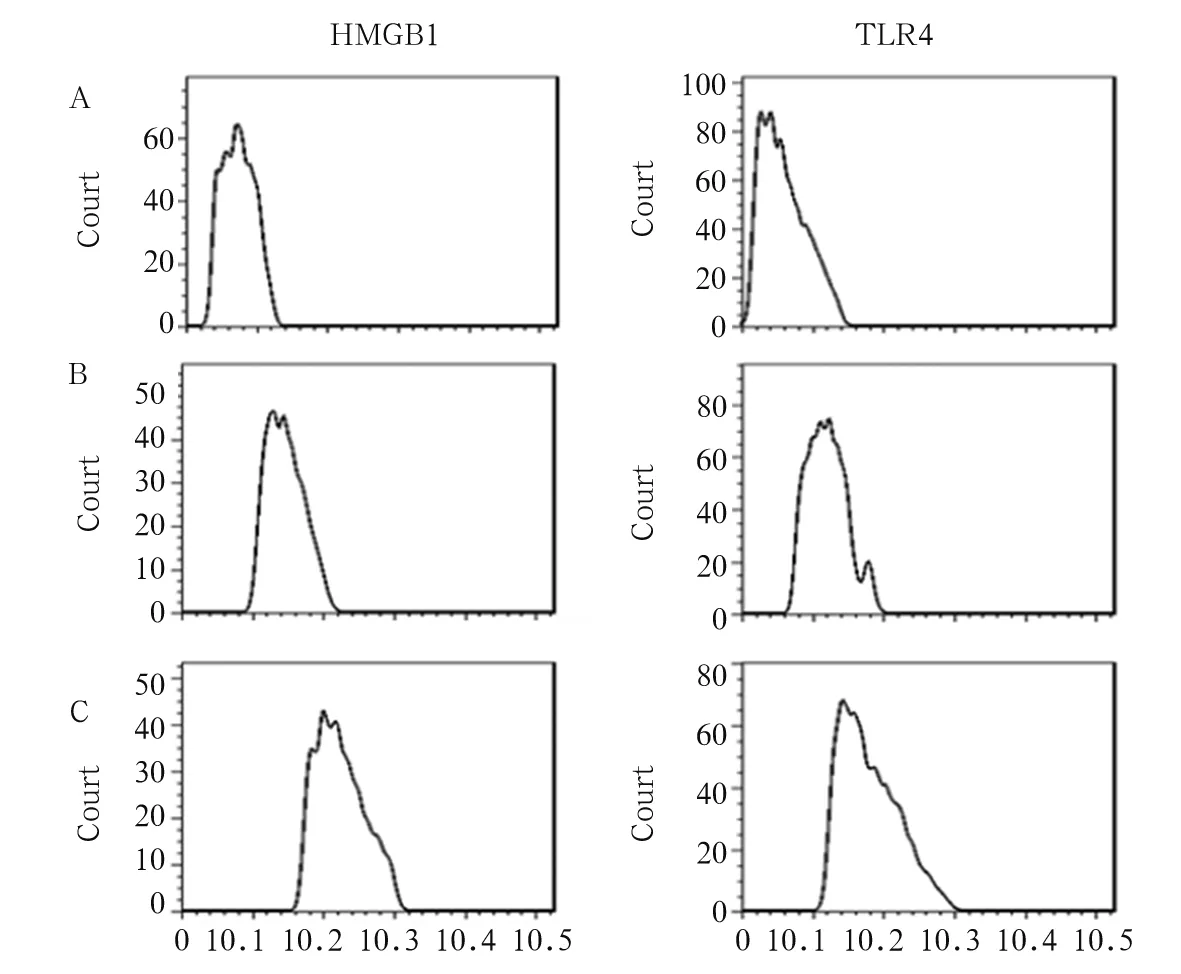
注:A 為正常對(duì)照組、B為單純高血壓組、C 為高血壓合并頸動(dòng)脈硬化組;縱坐標(biāo)為細(xì)胞數(shù),橫坐標(biāo)為熒光強(qiáng)度;峰值越右移,熒光強(qiáng)度越強(qiáng),HMGB1和TLR4蛋白表達(dá)量越高。
圖1 流式細(xì)胞術(shù)檢測(cè)各組外周血單核細(xì)胞HMGB1和TLR4蛋白水平表達(dá)
2.4 血清HMGB1、TLR4、IL-17、IL-6的相關(guān)性 Spearman相關(guān)性分析顯示,高血壓患者血清HMGB1、TLR4水平與IL-17、IL-6水平呈正相關(guān)。見表2。

表2 HMGB1、TLR4水平與IL-17、IL-6水平相關(guān)性
3 討論
頸動(dòng)脈是高血壓最易累及病變的大血管。由于長(zhǎng)期處于壓力超負(fù)荷狀態(tài),血管平滑肌細(xì)胞和成纖維細(xì)胞增生遷移,表現(xiàn)為血管壁增厚和管腔縮小,最終導(dǎo)致頸動(dòng)脈硬化[8]。目前研究發(fā)現(xiàn),無論是高血壓還是頸動(dòng)脈硬化,都與細(xì)胞炎性反應(yīng)密切相關(guān),炎性反應(yīng)因子可作為預(yù)測(cè)心腦血管疾病發(fā)生的重要指標(biāo)[9]。
研究發(fā)現(xiàn),HMGB1在AngⅡ誘導(dǎo)的血管平滑肌細(xì)胞表型轉(zhuǎn)化模型中升高,表現(xiàn)為收縮蛋白的下調(diào)和合成蛋白的上調(diào),HMGB1和氯沙坦基因敲除模型可阻斷表型轉(zhuǎn)化[10]。當(dāng)HMGB1刺激培養(yǎng)的人血管平滑肌細(xì)胞時(shí),IL-1β的生成明顯增加。HMGB1還增加NLRP3炎癥成分的表達(dá),包括NLRP3、ASC和caspase-1。在TLR 4缺陷細(xì)胞中,HMGB1誘導(dǎo)的caspase-1表達(dá)明顯減弱,轉(zhuǎn)染caspase-1 siRNA的細(xì)胞以及TLR4單克隆抗體或siRNAs處理的細(xì)胞,IL-1β的產(chǎn)生均明顯降低[11]。在冠心病患者血清中,IL-6和TLR 4內(nèi)源性配體HMGB1水平明顯高于正常人。冠心病患者血清HMGB1水平與IL-6水平呈正相關(guān),HMGB 1和IL-6在冠心病患者動(dòng)脈粥樣硬化組織中均有表達(dá)[12]。在缺氧導(dǎo)致的新生兒肺動(dòng)脈高壓中,患兒血清HMGB1水平明顯高于健康對(duì)照組,肺動(dòng)脈高壓消解后HMGB1水平顯著降低,且HMGB1的變化與血清TNF-α和IL-6水平呈正相關(guān)[13]。已有研究證實(shí),血漿IL-17水平與頸動(dòng)脈內(nèi)中膜厚度值呈正相關(guān),提示原發(fā)性高血壓患者隨著頸動(dòng)脈內(nèi)中膜厚度增厚,IL-17濃度相應(yīng)增高,表明血漿IL-17的濃度是間接反映高血壓并動(dòng)脈硬化的進(jìn)展程度的重要指標(biāo)[14]。HMGB1、TLR4在高血壓促炎過程中擔(dān)任著重要角色,可能成為高血壓患者血管重塑的新的生物標(biāo)志物。
本研究顯示,高血壓合并頸動(dòng)脈硬化組患者血清HMGB1和TLR4表達(dá)水平高于單純高血壓組,單純高血壓組血清HMGB1和TLR4表達(dá)水平高于對(duì)照組,高血壓患者通常存在高HMGB1和TRL4血癥,說明長(zhǎng)期高血壓可導(dǎo)致機(jī)體的慢性炎癥反應(yīng)。外周血單核細(xì)胞的HMGB1和TRL4水平顯著高于對(duì)照組,說明高血壓狀態(tài)下炎癥因子HMGB1和TRL4蛋白表達(dá)增高。本研究檢測(cè)HMGB1、TRL4在血清和單核細(xì)胞中的表達(dá)水平,旨在從兩個(gè)不同的方面確定高血壓狀態(tài)下慢性炎癥的存在。本研究還發(fā)現(xiàn),高血壓合并頸動(dòng)脈硬化患者通常存在高IL-17和IL-6血癥,血清IL-17和IL-6水平顯著高于單純高血壓組、對(duì)照組。線性相關(guān)分析結(jié)果顯示,HMGB1、TRL4水平與IL-17、IL-6水平呈正相關(guān),提示原發(fā)性高血壓患者隨著頸動(dòng)脈內(nèi)中膜厚度增厚,HMGB1和TRL4水平升高,IL-17和IL-6濃度也相應(yīng)增高,表明HMGB1和TRL4是參與高血壓及其并發(fā)癥進(jìn)展的重要因素。其機(jī)制可能為:HMGB1和TRL4結(jié)合,啟動(dòng)炎癥反應(yīng),炎性細(xì)胞因子可通過多種途徑進(jìn)入或作用于平滑肌細(xì)胞,導(dǎo)致頸動(dòng)脈硬化。
綜上所述,高血壓合并頸動(dòng)脈硬化患者外周血炎性因子活性和蛋白表達(dá)水平表達(dá)增加,檢測(cè)外周血生物學(xué)指標(biāo)可為頸動(dòng)脈硬化早期診斷及臨床治療確定靶標(biāo)。

