Au-Pd/ZrO2 可見光下催化苯甲醇氧化反應條件探索
白紅亮,王俊生,王 艷
(1.內蒙古自治區水利水電勘測設計院,內蒙古呼和浩特010010;2.內蒙古自治區電力科學研究院;3.內蒙古化工職業學院)
苯甲醛是有機合成中一個非常重要的中間體,在化學工業、食品、醫藥、染料等領域具有廣泛的應用。 傳統方法生產苯甲醛主要采用氯化芐水解或甲苯直接氧化等,得到的苯甲醛中或是含氯離子,或是苯甲醛產率低[1],限制了這些方法的發展。 近年來,采用苯甲醇選擇性催化氧化生產苯甲醛被認為是“綠色”催化合成技術,備受關注且有關報道較多,如T.Mitsudome 等[2]報道水滑石負載Ag 在130 ℃反應10 h,苯甲醇轉化率為100%,苯甲醛選擇性為90%。G.Zhao 等[3]報道以Au/Ni-纖維作為催化劑,以氧氣為氧化劑,在280 ℃下苯甲醇轉化率達到99%,苯甲醛選擇性為98%。 J.Fan 等[4]采用了具有介孔結構的K-Cu-TiO2催化劑,氧氣作為氧化劑,在203~223 ℃下,苯甲醇轉化率為72%,苯甲醛選擇性為98%。 這些報道的負載型催化劑均可高效催化苯甲醇脫氫生產苯甲醛, 但是反應都是需要加熱到一定溫度下才能進行。 因此,開發一種在室溫下能催化苯甲醇脫氫生產苯甲醛的催化劑很值得期待而且具有一定意義。
自1973 年G.C.Bond 等[5]發現Au 能催化烯烴加氫反應后,Au 作為催化劑的研究越來越多[6-7]。Au納米粒子具有表面等離子體共振(LSPR)效應[8],在紫外光區和可見光區具有強烈的吸收。 LSPR 效應是Au 納米粒子導帶上電子震蕩, 與入射光產生電磁共振,在Au 納米粒子表面形成高能電子,這些高能電子可以被激發向反應體系提供電子而激活反應物分子, 同時高能電子也可以躍遷回低軌道向反應提供能量,促進反應發生,所以Au 納米粒子低溫下可被用于光催化有機合成反應[9-11]。
本工作制備了Au-Pd/ZrO2雙金屬催化劑,在溫和條件下用于光催化苯甲醇氧化生產苯甲醛反應。探索了Au-Pd/ZrO2雙金屬催化劑光催化苯甲醇氧化生產苯甲醛反應的最佳條件。
1 實驗部分
1.1 實驗試劑
氯金酸(HAuCl4),純度為99%;氯化鈀(PdCl2),純度為59.8%;氧化鋯(ZrO2),純度為49%;賴氨酸(C6H14N2O2),純度為97%;硼氫化鈉(NaBH4),純度為98%;鹽酸(HCl),分析純;無水乙醇(C2H5OH),分析純;苯甲醇(C7H7OH),純度為98%。
1.2 催化劑的制備
稱取一定量載體ZrO2粉末于500 mL 燒杯中,加入50 mL 二次蒸餾水,磁力攪拌10 min,于超聲清洗儀中超聲10 min,磁力攪拌同時緩慢滴加HAuCl4(或PdCl2)溶液,約30 min 滴加完畢,然后逐一滴加0.53 mol/L 的L-賴氨酸溶液,0.35 mol/L 的NaBH4溶液, 最后加入0.3 mol/L 的HCl 溶液, 使溶液pH保持在8~10,繼續磁力攪拌溶液1 h,然后保鮮膜密封陳化24 h,去清液過濾保留沉淀,并將沉淀用二次水和無水乙醇洗滌,最后將沉淀物置于60 ℃烘箱中12 h,取出收集后放置在干燥器中待用。 根據HAuCl4和PdCl2加入量不同,分別制得Au(3%)/ZrO2,Au-Pd(1∶1)/ZrO2,Au-Pd(2∶1)/ZrO2,Au-Pd(1∶2)/ZrO2,Pd(3%)/ZrO25 種催化劑(各Au-Pd 雙金屬催化劑中Au 和Pd 的總質量分數為3%)。
1.3 苯甲醇催化氧化反應
稱取一定量催化劑和堿于50 mL 圓底燒瓶中,再量取5.0 mL 溶劑和1.0 mmol 反應物苯甲醇于圓底燒瓶中,光反應時,用LED 燈(200 W,波長為200~800 nm)作為照射光源,燈距離反應裝置20 cm,反應過程中磁力攪拌。 為對比反應效果,同時進行暗反應,操作方法同上,但暗反應過程中裝有試樣的燒瓶用錫紙包裹緊密,不被LED 燈光照射。 反應12 h 結束,對光、暗反應溶液取樣,用氣相色譜(GC)進行分析。
2 結果與討論
2.1 X 射線衍射(XRD)分析
圖1 是ZrO2及以ZrO2為載體所制備的負載不同比例金鈀催化劑的XRD 譜圖。 由圖1 可見,所有譜圖 在2θ 為24.1、28.1、31.5、34.1、34.4、40.7、49.3、50.1°處有明顯的衍射峰,這些衍射峰對應于ZrO2的(011)、(-111)、(111)、(002)、(020)、(-211)、(022)、(220)晶面。 負載不同比例金鈀催化劑的譜圖沒有Au 和Pd 的特征衍射峰,原因可能是由于Au、Pd 含量低或者Au、Pd 形成了無定形納米粒子所致[12-13]。
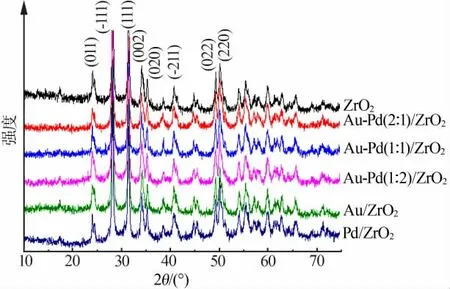
圖1 不同催化劑的XRD 譜圖
2.2 紫外-可見漫反射光譜(UV-vis DRS)分析
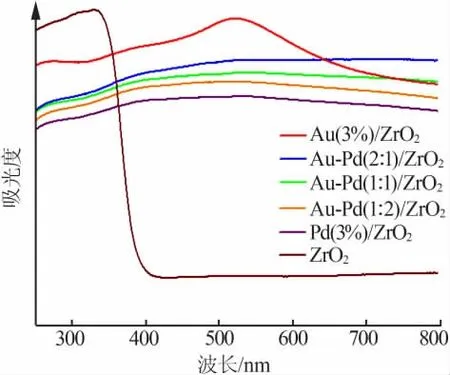
圖2 不同催化劑的UV-vis DRS 譜圖
為了解Au(3%)/ZrO2、Au-Pd(1∶1)/ZrO2、Au-Pd(2∶1)/ZrO2、Au-Pd(1∶2)/ZrO2、Pd(3%)/ZrO2及ZrO2對光的響應情況,對所制備的催化劑及ZrO2進行了紫外-可見漫反射光譜測試,結果見圖2。圖2 顯示,金鈀雙金屬催化劑與單金屬金、 鈀及載體的紫外-可見漫反射光譜有較大區別。載體ZrO2在可見光區沒有吸收;Au/ZrO2在可見光區530 nm 處有較強吸收峰,主要歸因于區域等離子體共振效應[14-15];在Au-Pd/ZrO2雙金屬催化劑的UV-vis 圖中, 沒有檢測到Au 納米粒子的吸收峰,說明Au、Pd 兩種元素之間協同效應使得Au 納米粒子的表面等離子體共振吸收峰消失,可進一步驗證Au-Pd 形成了雙金屬催化劑。
2.3 透射電子顯微鏡(TEM)分析
圖3 是Au-Pd(1∶2)/ZrO2催化劑的TEM 圖。 從圖3 觀察到,制備的催化劑中金、鈀以球形顆粒均勻分散在載體上,幾乎沒有團聚;對TEM 照片中大量金、 鈀顆粒粒徑進行測量, 測量結果繪制粒徑分布圖,見圖4。 圖4 顯示其粒徑均小于8 nm,平均粒徑為5.5 nm。其他幾種催化劑的TEM 測試也得到相同結果,由此說明獲得的是納米級負載型催化劑。

圖3 Au-Pd(1∶2)/ZrO2 催化劑的TEM 圖
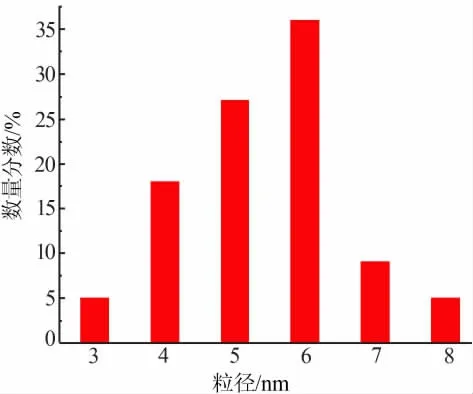
圖4 Au、Pd 納米粒子的粒徑分布圖
3 Au-Pd/ZrO2 納米粒子催化苯甲醇氧化反應
3.1 溶劑對苯甲醇氧化反應的影響
反應物苯甲醇為1.0 mmol、反應時間為12 h、反應溫度為(35±3)℃、堿為1.0 mmol KOH、催化劑Au-Pd(1∶1)/ZrO2用量為50 mg、溶劑用量為5 mL 的條件下, 考察不同溶劑對苯甲醇氧化反應生成苯甲醛的影響,結果見表1。 由表1 可知,苯甲醇氧化反應時溶劑不同,苯甲醇轉化率、苯甲醛的產率差別較大;反應過程中,隨反應溶劑極性增強,苯甲醛產率呈現出先增大后減小的趨勢, 可能是因為溶劑的極性過強,導致催化劑的穩定性降低[16]。溶劑為異丙醇時,苯甲醇轉化率、苯甲醛產率最高,光照時苯甲醛產率達到62.0%。
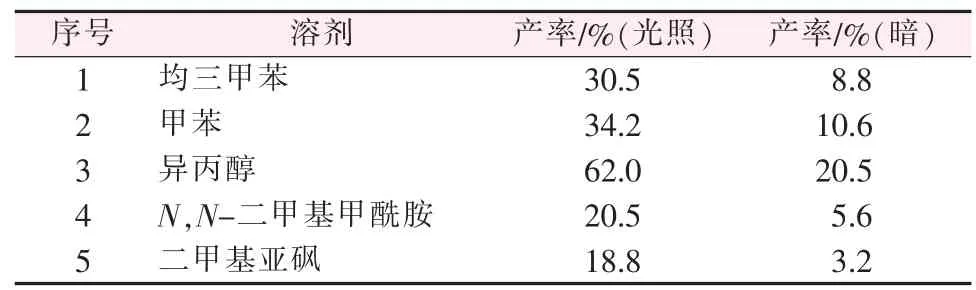
表1 不同溶劑對苯甲醇氧化反應的影響
3.2 堿和催化劑組成對苯甲醇催化氧化反應的影響
為了探尋Au-Pd/ZrO2雙金屬納米粒子催化苯甲醇氧化反應的最佳條件, 在反應過程中固定金鈀總負載量為3%, 改變Au-Pd/ZrO2納米催化劑中金鈀比例, 并且反應時采用了Na2CO3、K2CO3、CsCO3、KOH、NaOH 等不同堿,催化苯甲醇氧化。 催化反應條件為苯甲醇用量為1.0 mmol、堿用量為1.0 mmol、催化劑用量為50 mg、溶劑異丙醇用量為5 mL、溫度為(35±3)℃、反應時間為12 h、空氣氣氛,結果見表2。
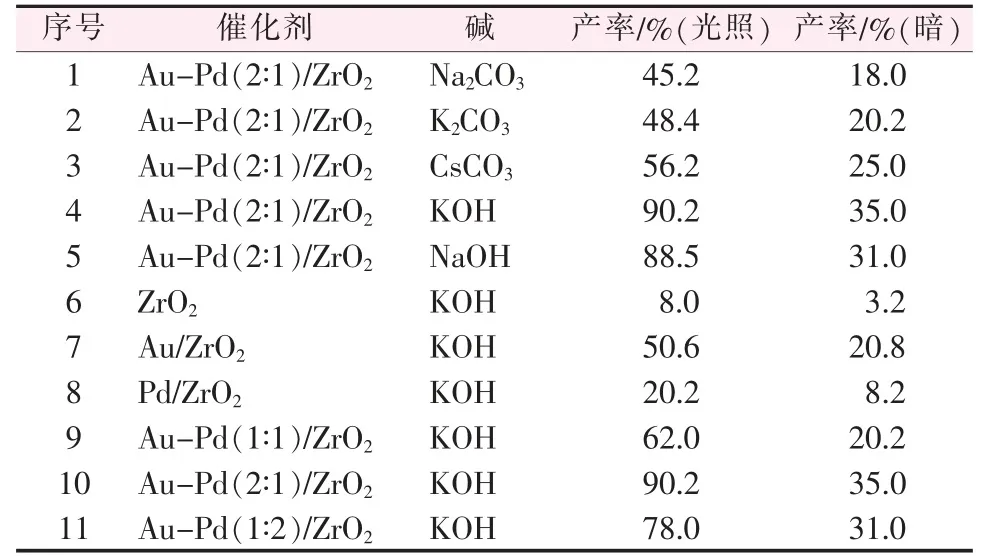
表2 不同催化劑和堿對苯甲醇氧化反應的影響
表2 數據顯示,在苯甲醇氧化反應中,催化劑組成和堿的種類影響了反應產物的產率。 從表2 可看出,無論采用哪一種堿,反應產率都明顯是光反應高于暗反應,但是當Na2CO3、K2CO3、CsCO3作為堿源時光催化劑活性相對于KOH、NaOH 堿源低。 KOH、NaOH為堿源時,苯甲醛產率很高,其原因可能是因為反應物對KOH、NaOH 等強堿更敏感[17]。 載體對苯甲醇氧化催化活性非常低, 單金屬金、 鈀有一定催化活性,但是沒有Au-Pd/ZrO2雙金屬催化劑的催化活性好, 產生上述現象歸因于雙金屬催化劑中Au 和Pd之間形成協同效應[18]。在雙金屬催化劑中,Au-Pd(2∶1)/ZrO2催化效果最佳,苯甲醛產率可達90.2%。
3.3 光波長對苯甲醇氧化反應的影響
為進一步證明Au-Pd/ZrO2雙金屬催化劑催化苯甲醇氧化反應是光催化反應, 測試了光照反應時不同光波長對苯甲醇氧化反應的影響。反應條件為:苯甲醇為1.0 mmol、KOH 為堿源(1.0 mmol)、Au-Pd(2∶1)/ZrO2催化劑為50 mg、溶劑為異丙醇(5 mL)、溫度為(35±3)℃、反應時間為12 h。 通過濾波片變化照射光的波長范圍,測試的波長范圍分別為400~800 nm、450~800 nm、500~800 nm、550~800 nm、600~800 nm,結果見圖5。 由圖5 可見,隨波長范圍的減小苯甲醇氧化反應的轉化率逐漸降低, 并且當波長范圍達到550~800 nm 時,苯甲醇氧化反應轉化率明顯降低。 這一結果與Au 納米粒子在光波長為520 nm 附近有強烈吸收現象一致,進一步說明Au-Pd/ZrO2雙金屬催化劑利用了可見光催化苯甲醇氧化反應。

圖5 波長對苯甲醇氧化反應的影響
4 結論
本文制備了不同金、鈀比例的Au-Pd/ZrO2催化劑并研究了Au-Pd/ZrO2光催化苯甲醇氧化生產苯甲醛反應。 研究結果表明:1)苯甲醇氧化反應時,催化劑組成、反應溶劑、反應用堿種類均影響苯甲醇氧化反應。2)通過光、暗反應測試對比以及改變反應時光波長,結果都證明Au-Pd/ZrO2雙金屬催化劑催化苯甲醇氧化反應是光催化反應。3)反應最佳條件為:反應溫度為(35±3)℃、催化劑Au-Pd(2∶1)/ZrO2為50 mg、溶劑為異丙醇、KOH(1.0 mmol)為堿源,在此條件下苯甲醇氧化生產苯甲醛反應效果最佳,苯甲醛產率可達90%以上。

