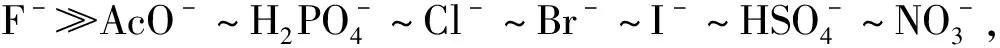一種新型識別F-的硝基脲酰肼熒光化學(xué)傳感器
李 丹,閆 冰,黃葦葦
(燕山大學(xué) 環(huán)境與化學(xué)工程學(xué)院,河北 秦皇島 066004)
0 引言
陰離子在自然界普遍存在[1-6]。在生物體中,遺傳信息DNA的載體是陰離子,大多數(shù)酶底物和輔因子(例如5′-三磷酸腺苷,簡稱ATP)也是陰離子。在鹵化物中,氯離子廣泛存在于細(xì)胞外液中,一旦調(diào)節(jié)不當(dāng)便會引發(fā)系列疾病,如囊性纖維化[7];碘離子是合成甲狀腺激素的必要物質(zhì)[8];碳酸氫根的存在對于維持體內(nèi)pH值是非常重要的。尤其是氟離子的檢測意義重大,因為它是人體骨骼和牙齒成型所必需的微量元素之一[9-10],但過量攝入氟離子會引起諸如骨質(zhì)疏松癥、膠原蛋白降解等許多問題,被統(tǒng)稱為氟中毒病[11-12]。由此可見,氟離子對人體是否有益直接依賴于它的濃度。根據(jù)世界衛(wèi)生組織(WHO)的規(guī)定,飲用水中氟離子的最高允許限值為1.5 mg/L。因此,設(shè)計具有選擇性識別特定陰離子的受體分子吸引了越來越多的科研人員的關(guān)注。
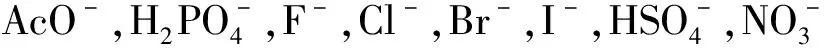
1 受體分子1的合成
1.1 實驗材料和儀器
除特別指明外,所用試劑均為市售分析純,使用之前未做純化處理。另外,實驗中用來配制溶液及清洗儀器所用的水均為蒸餾水。二甲基亞砜(DMSO)使用之前加入少許氧化鈣(CaO),室溫干燥24 h后,減壓蒸餾得到。乙醇使用之前經(jīng)金屬鎂條處理,然后蒸餾后得到。四丁基銨鹽陰離子使用前用干燥劑五氧化二磷(P2O5)在60 ℃下真空干燥24 h。
本實驗過程中所用到的實驗儀器主要有XT-4熔點儀(北京泰克儀器有限公司);DHG-101-3A電熱恒溫鼓風(fēng)干燥箱(鄭州予華儀器制造有限公司);RF-02B旋轉(zhuǎn)蒸發(fā)儀(上海普渡生化科技有限公司);Aglient QQQ MS 6460質(zhì)譜儀(安捷倫公司);UNITY-plus 400 MHz核磁共振波譜(美國Varian公司);FT-IR650紅外波譜儀(天津港東儀器有限公司);VarioEL元素分析儀(德國賽明公司);Shimadzu UV2450紫外分光光度計(日本島津公司);HITACHI F-7000熒光光譜儀(日本日立公司)等。
1.2 受體分子1的合成路線
受體分子1的合成路線如圖1所示。參考文獻(xiàn)[13-14]方法,在氯化氫氣氛下,以蒽為原料與低聚甲醛在1,4-二氧六環(huán)中反應(yīng)得到中間體9,10-二氯甲基蒽M1。M1進(jìn)一步氧化得到蒽-9,10-二醛M2。以三光氣為原料與鄰硝基苯胺在乙酸乙酯中反應(yīng)得到中間體鄰硝基異氰酸酯。鄰硝基異氰酸酯和水合肼進(jìn)一步反應(yīng)得到中間體鄰硝基苯基氨基脲M3。M2與M3在乙醇中加熱回流得到受體1。
圖1 受體1的合成路線
Fig.1 The synthesis route of1
1.3 受體分子1的合成
在加熱回流的條件下,將0.234 g M2溶于適量的絕對乙醇中,向該溶液中緩慢滴加0.424 g M3的乙醇溶液。滴完后,滴加幾滴冰乙酸,有紅色沉淀生成,繼續(xù)回流2 h。過濾,用熱乙醇洗滌,干燥稱得橙色固體受體分子1為0.452 g,產(chǎn)率為84 %,m.p.:314~316 ℃。1H NMR(400 MHz,DMSO-d6)δH:7.24(t,2H,Anthracene-H),7.77(d,4H,Anthracene-H),8.17(s,2H,Anthracene-H),8.65(s,4H,Ar-H),8.98(s,2H,Ar-H),9.22(s,2H,C-H),10.88(s,2H,N-H),11.51(s,2H,C-H),11.64(s,2H,N-H);([M+H]+):591.2;C30H22N8O6的元素分析,理論計算值:C,61.01;H,3.75;N,18.97;檢測值:C,60.88;H,3.66;N,18.83;IR(KBr):3 435 cm-1:νN-H,3 121 cm-1:νC-H,2 976 cm-1:νC-H,1 711 cm-1:νC=O,1 507 cm-1:νC=N,1 345 cm-1:δC-H,738 cm-1:δAr-H。
2 結(jié)果與討論
2.1 受體分子1與陰離子的紫外-可見光譜分析
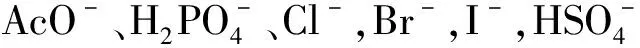
圖2 受體1加入不同陰離子的UV-vis光譜變化
Fig.2 The UV-vis spectra of different anions for acceptor molecule1
圖3 向受體1的DMSO溶液分別加入不同陰離子引起溶液顏色的變化
Fig.3 Color changes of receptor1in DMSO in absence and presence of anions
接著利用紫外吸收方法研究了298 K下,在DMSO溶液中受體分子和F-之間的相互作用。如圖4所示,受體分子1(2×10-5M)在275 nm,425 nm處有兩個明顯的主吸收峰。隨著F-的不斷加入,275 nm,425 nm處的吸收強(qiáng)度逐漸降低,并且在525 nm處出現(xiàn)一個新的吸收峰,同時在525 nm,325 nm處的吸收強(qiáng)度慢慢增強(qiáng)。這是由于受體分子1中的識別位點-NH本身是弱的電子供體,當(dāng)F-加入后,F(xiàn)-與受體分子1之間通過氫鍵結(jié)合,使-NH上的電子密度增大,供電子能力增強(qiáng),這時候,電子在分子內(nèi)迅速轉(zhuǎn)移到與之相鄰的苯環(huán)上,使得受體分子1在525 nm吸收峰出現(xiàn)了紅移的現(xiàn)象。同時,受體分子1溶液的顏色由淺黃色變?yōu)樯钭仙4送猓瑥膱D4還可以清楚地看到在280 nm、355 nm和455 nm處有3個等吸收點。這說明在滴定過程中,1與F-之間形成了具有確定計量比的主客體絡(luò)合物[15]。
圖4 受體1滴定F-的吸收光譜變化
Fig.4 UV-vis spectra changes of solution1upon addition of F-in DMSO
2.2 受體分子1與陰離子的熒光光譜分析
圖5為當(dāng)激發(fā)波長λex=400 nm時,在DMSO溶液中,加入F-后,對受體分子1(2×10-5M)的熒光光譜產(chǎn)生的影響。當(dāng)沒有加入F-時,受體分子1表現(xiàn)出較弱的熒光強(qiáng)度,隨著F-的不斷加入,525 nm處的熒光強(qiáng)度顯著增強(qiáng)。這可能是由于受體1與F-結(jié)合后,形成的受體與陰離子絡(luò)合物剛性增加,一方面通過分子運動引起的損失減少,熒光量子產(chǎn)率提高;另一方面分子共面性增加,有利于Frank-Condom躍遷的實現(xiàn),熒光強(qiáng)度增強(qiáng)。由圖5插圖還可以看到在紫外燈365 nm的激發(fā)下受體1溶液以及1與F-相互作用的熒光照片,可以明顯的看出熒光強(qiáng)度增加。
圖5 受體1滴定F-的熒光光譜變化
Fig.5 Fluorescence emission changes of receptor1upon the addition of F-
2.3 受體分子1與陰離子的1H NMR滴定分析
采用核磁滴定的方法進(jìn)一步探究受體分子1識別F-的機(jī)理,研究了加入F-前后受體分子1(1.0×10-2M)在DMSO-d6中的質(zhì)子位移的變化。從圖6可以看出,出現(xiàn)在11.64 ppm和10.88 ppm是受體上-NH的質(zhì)子峰,分別標(biāo)記為Ha和Hb。當(dāng)加入0.4摩爾當(dāng)量的F-時,Ha 和Hb質(zhì)子峰的信號開始減弱,同時苯環(huán)上的-H也略微向高場移動。這是由于1與F-結(jié)合后使脲上的-NH的電荷密度增大,同時由于苯環(huán)的拉電子效應(yīng),促進(jìn)受體分子內(nèi)的電子從脲上的-NH向苯環(huán)移動,使苯環(huán)上的電子密度增大,苯環(huán)上氫原子的化學(xué)位移向高場移動,這樣可以推斷受體和F-形成了氫鍵。隨著F-濃度的增大,Ha信號比Hb的信號變化的要明顯,最終接近消失,這可能是由于Ha所連接的苯環(huán)具有的拉電子效應(yīng),使Ha比Hb活潑更易離去,發(fā)生去質(zhì)子化過程。
圖6 向受體1加入F-的氫譜圖
Fig.61H NMR of adding F-to receptor1in DMSO-d6
2.4 受體分子1與陰離子的結(jié)合常數(shù)
選取波長為527 nm處的熒光數(shù)據(jù)進(jìn)行計算擬合,得到受體分子1與F-的Hill方程為Y=2.019 1X+5.202 6,其中Hill系數(shù)為n=2.019 1(n≈2),說明受體1與F-的結(jié)合比為1∶2,結(jié)合常數(shù)lgKass為5.20,見圖7。
圖7 受體1的熒光強(qiáng)度在525 nm(F525)與不斷變化的log[A]的Hill方程
Fig.7 The fluorescence intensity of1at 525 nm(F525)and changing log[A]Hill equation
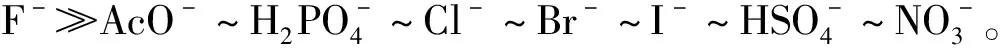
表1 受體1與不同陰離子的結(jié)合常數(shù)
Tab.1 Binding constants of receptor1with different anions

陰離子lgKassaF-5.20AcO-NDbH2PO-4NDbCl-NDbBr-NDbI-NDbHSO-4NDbNO-3NDb
注:a由熒光光譜數(shù)據(jù)計算得出;bND光譜變化太小未得到結(jié)合常數(shù)。
根據(jù)以上的實驗結(jié)果,推測受體分子1與F-的結(jié)合方式為圖8所示。
圖8 受體1與F-在溶液中可能的結(jié)合模式
Fig.8 Possible binding modes of receptor1and F-in solution
3 結(jié)論