胃癌的脈管侵犯及預后影響因素
楊玉杰,黃曉東,楊超,程煌榮,黎華麗,鄭勇斌
武漢大學人民醫院,武漢 430060
胃癌是全球常見的惡性腫瘤之一,嚴重威脅人們的身體健康[1]。近年來,胃癌患者的有效治療手段以根治性手術為主并輔以化學藥物治療,患者預后得到明顯改善,但術后仍然普遍面臨復發轉移風險[2]。隨著腫瘤分期的進展,腫瘤細胞侵入腫瘤附近組織的血管和淋巴管,脈管侵犯(LBVI)是不同類型癌癥的腫瘤細胞發生擴散和轉移的關鍵環節[3~6]。有學者報道,在淋巴結轉移陰性的Ⅱ期胃癌患者中,LBVI是其不良預后的重要指標[7]。LBVI作為一種預后不良的獨立指標,對于指導胃癌患者進行合理的手術、選擇輔助治療或新輔助治療具有重要意義。盡管超聲胃鏡、CT和MRI等影像學技術被廣泛用于胃癌患者術前檢查,但是LBVI很難有效檢測,需要術后組織病理學診斷。目前,已有研究從患者術前腫瘤相關標志物、中性粒細胞與淋巴細胞比值(NLR)、PLT與淋巴細胞比值(PLR)等檢驗及CT、MRI等檢查對LBVI進行預測,但均未能達到預期效果[8~10]。本文回顧性分析了356例胃癌患者的臨床病理資料,并探討胃癌發生LBVI及預后的危險因素,旨在為胃癌患者的治療及預后評估提供參考。
1 資料與方法
1.1 臨床資料 選取2015年6月~2018年6月在武漢大學人民醫院行胃癌根治術的患者356例。納入標準:①原發性胃癌并行胃癌根治術;②術后病理證實為胃癌;③術前均未行放化療及生物靶向治療;④臨床病理資料和隨訪結果完整。排除標準:①胃癌復發行手術者;②合并其他系統惡性腫瘤者;③術后其它意外原因所致的死亡;④臨床病理資料及隨訪缺失患者。根據是否發生LBVI分為LBVI陽性者(221例,中位生存時間26個月)、LBVI陰性者(135例,中位生存時間31個月)。
1.2 研究方法 收集患者以下資料:①一般指標:性別、年齡;②炎癥間接比值指標:NLR、PLR,依據診斷性ROC曲線最佳cut-off值確定指標分界值;③術前實驗室檢測指標:中性粒細胞絕對值、淋巴細胞絕對值、超敏CRP、CEA、CA72-4、CA199、CA125等指標臨界值采用本實驗室檢查正常值的上限;④術后病理資料:分化程度(參照日本胃癌處理公約第15版規定)、腫瘤直徑、T分期、淋巴結轉移、TNM分期、LBVI。術后患者的隨訪由醫院隨訪組及胃腸外科工作人員定期通過電話隨訪及門診隨訪等形式完成,隨訪截止日期為2018年12月,總生存時間為手術日期至隨訪截止日期或死亡日期。
1.3 統計學方法 采用SPSS23.0統計軟件。采用χ2檢驗比較LBVI陽性者和LBVI陰性者的臨床資料,應用多因素Logistic回歸分析法分析胃癌發生LBVI的危險因素;對LBVI陽性與陰性患者應用Kaplan-Meier法計算中位生存時間,并繪制生存曲線,采用單因素及多因素COX比例風險回歸模型分析預后危險因素。P<0.05為差異有統計學意義。
2 結果
2.1 胃癌發生LBVI的影響因素 單因素分析顯示,性別、超敏CRP、CEA、分化程度、腫瘤直徑、T分期、淋巴結轉移、TNM分期是胃癌發生LBVI的影響因素(P均<0.05),詳見表1。多因素回歸分析顯示,腫瘤分化不良、直徑大、浸潤深度深、淋巴結轉移、TNM分期晚是胃癌發生LBVI的危險因素(P均<0.05),詳見表2。

表1 胃癌發生LBVI的單因素分析結果
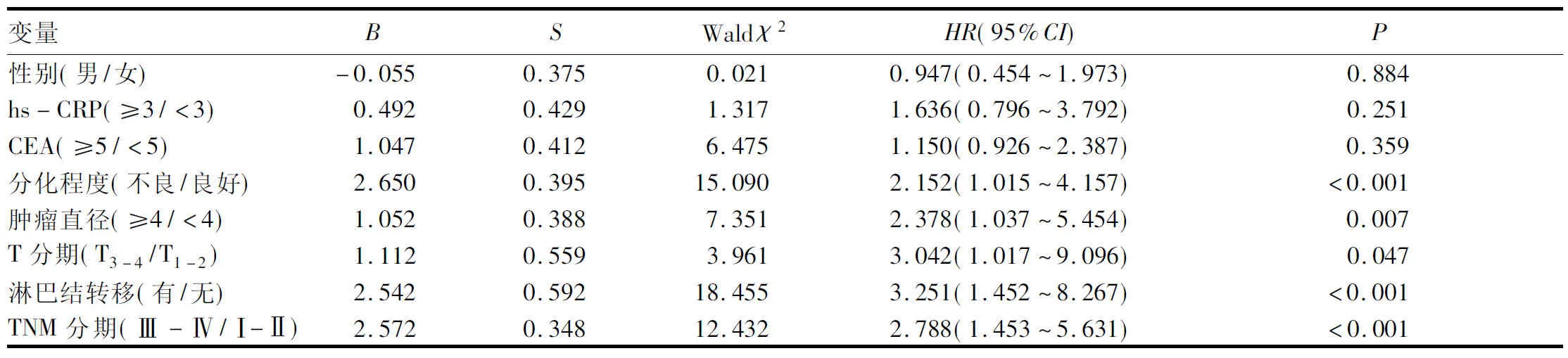
表2 胃癌發生LBVI的多因素分析結果
2.2 胃癌預后的影響因素 單因素分析顯示,腫瘤分化程度、腫瘤直徑、浸潤深度、淋巴結轉移、TNM分期是胃癌預后的影響因素(P均<0.05),詳見表3。多因素分析顯示,腫瘤分化不良、浸潤深度深、淋巴結轉移、TNM分期晚、LBVI是胃癌預后的危險因素(P均<0.05),詳見表4。

表3 胃癌預后的單因素分析結果
3 討論
胃癌常表現為腹痛、進食后飽脹、黑便等,其非特異性的消化道癥狀容易被患者所忽視,大部分患者就診時已錯過最佳治療時機。胃癌的治療方式主要是以根治性手術切除原發病灶為主,對分期較晚的患者術后輔以新輔助化療或新輔助放療,其他的治療方式還有靶向治療、免疫治療等[11]。原發腫瘤切除后發生腫瘤復發及轉移更是影響胃癌患者術后生存時間的主要原因,腫瘤的轉移多經過血行或淋巴轉移,發生LBVI是腫瘤轉移的一個征象[12]。有研究顯示,LBVI是影響胃癌預后的獨立預測因子,并且是胃癌術后復發的重要危險因素之一[13]。腫瘤對大血管的侵犯可經術前影像學檢查或術中探查發現,但微小的LBVI僅能在術后病理中發現,因此研究胃癌發生LBVI的影響因素具有重要意義。
有文獻[13]報道,胃癌伴LBVI的發生率約為34.3%。而本研究中LBVI的發生率達到了62.1%,此差異可能是各研究中心對LBVI的診斷未達成共識以及納入研究的樣本量不足等所致。Gao等[13]和Li等[14]發現,胃癌發生LBVI與分化程度、腫瘤大小、腫瘤浸潤深度以及淋巴結轉移相關。本研究顯示,分化不良的胃癌患者LBVI發生率明顯高于分化良好組,提示分化不良的腫瘤容易發生侵襲。本研究還發現,腫瘤直徑大者容易發生LBVI,此結果與Gao等[13]研究結果一致,說明腫瘤生長速度快或者分期較晚,越有可能發生LBVI。此外,腫瘤浸潤深度以及淋巴結轉移也與LBVI密切相關。本文結果顯示,浸潤深度為T3~T4期的胃癌發生LBVI的相對危險度是T1~T2期的3.042倍,淋巴結轉移陽性胃癌患者LBVI的相對危險度是未發生淋巴結轉移的3.251倍,此結果與李禹等[15]文獻報道相似。
早期胃癌是病灶浸潤黏膜或黏膜下層,而無論有無淋巴結轉移。隨著腫瘤進展,腫瘤越可能發生LBVI及微轉移。Liu等[16]發現,T1期的早期胃癌患者LBVI并非其預后的危險因素。而對于進展期胃癌而言,腫瘤浸潤深度增加,淋巴轉移率高,LBVI以及轉移的發生機會隨之增大,預后相對較差。Kim等[17]報道,LBVI對胃癌患者的生存有顯著影響,但并未被確立為一個獨立的預后因素,LBVI與腫瘤的進展密切相關,可能是導致這種陰性結果的原因。Du等[18]和Zhao等[19]發現,在淋巴結轉移陰性的胃癌患者中,LBVI是其獨立預后標志物;Li等[14]的研究也表明,LBVI是胃癌術后復發及預后不良的獨立指標,確定個體治療的方案應考慮LBVI的狀態。本研究表明,胃癌發生LBVI的中位生存時間短于未發生LBVI組,且COX多因素回歸分析表明胃癌發生LBVI的死亡風險是無LBVI的1.899倍。LBVI是胃癌侵襲的潛在標志,可提供更多關于腫瘤復發和預后的風險信息。在目前的TNM分期系統中加入LBVI評估可能為評估胃癌預后提供更準確的風險分層,以便制定更合適的治療策略。最近的隨機對照試驗證明了對于II期或III期接受D2胃切除手術的胃癌患者,術后以卡培他濱加奧沙利鉑的輔助治療方案有更好的預后[20]。
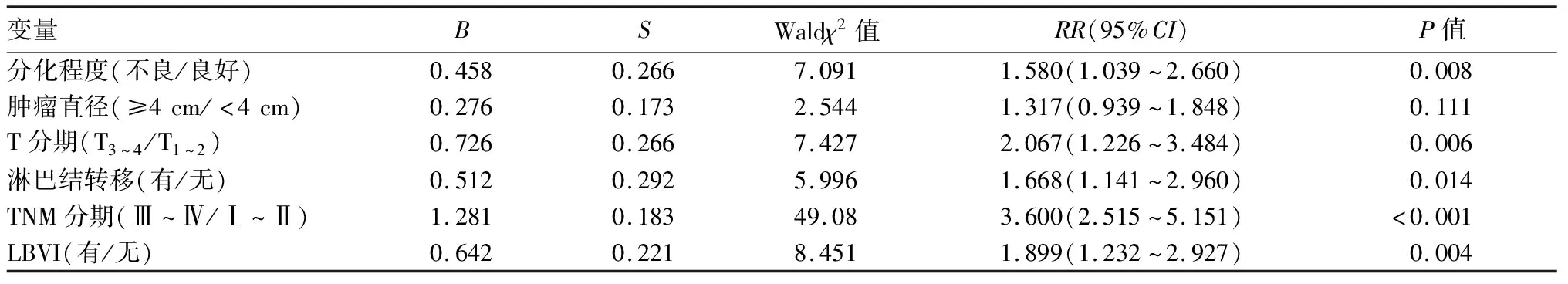
表4 胃癌預后的多因素分析結果
總之,腫瘤分化不良、直徑大、浸潤深度深、淋巴結轉移及TNM分期晚的胃癌患者更易發生脈管浸潤;腫瘤分化不良、浸潤深度深、淋巴結轉移及TNM分期晚的胃癌預后較差。

