一鍋法合成含三氟甲基四氫苯并吡喃酮衍生物的研究
李冬梅,崔瀟婷
(江蘇農牧科技職業學院,江蘇 泰州 225300)
苯并吡喃及其衍生物廣泛存在于各種天然有機化合物中,尤其是在植物,很多都具有抗炎和抗菌的活性,在醫藥方面有著廣泛的應用。其中苯并二氫吡喃衍生物可作用于乳腺癌細胞[1],還可以抗骨質疏松以及降血糖[2-3]。因此,苯并吡喃及其衍生物一直是藥理學家們和有機合成化學家們研究的興趣所在。傳統的合成方法往往采用多步合成的方法,導致操作繁瑣,分離和純化復雜,因此三組分及以上的一鍋法一直是近年來藥物化學或有機化學各領域研究的熱點[4-6]。
Hantzsch反應一直是近幾年研究得比較多的一類反應[7-9]。S K Ko等[10]報導了以碘作為催化劑得到二氫吡喃化合物(DHPs)的合成方法:

本文綜合文獻方法,設計了一種新的含氟二氫苯并吡喃酮衍生物的合成路線。因為三氟乙酰乙酸乙酯方便易得,所以我們用三氟乙酰乙酸乙酯作為含氟砌塊,和1,3-環己二酮(2)、芳醛(1a-e)為反應底物,I2/NH4OAc體系中,室溫下反應,僅需幾分鐘反應就能完成,見表1。


表1 2-三氟甲基-3,4,7,8-四氫-2H-苯并吡喃酮衍生物的合成
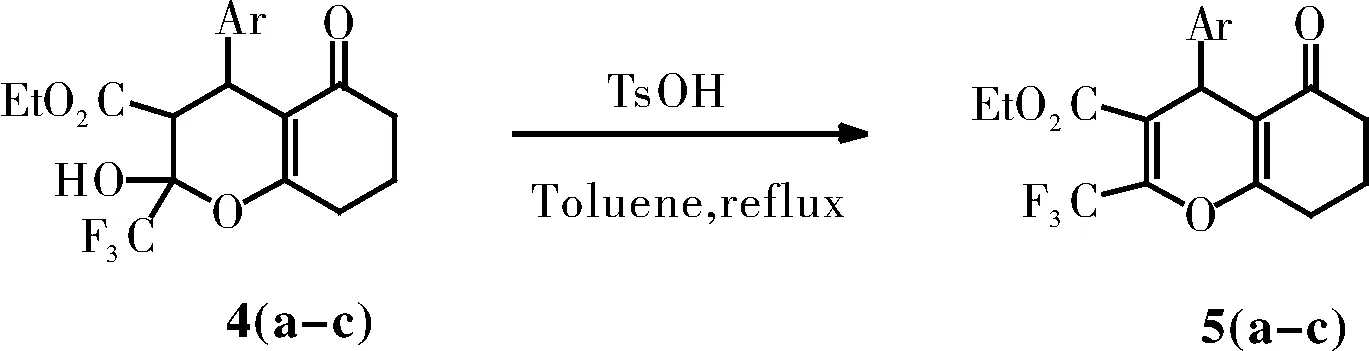
接著我們還探索了化合物4(a-c)的脫水反應,化合物4在POCl3/Py、concd. H2SO4、P2O5等條件下都不能脫水;只有在p-TsOH(1.2 equiv.)/Toluene條件下加熱回流,脫水反應才能夠發生。該反應用19F NMR跟蹤反應物的轉化情況,12 h后顯示反應物并沒有完全轉化,延長至24 h分離,產率分別為63%,75%,78%。
1 實 驗
1.1 儀器與試劑
1H-NMR譜用Bruker AM-300 (300 MHz) 型核磁共振儀測定,TMS作內標;19F-NMR譜用Bruker AM-300 (282 MHz) 型核磁共振儀測定,以CF3Cl為外標,高場為負。除非特殊說明核磁共振測定均用CDCl3作溶劑。紅外光譜(IR)用Perkin-Elmer 983型紅外分光光度計測定,固體樣品采用KBr壓片法,液體樣品采用液膜法。低分辨質譜用HP 5989A型質譜儀測定,電子能量為70 eV;高分辨質譜用Finnigan MAT 8430型質譜儀測定。X-ray由Rigaku FCR Diffractimer測定。元素分析均由本所分析測試中心測定。熔點未經校正。柱層析用煙臺化工廠生成的硅膠-H (10~40 μ)。所用溶劑和試劑除特殊說明外均按標準方法純化或處理。
1.2 典型操作
1.2.14的合成通法
室溫下向1,3-環己二酮(0.112 g,1 mmol)的DMF (5 mL)溶液中加入等當量的苯甲醛1a(0.106 g,1 mmol)三氟乙酰乙酸乙酯2(0.184 g,1 mmol)和醋酸銨(0.077 g,1 mmol)后,再加入催化量(0.3 equiv.)的I2(0.076 g,0.3 mmol),室溫攪拌約5 min后,TLC顯示反應完全。常規處理,乙酸乙酯萃取后旋干溶劑,得粗產率92%,乙醇重結晶。
4a:白色固體; Mp. 188~192 ℃;FT-IR υmax(KBr, cm-1): 3465, 3050, 2985, 2774, 2585, 1741, 1610, 1373, 1354, 1238, 1193, 1162, 1018, 704, 619;1H NMRδH(CDCl3): 7.26~7.08(m, 5H, ArH), 5.57(s, 1H, OH), 4.04(q, 2H,J=7.2 Hz, CH2), 3.94(d, 1H,J=11.7 Hz,CH), 2.98(d, 1H,J=11.7 Hz, CH), 2.60(m, 2H, CH2), 2.34(m, 2H, CH2), 2.04(m. 2H, CH2), 1.00(t, 3H,J=7.2 Hz, CH3);19F NMR(CDCl3, 282 MHz) δ -84.19(s, 3F); MS(70 eV, EI) m/z(%): 384(M+, 3.46), 311([M-CO2Et]+, 47.32), 241([M-1-CF3-CO2Et]+, 100), 199([M-1-CF3COCH2CO2Et]+, 33.20), 69(CF3+, 66.20); Anal.calcd for C19H19O5F3: C, 59.38; H, 4.95; Found: C, 59.29; H, 4.78。
4b:白色固體; Mp. 208~210 ℃; FT-IR υmax(KBr, cm-1): 2980, 2773, 2584, 1738, 1609, 1477, 1430, 1373, 1357, 1083, 1069, 1030, 1015, 970, 791, 697;1H NMRδH(CDCl3): 7.26~6.98(m, 4H, ArH), 5.53(s, 1H, OH), 4.08(q,J=7.2 Hz, 2H, CH2), 3.92(d,J=11.7 Hz, 1 H, CH), 2.92(d,J=11.7 Hz, 1 H, CH), 2.61(m, 2 H, CH2), 2.32(m, 2 H, CH2), 2.04(m. 2 H, CH2), 1.04(t,J=7.2 Hz, 3 H, CH3);19F NMR(CDCl3, 282 MHz)δ-84.14(s, 3F);MS(70 eV, EI) m/z(%): 420/418(M+, 2.70/6.92), 236/234([M- CF3COCH2CO2Et]+, 2.63/33.46), 199([M-Cl-CF3COCH2CO2Et]+, 100), 155([CF3COCH2CO2Et-CF3]+, 48.46), 69(CF3+, 34.39); Anal.calcd for C19H18ClO5F3: C, 54.48; H, 4.30; Found: C, 59.24; H, 4.32。
4c:白色固體; Mp. 190~192 ℃; FT-IR υmax(KBr, cm-1): 2980, 2777, 2586, 1741, 1607, 1517, 1427, 1372, 1355, 1192, 1163, 1030, 1018, 729, 515;1H NMRδH(CDCl3): 7.26~6.96(m, 4 H, ArH), 5.57(s, 1 H, OH), 4.05(q,J=7.2 Hz, 2H, CH2), 3.91(d,J=11.7 Hz, 1 H, CH), 2.96(d,J=11.7 Hz, 1 H, CH), 2.60(m, 2 H, CH2), 2.30(m, 2 H, CH2), 2.28(s, 3 H, CH3), 2.03(m. 2 H, CH2), 1.03(t,J=7.2 Hz, 3 H, CH3);19F NMR(CDCl3, 282 MHz)δ-84.21(s, 3F); MS(70 eV, EI) m/z(%): 398(M+, 12.24), 325([M-CO2Et]+, 13.65), 255([M-1-CF3-CO2Et]+, 36.85), 213([M-1-CF3COCH2CO2Et]+, 31.03), 199([M-CF3COCH2CO2Et-CH3]+, 100), 69(CF3+, 15.95);Anal.calcd for C20H21O5F3: C, 60.30; H, 4.28; Found: C, 60.20; H, 5.42。
4d:白色固體; Mp. 182~184 ℃; FT-IR υmax(KBr, cm-1): 3566, 2963, 2779, 2585, 1741, 1608, 1514, 1466, 1373, 1355, 1236, 1189, 1163, 1128, 1112, 1069, 1031, 1018, 971, 837, 525;1H NMRδH(CDCl3): 7.03~6.79(m, 4 H, ArH), 5.58(s, 1 H, OH), 4.07(q,J=7.2 Hz, 2H, CH2), 3.91(d,J=11.7 Hz, 1 H, CH), 2.96(d, 1 H,J=11.7 Hz, CH), 2.58(m, 2 H, CH2), 2.31(m, 2 H, CH2), 2.02(m. 2 H, CH2), 1.04(t,J=7.2 Hz, 3 H, CH3);19F NMR(CDCl3, 282 MHz) δ -84.06(s, 3F); MS(70 eV, EI) m/z(%): 414(M+, 16.36), 341([M-CO2Et]+, 15.81), 271([M-1-CF3-CO2Et]+, 42.61), 229([M-1-CF3COCH2CO2Et]+, 100), 199([M-CF3COCH2CO2Et-OCH3]+, 60.75), 69(CF3+, 33.46); Anal.calcd for C20H21O6F3: C, 57.97; H, 5.07; Found: C, 57.76; H, 5.20。
4e:白色固體; Mp. 208~210 ℃; FT-IR υmax(KBr, cm-1): 3091, 2989, 2785, 1734, 1612, 1521, 1373, 1348, 1241, 1206, 1163, 1028, 1010, 734;1H NMR δH(DMSO-d6): 8.22(d, 2 H, ArH), 7.55(d, 2 H, ArH), 4.22(s, 1 H, OH), 4.03(q,J=7.2 Hz, 2H, CH2), 3.96(d,J=11.7 Hz, 1H, CH), 2.93(d,J=11.7 Hz, 1H, CH), 2.65(m, 2 H, CH2), 2.31(m, 2 H, CH2), 2.06(m. 2 H, CH2), 1.05(t,J=7.2 Hz, 3 H, CH3);19F NMR(DMSO-d6, 282 Hz) δ -81.38(s, 3F); MS(70 eV, EI) m/z(%): 429(M+, 34.34), 356([M-CO2Et]+, 36.25), 286([M-1-CO2Et-CF3]+, 100), 244([M-1-CF3COCH2CO2Et]+, 11.93), 198([M-1-NO2-CF3COCH2CO2Et]+, 54.27), 115([CF3COCH2CO2Et-CF3]+, 81.88), 69(CF3+, 69.53); Anal.calcd for C19H18NO7F3: C, 53.15; H, 4.20; N, 3.26; Found: C, 53.26; H, 4.27; N, 3.10。
1.2.25的合成通法
在新蒸的5 mL甲苯中加入2-三氟甲基-3,4,7,8-四氫-2H-苯并吡喃酮4a(0.104 g,0.27 mmol)和1.2 equiv.的對甲苯磺酸(0.056 g,0.32 mmol),加熱至回流12 h,TLC顯示反應完全,旋干溶劑,柱層析分離,以石油醚/乙酸乙酯(5:1/V:V)為淋洗劑得2-三氟甲基-7,8-二氫-4H-苯并吡喃酮衍生物5a(0.231 g,63%)。
5a:無色油狀物; FT-IRυmax(cm-1): 3063, 3030, 2960, 1736, 1676, 1643, 1455, 1376, 1033, 700;1H NMRδH(CDCl3): 7.22~7.13(m, 5H, ArH), 4.68(s, 1H, CH), 4.04~3.97(q,J=7.2 Hz, 2H, CH2), 2.55(m, 2H, CH2), 2.28(m, 2H, CH2), 1.97(m, 2H, CH2), 1.02(t,J=7.2 Hz, 3H, CH3);19F NMR(CDCl3, 282 MHz)δ-67.01(s, 3F); MS(70 eV, EI) m/z(%): 366(M+, 100), 337([M-Et]+, 53.60), 317([M-1-F-Et]+, 84.19), 289([M -C6H5]+, 45.13), 69(CF3+, 7.39), 55(C4H7+, 40.00); Anal.calcd for C19H17F3O4: C, 62.30; H, 4.64; Found: C, 62.04; H, 4.83。
5b:黃色油狀物; FT-IRυmax(cm-1): 2961, 1737, 1675, 1643, 1373, 1209, 1182, 1155, 1033, 802, 689;1H NMRδH(CDCl3): 7.19~7.08(m, 4H, ArH), 4.67(s, 1H, CH), 4.05~4.02(q,J=7.2 Hz, 2H, CH2), 2.59(m, 2H, CH2), 2.30(m, 2H, CH2), 1.98(m, 2H, CH2), 1.06(t,J=7.2 Hz, 3H, CH3);19F NMR(CDCl3, 282 MHz)δ-66.94(s, 3F); MS(70 eV, EI) m/z(%): 402/400(M+, 5.61/18.65), 372/370([M-Et-H]+, 15.29/48.93), 352/350([M-2H-F-Et]+, 34.96/86.35), 289([M-ClC6H4]+, 80.48), 261(M+-ClC6H4-2CH2, 61.47), 69(CF3+, 24.40), 55(C4H7+, 100); HRMS for C19H16F3O4Cl: Calcd: 400.0689; Found: 400.0695。
2 化合物結構的鑒定及可能的機理
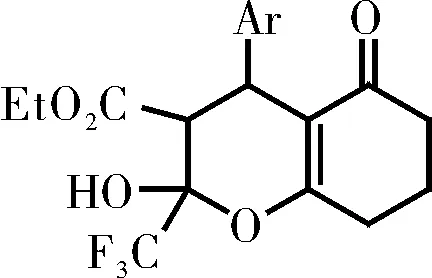
對4a進行四譜解析。1H NMR (CDCl3)譜共有八組峰組成:7.26~7.08(m, 5H, ArH), 5.57(s, 1H, OH), 4.04(q, 2H,J=7.2 Hz, CH2), 3.94(d, 1H,J=11.7 Hz, CH), 2.98(d, 1H,J=11.7 Hz, CH), 2.60(m, 2H, CH2), 2.34(m, 2H, CH2), 2.04(m. 2H, CH2), 1.00(t, 3H,J=7.2 Hz, CH3) ppm,表明該化合物含有五個芳氫,一個羥基氫,一個乙氧基,3.94 ppm和2.98 ppm處的兩組相互偶合的dd峰說明存在一對相鄰的次甲基,另外還有三對相鄰亞甲基上的氫。19F NMR 譜中,CF3的化學位移在-84.19 ppm,表明CF3和飽和碳原子相連。4a的MS顯示如下:(70 eV, EI)m/z(%): 384(M+, 53.46), 241(M+-1-CF3-CO2Et, 100), 311(M+-CO2Et, 47.32), 69(CF3+, 66.20)。在它的IR譜中,3465 cm-1、1741 cm-1處的吸收帶說明其結構中包含有OH和COOEt。元素分析表明不含氮。因此可能的結構為:
3 結 論
本實驗重點研究了不同的芳醛、環己二酮及三氟乙酰乙酸乙酯在痕量碘作為催化劑,一鍋法合成2-三氟甲基-3,4,7,8-四氫-2H-苯并吡喃酮衍生物的反應。本工藝反應條件溫和,反應時間短,操作簡單易行,環境友好且收率較高,適合規模化生產2-三氟甲基-3,4,7,8-四氫-2H-苯并吡喃酮衍生物。同時考察了2-三氟甲基-3,4,7,8-四氫-2H-苯并吡喃酮衍生物的脫水反應,發現僅在劇烈條件下反應才得以進行。

