青蒿素--環糊精包合物聯合雙硫侖抑制腸癌肝轉移的體內活性研究
馮冰玉,祖元剛,魏亮,吳比,吳斌,張東,姜守剛※
(1.東北林業大學化學化工與資源利用學院,黑龍江 哈爾濱 150040;2.東北林業大學,森林植物生態學教育部重點實驗室,黑龍江 哈爾濱 150040;3.東北林業大學,生物資源利用國家地方聯合工程實驗室,黑龍江 哈爾濱 150040)
結腸癌是消化道最常見的惡性腫瘤之一,是一種嚴重危害人類健康的惡性腫瘤。結直腸癌最常見的轉移部位是肝臟[1],約25%的患者確診為結直腸癌時已出現肝轉移,另有約50%的患者在術后3年內出現肝轉移[2]。結腸癌的治療手段有很多,如手術治療、放射治療、臨床化療等方法。其中,手術治療適用于早期的結腸癌,癌細胞局部浸潤范圍小,且沒有出現轉移或者轉移的數目和范圍較小的情況,但是對于晚期的癌癥,局部浸潤則比較廣泛,故不適用手術治療。化療是腸癌肝轉移的主要治療手段,但化療的毒副作用大且易耐藥。以5-氟尿嘧啶為基礎的化療是最常用的治療方案,有50%的轉移性腸癌對該治療方案產生耐藥,而耐藥后急需有效的臨床用藥[3]。而近年來的研究表明,中藥可以用于即不能接受手術,又無法進行放療、化療患者的治療。
青蒿素是一種含過氧基團的倍半萜內酯化物,由我國中醫研究院中藥研究所于1971年從菊科植物黃花蒿(Artemisia annua)葉中提取分離得到[4]。青蒿素不僅對瘧疾有很好的治療效果,而且治療抗原發腸癌也有效果[5],但無治療腸癌肝轉移的報道。研究表明,青蒿素及其衍生物能降低細胞內線粒體跨膜電位,使線粒體中的Ca2+流入細胞質,從而致使腫瘤細胞死亡[6]。本試驗將青蒿素用-環糊精進行包合形成青蒿素-環糊精包合物,避免了強酸性胃液對青蒿素的破壞,青蒿素-環糊精包合物在結腸處釋放青蒿素,再聯合具有抗腸癌的雙硫侖進行聯合給藥[7],研究其聯合給藥抑制腸癌肝轉移方面的作用。
1 材料與方法
1.1 試驗材料
1.1.1 材料與試劑 青蒿素、雙硫侖、-環糊精、福爾馬林固定液(上海源葉生物科技公司);清潔級BABL/c小鼠(哈爾濱醫科大學附屬二院動物中心);奧沙利鉑(江蘇恒瑞醫藥股份有限公司);結腸癌CT26.WT細胞(北京協和醫院細胞中心);RPMI 1640 培養基、青鏈霉素混合液(HyClone公司);胰蛋白酶(Sigma公司);優級胎牛血清(中國科學院天津灝洋生物)。
1.1.2 試驗儀器 ALC-1104型分析天平(北京賽多利斯儀器系統有限公司);DK-8D型電熱恒溫水槽(上海森信實驗儀器有限公司);FLC-3 型生物潔凈工作臺(北京東聯哈兒儀器制造有限公司);YXQ-LS-75SII型立式壓力蒸汽滅菌器(上海博訊實業有限公司);22R型高速離心機(德國Heraeus sepatech 公司);Eclipse TS100 型培養倒立顯微鏡(Nikon 公司);E191IR 型CO2細胞培養箱(美國西蒙有限公司);紫外線殺菌燈車(江陰市飛揚器械有限公司);Zf11-01 型潔凈動物飼養柜(東北林業大學植物藥工程研究中心設計監制)。
1.2 試驗方法
1.2.2 青蒿素標準曲線的建立 分別稱取已配制好的青蒿素母液 0.2、0.4、0.6、0.8、1.0、1.2、1.4mL于 10mL容量瓶內,依次加入95%的乙醇1.8、1.6、1.4、1.2、1.0、0.8、0.6 mL,再分別加入 0.2%的NaOH 溶液 8.0 mL 定容至10.0 mL,配制成濃度為0.02、0.04、0.06、0.08、0.10、0.12、0.14 mg/mL 的標準溶液。在 50 ℃水浴加熱30 min 后流水冷卻至室溫,測定吸光度,繪制標準曲線。
1.2.3 小鼠結腸癌CT26.WT 細胞懸液的制備 將小鼠結腸癌CT26.WT細胞培養在RPMI 1640 培養液(含10%胎牛血清+1%青鏈霉素)中,置于37 ℃、5% CO2的細胞培養箱中培養。取對數生長期的細胞,加入1 mL 消化液(0.05%胰酶+0.02%EDTA)進行消化,吹打均勻后離心(2 000 r/min,離心時間10 min),將上清液輕輕緩慢地移走,加入適量的生理鹽水稀釋剩下的細胞沉淀物,制成單細胞懸液,用細胞計數板進行計數,并調節細胞濃度至1 106個/mL。細胞懸液制備完成置于無菌的條件下備用。
1.2.4 腸癌肝轉移模型的建立 采用脾臟種植法構建小鼠腸癌肝轉移模型[9]。將BABL/c 小鼠首先進行稱重并記錄,配制15%烏拉坦溶液,采用腹腔注射的方法對小鼠進行麻醉處理,觀察到小鼠沒有痛覺,角膜反射開始表現出遲鈍,呼吸均勻而深沉時表明小鼠麻醉深度適宜,可以開始進行造模。對小鼠進行常規消毒后,于小鼠左側背部剃毛,對剃毛處進行局部清洗和皮膚消毒后,將小鼠固定在手術臺,于左側背部進行約1.0 cm 的斜切口,待脾臟暴露后,將脾臟下極輕輕地提出腹腔,用1mL無菌注射器(30 號針頭)吸取0.1mL CT26.WT 單細胞懸液(1 106個/mL),于脾上極被膜下緩慢進針5 mm,緩慢注入CT26.WT 細胞,見被膜腫脹變白時暫停注射,待脾臟回血恢復正常時接著進行注射,注射時間約5 min,注射完畢緩慢拔出針頭,并用消毒棉簽壓迫針眼止血約2~3 min,將脾臟納回,用手術縫合線逐層關腹,待小鼠度過麻醉時間,恢復清醒后進行常規飼養,自由進食進水。
1.2.5 分組及給藥 選取一定數量周齡4~6 周、體重18~20 g 的雄性BABL/c小鼠,采用上述造模方法進行造模,將小鼠隨機分成3 組,每組6 只,分為空白組(生理鹽水)、給藥組(青蒿素--環糊精包合物聯合雙硫侖)、陽性對照組(奧沙利鉑)。空白組和陽性對照組采用腹腔注射的方式給藥,給藥組采用灌胃的方式進行給藥,連續給藥7 d,每5 d 對小鼠進行稱重,用重復測量法分析藥物對各組小鼠體重的影響,觀察小鼠的狀態,記錄和分析小鼠的生存期。
1.2.6 病理學檢查 通過對結腸癌肝轉移的 BABL/c小鼠進行病理分析,來判斷藥物對于轉移的抑制情況。每組隨機選取一只小鼠,在給藥10 d 后處死,取出完整的肝臟,用生理鹽水將其清洗干凈,并用4%的多聚甲醛溶液將其固定12~14 h,經過脫水、透明、石蠟包埋、切片、HE染色及封固一系列操作,在顯微鏡下進行病理學觀察和分析。
2 結果與分析
2.1 青蒿素--環糊精包合物的紅外光譜圖
從青蒿素的譜圖(圖1A)可以看出,主要特征吸收峰在 1 738 cm-1的 C=O 的伸縮振動,1 116 cm-1的C—O—C 的伸縮振動,724 cm-1的O—O 的伸縮振動,2 870~3 000 cm-1的 C—H 伸縮振動。從-環糊精的譜圖(圖1B)可以看出,主要在3 400 cm-1有—OH的彎曲振動,2 937 cm-1有甲基、亞甲基C—H 的伸縮振動,1 417 和1 295 cm-1的—OH 平面彎曲振動等較強吸收峰。而青蒿素與-環糊精物理混合的譜圖(圖1C)可以看出青蒿素的主要吸收峰還在,只是在其基礎上疊加了-環糊精的吸收峰。比較青蒿素與-環糊精物理混合(圖1C)與青蒿素包合物(圖1D)的紅外光譜圖可以發現2 個譜圖明顯不同,表明青蒿素進入-環糊精疏水腔內,主客體間相互作用,在范德華力、色散力、靜電作用力以及氫鍵等因素的影響下,沒有形成新的化學鍵,因此,可以看到譜圖中客體的峰形有所變寬,峰強度減弱,且有一些較弱的吸收峰消失,由于沒有新鍵的形成,所以,包合物中吸收峰的位移不大,且無新峰出現,說明已形成較穩定的包合物。
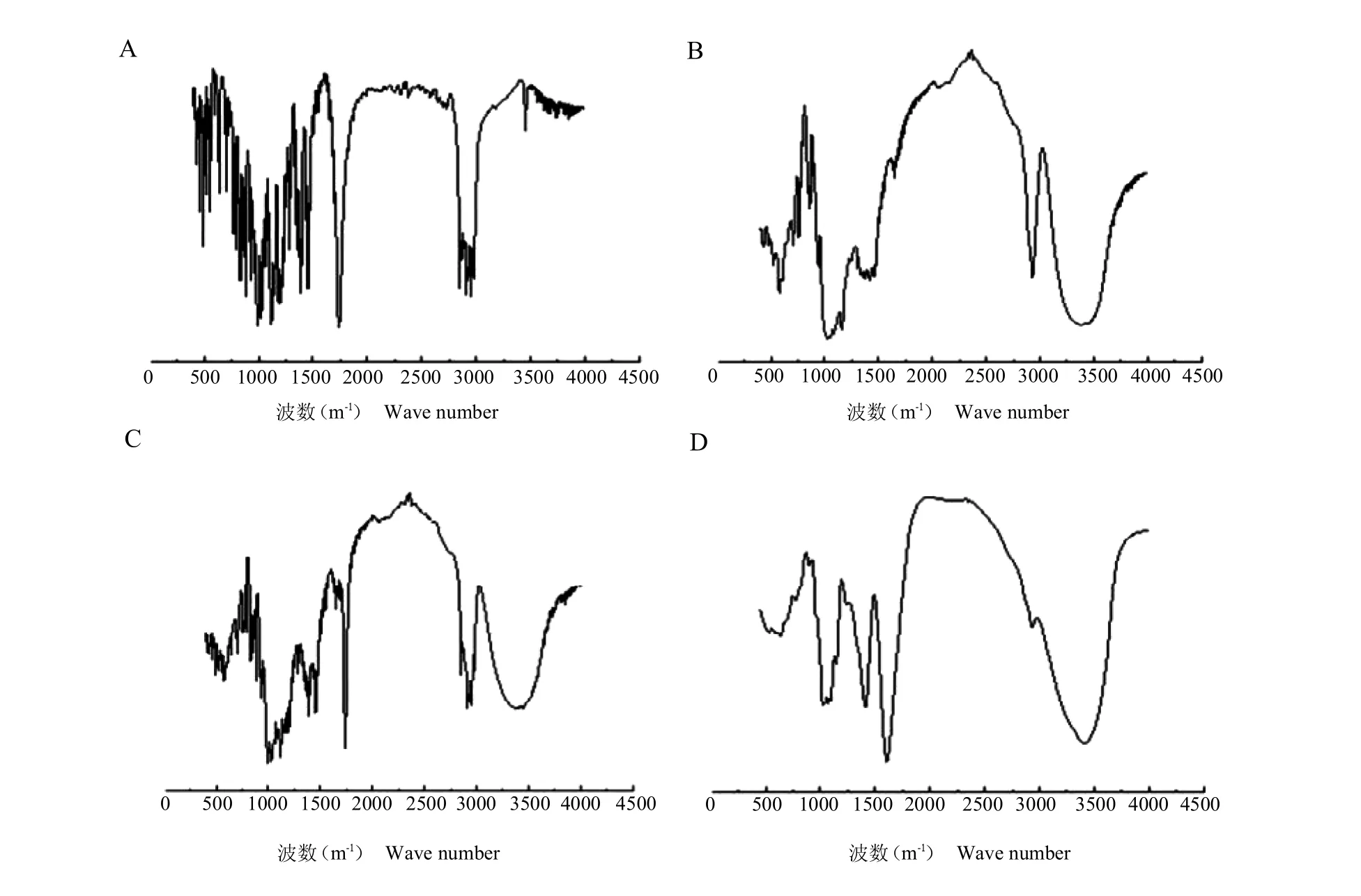
圖1 青蒿素(A)、-環糊精(B)、青蒿素與-環糊精物理混合(C)、青蒿素包合物(D)的紅外光譜圖Fig.1 Infrared spectra of artemisinin(A),-cyclodextrin(B),physical mixing of artemisinin and -cyclodextrin(C)and artemisinin inclusion complex(D)
2.2 青蒿素包合物載藥量的測定
根據“1.2.1”的方法測出不同濃度青蒿素的吸光度,以濃度為橫坐標、吸光度為縱坐標繪制青蒿素的標準曲線,得標準方程為Y=1.085X+1.1491(R2=0.99653)。根據標準方程計算包合物的載藥量為 17.0%±0.4%(n=3)。
2.3 腸癌肝轉移模型的建立
觀察小鼠在接種CT26.WT細胞后的生活狀態,于接種后第1 天,明顯可以觀察到小鼠的活動減少,進食進水量減少。第2 天起,小鼠的精神狀態慢慢恢復,活動如常,進食進水量恢復正常。接種后10 d 左右,小鼠出現體態逐漸消瘦,攝食量減少,精神狀態不佳,可于腹部觸及腫塊。接種后15 d 左右,小鼠明顯消瘦,行動遲緩,精神狀態萎靡不振。將自然死亡的小鼠肝臟完整剖出,可見肝臟廣泛分布著灰白色腫瘤組織。由此可見,已成功建立了小鼠結腸癌肝轉移模型。
2.4 模型小鼠體重變化情況分析
接種前的小鼠均活動正常,自由進食進水,精神狀態比較活潑。分別在接種當天,接種后第1 天、第5天、第10 天、第15 天測定并記錄小鼠的體重,小鼠體重變化結果如圖2 所示。從圖2 可以看出,各組小鼠的體重在接種后第1 天均出現了減輕的情況,空白組和給藥組的小鼠體重自接種后第2 天起開始逐漸增加;而陽性對照組小鼠的體重則是自接種后第1 天至第5 天小鼠的體重均呈現下降的趨勢,從第6 天起小鼠的體重才逐漸上升,最后陽性對照組小鼠的體重低于其他兩組小鼠的體重,說明奧沙利鉑毒副作用高于其他兩組。
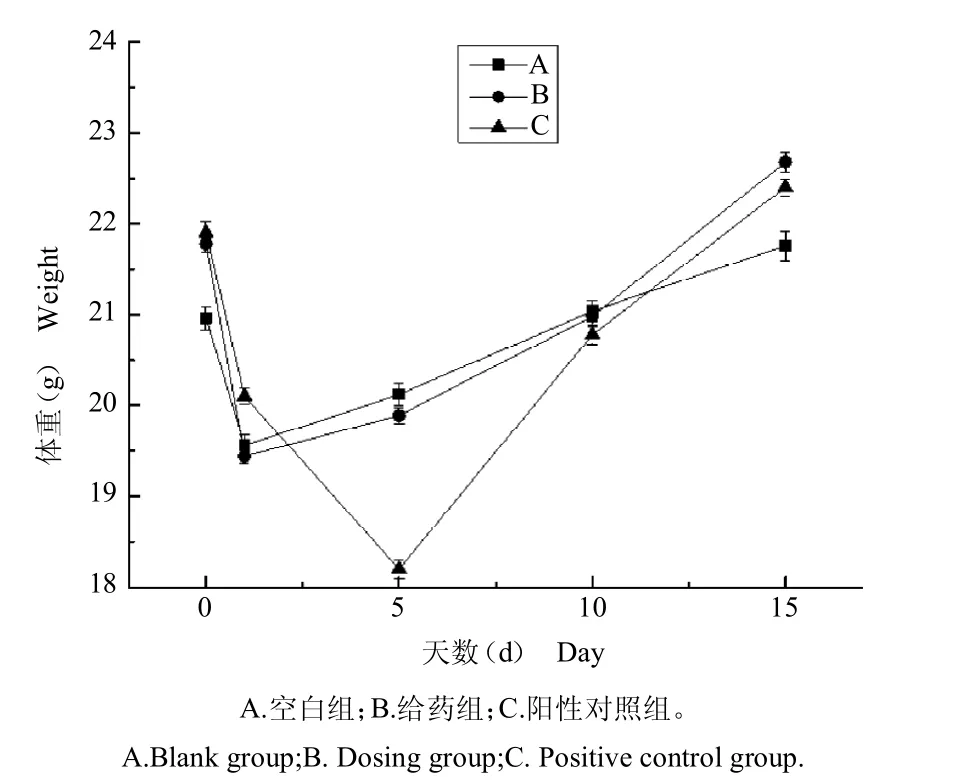
圖2 模型小鼠的體重變化Fig.2 Weight changes of model mice
2.5 模型小鼠生存期分析
自小鼠接種后,每天觀察小鼠的生存狀態,精神狀態并記錄生存期。對各組的小鼠采用 SPSS 17.0 軟件中Kaplan-Meier法進行生存期分析,生存曲線如圖3 所示。分析結果顯示,空白組、給藥組、陽性對照組平均生存期分別為(19.16±2.03)、(28.33±3.68)、(33.83±2.27)d。因此,給藥組的生存期顯著長于空白組,說明青蒿素--環糊精聯合雙硫侖給藥可作為治療結腸癌肝轉移的二線臨床備選藥物。
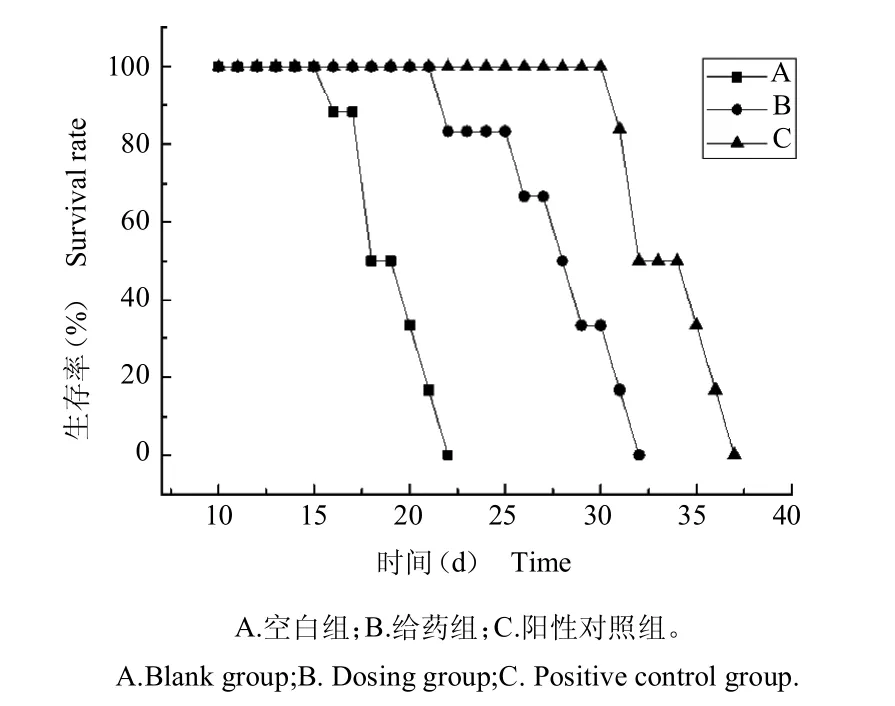
圖3 模型小鼠的生存期曲線Fig.3 Survival time curve of model mice
2.6 模型小鼠肝臟標本觀察
于接種后10 d 處死小鼠,完整剖出其肝臟,肝臟標本如圖4 所示。從圖4 可以看出,空白對照組,肝臟表面分布著較多的大小不一的腫瘤結節,部分肝臟組織被腫瘤結節所代替[10];給藥組,肝臟有著較少的腫瘤結節分布,其數量遠少于空白對照組;奧沙利鉑陽性對照組,其表面幾乎沒有轉移的腫瘤結節。結果表明,聯合用藥具有顯著的抑制結腸癌肝轉移的活性。
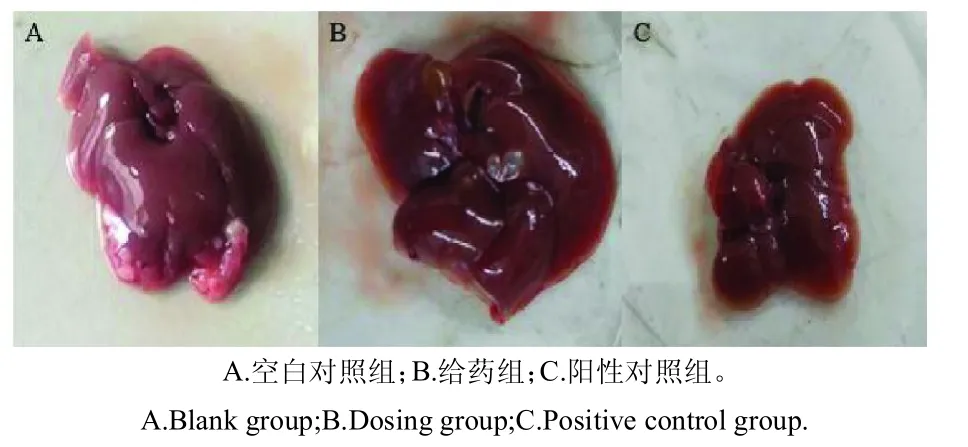
圖4 模型小鼠肝臟標本Fig.4 Liver specimens from model mice
2.7 病理學觀察結果
對模型小鼠的肝臟進行HE染色,并做病理分析,在放大倍數為100 倍的顯微鏡下觀察,其結果如圖5所示。圖5A 為空白對照組,箭頭所指a 處為正常的細胞,箭頭所指b處細胞核質比顯著增高,體現出了團聚現象,說明腫瘤細胞復制劇烈[11]。圖5B 為聯合給藥組,可以看到轉移瘤的細胞數量明顯減少,并且腫瘤細胞團聚現象沒有圖A 那樣密集,說明聯合給藥在一定程度上抑制了腫瘤細胞的轉移。圖5C 為奧沙利鉑組,其中腫瘤細胞的核質比與正常細胞相差不大,抑制了腫瘤細胞的復制。
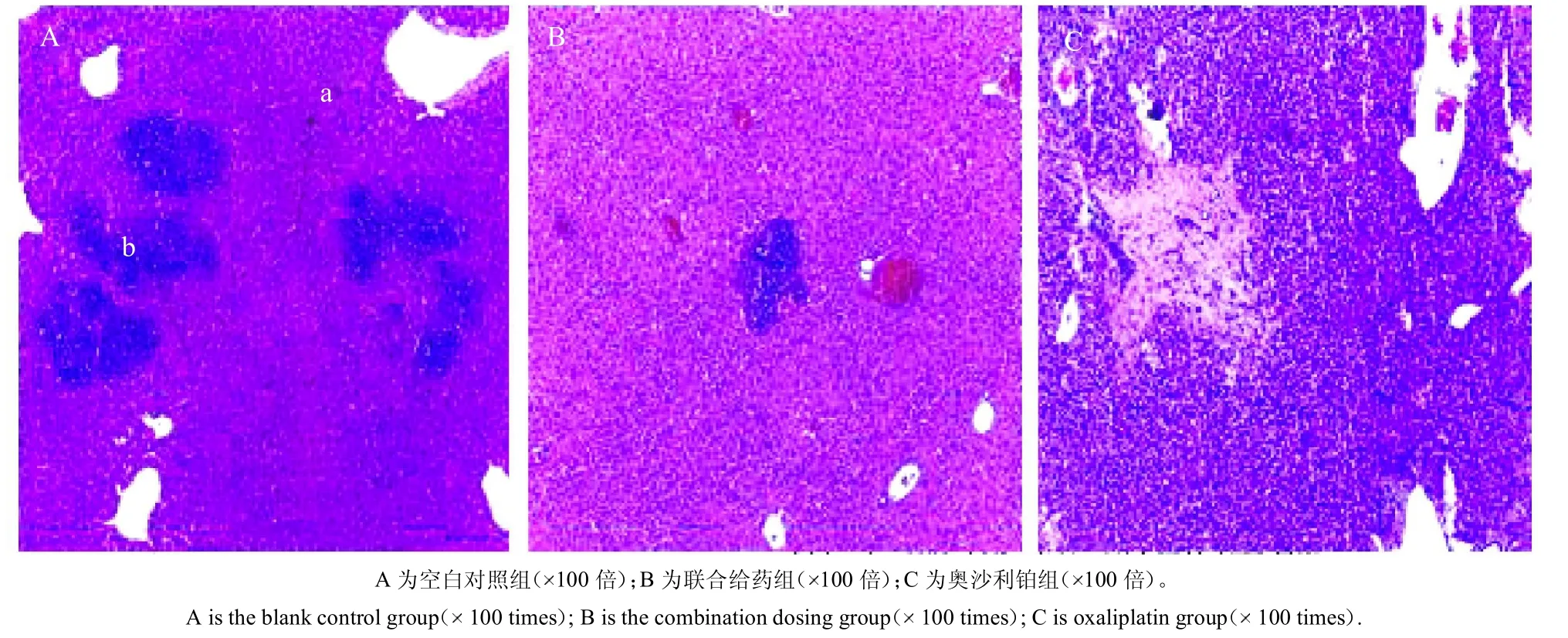
圖5 模型小鼠肝臟HE 染色后切片圖像Fig.5 Slice images of model mouse liver after HE staining
3 結論
通過建立腸癌肝轉移模型,比較聯合給藥組平均生存期、肝組織切片腫瘤轉移數和病理腫瘤細胞復制等試驗,發現不論青蒿素還是青蒿素--環糊精包合物給藥抑制腸癌肝轉移效果不顯著,可能是因為青蒿素治療腫瘤的主要機理是其過氧基團與腫瘤中過量的鐵二價離子反應生成氧自由基而殺傷腫瘤細胞[12]。但由于鐵主要儲存在肝[13],即使腸癌腫瘤細胞比正常的腸細胞中鐵二價離子濃度高,但當其肝轉移后,不論青蒿素還是青蒿素--環糊精包合物都不具有腸癌的靶向性,達不到有效的治療濃度,所以,抑制腸癌肝轉移效果不顯著。考慮到即使與具有抗腸癌的雙硫侖聯合給藥,其生存期也短于陽性對照組,有必要把青蒿素裝載到腫瘤靶向性載體中,提高其抗腸癌肝轉移活性。

