西達本胺聯合雷利度胺和地塞米松治療多發性骨髓瘤的臨床研究
宮敬智,楊 雷,白培清,孫小燕,金建剛,張維蓮,郜小岳,秦玉柱
多發性骨髓瘤是指漿細胞異常增生的惡性腫瘤,在所有腫瘤中所占比例為1%[1]。多發性骨髓瘤多見于50~60歲的中老年病人,男性多于女性[2];該病病因不明,可能與病毒感染、電離輻射、接觸毒物、慢性抗原刺激、遺傳因素等有關[3-4]。多發性骨髓瘤的治療手段為化學治療、干擾素α治療和骨髓移植,其中化療藥物包括雷利度胺、硼替佐米、沙利度胺等[5-6],但難治及復發概率較大,難以有效控制病情。本研究采用了西達本胺聯合雷利度胺和地塞米松治療多發性骨髓瘤旨在探討其應用價值。現報告如下。
1 資料和方法
1.1納入及排除標準
1.1.1納入標準:所有患者均符合2015年修訂的《中國多發性骨髓瘤診治指南》中的診斷標準[7];均為活動性多發性骨髓瘤[8];患者臨床及隨訪資料完整;患者及其家屬對本研究知情同意。
1.1.2排除標準:冒煙型多發性骨髓瘤[9];合并其他惡性腫瘤、嚴重腎功能損害、血液系統疾病、免疫系統疾病等基礎疾病患者;有相關藥物過敏史
1.2一般資料 選取我院2016年4月—2019年4月收治的多發性骨髓瘤患者62例,按治療方案的不同分為觀察組和對照組,每組31例。對照組給予雷利度胺和地塞米松;觀察組在對照組基礎上加用西達本胺。對照組男18例,女13例;年齡42~85(59.60±8.34)歲;病程4月~3年(11.50±7.06)月;初發多發性骨髓瘤14例,應用含沙利度胺方案治療后無效或復發多發性骨髓瘤17例;按多發性骨髓瘤免疫分型[5]:IgG型14例,IgA型7例,IgD型3例,IgM型1例,輕鏈型6例,無雙克隆型、IgE型及非分泌型患者;按國際分期體系[6](ISS)多發性骨髓瘤分期:ⅡA期5例,ⅡB期3例,ⅢA期19例,ⅢB期4例。觀察組男20例,女11例;年齡45~83(58.82±7.71)歲;病程3月~2.5年(10.75±6.82)月;初發性多發性骨髓瘤12例,應用含沙利度胺方案治療后無效或復發多發性骨髓瘤19例;按多發性骨髓瘤免疫分型:IgG型16例,IgA型6例,IgD型1例,IgM型1例,輕鏈型7例,無雙克隆型、IgE型及非分泌型患者;按ISS分期:ⅡA期6例,ⅡB期4例,ⅢA期18例,ⅢB期3例。2組年齡、病程、免疫分型等一般資料比較差異無統計學意義,具有可比性(P>0.05)。見表1。

表1 2組多發性骨髓瘤患者一般資料比較
注:對照組給予雷利度胺和地塞米松,觀察組對照組基礎上加用西達本胺;ISS分期為多發性骨髓瘤國際分期體系
1.3治療方法 對照組給予雷利度胺和地塞米松治療:雷利度胺10 mg/d,口服,1~21 d;地塞米松40 mg/d,分2次口服,1~4 d、9~12 d、17~20 d。觀察組在對照組基礎上加用西達本胺治療:西達本胺30 mg/d,早餐后30 min口服,每周2次,28 d為1療程。治療2~8個療程,每隔2個療程復查患者基本情況,有效則繼續治療,無效則停藥。2組患者均隨訪2年。
1.4觀察指標
1.4.1臨床療效:參考2015年修訂的《中國多發性骨髓瘤診治指南》[7]中的療效評判標準進行評估,分為完全緩解(血清、尿免疫固定電泳陰性,軟組織漿細胞瘤消失,骨髓中漿細胞<5%);接近完全緩解(血清、尿免疫固定電泳弱陽性,軟組織漿細胞瘤基本消失);部分緩解(血清M蛋白減少≥50%,24 h尿M蛋白減少≥90%或降至<200 mg/24 h,漿細胞瘤縮小≥50%);輕微反應(血清M蛋白減少25%~49%,24 h尿M蛋白減少50%~89%,漿細胞瘤縮小25%~49%);無變化(不符合上述要求者)。臨床有效率=(完全緩解+接近完全緩解+部分緩解)/總例數×100%。
1.4.2實驗室檢查:采集患者入院第2天及治療后清晨空腹外周靜脈血,檢測血紅蛋白、血清肌酐、血清M蛋白、骨髓漿細胞。采用自動生化儀檢測血清肌酐,采用血清蛋白電泳聯合免疫固定電泳檢測血清M蛋白。
1.4.3不良反應:記錄2組患者有無乏力、胃腸道反應、發熱、皮疹等情況。

2 結果
2.1臨床療效比較 觀察組總有效率為83.87%,對照組總有效率為61.29%;觀察組總有效率顯著高于對照組(P<0.05)。見表2。

表2 2組多發性骨髓瘤患者臨床療效比較[例(%)]
注:對照組給予雷利度胺和地塞米松,觀察組在對照組基礎上加用西達本胺;與對照組比較,aP<0.05
2.2實驗室指標比較 2組治療前血紅蛋白、血清肌酐、血清M蛋白、骨髓漿細胞比較差異無統計學意義(P>0.05)。與治療前比較,2組治療后血紅蛋白升高、血清肌酐、血清M蛋白、骨髓漿細胞降低,且觀察組上述指標均優于對照組,差異有統計學意義(P<0.05)。見表3。
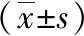
表3 2組多發性骨髓瘤患者治療前后實驗室指標比較
注:對照組給予雷利度胺和地塞米松,觀察組在對照組基礎上加用西達本胺;與治療前比較,aP<0.05;與對照組比較,cP<0.05
2.3不良反應發生率比較 觀察組不良反應發生率為16.13%,對照組不良反應發生率45.16%;觀察組總不良反應發生率低于對照組,差異有統計學意義(P<0.05)。見表4。

表4 2組多發性骨髓患者不良反應發生率比較[例(%)]
注:對照組給予雷利度胺和地塞米松,觀察組對照組基礎上加用西達本胺;與對照組比較,aP<0.05
3 討論
多發性骨髓瘤是指骨髓內有異常漿細胞增殖,引起骨骼破壞,骨髓造血功能衰竭,產生異常增多的單克隆免疫球蛋白,導致貧血、腎功能損害的漿細胞疾病[10]。多發性骨髓瘤在血液系統惡性疾病中約占10%,在我國的發病率約為1/10萬[11];該病預后差,未經治療的中位生存期為6個月,化療后的中位生存期為3年內[12]。多發性骨髓瘤細胞對骨骼產生破壞作用,主要表現為骨痛、骨骼變形、病理性骨折,局部浸潤可出現截癱、漿細胞白血病、骨髓瘤腎等,骨髓瘤細胞分泌的M蛋白可引起繼發感染、貧血、雷諾現象等[13-16],對患者健康造成極大威脅。
多發性骨髓瘤初始治療多選擇骨髓移植或沙利度胺單藥、硼替佐米聯合沙利度胺或潑尼松維持治療,產生耐藥者可給予來那度胺聯合地塞米松或硼替佐米及地塞米松等[17],但仍有較大部分患者復發概率較大。雷利度胺是第二代免疫調節劑,為改良沙利度胺分子骨架而成,具有誘導骨髓瘤細胞凋亡作用,且能克服藥物抵抗,臨床療效較沙利度胺更高,對于存在地塞米松抵抗的骨髓瘤細胞同時可對地塞米松抗腫瘤的作用增強。有研究表明,雷利度胺聯合小劑量地塞米松方案治療多發性骨髓瘤,患者疾病進展時間可有效延長,在復發難治性多發性骨髓瘤患者中疾病進展時間可達11.3個月[18-19]。雷利度胺雖是沙利度胺的結構類似物,但不良反應與其不同,嚴重者多表現為骨髓抑制、粒細胞缺乏、血小板減少、貧血、感染等[20],停藥后可恢復。
西達本胺是一種化學結構全新的組蛋白脫乙酰化酶抑制劑,是目前臨床上的新藥,可改變染色質結構,對靶基因表達產生影響,選擇性高,在肺癌、結腸癌、乳腺癌、肝癌等惡性腫瘤中均有抑制、殺傷作用,具有廣譜抗腫瘤活性。有研究表明,西達本胺可促使骨髓瘤細胞DNA凋亡、對其增殖產生抑制作用[21]。西達本胺在惡性腫瘤患者中具有耐受性,作用靶點特異。其作用機制尚未明確,可能與通過觸發外源性凋亡通路,上調凋亡基因、下調抗凋亡基因等有關。同時,西達本胺可以使骨髓瘤細胞停滯于G0/G1期,抑制細胞增殖。
本研究結果顯示,觀察組總有效率顯著高于對照組。2組患者治療前的實驗室指標血紅蛋白、血清肌酐、血清M蛋白、骨髓漿細胞比較差異無統計學意義;治療后血紅蛋白升高,血清肌酐、血清M蛋白、骨髓漿細胞降低,觀察組優于對照組。觀察組總不良反應發生率低于對照組。由此可見,西達本胺聯合雷利度胺和地塞米松治療多發性骨髓瘤效能更高。
綜上所述,西達本胺聯合雷利度胺和地塞米松可有效抑制多發性骨髓瘤血清M蛋白及骨髓漿細胞升高,改善貧血、腎功能不全癥狀,臨床療效及安全性較雷利度胺和地塞米松治療更高。

