SiO2納米孔對常見工業廢氣吸附的分子動力學研究
白 俊,周春宇,段 鈺,謝 鑫,梁俊璽,孫初鋒
(1.西北民族大學 化工學院,甘肅 蘭州 730030;2.甘肅省高校環境友好型復合材料及生物質利用省級重點實驗室,甘肅 蘭州 730030)
通常來說納米孔被定義為內徑尺寸介于1~100 nm之間的微小孔洞[1]。納米孔材料較好的穩定性和耐用性使得其在保證吸附劑嚴格溫度、壓力和其他化學條件下能夠進行有效吸附,并且有較長的使用壽命和實用價值,這使得納米孔材料吸附劑被廣泛應用。穩定的反應條件、精確地合成方法以及成熟的納米孔合成技術是制備高效的納米孔材料的必備條件[2]。評判納米孔材料的合成成功與否不僅要看合成的納米孔材料是否具有高吸附量,其材料的穩定性也是納米孔材料合成的一個重要條件[3-4]。
多孔材料近些年來非常受歡迎,目前被廣泛應用于催化,吸附等領域[6-8]。在1992年首次報道合成MCM-41后,石英以其豐富的儲量,二氧化硅多孔材料被認為是最有前景的吸附劑。一些專家研究了吸附具有不同幾何形狀的納米二氧化硅材料中流體的結構和動力學[5],眾所周知的是CO2在二氧化硅中的運移,這些研究為納米過濾[9],分離[10]和催化等技術的應用提供了理論借鑒。這些研究為分子的捕獲和儲存提供了重要的依據,使人們清楚地認識到納米孔內氣體的行為與其吸附和擴散性質有關,而且二氧化硅中的選擇性吸附仍有待進一步研究,這對于設計不同氣體的吸附劑至關重要。
碳納米管具有較高的氣體吸附選擇性。相比之下,二氧化硅納米孔內氣體的情況受到的關注較少,尤其是在單純實驗研究方面。近年來,通過計算機模擬研究了簡單流體的動力學行為,發現在二氧化硅表面附近表現有CO2富集。顯然,分子水平上的模擬為多孔二氧化硅的應用提供了一種補充實驗的手段。最著名的例子是MCM-41,其具有有序的六面體結構,中孔的尺寸范圍2~10 nm。它們可以表現出大的表面積(高達約1000 m2/g),大孔體積(接近1 cm3/g),孔徑分散小,熱穩定性高。納米細化還導致吸收的分子的擴散率較低,其中在1 nm直徑的孔中最為常見。
此外,Gadikota等人提出氣體粘土表面的親和力與吸附分子的大小有關。 在這些先前研究的推動下,在這項工作中,我們將展示分子動力學模擬的結果,該模擬揭示了限制在羥基化二氧化硅納米孔內的不同氣體的行為,來判斷使用二氧化硅納米孔作為氣體的吸附劑是否合適。其中利用NVT系綜分子動力學模擬和巨正則蒙特卡洛方法(GCMC),Bourg和Steefel等人分別在273 K,298 K和300 K進行模擬7種單組分氣體分子在1nm直徑的二氧化硅孔隙中的吸附。
通過對SiO2納米孔對工業常見廢氣(CH4、CO2、SO2、NO2、CO、HF、H2S)的吸附模擬研究,為進一步揭示硅膠吸附劑的吸附機理以及應用于氣體吸附方面的SiO2納米新材料的生產應用提供了一定理論基礎。
1 模擬計算方法
利用MS軟件中COMPASS力場進行建模,利用溫度等溫線完成體系壓力的確定。為了使模擬體系接近真實體系,模型的構建采用三維周期性邊界條件,選取能量最低、體系最穩定的周期邊界作為初始構型,對SiO2納米孔模擬體系進行能量優化處理,使得體系達到平衡狀態,最后對模擬體系吸附分子進行MSD和RDF模擬計算。本文中的所有的模擬操作全部在Materials Studio 6.0版本上進行。
2 模型構建與優化
首先建立七種工業污染氣體(CH4、SO2、CO2、NO2、HF、H2S、CO)分子模型,然后建立SiO2吸附模型,通過系統導入SiO2分子模型,調整參數構建超晶胞,從SiO2納米超晶胞中心刪除一定孔徑的原子,得到內徑為1 nm的SiO2納米孔。根據需要可在SiO2吸附模型中改變參數,得到1.5 nm和2 nm孔徑的SiO2吸附模型。實驗為了使結構達到最優化的構型,所有原子在能量最小化階段保持松弛不被約束。其次對優化后的吸附系統進行分子動力學模擬,采用NVT系綜,模擬運行時間為100 ps,時間步長為1 fs,每1 ps輸出一次結果并保存所有構型,采用恒溫器控制溫度(298 K、323 K、273 K三個體系)。
3 實驗現象分析
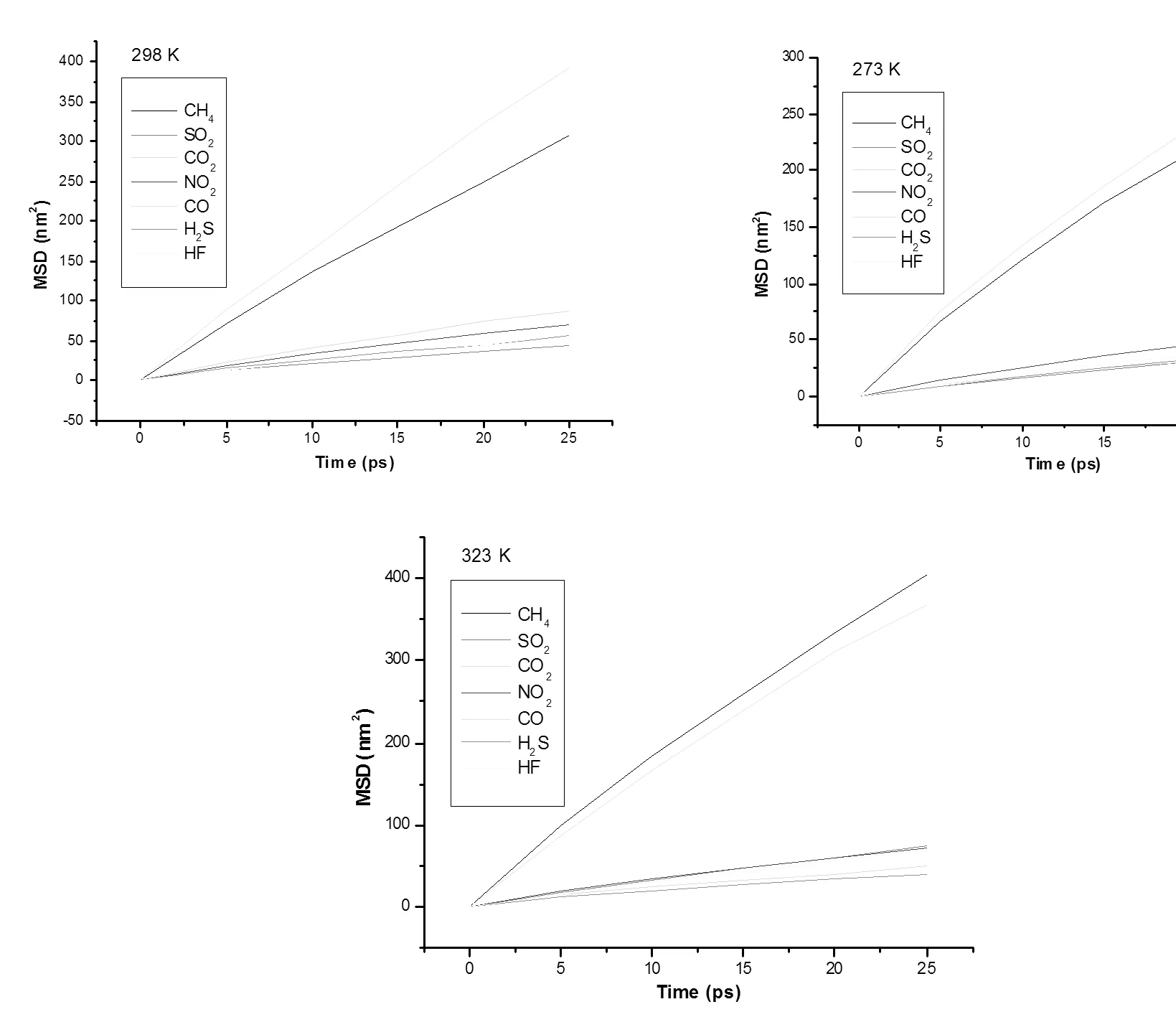
圖1 在不同溫度下給定氣體的MSD與時間的關系
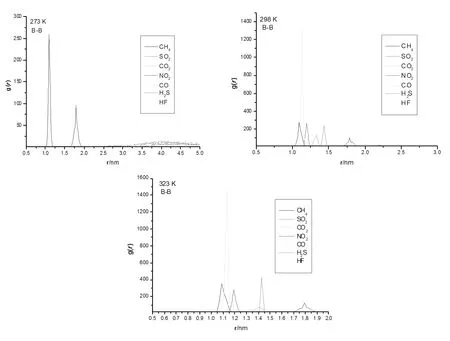
圖2 在不同溫度下給定氣體分子的RDF圖
為了提高計算效率,在分子動力學模擬階段石英砂層被固定,這種處理方法是合理的,因為石英砂通常可以被作為理想的平面處理,最后對所得的模擬結果進行分析對比。
在吸附過程中,首先進行的是323 K,6000 kPa(通過溫度等溫線確定)、1 nm孔徑等恒定參數的分子動力學模擬計算,以溫度為323 K時SiO2納米孔氣體的吸附情況為例,我們發現CH4、CO的吸附狀態是最完美的,基本吸附在SiO2納米孔內壁周圍;SO2、CO2吸附情況類似,除了在SiO2納米孔內壁周圍有大量分子,在空腔中也分布一些分子,但是相對于內壁周圍分布的分子,空腔中分布的分子相對較少;從HF、H2S吸附構型中可以看到,HF分子除了在SiO2納米孔內壁周圍有部分分子外,SiO2納米孔空腔中分布有大量分子,同時可以看到空腔中分子的數量明顯比孔壁周圍分布的分子數量多很多。
通過氣體吸附的MSD和RDF 數據分析可以看到,吸附狀態并不能完全說明氣體的吸附能力,但是往往吸附狀態最好的構型,其對應的氣體吸附體系反映的吸附能力也是最強的。
4 實驗結果與討論
(1)在單組分氣體吸附體系中,CH4和CO在SiO2納米孔中吸附的分子數量是七個吸附體系中吸附數目最少的,即其吸附能力是最弱的。但兩者在SiO2納米孔中的吸附狀態均為束縛態,其吸附狀態是最好的。另外,對于SO2、CO2、H2S和HF四個吸附體系吸附狀態類似,即其氣體分子除在SiO2納米孔內壁周圍有大量分布外,在孔腔中也有一部分分布,其中HF的總分子吸附量很高,表現其孔對其具有最強的吸附能力。值得注意的是,在NO2吸附體系中,氣體分子與SiO2納米孔某側具有非常強的相互作用力,導致其出現單側吸附的特殊吸附現象。根據氣體在SiO2納米孔中吸附分子數量的多少,其被吸附能力的順序可預測為:HF﹥CO2﹥H2S﹥NO2﹥SO2﹥CH4﹥CO。
(2)隨著溫度的變化,被研究氣體在SiO2納米孔中的擴散強度發生了變化,同時,其孔對氣體的吸附能力及氣體在其孔內的吸附狀態也發生了變化。根據不同溫度下氣體在SiO2納米孔中擴散速率以及在其孔中存在的分子數可以得到,吸附體系中氣體的擴散能力及其孔對其的吸附能力與溫度有關。CH4、SO2、NO2、HF吸附體系隨著溫度的升高而升高,其氣體擴散能力增強,而對于CO2、CO、H2S吸附體系,其氣體擴散能力先增后減。當對SiO2納米孔對氣體的吸附能力進行觀察,CH4、HF、H2S吸附體系隨著溫度升高而升高,顯示其吸附能力降低;NO2吸附體系,先降低后增加;CO2吸附體系,先增后減;SO2、CO吸附體系,吸附能力沒有發生太大變化。值得注意的是隨著溫度的變化,NO2吸附體系出現了不同側吸附的現象且吸附出現位置沒有規律性,而在其他吸附體系中,氣體的吸附狀態在不同溫度下沒有發生太大的變化。
目前為止,僅僅針對CH4、SO2、CO2、NO2、HF、H2S、CO七種氣體基于SiO2納米孔的吸附情況進行了初步研究,總體來看,本研究尚且存在諸多不足之處,需要在后續工作中進一步完善,后續研究會探究壓強、孔徑接觸面積以及尺寸等因素對吸附體系氣體吸附的影響,另外很多吸附情況涉及的機理問題,解釋的還不夠完善,后續通過結合大量的實驗數據以及優秀研究者的文獻來進一步充實本文所涉及的機理問題。

