兩 個(gè) 釩 同 多 酸 化 合 物 的 光 譜 測 試
陳義平, 孫瑞卿, 楊 珍
(1.福州大學(xué) 化學(xué)學(xué)院,福州 350116; 2.福州大學(xué) 結(jié)構(gòu)化學(xué)國家重點(diǎn)實(shí)驗(yàn)室,福州 350002)
0 引 言
釩(V)同多酸化合物屬于多核金屬-氧簇化合物。釩在形成多酸化合物時(shí)通常有VIII、VIV和VV,它們以四方錐、八面體、三角雙錐等形式通過共點(diǎn)、共邊或共面的方式連接[1],組成釩多酸化合物中簇單元的基本構(gòu)造單元。由于釩具有多種價(jià)態(tài),并且配位方式靈活,導(dǎo)致其多酸化合物的結(jié)構(gòu)多樣,表現(xiàn)出豐富的理化性質(zhì),在光學(xué)[2-3]、磁學(xué)[4-5]、離子交換[6]、催化[7-9]和藥物化學(xué)[10]等方面具有較好的應(yīng)用前景。
近年來,部分學(xué)者嘗試采用多種方法對多酸化合物進(jìn)行表征,研究結(jié)構(gòu)與性能的關(guān)系。筆者曾對多酸化合物的水熱合成條件進(jìn)行了探索[11],在此基礎(chǔ)上,本文利用X射線粉末衍射、紅外光譜、二維紅外相關(guān)光譜、固體紫外漫反射光譜、熱重及高溫紅外光譜等技術(shù)對本文所合成的多酸化合物1和2進(jìn)行研究。
1 實(shí)驗(yàn)部分
1.1 化合物的合成
1.1.1 化合物1的合成
(1) 原料。Na2TeO30.51 mmol,Na3VO4·12H2O 1.99 mmol,LiOH·H2O 1.02 mmol,NH4Cl 2.01 mmol,乙二胺0.2 mL,乙醇6.00 mL(體積分?jǐn)?shù)為50%的溶液)。
(2) 反應(yīng)條件。用濃鹽酸調(diào)節(jié)上述混合液pH為6.6,在不銹鋼高壓反應(yīng)釜中130 ℃恒溫82 h。
(3) 結(jié)果。暗紅色塊狀晶體,按釩計(jì)算產(chǎn)率約為42%。
1.1.2 化合物2的合成
(1) 原料。Na3VO4·12H2O 0.45 mmol,Cu(NO3)2·3H2O 0.64 mmol,CsOH 1.24 mmol,乙二胺0.12 mL,H2O 6.00 mL。
(2) 反應(yīng)條件。用濃鹽酸和氫氧化鈉溶液調(diào)節(jié)pH為5.3,在不銹鋼高壓反應(yīng)釜中100 ℃恒溫11 h。
(3) 結(jié)果。棕褐色片狀晶體,按釩計(jì)算產(chǎn)率約為31%。
1.2 測試儀器與條件
表1為測試儀器及測試內(nèi)容與測試條件。

表1 測試儀器及測試內(nèi)容、測試條件
2 測試結(jié)果分析
2.1 化合物的結(jié)構(gòu)特征
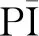
化合物[Cu(en)2]3[V10O28]·6H2O為單斜晶系,P21/c空間群。最小不對稱單元由1/2個(gè)[V10O28]6-陰離子和3/2個(gè)[Cu(en)2]2+陽離子構(gòu)成。Cu2位于對稱軸上,其他原子位于一般等效點(diǎn)上。在化合物2中,[V10O28]6-由2個(gè){VO6}共用6條邊、4個(gè){VO6}共用5條邊、4個(gè){VO6}共用4條邊連接而成,其中V=Ot鍵長0.160 8~0.161 9 nm,V—Oμ鍵長0.169 1~0.223 7 nm,V—O—V鍵角83.36°~175.94°,如圖3所示。根據(jù)價(jià)鍵(BVS)[13]計(jì)算結(jié)果,V的價(jià)態(tài)為+5價(jià)。每個(gè)[V10O28]6-通過與周圍8個(gè)[Cu(en)2]2+及游離的水分子形成N—H…O、C—H…O和O—H…O氫鍵而互相連接,形成三維超分子網(wǎng)絡(luò)結(jié)構(gòu)(見圖4),部分氫鍵列于表3,其中O11、O12、O13、O14為端氧,O4和O10為橋氧。
圖1 化合物1不對稱單元圖
對稱操作符:a) 2+x,-1+y,z;b) 1-x,1-y,1-z;c) 2-x,1-y,-z
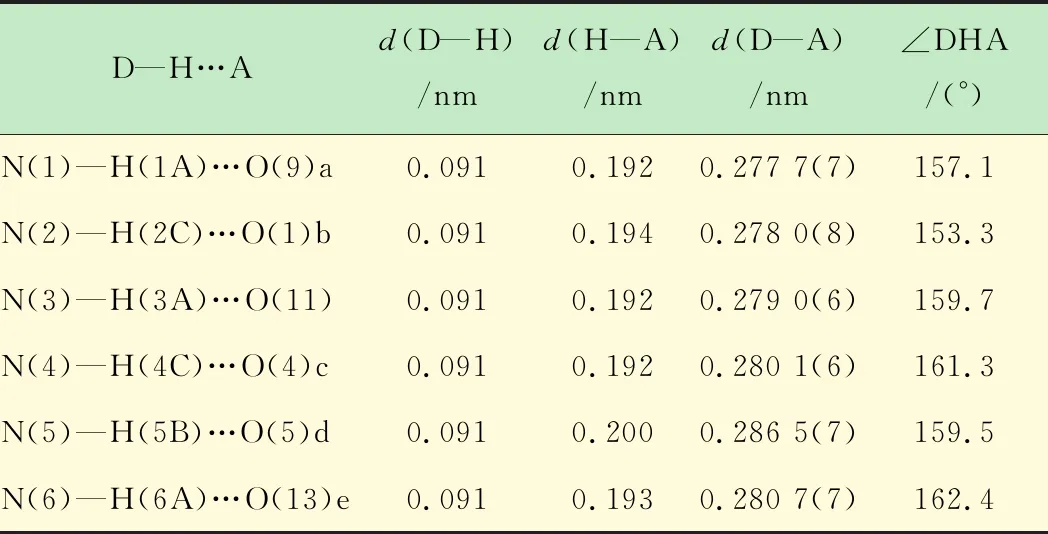
表2 化合物1部分氫鍵列表
對稱操作符:a) -x,1-y,1-z;b)x-1,y+1,z+1;
c) 1-x,-y,1-z;d) 1,y+1,z;e) -x,1-y,-z
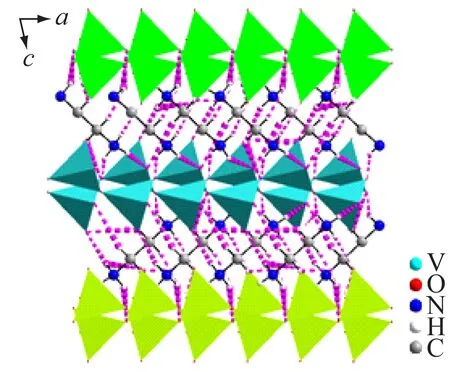
綠、藍(lán)綠、黃綠色多體面代表{VO4}四面體,粉紅點(diǎn)線代表N—H…O和C—H…O氫鍵(省略氫原子)
圖2 化合物1三維堆積圖
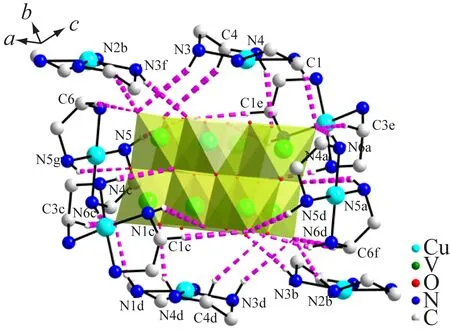
對稱操作符:a)x-1,y,z;b)x,y-1,z;c)x,0.5-y,z-0.5;d) 1-x,-y,-z;e) 1-x,y-0.5,0.5-z;f) 1-x,1-y,-z;g) 2-x,-y,-z
圖3 化合物2的配位環(huán)境圖和氫鍵
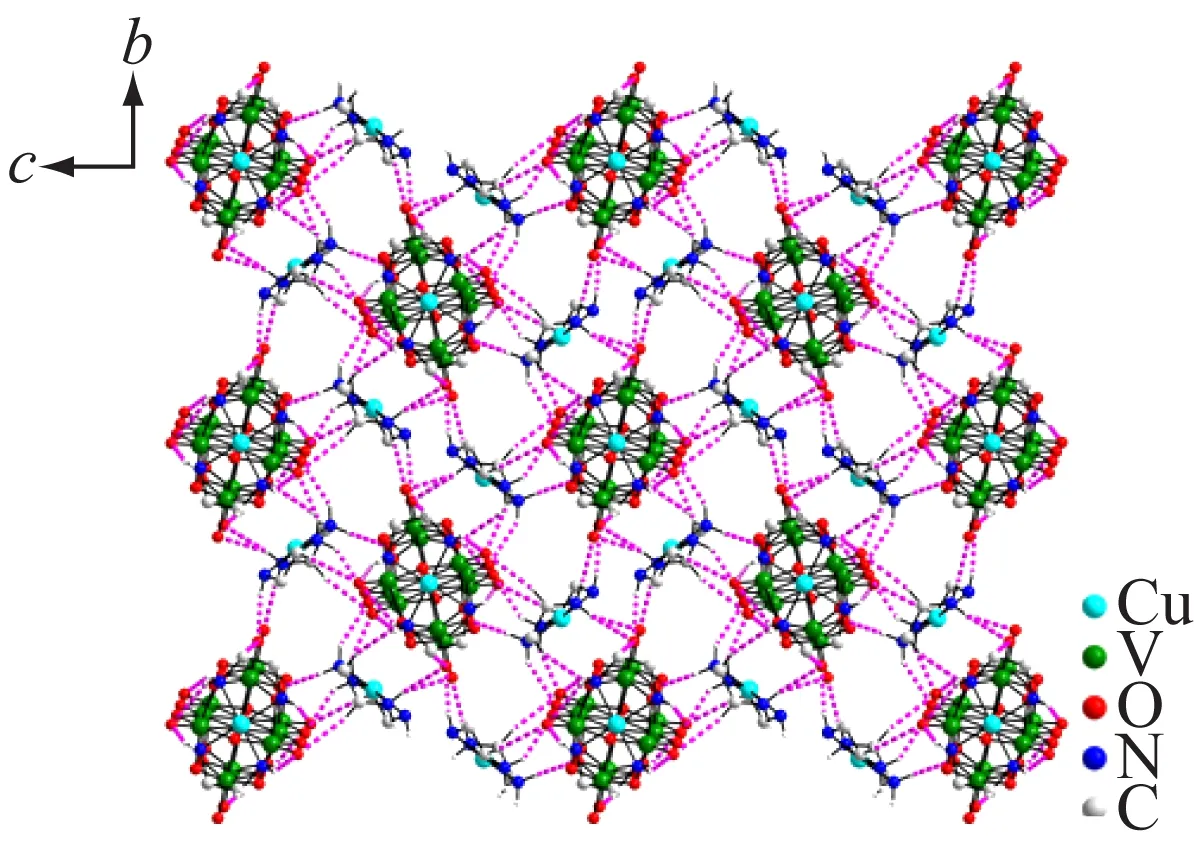
圖4 化合物2沿a軸方向的三維堆積圖
2.2 化合物的X-射線粉末衍射
X-射線粉末衍射是確定化合物晶體結(jié)構(gòu)及物相分析的有效手段。化合物1、2的實(shí)驗(yàn)數(shù)據(jù)圖和模擬衍射圖(見圖5)顯示,實(shí)驗(yàn)數(shù)據(jù)主要衍射峰位置與模擬衍射峰位基本一致,表明所制備的化合物為純相[14],可用于其他性質(zhì)的表征。
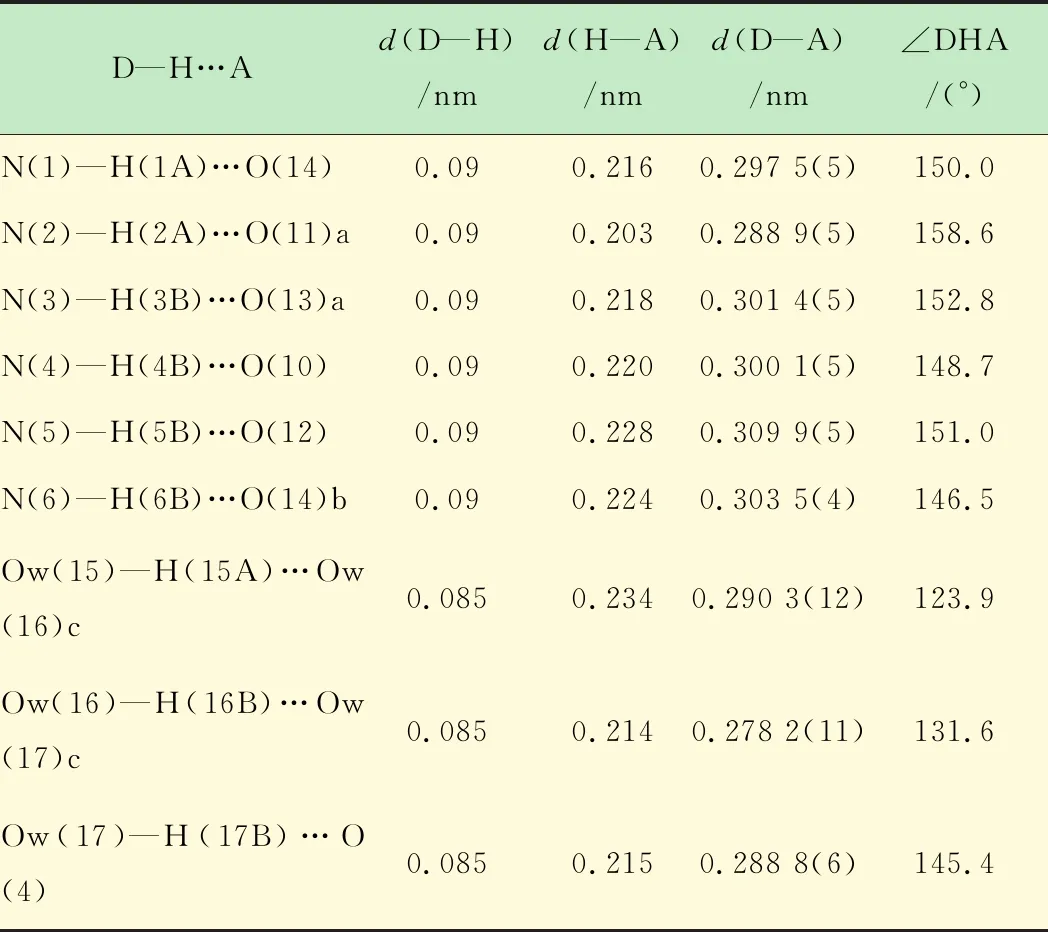
表3 化合物2部分氫鍵列表
對稱操作符:a) -x+1,-y+1,-z;b)x+1,y,z/2;c) -x+2,y-1/2,-z+1/2
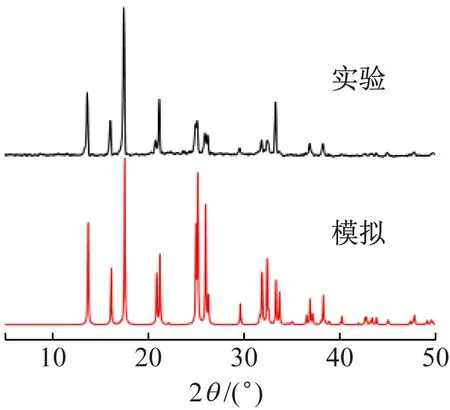
(a) 化合物1
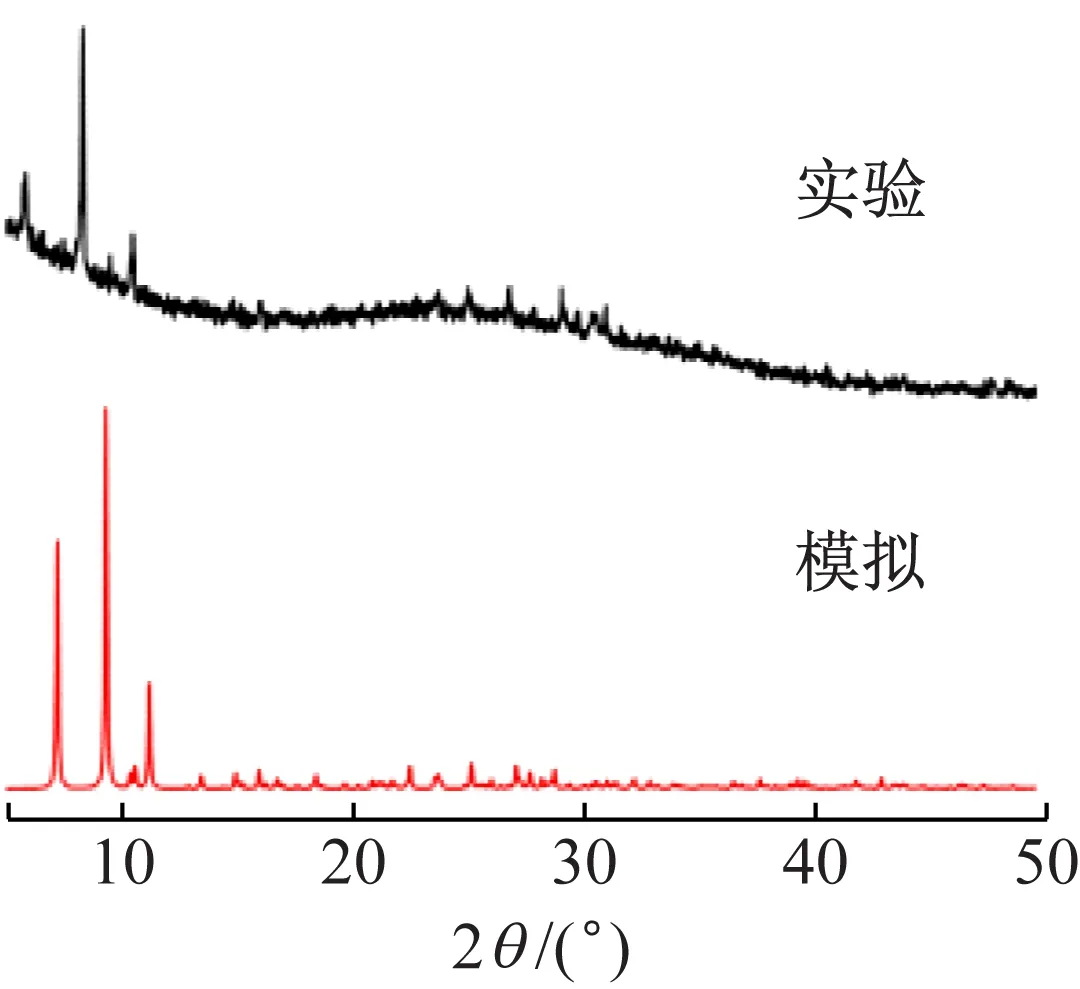
(b) 化合物2
2.3 化合物的紅外光譜和二維紅外相關(guān)光譜
化合物1,2的紅外光譜如圖6所示,兩個(gè)化合物中的釩均為+5價(jià)。化合物1釩為四配位,V=Ot和V—Oμ均與乙二胺形成N—H…O或C—H…O氫鍵,V=Ot和V—Oμ的伸縮振動吸收峰分別位于931、907 cm-1及820、770、674 cm-1。化合物2釩為五配位,所有V=Ot和部分V—Oμ與胺合金屬陽離子或游離的水分子形成N—H…O或C—H…O或O—H…O氫鍵,V=Ot和V—Oμ的伸縮振動吸收峰分別位于947、926、907 cm-1及818、725 cm-1[15]。兩個(gè)化合物的釩氧伸縮振動吸收峰位均向低波數(shù)方向移動。配體乙二胺及化合物1、2的紅外伸縮振動吸收峰見表4。
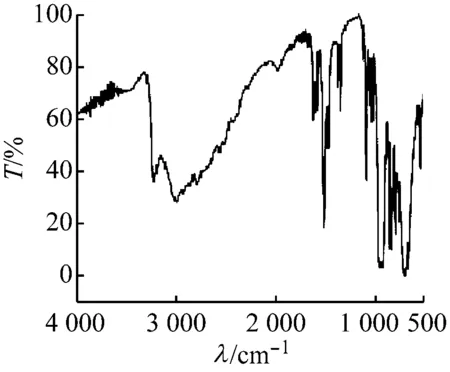
(a) 化合物1
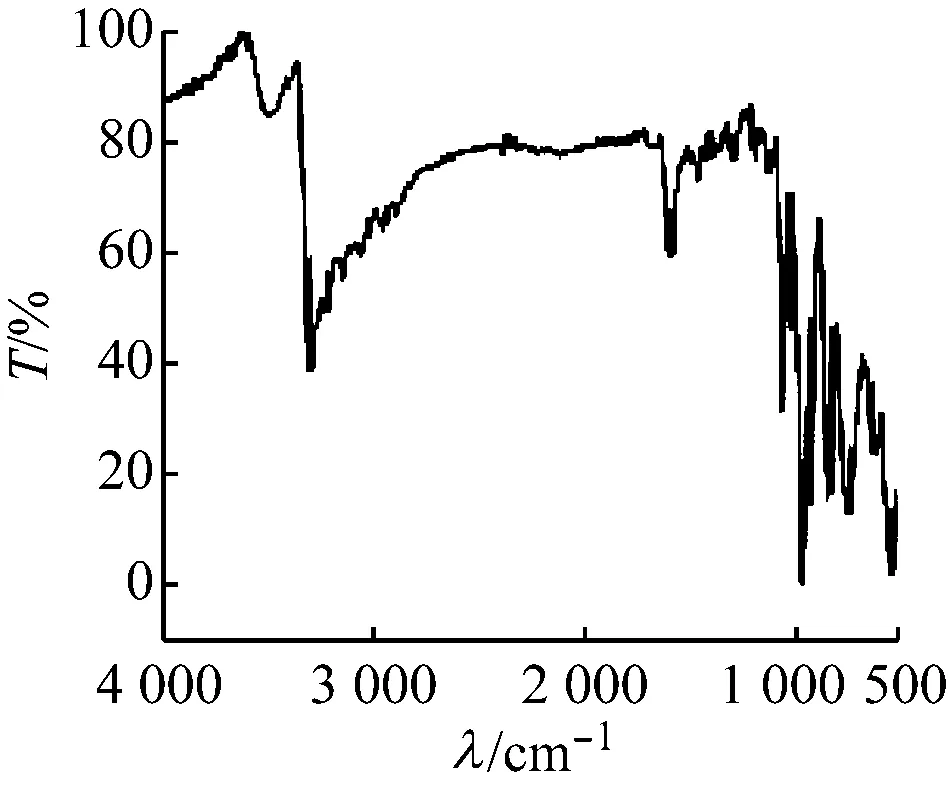
(b) 化合物2
圖6 化合物 1,2的紅外光譜圖
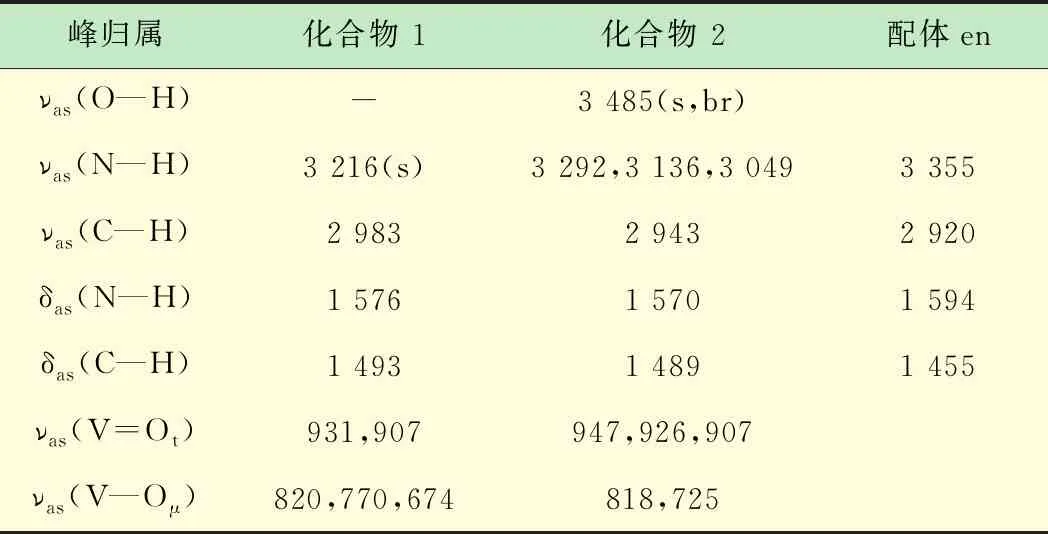
表4 化合物1、2及配體的部分紅外振動吸收峰
由于一維紅外光譜較難區(qū)分釩多酸化合物不同簇籠的振動信息,因此,利用熱微擾附件,在50~120 ℃對化合物進(jìn)行二維紅外相關(guān)光譜的測試并進(jìn)行分析。圖7(a)化合物1的同步相關(guān)圖顯示,在主對角線上的3 225、3 118 cm-1出現(xiàn)了很強(qiáng)的自動峰,表明N—H的伸縮振動對熱微擾比較敏感,(3 225,3 118 cm-1)的交叉峰為負(fù),說明N—H的反對稱和對稱伸縮振動不同步,結(jié)合圖7(b)的異步圖,(3 225,3 118 cm-1)的交叉峰亦為負(fù),根據(jù)Noda[16]規(guī)則,可判斷νas(N—H)對熱變化響應(yīng)先于νs(N—H)發(fā)生。在圖7(c)的主對角線上出現(xiàn)了較強(qiáng)的V—Oμ自動峰,位于824、801、632 cm-1,而V=Ot的自動峰位于943,884 cm-1,同步圖中(824,884 cm-1)的交叉峰為負(fù),圖7(d)異步圖中,交叉峰亦為負(fù),通過自動峰的強(qiáng)度及同步異步圖正負(fù)相關(guān)性[16]比較,可知ν(V—Oμ)比ν(V=Ot)對外界的熱微擾更敏感,且ν(V—Oμ)對熱微擾的響應(yīng)先于ν(V=Ot)進(jìn)行。
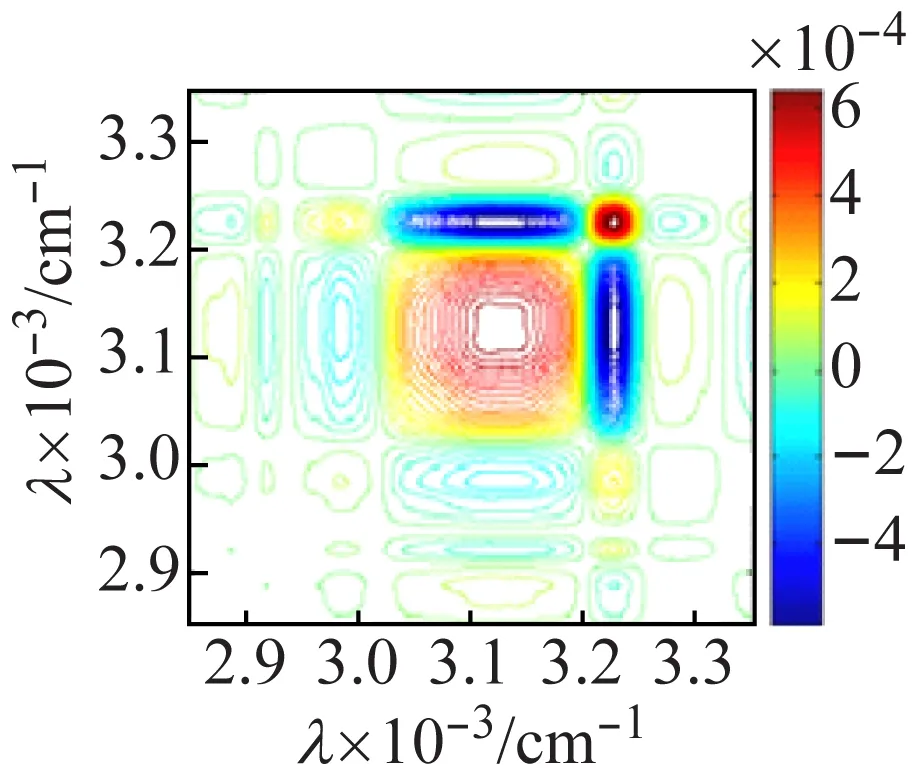
(a) 同步圖
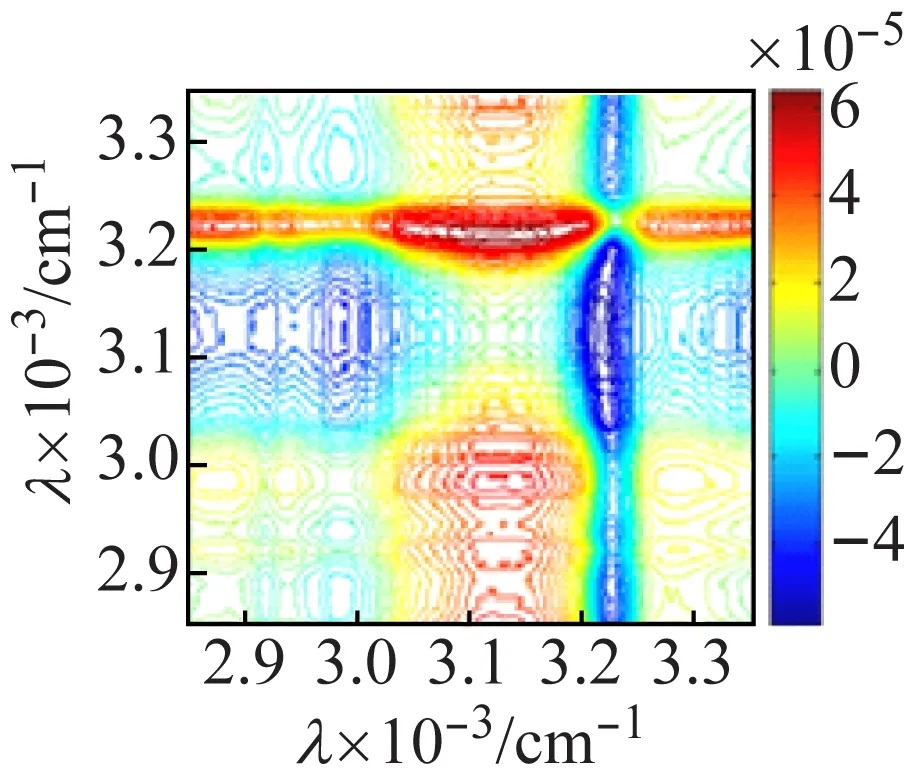
(b) 異步圖
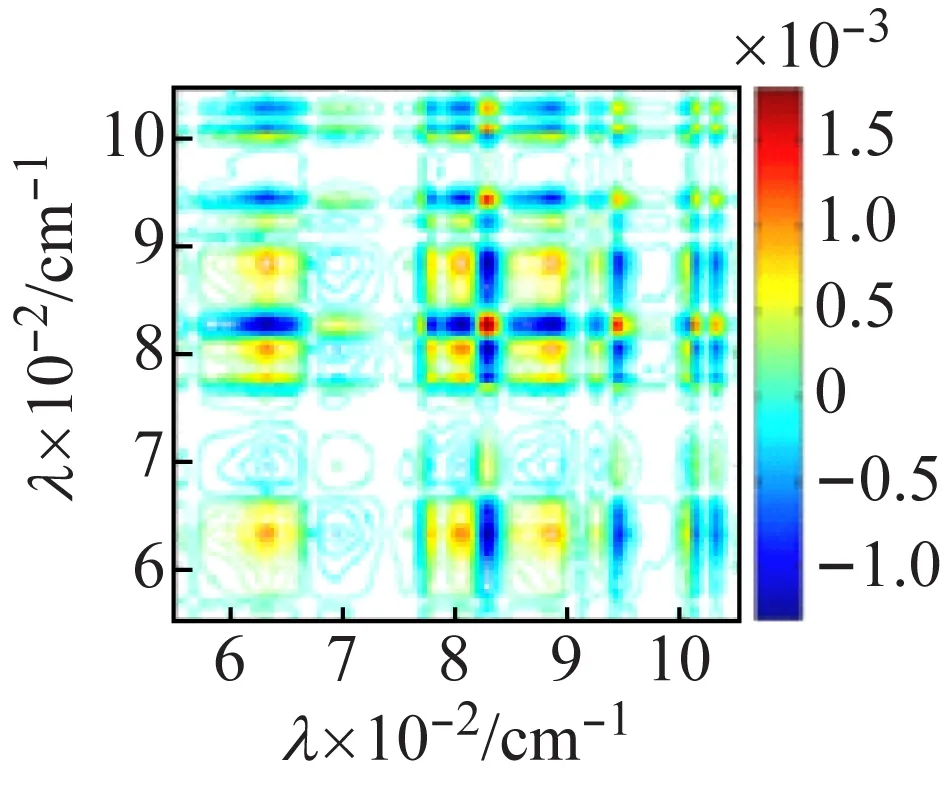
(c) 同步圖
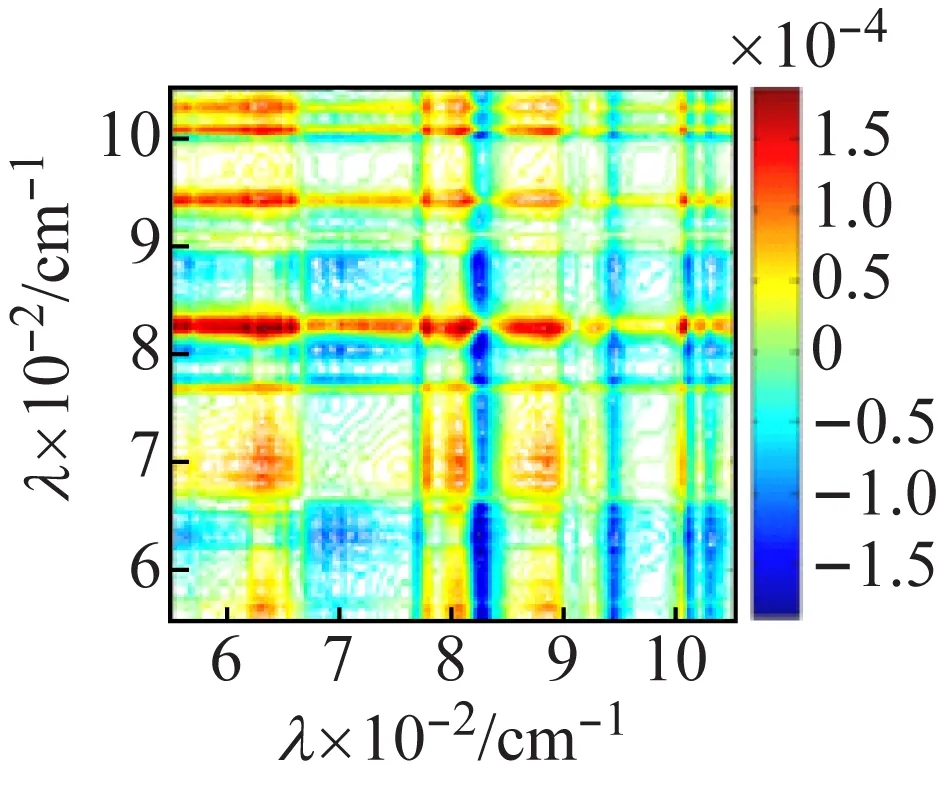
(d) 異步圖
圖8(a)的同步圖中,化合物2在3 265、3 200 cm-1處有很強(qiáng)的熱響應(yīng),對應(yīng)于ν(O—H);在3 120、3 076 cm-1處的自動峰對應(yīng)于ν(N—H)的熱響應(yīng)。由于與多酸陰離子[V10O28]6-上的O原子形成較強(qiáng)的氫鍵,使O—H和N—H的熱響應(yīng)均向低波數(shù)方向移動,同步圖(a)和異圖步(b)中(3 265,3 120 cm-1)處交叉峰均為正,說明ν(O—H)對外界熱微擾的響應(yīng)先于ν(N—H)發(fā)生。圖8(c)中,ν(V=Ot)熱響應(yīng)峰位于971、916 cm-1處;ν(V—Oμ) 熱響應(yīng)峰位于801、714 cm-1處。根據(jù)Noda[16]規(guī)則,結(jié)合同步異步圖各交叉峰的強(qiáng)度和正負(fù)號,可判斷V=Ot比V—Oμ對熱微擾更敏感且對熱微擾的響應(yīng)也更快。化合物1和化合物2的V=Ot、V—Oμ對熱微擾的敏感性及響應(yīng)速度差異,是由于化合物1形成一維鏈狀結(jié)構(gòu),簇籠是無限的,因此釩橋氧對熱響應(yīng)更敏感;而化合物2中所有釩端氧均與乙二胺或水形成很強(qiáng)的氫鍵,呈孤立結(jié)構(gòu),簇籠是有限的,因此在熱微擾中,氫鍵起主要作用,故釩端氧比釩橋氧對熱響應(yīng)更敏感更快。
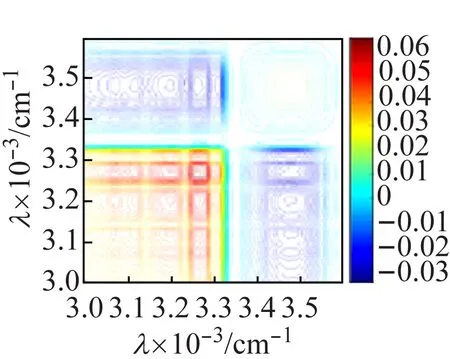
(a) 同步圖
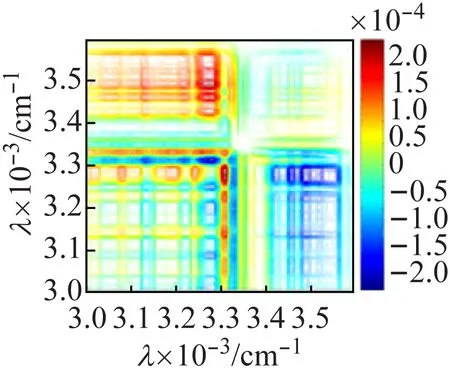
(b) 異步圖
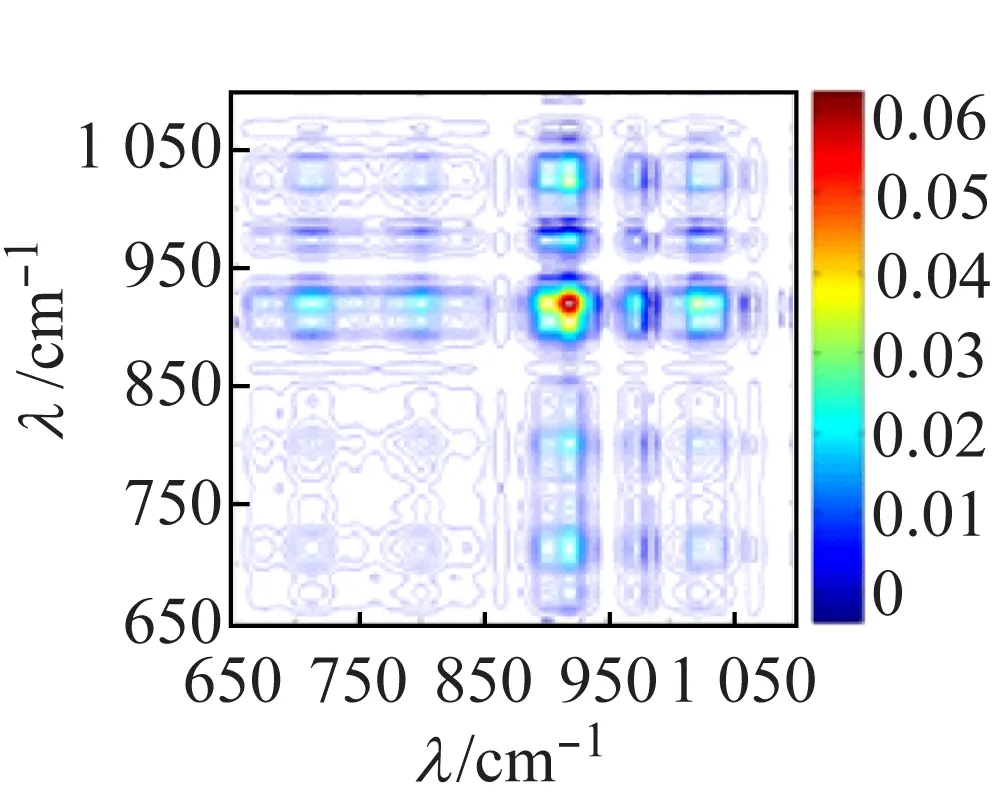
(c) 同步圖
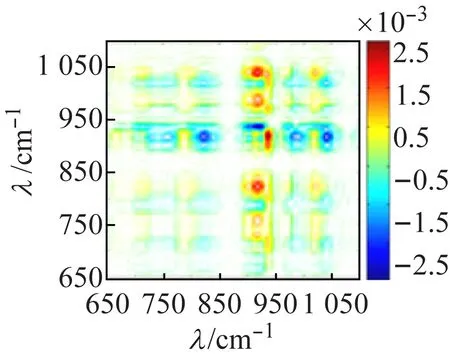
(d) 異步圖
2.4 化合物的固體紫外-可見漫反射光譜
化合物1在200~400 nm間有3個(gè)比較明顯的漫反射峰,分別位于230、291、328 nm處,為O→V的荷移躍遷(見圖9,表5)。化合物2在298、359 nm處有2個(gè)寬化的漫反射峰,為O→V的荷移躍遷;在550~650 nm 處還出現(xiàn)了Cu2+的d→d躍遷。
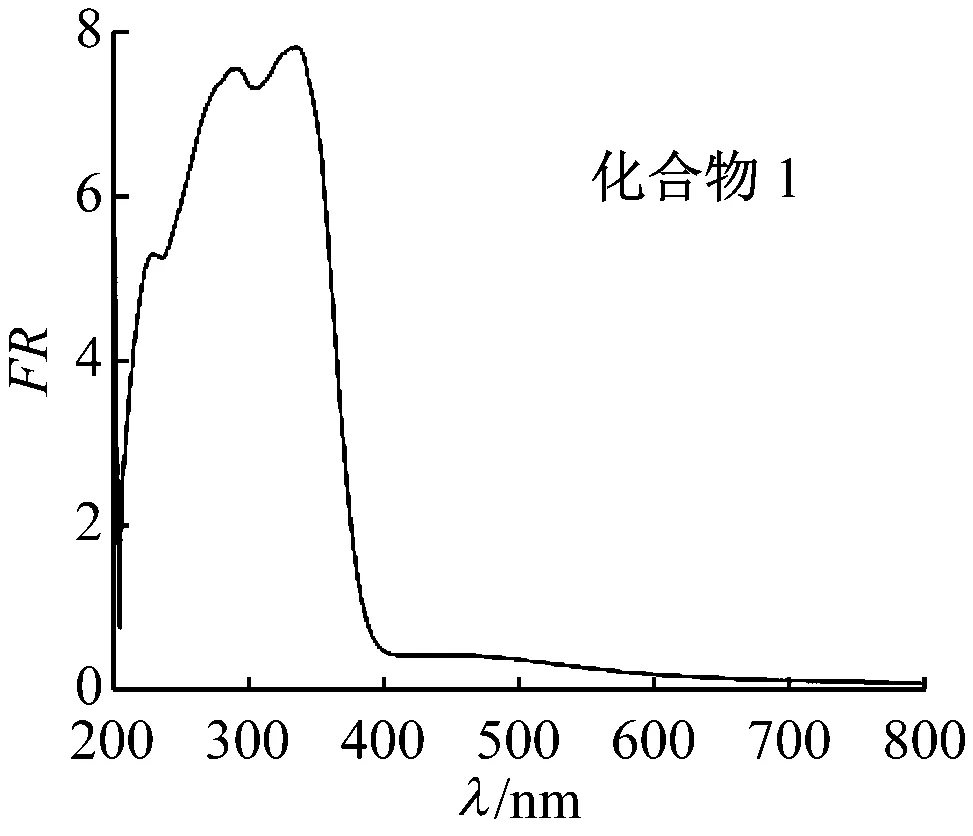
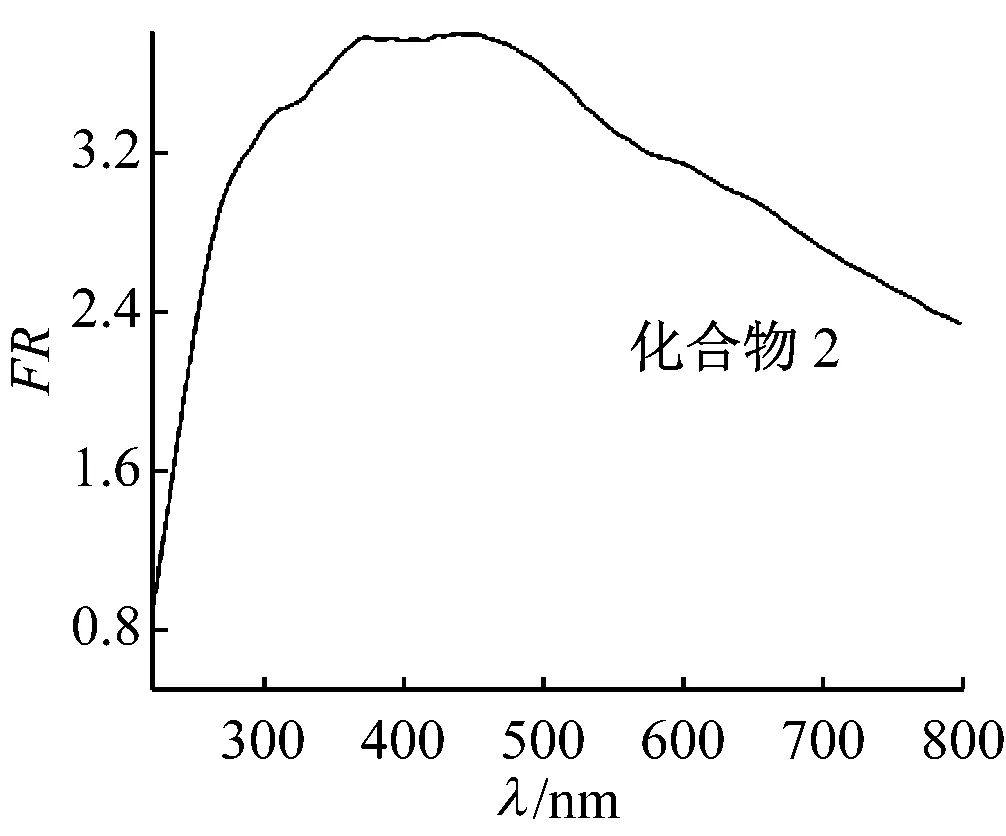
圖9 化合物1,2的固體紫外漫反射光譜
2.5 化合物的熱重分析
化合物1在50~600 ℃的熱失重分2個(gè)階段。第1階段失去3個(gè)雙質(zhì)子化的乙二胺分子(160~390 ℃),失重為20.8% ,理論失重為23.8%。第2階段為釩多酸陰離子骨架坍塌(410~600 ℃),失重為12.6%,整個(gè)過程總失重為33.4%,理論總失重為30%(見圖10、表6)。

表5 化合物的固體紫外漫反射光譜帶
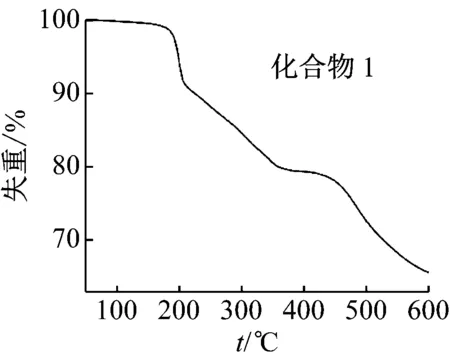
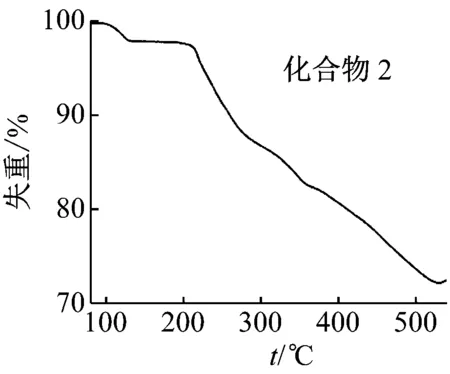
圖10 化合物1,2的熱重曲線
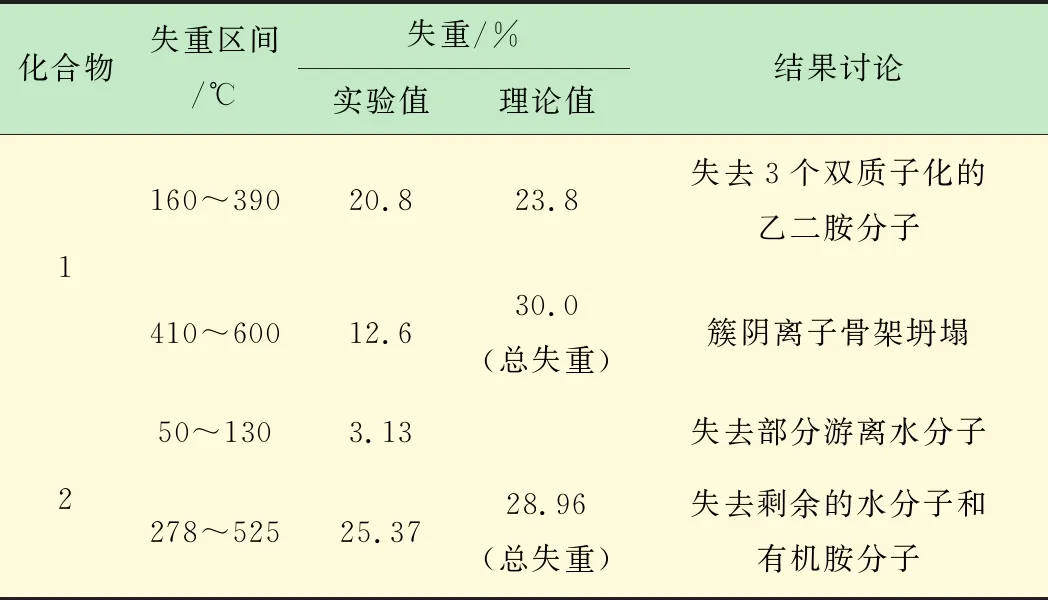
表6 化合物的熱失重值
化合物2在50~530 ℃的熱失重分2個(gè)階段。第1階段失去部分游離水分子(50~130 ℃),失重3.13%;第2階段失去剩余的水分子和[Cu(en)2]2+上的乙二胺分子,失重25.37%,整個(gè)過程總失重為28.50%,理論總失重為28.96%(見圖10、表6)。
熱重分析表明,釩同多酸化合物中的游離水分子最先失去,其次是質(zhì)子化的乙二胺,再次為[Cu(en)2]2+上的乙二胺分子,達(dá)到一定溫度后,釩多酸骨架坍塌。
2.6 化合物的高溫紅外光譜
高溫紅外光譜分析可以進(jìn)一步檢驗(yàn)二維紅外相關(guān)光譜、熱重分析結(jié)果。
根據(jù)圖11(a),隨著溫度的升高,化合物1的N—H和C—H伸縮振動吸收峰逐漸變小,峰形寬化變平,當(dāng)溫度升至300 ℃時(shí),則不再出現(xiàn);當(dāng)溫度升至400 ℃時(shí),在820、770、674 cm-1處,釩簇單元的V—Oμ的伸縮振動吸收峰不再出現(xiàn);當(dāng)溫度升至540 ℃時(shí),931 cm-1處還存在V=Ot伸縮振動吸收峰,說明V—Oμ比V=Ot先斷裂失去。
根據(jù)圖11(b),當(dāng)溫度升至300 ℃時(shí),化合物2的N—H和C—H伸縮振動吸收峰不再出現(xiàn);當(dāng)溫度升至355 ℃時(shí),在818、725 cm-1處,釩簇單元的V—Oμ的伸縮振動吸收峰不再出現(xiàn);當(dāng)溫度升至500 ℃時(shí),947 cm-1處還存在V=Ot的伸縮振動吸收峰,說明釩橋氧鍵比釩端氧鍵先斷裂。
高溫紅外光譜顯示,隨著溫度上升,化合物結(jié)構(gòu)發(fā)生變化、失去小分子的次序?yàn)椋河坞x水分子、游離有機(jī)胺分子、[Cu(en)2]2+上的有機(jī)胺分子,在較高溫度時(shí),簇陰離子骨架坍塌。化合物高溫紅外光譜特征與熱重分析基本吻合。
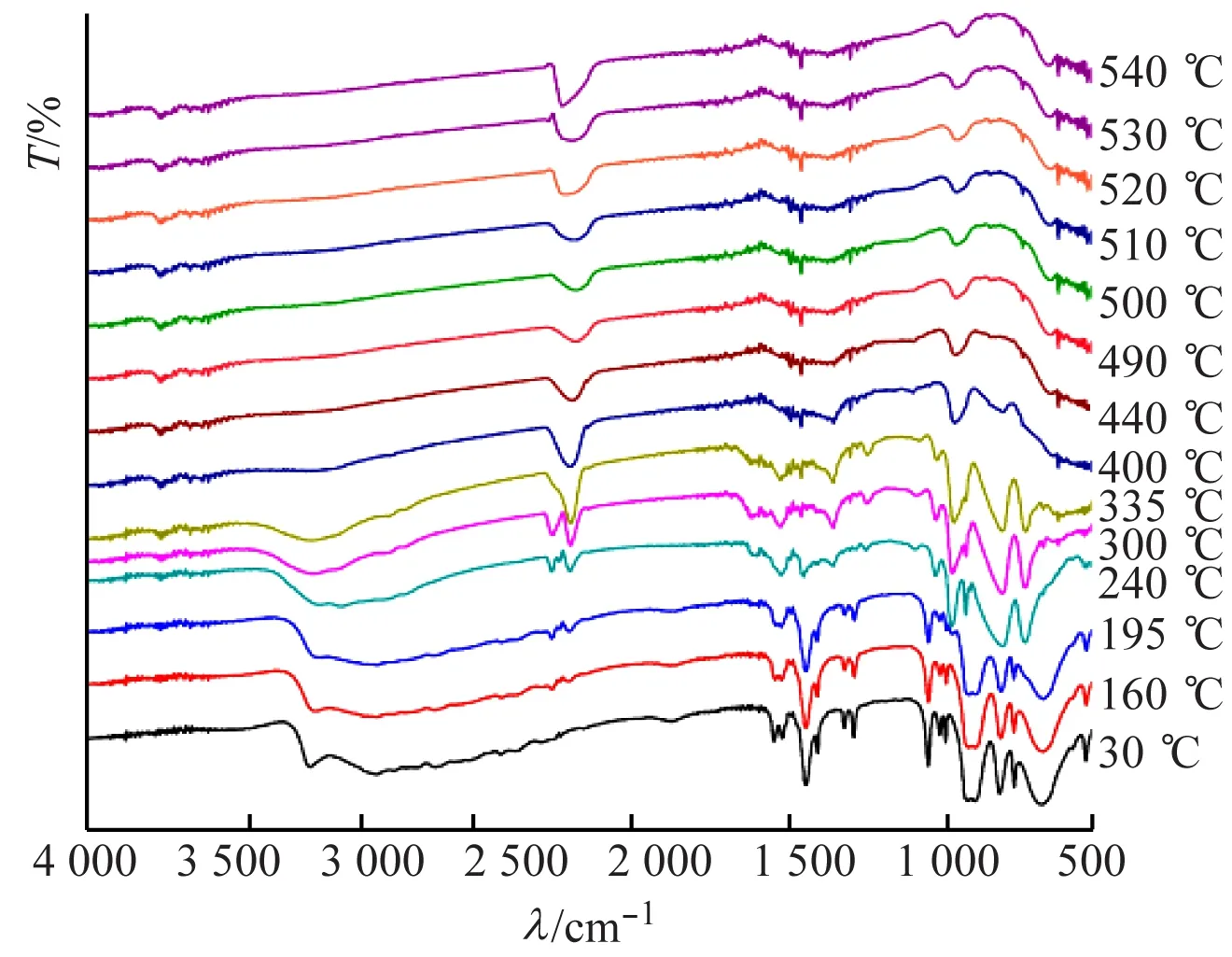
(a) 化合物1
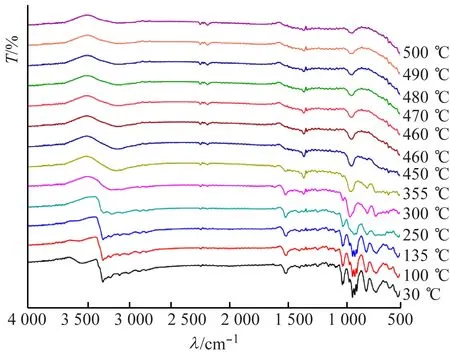
(b) 化合物2
3 結(jié) 語
光譜測試技術(shù)是研究釩多酸化合物結(jié)構(gòu)與性能間關(guān)系的重要手段[17]。本文通過對合成化合物的光譜分析,讓學(xué)生掌握多種譜學(xué)性質(zhì)分析方法的適用范圍及特點(diǎn),包括X-射線單晶衍射確定晶體結(jié)構(gòu),X-射線粉末衍射進(jìn)行物相分析,紅外光譜獲得官能團(tuán)特征頻率,二維紅外相關(guān)光譜研究化合物對外界微擾的響應(yīng)及官能團(tuán)對外界微擾的響應(yīng)次序,紫外-可見漫反射光譜顯示電子能級及LMCT躍遷,熱重分析獲得化合物在升溫過程中質(zhì)量變化,高溫紅外光譜進(jìn)一步顯示化合物熱穩(wěn)定性等。通過光譜測試分析,驗(yàn)證化合物結(jié)構(gòu)的準(zhǔn)確性,并進(jìn)一步探索研究結(jié)構(gòu)與性能間的關(guān)系。
- 實(shí)驗(yàn)室研究與探索的其它文章
- 高 校 輻 射 安 全 管 理 的 實(shí) 踐 與 探 索
- 基于語言信息的經(jīng)管類實(shí)驗(yàn)教學(xué)質(zhì)量評價(jià)方法及應(yīng)用
- 日本產(chǎn)學(xué)官合作國際化人才培養(yǎng)模式改革的啟示
——以日本名古屋大學(xué)為例 - 本科生分子生物學(xué)實(shí)驗(yàn)延伸課堂的教學(xué)實(shí)踐
- 基于QFD理論的經(jīng)營管理虛擬仿真實(shí)訓(xùn)課程教學(xué)設(shè)計(jì)
- 肩負(fù)起新時(shí)代高校育人的歷史使命
——淺談新時(shí)代《實(shí)驗(yàn)室研究與探索》期刊的責(zé)任與擔(dān)當(dāng)

