卡維地洛預處理對缺氧/復氧誘導心肌H9C2細胞凋亡的影響及其機制
趙勇,徐巖,姬婷婷
(安徽醫科大學附屬阜陽醫院,安徽阜陽236000)
急性心肌缺血可直接導致心肌細胞死亡,再灌注后也會引起心肌細胞凋亡[1]。急性心肌缺血動物實驗表明,細胞凋亡主要發生在缺血壞死區域周圍,可促進梗死面積的擴大[2]。因此,減輕缺血再灌注損傷所致心肌細胞凋亡對于減小梗死面積具有重要意義。在心肌組織中Toll樣受體(TLRs)主要表達TLR2和TLR4,而TLR4/NF-κB信號通路是參與細胞凋亡的重要信號通路之一[3,4]。β-arrestin2為NF-κB的調控蛋白,參與TLR4/NF-κB信號通路調控。卡維地洛為第三代β受體阻滯劑,在非選擇性阻斷β受體的同時,還選擇性阻斷α1受體,并具有鈣拮抗作用,能顯著改善心肌梗死、心衰患者的預后,但是其作用機制相關報道較少[5]。2015年11月~2017年11月,本研究觀察了不同濃度卡維地洛預處理對缺氧/復氧后心肌細胞凋亡的影響,并探討其機制是否與β-arrestin2及TLR4/NF-κB信號通路有關。現報告如下。
1 材料與方法
1.1 材料 細胞:心肌H9C2細胞(簡稱H9C2細胞)由安徽醫科大學基礎醫學院提供。主要藥品及試劑:卡維地洛購于山東齊魯制藥有限公司,胎牛血清購于美國Hyclone公司,SDS-PAGE凝膠配制試劑盒、RIPA細胞裂解液購于碧云天生物技術有限公司,電化學發光(ECL)試劑盒購于美國Pierce公司,TLR4封閉抗體購于德國CST公司,熒光測定TUNEL凋亡檢測系統購于美國Promega公司。主要儀器:EPS300型電泳儀購于上海天能科技有限公司,熒光定量PCR儀ABI7500購于美國ABI公司,Modulus多功能光度計購于美國BioSystems公司,倒置熒光顯微鏡購于日本Olympus公司。
1.2 細胞分組處理 將對數生長期的H9C2細胞分為模型組、低劑量卡維地洛組、中劑量卡維地洛組、高劑量卡維地洛組、TLR4封閉抗體組和對照組。對照組在37 ℃、5% CO2的無菌培養箱中培養12 h,常規換液,其余各組參照Esumi等[6]的方法建立細胞缺氧/復氧模型。低、中、高劑量卡維地洛組及TLR4封閉抗體組分別在缺氧/復氧損傷前30 min加入1、5、10 μmol/L卡維地洛及20 μg/mL TLR4封閉抗體進行預處理。
1.3 細胞凋亡率檢測 采用TUNEL法。取各組細胞,加入配置好的TUNEL檢測液,制成載玻片。在熒光顯微鏡下分析樣本,用標準的熒光過濾裝置在(520±20)nm波長下觀察熒光素-12-dUTP摻入并定位的綠色熒光,>620 nm波長下觀察碘化丙啶定位的紅色熒光。紅色熒光表示存活細胞與凋亡細胞的細胞核,綠色熒光表示凋亡細胞的細胞核。計數視野內的凋亡細胞與總細胞,計算細胞凋亡率。
1.4 凋亡相關蛋白Bax、Bcl-2表達檢測 采用Western blotting法。取各組細胞,加入細胞裂解液提取總蛋白,BCA法測定蛋白濃度;配制SDS-PAGE凝膠,以每孔25 μg等質量上樣,濃縮膠所用電壓為80 V,時間為30 min;分離膠所用電壓為120 V,時間為1 h;待溴酚藍剛跑出時終止電泳。采用半干轉膜法將蛋白轉到聚偏二氟乙烯(PVDF)膜上,5%脫脂奶粉封閉2 h;加入一抗(1∶1 000)孵育過夜,TBST洗膜3次,加入二抗(1∶10 000)孵育,TBST洗膜3次,ECL顯色。以β-actin作為內參,采用Image J軟件進行灰度值分析,計算目的條帶與內參條帶灰度值的比值。
1.5 TLR4、NF-κB、β-arrestin2 mRNA表達檢測 采用實時熒光定量PCR法。取各組細胞,加入TRIzol試劑提取總RNA,微量核酸定量儀定量檢測各樣本RNA濃度及純度合格后,參照反轉錄試劑盒說明書逆轉錄RNA合成cDNA。TLR4上游引物5′-TCATGCTTTCTCACGGCCTC-3′,下游引物5′-AGGAAGTACCTCTATGCAGGGAT-3′,引物長度142 bp;NF-кB上游引物5′-ACGATCTGTTTCCCCTCATC-3′,下游引物5′-TGCTTCTCTCCCCAGGAATA-3′,引物長度150 bp;β-arrestin2上游引物5′-CACAAAAGGAACTCCGTGCG-3′,下游引物5′-AGACATGAGGAAGTGGCGTG-3′,引物長度105 bp;內參β-actin上游引物5′-CGCGAGTACAACCTTCTTGC-3′,下游引物5′-CGTCATCCATGGCGAACTGG-3′,引物長度70 bp。PCR反應體系20 μL: 2×Goldstar Taqman mixture 10 μL,上、下游引物各0.4 μL,Probe 0.4 μL,模板DNA 2 μL,Rnase Free water 6.8 μL。PCR反應條件:95 ℃預變性10 min;95 ℃變性15 s,退火15 s,60 ℃延伸1 min,共40個循環。采用2-ΔΔCt法計算TLR4、NF-κB、β-arrestin2 mRNA相對表達量。
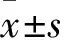
2 結果
2.1 各組細胞凋亡率及Bax、Bcl-2蛋白表達比較 與對照組比較,其余各組細胞凋亡率、Bax蛋白表達均升高,Bcl-2蛋白表達降低,以模型組變化最明顯(P均<0.05)。低、中、高劑量卡維地洛組細胞凋亡率、Bax蛋白表達均依次降低,Bcl-2蛋白表達均依次升高(P均<0.05)。見表1、圖1。
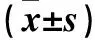
表1 各組細胞凋亡率及Bax、Bcl-2蛋白表達比較
注:與對照組比較,aP<0.05;與模型組比較,bP<0.05;與低劑量卡維地洛組比較,cP<0.05;與中劑量卡維地洛組比較,dP<0.05。
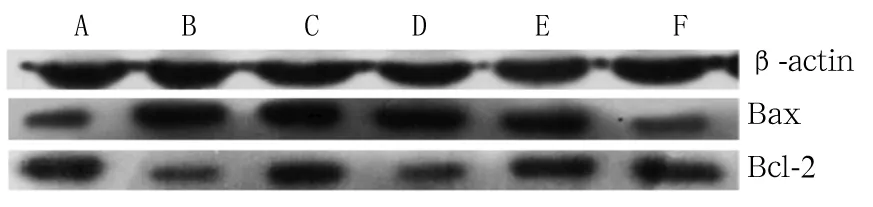
注:A為對照組,B為模型組,C為低劑量卡維地洛組,D為中劑量卡維地洛組,E為高劑量卡維地洛組,F為TLR4封閉抗體組。
圖1各組Bax、Bcl-2蛋白表達情況(Western blotting法)
2.2 各組TLR4、NF-κB、β-arrestin2 mRNA表達比較 與對照組比較,模型組TLR4、NF-κB mRNA表達均升高,β-arrestin2 mRNA表達均降低,TLR4封閉抗體組NF-κB mRNA表達降低(P均<0.05)。與模型組比較,TLR4封閉抗體組及低、中、高劑量卡維地洛組TLR4、NF-κB mRNA表達均降低,TLR4封閉抗體組及高劑量卡維地洛組β-arrestin2 mRNA表達均升高(P均<0.05)。與低劑量卡維地洛組比較,中、高劑量卡維地洛組TLR4、NF-κB mRNA表達均降低,β-arrestin2 mRNA表達均升高(P均<0.05)。見表2。
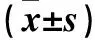
表2 各組TLR4、NF-κB、β-arrestin2 mRNA表達比較
注:與對照組比較,aP<0.05;與模型組比較,bP<0.05;與低劑量卡維地洛組比較,cP<0.05;與中劑量卡維地洛組比較,dP<0.05。
3 討論
心肌再灌注是治療急性心肌梗死的重要措施,但隨著心肌細胞缺血情況的改善,再灌注損傷成為患者預后不良的重要原因[7,8]。Gottlieb等[9]在家兔離體心臟再灌注模型中發現,家兔心臟缺血30 min、4.5 h時均無細胞凋亡發生,而缺血30 min再灌注4 h后出現明顯的心肌細胞凋亡。卡維地洛是一種新型非選擇性腎上腺素能受體阻滯劑,可以阻斷β1、β2和α1受體,且不增加心肌對兒茶酚胺的敏感性,具有良好的無內在擬交感活性、極強的抗氧化損傷作用等。卡維地洛對細胞信號傳導的影響可以通過多種通路進行,如下調miRNA表達、抑制AKT/XIAP信號通路等[10,11]。但是,卡維地洛減輕心肌細胞缺血再灌注損傷的分子機制尚不清楚。
Bcl-2家族蛋白是第一個被發現與凋亡有關的蛋白,該家族蛋白具有很多同源基因或蛋白,其中研究比較廣泛的是具有抑制細胞凋亡作用的Bcl-2、McLI、Al、Befl以及具有促進細胞凋亡作用的Bax、Bad、Bik等。研究表明,Bcl-2可通過直接抗氧化作用[12]、抑制Caspase激活[13]、維持細胞內鈣平衡、抑制核酸內切酶等途徑抑制細胞凋亡。本研究結果顯示,與對照組比較,其余各組細胞凋亡率、Bax蛋白表達均升高,Bcl-2蛋白表達均降低,以模型組變化最明顯,而低、中、高劑量卡維地洛組細胞凋亡率、Bax蛋白表達均依次降低,Bcl-2蛋白表達均依次升高;這說明卡維地洛可減輕H9C2細胞缺氧/復氧造成的細胞凋亡,并具有濃度相關性。
TLR4是人類發現的首個TLRs相關蛋白,幾乎在所有細胞中均有表達,并參與動脈粥樣硬化、血栓、心肌重構、缺血再灌注損傷甚至瓣膜性疾病等心血管疾病的病理過程。TLR4被激活后啟動信號通路,轉運到細胞內并活化NF-κB;而NF-κB是調控多種基因轉錄的重要因子,在細胞凋亡調控、免疫應答、炎癥反應中發揮重要作用[14]。β-arrestin2是NF-κB的負調控因子,可招募CARMA3到溶血磷脂酸(LPA)受體,在GPCR介導的NF-κB信號通路中發揮重要作用[15]。本研究結果顯示,TLR4封閉抗體組細胞凋亡率、Bax蛋白表達均低于模型組,Bcl-2蛋白表達高于模型組,說明凋亡相關蛋白Bcl2、Bax表達受TLR4信號通路調控,TLR4信號通路參與了心肌細胞缺氧/復氧過程中的細胞凋亡;模型組TLR4和NF-κB mRNA表達明顯高于對照組,而TLR4封閉抗體組TLR4和NF-κB mRNA表達均低于模型組,β-arrestin2 mRNA表達高于模型組;結合細胞凋亡結果,證實β-arrestin2對TLR4具有負調節作用,且TLR4/NF-κB信號通路與缺氧/復氧損傷導致的心肌細胞凋亡有關。本研究中,低、中、高劑量卡維地洛組TLR4、NF-κB mRNA表達均低于模型組,以中、高劑量卡維地洛組變化更明顯,說明中等劑量的卡維地洛即可抑制TLR4/NF-κB信號通路;但是,低、中、高劑量卡維地洛組β-arrestin2 mRNA表達逐漸升高,與TLR4、NF-κB mRNA表達變化并不同步,說明卡維地洛既可以直接抑制TLR4/NF-κB信號通路,又可通過增加β-arrestin2表達而負調控TLR4/NF-κB信號通路。
綜上所述,卡維地洛預處理能夠減輕缺氧/復氧誘導的H9C2細胞凋亡,并呈濃度相關性,其機制可能與升高β-arrestin2表達及抑制TLR4/NF-κB信號通路有關。

