102例注射用腦蛋白水解物不良反應分析
宋 濱,劉承啟,姜 華
(淄博市藥品不良反應監測中心,山東 淄博 255020)
注射用腦蛋白水解物為豬腦組織提分離、精制而得的無菌制劑,內含約16種游離氨基酸及少量肽。本品可透過血腦屏障進入神經細胞,以多種方式作用于中樞神經,調節和改善神經元的代謝,促進突觸的形成,誘導神經元的分化,保護神經細胞免受各種缺血和神經毒素的損害[1]。臨床主要用于顱腦外傷、腦血管病后遺癥伴有記憶力減退及注意力集中障礙的癥狀改善[2]。本文對注射用腦蛋白水解物引起的102例藥品不良反應(ADR)報告進行統計和分析,了解其ADR發生特點,為指導臨床合理用藥提供參考。
1 資料與方法
1.1 資料來源
報告來源于2012~2016年淄博市藥品不良反應監測中心收集到的102例注射用腦蛋白水解物不良反應報告。
1.2 統計方法
采用回顧性研究方法,對患者年齡、性別、用法用量、ADR發生時間、累及系統-器官、嚴重的不良反應、ADR轉歸等進行了統計分析。
2 結果
2.1 年齡與性別分布
102 例報告中,男女比例為1.08:1,表明ADR發生率與性別關系不大。患者最小年齡29歲,最大年齡91歲,平均年齡65歲。從年齡段看,51~80歲患者占絕大多數,比例為78.43 %。結果見表1。
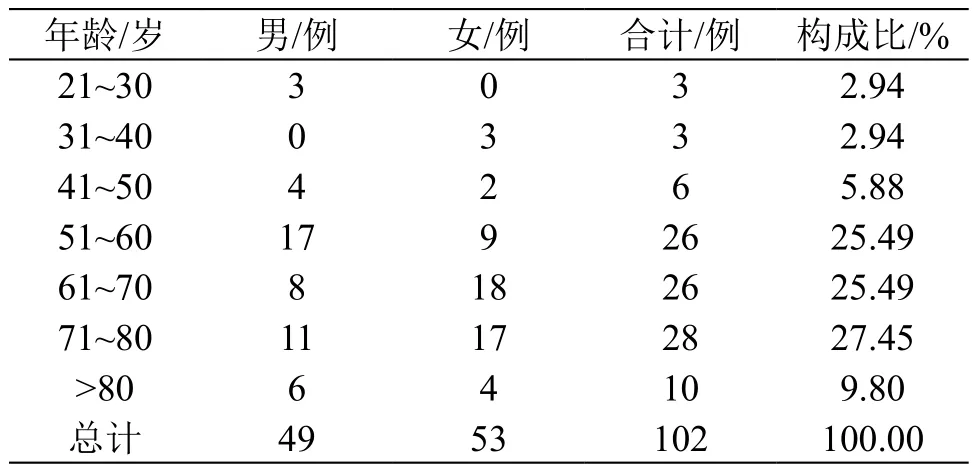
表1 ADR患者年齡與性別分布
2.2 用法用量情況
102 例報告中,用法均為靜脈滴注,每日一次。日劑量為60~180 mg共94例,日劑量低于60 mg共8例,日劑量為120 mg用藥時不良反應發生率最高。僅27例報告中上報溶媒信息,其中21例生理鹽水,6例葡萄糖注射液。結果見表2。
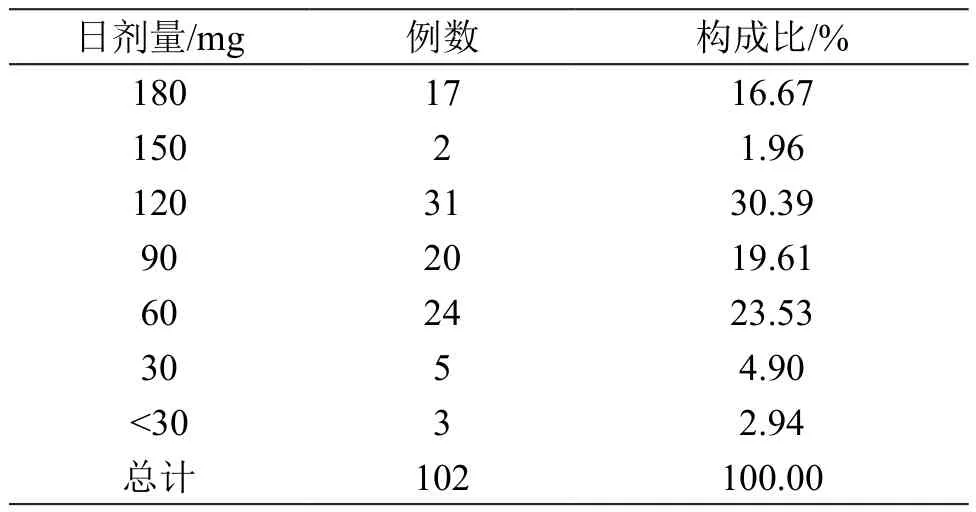
表2 ADR患者日劑量分布
2.3 ADR發生時間
102 例報告中,ADR主要發生在30 min以內,共55例,占53.92 %;30 min以上共16例,占15.69 %;發生時間不詳,共31例。結果見表3。

表3 ADR發生時間
2.4 ADR累及器官-系統及臨床表現
102 例報告共包含不良反應192例次,累及皮膚及其附件、呼吸系統、全身性損害、神經系統、消化系統等多個系統-器官。其中皮膚及其附件損害占比最大,為46.88 %。結果見表4。
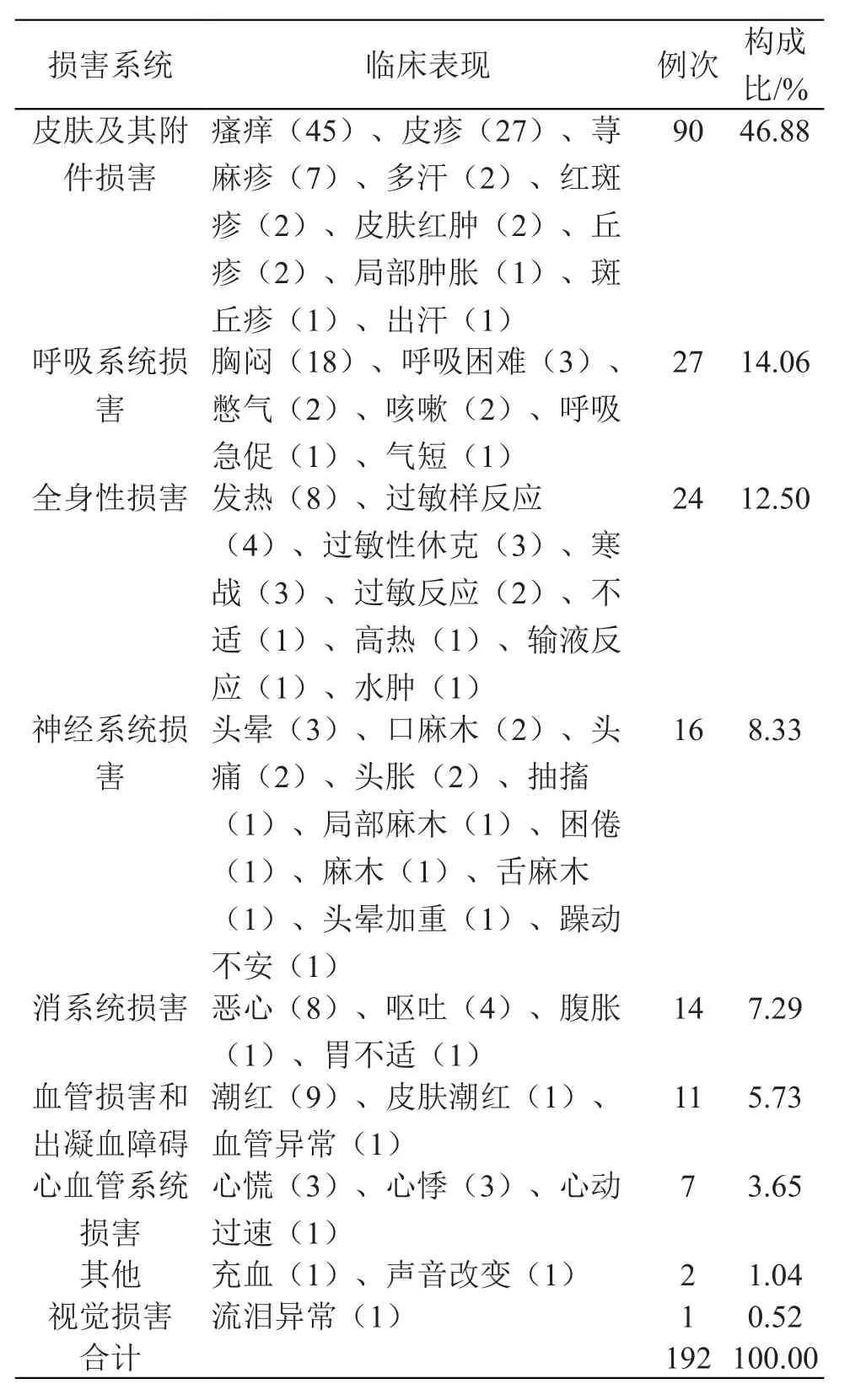
表4 ADR累及器官-系統及臨床表現
2.5 嚴重ADR報告情況
102 例報告中,嚴重不良反應30例,占29.41 %。30例嚴重報告,男女比例為1.73:1,51~80歲患者占比高達80.00 %;日劑量為120 mg時不良反應發生率最高,其次為90 mg日劑量;ADR主要發生在30 min以內,共20例,占66.67 %;主要臨床表現為瘙癢、胸悶、皮疹、過敏樣反應、過敏性休克、呼吸困難等癥狀。
2.6 ADR轉歸
102 例報告中,ADR治療64例,未治療38例;29例好轉,73例治愈,無死亡病例,說明由注射用腦蛋白水解物引起的不良反應可控可治。
3 討論
3.1 中老年患者不良反應發生率高
102 例報告中,51~80歲患者占比達78.43 %,與注射用腦蛋白水解物的適用癥有關。注射用腦蛋白水解物臨床主要用于顱腦外傷、腦血管病后遺癥伴有記憶減退及注意力集中障礙的癥狀改善的治療,而此類疾病多發生于老年人中,故本品使用頻率高,藥品不良反應發生率相應增高[1]。因此,中老年患者用藥時應注意用藥反應,一旦發現不良反應,應及時停藥,并給予對癥治療,防止不良反應惡化。
3.2 存在溶媒選擇不合理情況
該藥說明說中規定用法為靜脈滴注,每日一次;用量為60~180 mg,用250 ml生理鹽水稀釋。102例報告中,用法均符合要求;94例給藥劑量符合要求,8例給藥劑量低于規定量;6例報告未按要求選擇溶媒。葡萄糖注射液的pH值為3.2~6.5,為酸性溶液,而注射用腦蛋白水解物的《藥品檢驗報告書》中其酸堿度檢查要求溶劑pH值為6.5~7.5,故應選擇偏中性的0.9 %氯化鈉注射液。溶劑選擇不當,藥物的有效性及安全性難以保障[3]。醫師應嚴格按照藥品說明書規定的劑量、稀釋溶媒用藥,避免不合理用藥。同時還應控制好給藥速度,國家食品藥品監督管理總局已于2016年11月10日下發公告,對腦蛋白腦蛋白水解物注射劑(包括注射用腦蛋白水解物及腦蛋白水解物注射液)說明書進行修訂,要求增加“使用過程中應嚴格按照說明書中規定的用法用量緩慢滴注,建議用藥起始10 min內滴注速度不超過30滴/min”警示語[4]。
3.3 不良反應多為速發型
102 例報告中,不良反應最早為首次用藥2 min后,最遲為5 d后;其中,30 min以內出現不良反應的比例最高,達到53.92 %,說明注射用腦蛋白水解物引起的不良反應主要為速發型。因此,注射用腦蛋白水解物用藥后30 min內應密切關注患者異常情況,發現不良反應,應立即停藥并及時處理,防止不良反應發展而對患者造成嚴重損害[5-6]。
3.4 不良反應累及器官-系統臨床表現
102 例報告累及多個系統-器官,其中以皮膚及其附件損害、呼吸系統損害及全身性損害不良反應較多。皮膚及其附件損害臨床主要表現為瘙癢、皮疹、蕁麻疹、皮膚紅腫、紅斑疹等癥狀;呼吸系統臨床主要表現為胸悶、呼吸困難、憋氣、咳嗽等癥狀;全身性損害主要表現為發熱、過敏樣反應、過敏性休克、寒戰等癥狀。因此,醫護人員應了解注射用腦蛋白水解物藥品說明書最新動態,熟悉不良反應發規律及必要護理知識,最大限度減少患者的身體傷害。
3.5 過敏性休克原因分析
102 例報告中,有3例患者發生過敏性休克,經地塞米松、腎上腺素等藥物治療后好轉或痊愈。文獻[7-11]還報道了4例患者使用注射用腦蛋白水解物后發生過敏性休克病例。引起過敏性休克的原因可能是:(1)由于本品為豬腦提取物,若在制備過程中水解物提取不完全,有微量蛋白質存在,這些成分有可能作為抗原或半抗原物質,進入體內刺激機體產生抗體或致敏淋巴細胞,誘發變態反應[11]。(2)可能與患者體質有關,由于患者本身對本品中某種成份敏感所致,有文獻[12]報道,1例對豬肉過敏患者在使用本品后發生過敏性休克。(3)可能與溶劑選擇不當和靜滴速度有關,本品說明書規定只能用生理鹽水稀釋,而且最新版藥品說明書中警示語提示,在使用本品時應緩慢靜滴,用藥起始10 min內滴注速度不超過30滴/min。
3.6 不良反應的預防與處理
鑒于注射用腦蛋白水解物存在的以上不良反應,醫護人員在使用本品前應仔細詢問患者用藥史和過敏史,對本品有過敏史的患者禁用,對過敏體質患者及有食物或藥物過敏史的患者慎用本品[13]。充分掌握該藥適用癥,嚴格按照藥品說明書規定選擇溶媒,并控制好滴注速度,避免不合理用藥。加強用藥后監測,尤其是用藥后30 min內,密切注意患者的用藥反應,出現異常情況及時停藥,并采取對癥治療,防止過敏性休克等嚴重不良反應的發生。

