浙江選考化學反應原理綜合試題常見失誤診斷
馮瑩 丁弘正
摘 要:化學反應原理綜合試題是浙江化學選考綜合大題中的重點和難點,本文從知識和思維兩個維度對學生在解題過程中出現的失誤進行診斷,并提出相應改進策略.
關鍵詞:選考;化學反應原理;失誤診斷
作者簡介:馮瑩(1991-),女,浙江紹興人,研究生,教育碩士,中學二級教師,研究方向:化學學科教學、化學教學診斷研究;
丁弘正(1990-),男,浙江紹興人,研究生,教育碩士,中學一級教師,研究方向:化學學科教學、化學教學診斷研究.
化學反應原理綜合試題是化學選考中的重點和難點,學生的得分率往往偏低,成為獲得高分的攔路虎.一道試題的解題失誤中可能包含了多種失誤類型.學生在分析自身解題失誤的原因時,往往存在歸因片面、不深入的情況,從而不能針對性地采取對策,導致了一些題一錯再錯,在考試中屢次失利.本文對失誤原因進行初步診斷,以期對學生有所幫助.
1 知識性失誤
1.1 知識模糊 概念不清
在解題過程中,學生往往會因為基本功不扎實,導致對相近知識點的記憶存在偏差.例如化學反應速率與化學平衡都受到溫度、濃度、壓強等因素的影響,一些學生經常錯誤的認為只要正反應速率增大,平衡就正向移動,或平衡正向移動一定是因為正反應速率增大了,忽略了平衡移動的方向是由正逆反應速率共同作用的結果,由其相對大小決定.
1.2 課本知識 不能拓展
一些讓學生感覺陌生的試題情景或考點,其實是源于課本知識的拓展,而學生在解題時無法將試題考查的內容與學過的課本知識進行聯系,缺乏舉一反三的能力,不能適應考查知識再生力的新情境、新問題.
在8 h時,反應體系內氫氣的量為mol(忽略其它副反應).
學生在解題時基本都能關注到無論生成四氫萘還是萘都有氫氣放出,也關注了各自的產率,但計算生成萘的同時所釋放的氫氣時,忽略了第一步反應中釋放的氫氣.
2.2 思維粗疏 片面膚淺
對于根據題示信息解釋原因類的試題,往往需要學生從多個角度綜合分析,因此容易出現思考不夠深入,不夠全面,或對題示挖掘不透徹,導致作答不完善的情況.
例5 (2019年3月紹興適應性考試30題節選)反應①在實際生產中常通入適量 O2,既降低能耗又提高產率,原因是.
例6 (2018年4月浙江選考30題節選)工業上多采用乙酸過量的方法,將合成塔中乙酸、乙醇和硫酸混合液加熱至110℃左右發生酯化反應并回流,直到塔頂溫度達到70~71℃,開始從塔頂出料.控制乙酸過量的作用有.
例5明確告知學生從“能耗”和“產率”兩個角度分析,學生出現漏答的情況就相對較少,而絕大多數題目則像例6一樣,并不會限定作答角度,化學反應速率、平衡移動方向、反應物或生成物是否易揮發、易分解、生成物是否容易分離等都會成為答題的角度,需要具體結合題示信息,包括文字、圖表等多樣化的形式,進行對比、判斷、分析.
2.3 錯誤類比 定勢束縛
復習階段,學生往往會針對某一題型反復操練,來不斷提升熟練程度,從而在解題時可以類比原有類似的題目,從而提升解題速度.一般而言,這樣的類比是有效的,但也容易讓思維固定化,出現一定的傾向性和局限性,從而導致解題失誤.
例7 (2016年4月浙江選考30題節選)實際操作中,應控制N2O4/H2O質量比高于5.11,對此請給出合理解釋.
例8 (2018年11月浙江選考30題節選)分析說明原料氣中N2過量的理由.
例7的參考答案為“為了提高N2O4濃度,有利于平衡正向移動,得到高濃度的硝酸.”學生在解答例8的問題時,便會進行類比,參考例7的解答模式,僅從平衡移動的角度進行考慮,沒有注意到題目中“ N2的吸附分解反應活化能高、速率慢,決定了合成氨的整體反應速率.”的表述,使得答案并不完整.
再如,學生都知道“催化劑不影響平衡移動”,平時的考察中也多為催化劑是否影響轉化率等.當題目中出現“選用高效率的催化劑有利于更快達到平衡”這樣的表述時,看到“催化劑”、“有利于”和“平衡”這樣的字眼,就認為表述有誤,忽略了這其實講的是催化劑對反應速率的影響,而非平衡.
2.4 以“質”代“量” 迷戀經驗
在化學反應原理大題中,往往會通過作圖的形式考查學生對化學平衡移動相關知識的綜合應用.一部分題目難度相對較低,學生可以結合常規解題經驗,根據條件改變對速率、平衡的影響,畫出趨勢即可.但也有一部分作圖會結合化學平衡常數等知識點考查,需要學生通過題示數據計算得出起點、終點或拐點的縱坐標數值.不少學生在解題時因為迷戀經驗,僅注意“質”的推斷,得到準確的變化趨勢,但忽略了給出的相關數據,沒有進行“量”的計算,不能拿到全分.
3 對策
3.1 回歸課本 消除盲點
許多知識性失誤的產生主要源于學生對課本知識的不熟悉,而無論考試怎么考,始終圍繞課本知識要點,圍繞需要落實的學科核心素養.
因此,學生在復習備考時,要注重回歸課本,落實核心知識要點,加深對知識點的理解,尤其注意消除原有知識盲點,仔細辨析相近概念,同時圍繞主線,通過類比、歸納等方式不斷拓展,形成清晰的知識脈絡體系.
3.2 建立模型 強化訓練
建立模型是學生化學學習的重要方法,也是化學學科核心素養之一.針對化學反應原理綜合試題,建立的模型包括知識模型和思維模型.
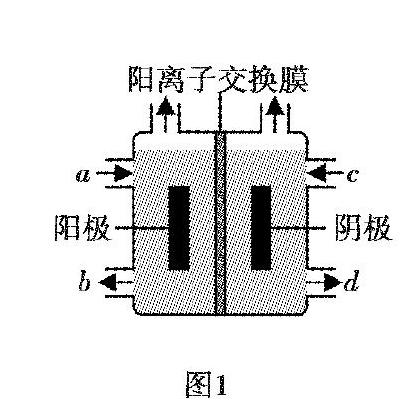
如電解池工作原理模型、轉化率或平衡轉化率隨溫度變化趨勢模型等屬于知識模型,單平衡體系、多平衡體系解題的一般思路、平衡常數應用的一般方法等屬于思維模型.正確建立知識模型有利于強化對知識的理解,也是建立思維模型的基礎.而正確建立思維模型,是對學生更高層次的能力要求,是落實發展核心素養和提升解題正確率的保障.
當然建模,尤其是思維層面的建模不能紙上談兵,需要配合相應的練習,在練習中強化鞏固,使建模更加嚴謹、科學和規范.
參考文獻:
[1]王后雄,王世存編著.新理念化學教學診斷學[M].北京:北京大學出版社,2014.
[2]丁弘正.高中生化學學習自我診斷能力現狀及提升策略研究[D]. 武漢:華中師范大學,2017.
(收稿日期:2019-05-28)

