抗CD19 CAR-T治療B淋巴細胞血液惡性腫瘤效果的Meta分析
束新輝,劉柳,胡明月,丁冰潔,周虎,宋永平
(1鄭州大學附屬腫瘤醫院 河南省腫瘤醫院,鄭州450000;2鄭州大學第一附屬醫院;3中南大學護理學院)
B淋巴細胞血液惡性腫瘤主要包括急性淋巴細胞白血病(ALL)、慢性淋巴細胞白血病(CLL)及B細胞淋巴瘤。隨著醫療技術的快速發展,靶向治療使得治療方案更具有針對性。Zhu等[1]采用Meta分析研究顯示,抗CD19嵌合抗原受體T細胞免疫(CAR-T)細胞治療B淋巴細胞惡性腫瘤的總緩解率為48%。但系統評價和Meta分析研究的結果差異較大,且未納入中文文獻。CAR-T治療是一項新型的治療技術,在我國的應用近兩年來增速明顯,截至2017年6月30日,中國學者在www.clinicaltrials.gov以及www.chictr.org.cn上登記的CAR-T細胞臨床試驗數量已經超過美國,成為世界上注冊該臨床試驗數量最多的國家[2]。本研究將全面檢索1980年至今的包括中文文獻的臨床研究,總結抗CAR-T細胞治療B淋巴細胞惡性腫瘤發展現狀,為我國CAR-T細胞治療的未來提供參考。
1 資料與方法
1.1 文獻納入和排除標準
1.1.1 納入標準 研究類型為臨床研究;無論有無設置對照組,對于是否為RCT無要求;研究對象均確診為B細胞淋巴惡性腫瘤,包括ALL、CLL及B細胞淋巴瘤;均使用抗CD19 CAR-T細胞治療;結局指標為總緩解率(ORR),即疾病減緩一定程度并保持一定時間的患者比例,包括完全緩解(CR)和部分緩解(PR)。
1.1.2 排除標準 無全面清楚的原始數據或數據類型無法納入統計分析;文章類型為綜述、會議摘要、病例報告、動物實驗、樣本量≤1等;未獲取完整數據的文章且未能與作者本人取得聯系。
1.2 文獻檢索策略 以“chimeric antigen receptor-modifed T cells”或“CD19 chimeric antigen receptor-modifed T cells”、 “CAR-T”、 “Anti-CD19 chimeric antigen receptor-modified T cells”、“ Chimeric Antigen Receptor Redirected T Cells”為檢索詞計算機檢索PubMed、EMbase等英文數據庫,以“CAR-T”、“嵌合抗原受體T細胞”、“CAR-T細胞療法”、“CD19嵌合抗原受體T細胞”、“B淋巴細胞血液惡性腫瘤”、“急性淋巴細胞白血病”、“慢性淋巴細胞白血病”、“淋巴瘤”為檢索詞計算機檢索CNKI、萬方等數據庫。此外,追溯納入文獻的參考文獻,以補充獲取相關文獻。檢索時間為1980年1月~2018年10月。語言限定為英語和漢語。
1.3 文獻納入和資料提取 兩名評價員獨立按照納入排除標準進行文獻閱讀和篩選,并交叉核對納入的文獻,對難以確定是否納入本研究的文獻通過討論或者由第三位資深評價員裁定。之后,采用統一表格對納入文獻進行資料提取。
1.4 文獻質量評價 納入RCT的偏倚風險評價采用Cochrane協作網推薦的RCT偏倚風險評價工具,納入非隨機對照研究的偏倚風險采用MINORS評分進行評價。
1.5 統計學方法 采用Cochrane協作網提供的Review Manager5.3軟件對數據進行分析。數據的效應指標均采用有效率P、標準誤(SE)及其95%可信區間(CI)。采用Review Manager5.3對數據進行敏感性分析,對每篇文獻逐一剔除進行分析,觀察其異質性的改變并采用倒漏斗圖評價其發表偏倚。
2 結果
2.1 文獻檢索結果 初檢出相關文獻1 092篇,通過篩選以及閱讀納入文章的參考文獻,最終納入文20篇[3~22],中文1篇、英文19篇,總樣本量為337例,大多數文章在制作CAR-T細胞時均為病毒轉錄且輸注CAR-T前進行化療。
2.2 納入文獻的基本特征與方法學質量評價 納入文獻的基本特征如發表時間、年齡、性別、診斷等的基本特征如下,見表1。納入研究全部為無對照組的臨床研究,用MINORS工具前8個條目對文獻進行質量評價。因CAR-T是一項新技術,納入文獻尚未有大樣本量的研究,質量評價條目2(納入患者的連貫性)和條目8(是否估算了樣本量)均為0分,見表2。
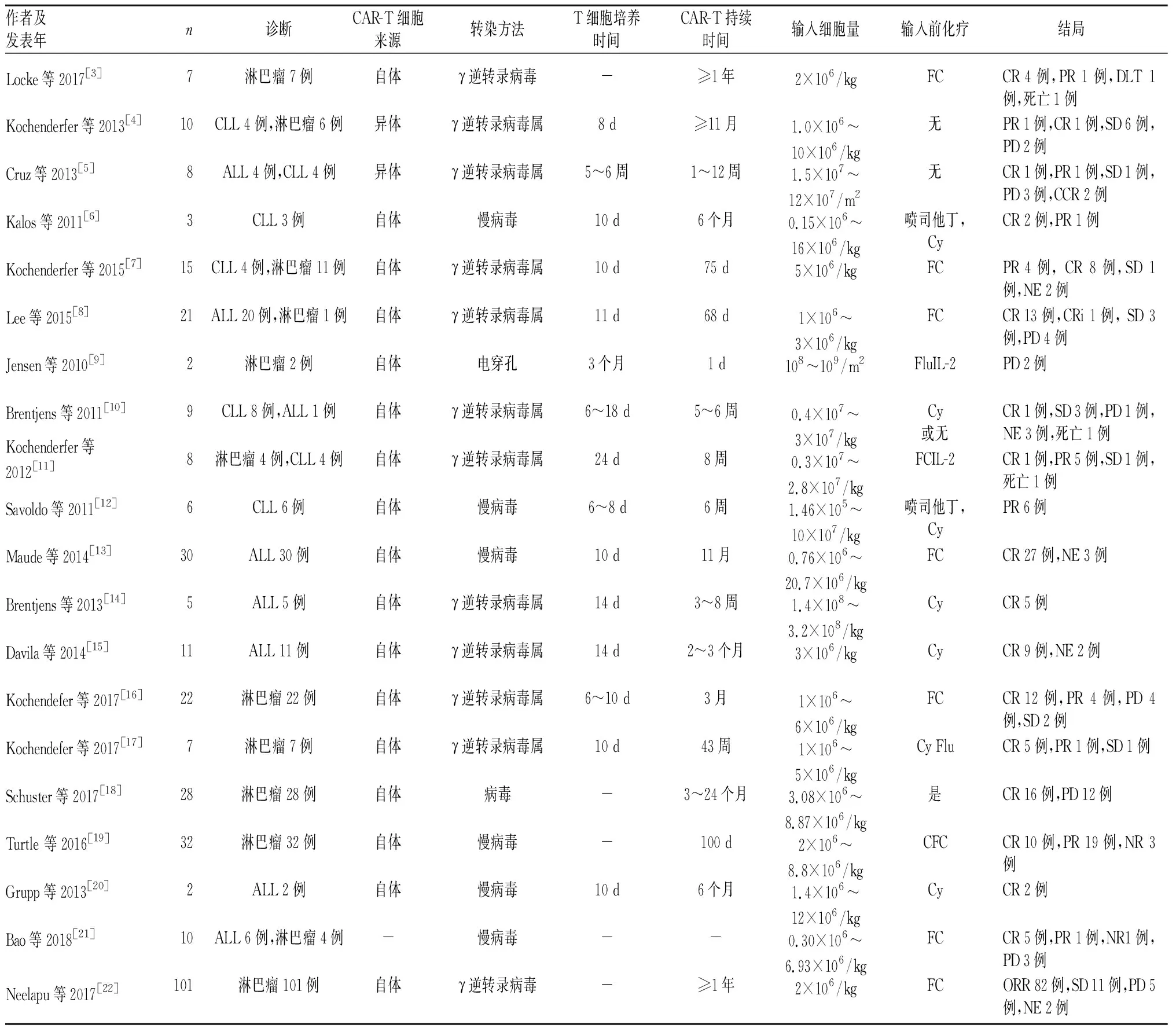
表1 納入文獻的基本特征
注:FC為氟達拉濱+環磷酰胺;CR為完全緩解;CCR為持續完全緩解;PR為部分緩解;NR為未緩解;PD為疾病進展;DLT為劑量限制性毒性;NE為未評價。
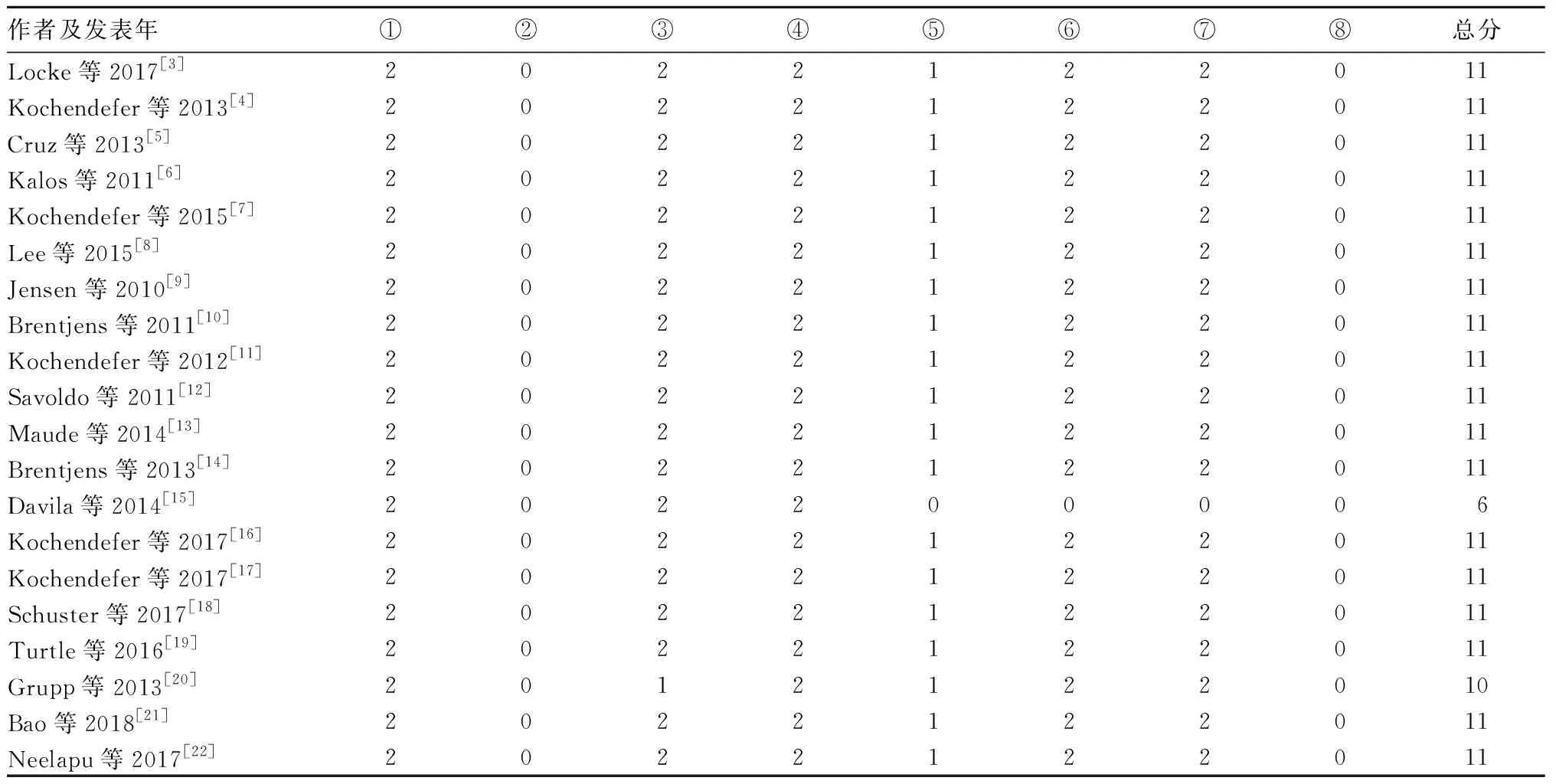
表2 文獻質量MINORS評價結果(分)
注:①為明確地給出了研究的目的;②為納入患者的連貫性;③為預期數據的收集;④為終點指標能恰當地反映研究目的;⑤為終點指標評價的客觀性;⑥為隨訪時間是否充足;⑦為失訪率低于5%;⑧為是否估算了樣本量。
2.3 ORR Meta分析結果 共納入19個研究。隨機效應模型Meta分析結果顯示,CAR-T用于B淋巴細胞血液惡性腫瘤患者的ORR為67%[95%CI(56%,79%),P<0.01]。見圖1。
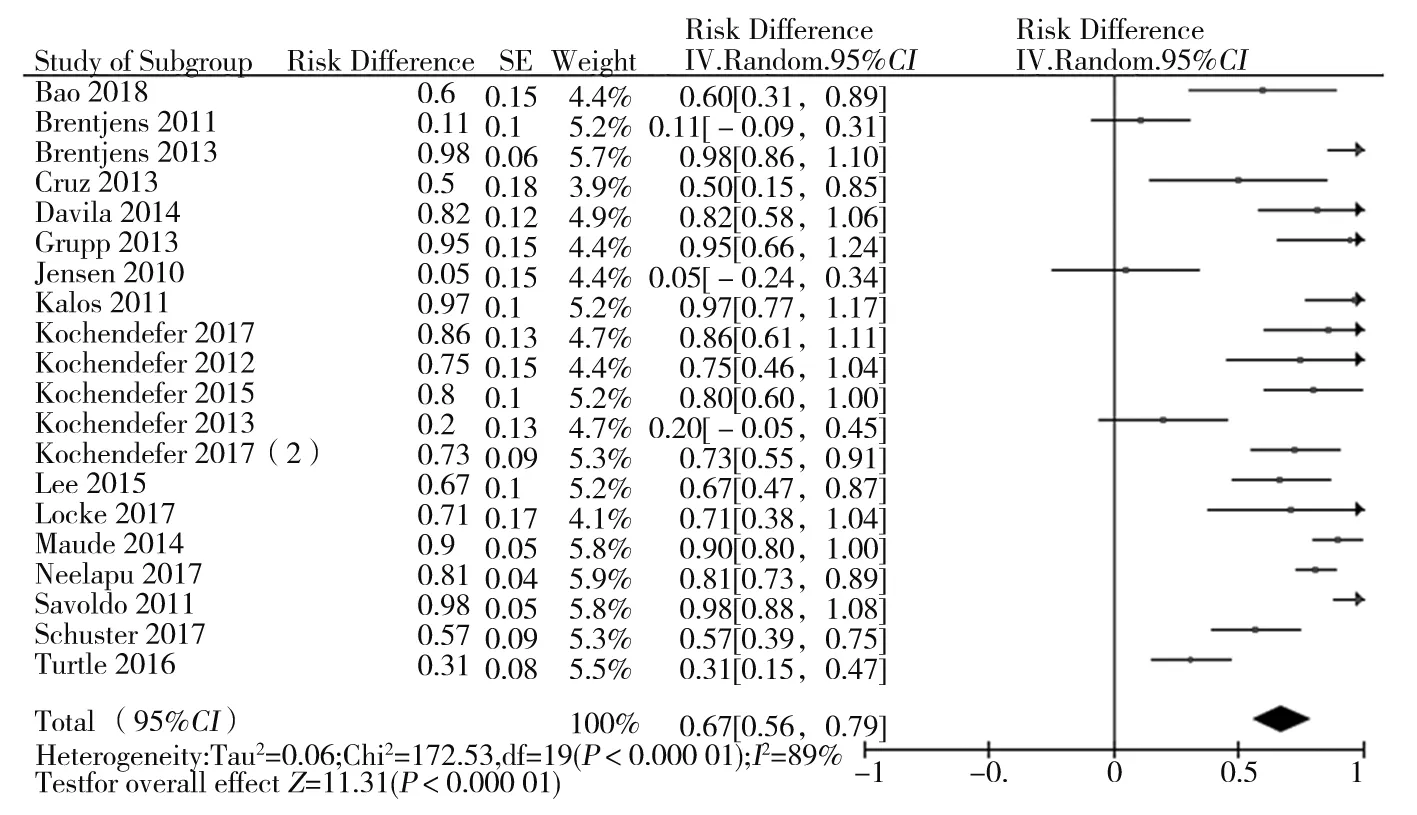
圖1 CAR-T細胞療法治療B淋巴細胞血液惡性腫瘤ORR的Meta分析結果
2.4 ORR亞組分析結果
2.4.1 不同疾病類型亞組分析結果 以疾病類型為亞組,隨機效應模型Meta分析結果顯示,CAR-T治療ALL的ORR為71%[95%CI(52%,91%),P<0.01],治療CLL的ORR為65%[95%CI(38%,91%),P<0.01],治療B細胞淋巴瘤的ORR為64%[95%CI(47%,75%),P<0.01]。見圖2。
2.4.2 不同CAR-T輸入劑量亞組分析結果 以CAR-T輸入劑量為亞組,隨機效應模型Meta分析結果顯示,CAR-T劑量≤1×107/kg用于治療B淋巴細胞血液惡性腫瘤的ORR為69%[95%CI(57%,81%),P<0.01],劑量>1×107/kg用于治療B淋巴細胞血液惡性腫瘤的ORR為73%[95%CI(50%,96%),P<0.01]。見圖3。
2.4.3 不同CAR-T細胞來源亞組分析結果 以CAR-T細胞來源為亞組,隨機效應模型Meta分析結果顯示,自體CAR-T細胞用于治療B淋巴細胞血液惡性腫瘤的ORR為71%[95%CI(59%,83%),P<0.01],異體CAR-T細胞用于治療B淋巴細胞血液惡性腫瘤的ORR為32%[95%CI(3%,61%),P<0.01]。見圖4。
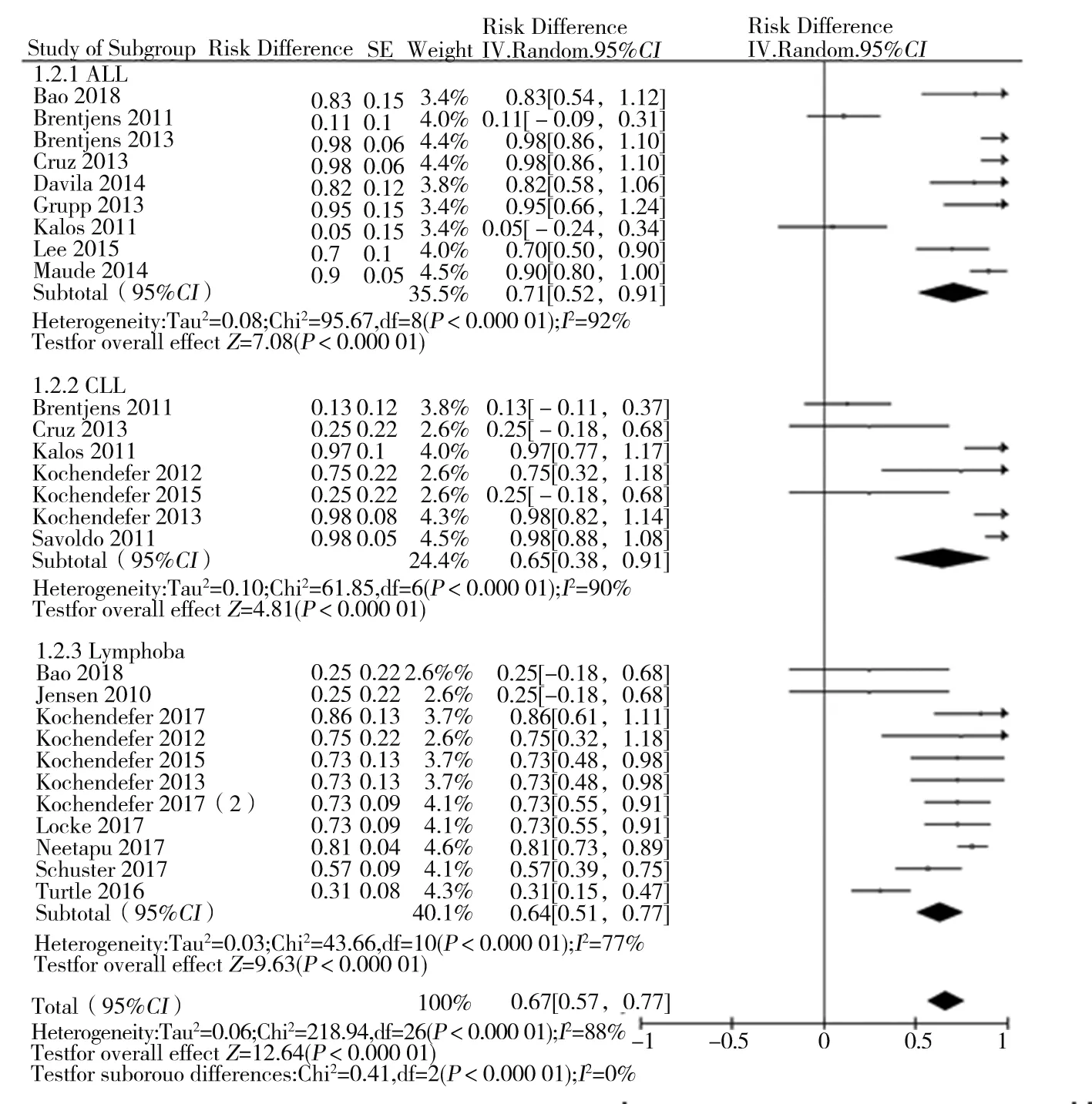
圖2 CAR-T細胞療法治療不同類型B淋巴細胞血液惡性腫瘤ORR的Meta分析結果
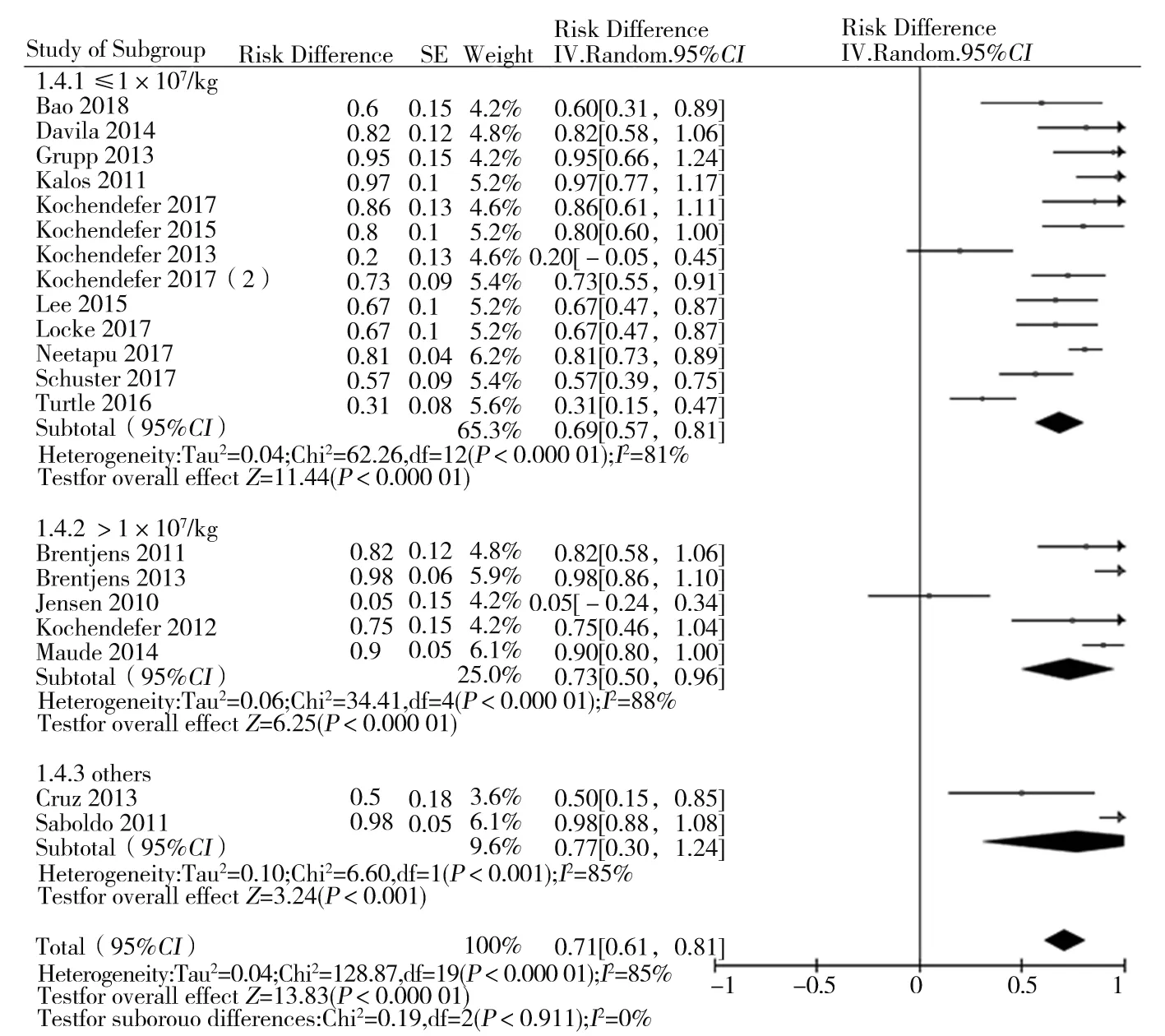
圖3 不同劑量CAR-T細胞輸注量治療B淋巴細胞血液惡性腫瘤ORR的Meta分析
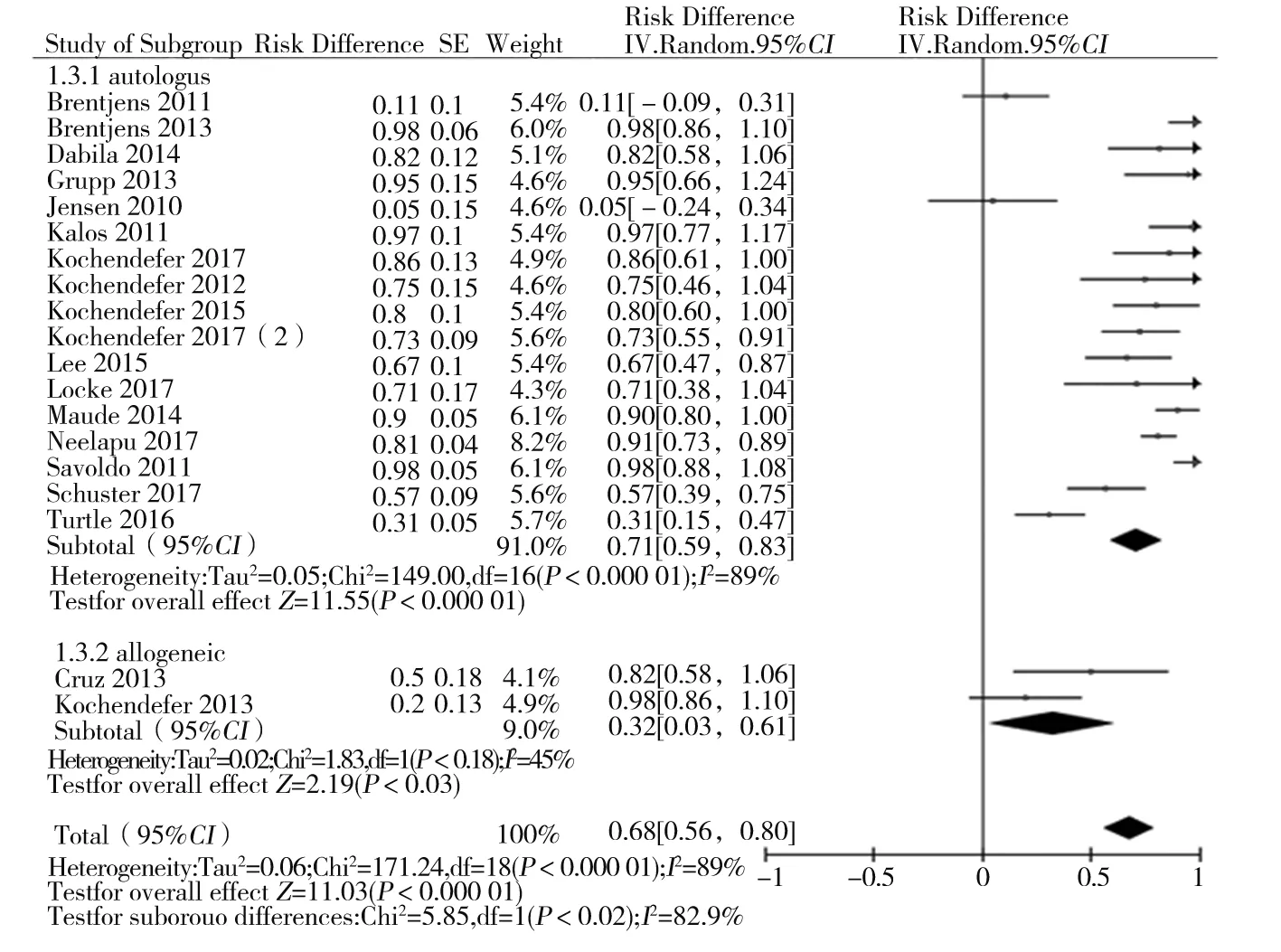
圖4 不同來源CAR-T細胞治療B淋巴細胞血液惡性腫瘤ORR的Meta分析
2.5 發表偏倚及敏感性分析 采用漏斗圖進行分析,顯示對稱結果較好,提示出現發表偏倚的可能性較低。見圖5。采用不同合并模型所得效應量間差異的方法進行敏感性分析,并比較逐項剔除每項研究后總效應量變化,Meta分析顯示合并結果無本質性改變,提示研究結果較為穩定。
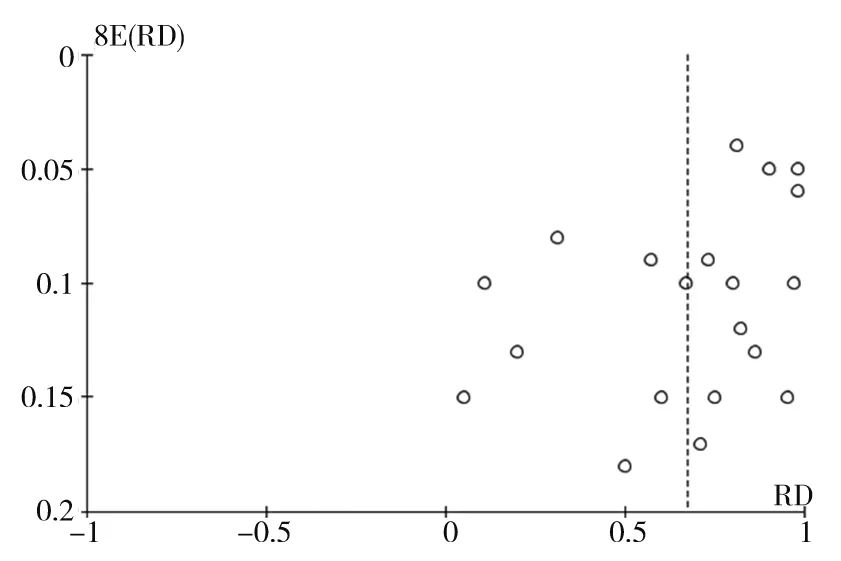
圖5 CAR-T細胞治療B淋巴細胞血液惡性腫瘤的漏斗圖
3 討論
20世紀80年代末提出的嵌合抗原受體(CAR)成為腫瘤免疫治療領域研究的熱點,為惡性腫瘤的治療帶來新的方向[23]。該方法使用患者來源的被CAR基因轉染的T淋巴細胞,將T細胞的生理功能與在非主要組織相容性復合體(MHC)限制性方式下識別表面抗原的能力結合起來。一旦輸入體內,工程化的T細胞會特異性靶向腫瘤相關抗原,并確保長期抗腫瘤記憶[23]。多數的淋巴系統惡性腫瘤起源于B細胞,并且多數細胞表面表達CD19,因此使用靶向CD19的CAR修飾的T細胞表達腫瘤細胞已經改變難治性/復發性B細胞的淋巴惡性腫瘤的治療方案。
CAR-T細胞治療作為一種新興的腫瘤免疫治療手段,在復發/難治性惡性B細胞腫瘤的治療方面具有巨大的潛力。雖然傳統的放化療、造血干細胞移植等治療方法延長了部分血液系統惡性腫瘤患者的生存時間,但是復發、難治甚至耐藥現象仍是目前面臨的巨大挑戰。而CAR-T細胞免疫治療因在腫瘤的治療中取得了突破性進展,成為血液系統等多種疾病治療的重要手段[24]。國內關于CAR-T細胞的個案研究報道大多數是抗CD19 CAR-T細胞療法對復發難治的急性B淋巴細胞白血病的應用,1篇文章報道出現靶抗原丟失及疾病復發1例[25],其他文獻均肯定了CAR-T對于急性B淋巴細胞白血病的治療效果,但細胞因子風暴、發熱、神經系統綜合癥、持久性等問題仍是影響治療效果和亟待解決的問題。本研究結果顯示,CAR-T對B淋巴細胞血液惡性腫瘤治療的ORR值為66%。與先前研究相比的Meta研究所得出的ORR值48%相比有所提高[1]。但本研究低于之前研究數據得出的ORR值(73%),其中可能的原因是納入研究標準不同,同時本研究又納入了近幾年的研究,并且去除了樣本量≤1的文獻。
本次研究納入文獻中,CAR-T細胞輸注劑量均在106~109/kg,可以基本認為是安全范圍,有個案分析報道1例接受單次劑量為1010/kg CAR-T細胞輸注的患者于5 d后死亡,本研究中大多文獻也均遵循劑量遞增策略。本研究結果提示,CAR-T細胞輸注劑量偏高的患者ORR高于輸注劑量偏低的患者,這可能與隨著CAR-T細胞輸注劑量增加、患者體內CAR-T細胞體內持續時間較長相關。一項研究通過對比6個月的無進展生存期(PFS)證實,在一定范圍內,CAR-T細胞輸注量越大、患者的PFS越長。CAR-T細胞輸注數量為小于108患者的PFS為54.5%,而CAR-T細胞輸注數量大于108患者的PFS為94.6%[1]。對劑量輸入要求做出統一標準存在一定的困難,因為各臨床試驗中CAR-T細胞結構、T細胞培養方法以及患者年齡、體質量、病情等不同,因此應該根據臨床前實驗結果,結合患者個體腫瘤類型、腫瘤負荷做出一些個性化調整。
本研究中僅有兩篇文獻[4,5]使用異體CAR-T細胞治療,均在異體造血干細胞移植后進行治療,經自體CAR-T細胞輸注治療的患者ORR值(71%)為經異體治療ORR(32%)的兩倍多,提示CAR-T細胞以自體為來源有較好的療效。雖然臨床以自體來源的CAR-T細胞為主,但異體來源的質量優于患者本身的CAR-T細胞仍存在優勢。本研究的兩篇研究所納入患者均未出現GVHD。Cruz等[5]研究顯示,經病毒修飾的異體CAR-T細胞能夠同時識別攜帶病毒的腫瘤和惡性腫瘤。造成經異體CAR-T細胞治療惡性淋巴細胞血液病的ORR較低的原因,可能是輸注CAR-T細胞前未化療,而化療能夠有效提高體內CAR-T細胞的存留時間并且有利于細胞擴增。但是由于現有研究顯示的文獻匱乏,針對不能夠使用異體細胞修飾的CAR-T治療療法能需要大樣本的研究證實有效性。

